胆囊次全切除术的合理运用
2023-01-13吴钢蔡端
吴钢,蔡端
(复旦大学附属华山医院 普外科,上海 200040)
腹腔镜胆囊切除术(laparoscopic cholecystectomy,LC)是治疗症状性胆囊结石等胆囊良性疾病的首选方法[1-2]。然而,LC引起的胆管损伤(bile duct injury,BDI)发生率约为0.2%~1.5%,仍然高于传统开腹胆囊切除术(open cholecystectomy,OC)的0.1%~0.2%[3]。随着胆囊切除安全理念(culture of safety in cholecystectomy,COSIC)的推广[4],外科临床始终在努力降低或避免血管-胆管损伤(vasculobiliary injury,VBI)等严重并发症所带来的巨大危 害[5]。在急性或慢性萎缩性胆囊炎、胆囊坏疽、胆囊周围组织致密粘连等情况下,解剖Calot三角十分困难和不安全,并可能导致VBI等致命性并发症[6-7]。因此,面对“困难”胆囊(difficult gallbladder,DGB)[8-10],当确保安全的关键显露(critical view of safety,CVS)无法实现时[11],为了降低VBI,胆囊次全切除术(subtotal cholecystectomy,STC)等纾困(bail-out)手术得到了广泛的运用[5,9,12]。STC是外科医师在遭遇极端客观困难的情况下明智的选择,在给患者提供安全、合理治疗的同时,可以避免严重并发症[7]。近年来,STC已在更多复杂的病例中得以运用。一项英国的全国性研究分析了2000—2019年间胆囊手术的应用趋势,结果提示,在纳入的1 234 319例接受胆囊手术的患者中,STC增加了716.6%(2000年217例,2019年1 772例)[13]。
LC和OC已经成熟,并建立了完善的诊疗规范。而STC是在DGB的前提下实施的,是一种旨在降低严重并发症的纾困手术,也称为“挽救技术”(salvage technique,rescue procedures)[11,14]。由于目前对STC的适应证和手术操作规范仍不统一[10],术前如何确定与STC相关的高危因素,针对STC如何手术决策及规范手术操作、并降低其特有的近期和远期并发症等问题均值得深入探讨。
1 胆囊次全切除术的界定和适应证
Bornman和Terblanche于1985 年首次明确描述了STC[15]。许多先前的文献中对胆囊部分切除术(partial cholecystectomy,PC)或STC并没有明确的界定,就外科术语而言,一个器官的部分与次全切除的范围是不同的。两者经常被混用,势必造成混淆[16]。目前“部分”一词已基本弃用,如果只切除胆囊体部、底部或更小的范围,描述为“胆囊体部切除术”或“胆囊底部切除术”可能更加合理[8]。Strasberg等[17]结合美国胃肠和内窥镜外科医师学会(the Society for American Gastrointestinal Endoscopic Surgeons,SAGES)2016年引入的术语,将STC定义为不解剖Calot三角,关闭在漏斗部近端的胆囊管开口,而在保留的与胆管相连的组织中没有胆囊部分残留[7,18]。近年来,大量针对STC的研究均基于这一概念[1,3,5,9]。
Strasberg等[4]以及Nassar等[11]引入COSIC以来,其中CVS技术作为一种确保手术安全的技术规范和教学手段,在LC中预防BDI的作用已获得了广泛的认可。然而,在困难的胆囊切除术(cholecystectomy,CCY)中,CVS往往无法实现[1]。为了保证患者的安全,避免严重的并发症,特别是BDI和大出血等,实施STC是主要的纾困手术之一[3,5]。综合文献,STC的适应证主要包括:Ⅱ级和Ⅲ级急性胆囊炎(acute cholecystitis,AC)并反复发作,坏疽性胆囊炎,胆囊积脓,胆囊穿孔,胆囊-消化道内瘘,严重硬化的萎缩性胆囊炎,“冰冻”三角,术前治疗性经内镜逆行胰胆管造影(endoscopic retrograde cholangiopancreatography,ERCP)和经皮经肝胆囊穿刺引流术(percutaneous transhepatic gallbladder drainage,PTGBD),上腹部手术史,Mirizzi综合征,肝硬化伴门脉高压,胆源性胰腺炎,胆道解剖异常等[2,8,19-23]。
大量的研究对术前预测LC难度进行了探索,世界急诊外科学会(the World Society of Emergency Surgery,WSES)开发了10 分制胆囊炎严重程度评分系统,≥5 分时为DGB,其中33%的LC患者中转开腹手术[24]。虽然美国麻醉师协会(American Society of Anesthesiologists,ASA)分级是反映患者总体健康状况的标准,但是该评分与手术难度之间也存在显著相关性。ChloeS研究小组的结果提示,1、2、3和4~5级患者的手术困难率分别为22%、32%、46%和73%[25]。研究表明,男性、高龄、肥胖、糖尿病等与STC密切相关[26-27]。
2 胆囊次全切除术的分型和手术方法
Henneman等[16]依据是否残留胆囊后壁和漏斗部残余结构的处理,将STC分为四种类型。Shin等[28]根据分离胆囊后壁的层次和对胆囊管的不同处理方式将STC分为三种类型。然而,上述分型均没有得到普遍的认可[17,29]。虽然STC的操作是在DGB的前提下进行的,但是仍然有必要将STC的具体过程确立为标准化的通用技术。厘清手术名称和分型有助于外科医师选择手术方式,并有助于这一领域的临床研究能够统一标准[30]。2016年Strasberg等[17]对STC的手术名称和操作进行了标准化,以漏斗-胆囊管残留组织的不同处理方式,将STC分为两型:“旷置”型STC(fenestrating STC,F-STC)和“重建”型STC(reconstituting STC,R-STC),近年来这一分型得到普遍认可[1,7,21,31-32],作者绘制分型见图1。
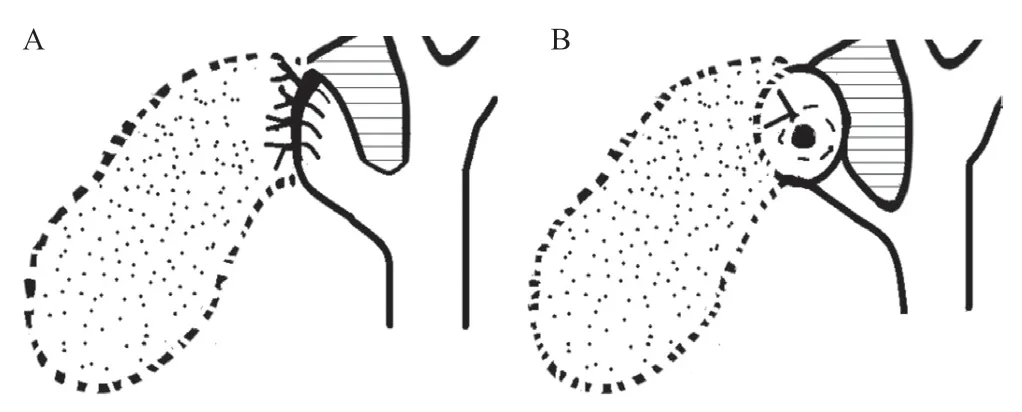
图1 胆囊次全切除术的分型
F-STC和R-STC均不解剖Calot三角,运用逆行漏斗技术(retro-infundibular technique)[19]、逆行胆囊底部入路(retrograde fundus first)、“中间优先”(middle-first)[21]、胆囊内途径(inside approach of the gallbladder)[23]等方法,切开胆囊后取净结石,尽可能多地切除胆囊组织直至漏斗的底部,胆囊后壁残留的黏膜组织可以通过切除,或者电凝、氩气刀等各种手术能量平台予以破坏即可。F-STC是将胆囊管开口不予处理或置入引流管,也可以使用可吸收缝线予以内荷包的方式闭合。由于炎症改变,肝总管、右肝管、Luschka胆管或血管可能粘附在胆囊管上,内荷包缝合时应防止进针太深,以防这些结构可能被结扎或损伤。而如果可以显露整个剩余的漏斗部,并且周围没有其他重要结构,则可以将残端予以缝合或用外科吻合器将其闭合,从而完成R-STC[17,30]。胆囊残端的可靠闭合可以降低胆漏的发生率,一些研究提示R-STC的近期结果更好[7,17,21]。F-STC和R-STC这两种技术是互补的,而术中发现和外科医师的专业知识及经验对两者的选择有较大的影响[14,32]。
3 胆囊次全切除术的近期和远期并发症
STC的手术操作技术存在显著的异质性,与残留胆囊黏膜的数量、残端的处理和引流管的放置等有关[3]。而STC的基础是DGB,其本身比一般的CCY具有更高的手术难度和风险,并可能有更高的并发症[1,33]。STC的主要近期外科并发症包括胆漏、腹腔内积液、膈下或肝下脓肿、出血以及BDI等[1,6,12]。STC最大的缺点是术后胆漏,发生率达 18%(221/1231)[8]。多项研究观察到F-STC术后胆漏的发生率高于R-STC[12,14,30]。但是,绝大多数的胆漏可以通过非手术方法解决,只有很少的病例需要行ERCP或再次手术[7,21,34]。更值得注意的是,STC实现了至关重要的预防BDI的目标。Elshaer等[8]的Meta分析提示,STC的BDI发生率为0.08%(1/1 231),低于TC的0.4%(668/162 464)。
胆囊残留部分的炎症,残留或再生的结石是导致STC远期并发症的主要原因,包括残余胆囊炎、残余胆囊结石、Mirizzi综合征和胆囊切除术后综合征(post cholecystectomy syndrome,PCS)等[17,35]。一项研究对纳入的108例F-STC、24例R-STC与317例TC进行了比较,结果提示R-STC组的远期并发症发生率较高,并直接与胆囊的残留相关[21]。
4 胆囊次全切除术的运用策略
4.1 纾困手术的意义和应用趋势
CVS强调只有在明确显露胆囊管及胆囊动脉后再进行下一步的操作[11,36],虽然严格遵守CVS对减少BDI非常重要,但CVS只是COSIC的一部分,而COSIC要求将安全放在首位[4,37]。当术者面临TC风险过大时,可以通过手术方法的调整和灵活使用纾困手段以安全处置DGB[10]。即为避免BVI等严重并发症,采取略偏离完成TC的初始目标而采用的挽救技术策略,在术中这也称之为“拐点”(inflection point),是指术中决定停止TC的尝试,改用其他方法完成手术的时间节点[38]。对术者来说,到达拐点一定比发生BDI要好得多。胆囊纾困手术主要包括腹腔镜胆囊次全切除术(laparoscopic subtotal cholecystectomy,LSC)、开腹胆囊次全切除术(open subtotal cholecystectomy,OSC)、胆囊切开取石术、胆囊底部切除术和胆囊造口术等[18]。所有这些备选方案的首要目标是保证患者的安全,核心是避免了在胆管和相关血管附近严重炎症纤维化区域进行危险的解剖操作[5,39]。
纾困手术的决策在DGB的病例中起着至关重要的作用,决定何时停止Calot三角的分离,选择纾困手术而不是TC,这可能是最具挑战性的策略调整[39]。术中应特别注意可能显示下一步操作有困难的迹象或者可能导致严重并发症的线索,例如:解剖结构混乱、解剖进展缓慢、原因不明的出血或胆漏、无法正常夹闭管状结构,或需要过多的血管夹等[37]。遭遇这些情况时往往需要调整手术方案,并意识到拐点的到来。虽然胆囊造口术、胆囊切开取石术和胆囊底部切除术等其他纾困手术后,患者往往需要再次手术[5];但是,权衡利弊,纾困手术最大的意义是避免了BDI等严重并发症的发生,这也是其最重要的临床价值,因而在DGB的使用率越来越高[8,22],这也显示了AC等胆囊良性疾病外科治疗方法的不断变化和发展。一项纳入290 855例胆囊手术的美国全国性研究报告分析了AC外科手术方式的趋势,结果提示,从2003 年到2014 年,LSC的比例增加了1倍多,而OSC的比例增加了5 倍[40]。该结果与最近发布的英国全国性研究相似[13],均反映了STC得到了更加普遍的运用。
4.2 腹腔镜胆囊次全切除与中转开腹的选择
当无法识别Calot三角的解剖结构时,腹腔镜中转开腹是常用的方法[10,35]。在一项Meta分析中,LC中转开腹率为8%[8]。中转开腹后最大的优势是触觉,可以提高对肝动脉、胆囊结石、胆囊管结石及胆总管结石的辨别和触探,并方便控制出血和缝合等操作。但是,困难的LC中转后术者面临的仍然是一个棘手的开腹手术,而中转后丧失了腹腔镜特有的放大作用,有时手术视野及暴露反而变差[31,37],尤其是对于体质量指数(body mass index,BMI)较高的患者,可能会带来更高的风险[41]。中转后既不能保证成功完成TC,大多数只能实施OSC,也不能降低或保证避免意外的VBI等[18,29,34],特别是术者对开腹胆管手术缺乏经验时,可能更加难以安全地继续手术,并最终可能导致更严重的并发症[16]。有研究提示,LC中转开腹手术病例的BDI明显增加[42]。同时,中转开腹也增加了术后伤口感染、腹腔粘连和切口疝等并发症,并导致下床活动时间推迟及住院时间延长[5,41]。
随着腹腔镜手术经验的增加和技术的成熟,LSC避免了在Calot三角处进行危险的解剖,已成为困难LC替代中转开腹的一种安全可行的方法,并可以避免大多数DGB患者中转开腹[3,16,20]。LSC为复杂胆囊炎患者提供了诸多的优势,包括高清腹腔镜的放大功能可以使解剖结构的识别更加容易,微创手术确保了伤口相关并发症非常低[6]。但是,STC的手术本身存在显著的异质性,因此,在对DGB选择LSC还是中转开腹时,需要结合术者的经验和患者的客观情况[3]。
4.3 胆囊全切除与次全切除的综合考量
安全的CCY是指对患者(无胆管/空腔脏器/血管等损伤)和术者(无纠纷或诉讼)都安全的手术。TC是首选的手术方法,只有当TC的风险超过可能的获益时,才将STC作为一种挽救手段,目的是成功避免严重并发症[7,29]。大多数医源性并发症是可以避免的,尤其是在遵守COSIC的情况下[11]。在DGB的情况下,执意完成TC的目标可能并不是最重要的,因为在这种情况下可能会导致VBI,从而危及患者的安全。而改行STC等纾困手术,可以使外科医师能够比较安全地完成手术[7]。
虽然有研究指出STC术后发生BDI的风险低于TC,但是其他并发症(胆漏、切口感染、出血、肝下积液、残留结石、残余胆囊炎和术后治疗性ERCP)和再次手术的必要性均高于TC[21,43]。而且,STC残端相关的并发症可能会在术后数年内发生[2]。在Kohga等[44]的研究中,23.7%的STC患者出现了远期并发症(胆总管结石、残余胆囊炎和结石)。这与DGB本身的炎症、手术操作的方式和许多STC患者的全身状况比较差等因素均有直接关系[43]。需要强调的是,STC并不等同于TC,并且不提倡不恰当地扩大STC的适应证。安全有效地完成手术是必须完成的目标,“安全”是指无BDI等严重并发症,“有效”是指无需再次手术干预。当遭遇DGB时,可以优先考虑LSC,而不是胆囊切开取石术、胆囊底部切除术或胆囊造口术等需要二次手术的方法。反之,执意为了避免二次手术,反复尝试在Calot三角区进行危险的解剖也是不可取的[17]。
查尔森合并症指数(Charlson comorbidity index,CCI)为3或4,AC反复发作,症状发作与手术的间隔时间较长,胆囊手术前的治疗性ERCP、PTGBD等,都与实施STC的比率显著增加密切相关[2,45]。在术前检查中影像学提示胆囊壁明显增厚(≥10 mm)[22],MRI提示胆囊壁呈低信号强度等,都是DGB的高危因素[46]。因此,对CCY的手术时机应该个体化综合评估,术前需要对可能面临DGB并可能实施STC的患者有所预判,并决定一些患者是否可以先采取非手术方法,治疗一段时间以后再重新评估,以期能够减少可以避免的STC。虽然随着器械的更新和技术的进步,AC不再被认为是LC的禁忌证,但是AC患者LC中转开腹的比率高于非AC患者。因此,许多研究建议,在症状出现后3~4 d内进行早期手术[22,47]。尽早对没有禁忌证的AC患者早期手术,以减少遭遇DGB的机会。对保守治疗有效的AC,2~3个月或更长时间后再行LC以提高TC的成功率[48]。
5 小结
综上所述,STC是遭遇DGB和可能发生BDI等严重并发症时,外科临床所采用的安全有效且具有实用价值的纾困手术。STC可以明显降低或避免BDI、VBI等致命性并发症,并可以在一次手术中解决问题,其近期和远期的治疗结果均在可以接受范围内。STC虽然不能替代TC,但是STC可以使DGB的并发症发生率接近于TC,尤其BDI更是低于TC。因此,在DGB条件下接受STC患者的治疗与通常条件下接受TC患者的安全都得到了保障。STC并不能等同于TC,所以,不提倡不恰当地扩大STC的适应证。拟行CCY前应对可能的DGB进行综合评估,能够减少可以避免的STC。
