聚维酮碘在白内障手术中的应用进展
2023-01-13刘建英万修华
刘建英 万修华
术后感染性眼内炎是白内障手术最严重的并发症之一,虽然发病率仅约0.076%[1],但病情发展迅速、治疗难度大且预后较差。研究[2]表明,眼睑和结膜囊内的菌群是引起术后眼内炎的主要病原体,病原体在术中或术后通过穿透性的手术切口进入前房、玻璃体腔可诱发眼内炎,因此术前杀灭眼睑和结膜囊的细菌对于预防术后眼内炎极为重要。为了降低术后眼内炎的风险我们采取术前3天预防性使用抗生素滴眼液、术前泪道冲洗、术前使用聚维酮碘(povidone-lodine,PVP-I)进行眼周消毒和结膜囊冲洗等多种措施,较其他措施,PVP-I消毒是降低眼内炎发病率达到II类证据的唯一技术[3],是预防术后眼内炎最重要的措施。PVP-I是一种高效的杀菌剂,对细菌、真菌、病毒以及衣原体等多种微生物都有广泛的杀灭作用,而且具有非选择性作用机制[4],通常可以防止细菌产生耐药性。因其对眼表的毒性反应可造成术后眼睛干涩、刺痛、结膜充血、角膜上皮粗糙、泪液减少等干眼表现,如何在保证其消毒效果的前提下最大程度减少其对眼表的损伤是一个值得探讨的问题,目前国内外对PVP-I的使用标准尚未达成共识,本文就PVP-I的作用机制、毒性和应用根据最新研究进行综述。
一、PVP-I及其作用机制
PVP-I是碘基杀菌剂,由聚乙烯吡咯烷酮(polyvinylpyrrolidone,PVP)和碘经过络合反应形成,于1956年在费城的工业毒理学实验室发现,是碘伏的一种。因其具备高效、广谱、应用范围广、杀菌速度快、刺激性小、成本低等优点,临床上广泛应用于外科手术前皮肤和黏膜的消毒,上世纪80年代开始应用于白内障术前消毒。
PVP是水溶性高分子表面活性剂,作为载体,本身无杀菌作用,碘以络合物的形式位于表面活性剂所形成的胶粒束中央被运载。在水溶液中,PVP-I是亲水性的,对细胞膜具有亲和作用,渗透性强,可以快速穿过细胞壁到达细胞膜和细胞质,不断释放出络合的碘与细菌的细胞膜和细胞质结合,利用游离碘的强氧化性,氧化膜蛋白和细胞质中的酶系统、蛋白质、肽类、巯基化合物、脂质和核酸等生物生存所必需的分子,使其结构改变,功能丧失,影响细菌脂质、蛋白质的合成和遗传信息的传递,从而发挥杀菌的作用[5]。PVP-I还具有乳化作用,能破坏细胞壁、使细胞膜通透性增高,提高PVP-I进入细胞的速度,进一步从络合物中释放游离碘,氧化膜蛋白并取代细胞内容物,直到可用碘耗尽。
二、PVP-I的毒性反应
由于PVP-I的非选择性作用机制[4],其也作用于正常细胞的膜蛋白,使用不当会对眼组织造成损伤,尽管毒性较低,但需引起重视。
1.PVP-I对角膜上皮的毒性PVP-I对角膜上皮的毒性已得到证实,毒性随PVP-I的浓度和暴露时间的增加而加剧[6]。Su等[7]把三组家兔使用5%的PVP-I消毒1次,每组暴露时间分别为1、3、10 min,7 d后检查角膜,扫描电镜观察到家兔的角膜上皮细胞的微绒毛都受到了损伤,暴露时间越长,微绒毛数量减少的幅度越大,裂隙灯下观察到角膜上皮的缺损范围也随暴露时长增加而增大(图1)。Ridder等[8]报告,单次使用5%的PVP-I会导致角膜染色在24小时内增加,可降低主观视觉舒适性,降低视力和对比敏感度,持续时间长达60 min。
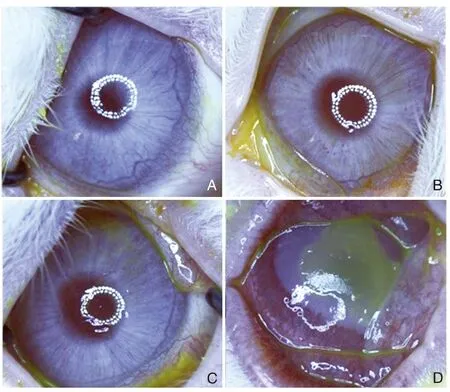
图1 第7天4组的荧光素染色的代表性图像[7]。a:对照组,角膜上皮未缺损;b:暴露时间1 min,角膜上皮轻微点状缺损;c:暴露时间3 min,角膜小块状上皮缺损;d:暴露时间10 min,角膜大片上皮缺损
2.VP-I对角膜基质的毒性 有学者发现PVP-I中的游离碘可以渗入甚至穿透角膜,浸润深度取决于暴露时间和浓度。在角膜使用浓度超过5%的PVP-I后发现从上皮到基质中有碘存在。然而,在施加0.5%~5%的浓度两分钟时,在角膜基质中没有发现碘。PVP-I对体外培养的角膜基质成纤维细胞有毒性,浓度仅0.25%的PVP-I作用2分钟即可对角膜基质成纤维细胞造成明显损伤。SuChou等[9]研究发现,0.1%或更高的PVP-I会导致角膜基质成纤维细胞死亡。
3.PVP-I对角膜内皮的毒性 在对家兔的研究中,国外学者使用5%的PVP-I直接注入前房,产生0.8%的房内浓度,兔内皮细胞受到损伤,但房内浓度分别为0.1%和0.08%时,没有发现内皮细胞损伤的证据。Elkitkat等[10]发现0.25%的PVP-I对兔角膜内皮细胞有毒性作用,第7天时细胞再生迹象明显,第14天内皮再生基本完成,但兔角膜内皮的再生和有丝分裂能力与人不同,对人角膜内皮细胞的毒性和恢复能力还需进一步研究。Shimada等[11]在白内障手术中用0.25%的PVP-I反复冲洗术野,术后第7天测得的角膜内皮细胞密度与对照组没有显著差异,内皮无损伤。年龄相关性白内障是最为常见的白内障类型,中老年人角膜内皮细胞比年轻人少,我们应尽量选择低浓度的PVP-I。术前用于结膜囊消毒的PVP-I因冲洗不充分可能在手术过程中进入前房,建议在使用高浓度PVP-I冲洗结膜囊后使用足量盐水冲洗。
4.PVP-I对结膜上皮的毒性 Su等[7]的一项研究表明,随着5%的PVP-I作用时间的增加,结膜杯状细胞密度降低,计数减少,单层上皮细胞变得更加普遍,并且在结膜上皮细胞中明显出现凋亡形态学变化,包括核分裂、染色质浓缩和周边迁移。他们注意到暴露时间依赖性的眼表病理生理变化与干眼综合征相似,其中包括杯状细胞密度降低、结膜上皮细胞大小增加、结膜鳞状化生等,但不能确定PVP-I的毒性是否会引起慢性损伤,因此需要进一步的临床研究来阐明PVP-I与眼表毒性的关系。
5.PVP-I对泪膜稳定性的影响 泪膜由外向内分为三层:脂质层、水液层、黏蛋白层。黏蛋白层能润滑眼和眼睑表面,将疏水性角膜上皮转化为亲水性,在泪膜与角膜表面的微绒毛粘附和稳定中起着重要作用。免疫荧光染色证实MUC5AC是结膜杯状细胞分泌的和角膜前泪膜主要的黏蛋白。许多研究人员已报道干眼症患者眼表黏蛋白表达减少,包括杯状细胞分泌的MUC5AC。Su等[7]研究发现PVP-I可使MUC5AC的产生减少,PVP-I引起的黏蛋白分泌减少干扰了泪膜最内层黏蛋白层的形成,即使在泪腺功能正常的情况下,也会导致泪液减少,泪膜稳定性下降,致使一部分患者术后出现干涩感和异物感。
6.PVP-I对视网膜的毒性 兔模型中,使用0.1%和0.3%的PVP-I玻璃体腔注射0.1 ml后发现视网膜电图和视网膜组织学检查未见明显异常[12]。另一使用兔模型的研究人员发现,0.05%-0.5%的PVP-I玻璃体腔注射后对眼底无明确毒性作用,5%的PVP-I被证明可导致严重的视网膜损伤[13]。一项评估PVP-I对视网膜影响的研究[14]得到了类似的结论,实验将 0.1 ml的 0.5%、1%、2% 和 5% PVP-I注射到兔眼中。在注射后 1、7 和 14 d记录视网膜电图并测量 b 波/a 波比。与盐水注射组相比,在0.5%、1% 和 2% 组没有观察到显着差异。注射后15 d进行病理检查,以视盘为中心垂直切片观察视网膜全周,在注射 5% PVP-I的组中,6 只眼睛都有广泛的炎症细胞浸润,有 5 只眼睛出现视网膜脱离。在 2% PVP-I作用下,6只眼睛中有2只出现视网膜变性和炎症细胞浸润。在浓度为 1% 时,6只眼睛中只有1只有局部炎症细胞浸润。浓度为 0.5% 时,未检测到视网膜异常。人体中,在玻璃体切割术中用0.025%的 PVP-I冲洗在术后未发现视网膜有明显异常[15]。
三、PVP-I在白内障手术中的应用
1.眼周消毒 眼周消毒用浸泡在5%或10%的PVP-I中的棉球消毒睫毛根部和睑缘,然后以眼裂为中心,由内到外向四周扩撒。上方达发际、内侧过鼻中线,下方到达上唇平面,外侧到耳根部,消毒区域呈四方形,重复1~2次。应避免消毒剂在眼睑内扩散,因为 5% 和 10% 的PVP-I会导致角膜损伤。消毒后需要2到3分钟的作用时间才能达到足够的杀菌效果,消毒后眼眶周围区域被5%或10%的PVP-I染成黄色,也方便识别术眼[16]。Wu等[17]强调使用未稀释的10%的PVP-I是进行皮肤消毒的关键一步,他们指出,与10%的PVP-I相比,用5%的PVP-I进行皮肤消毒会增加眼内炎的风险。
2.结膜囊冲洗 白内障术前使用PVP-I进行结膜囊冲洗已经得到眼科界的广泛认可,但目前用于结膜囊冲洗的PVP-I浓度和暴露时间缺乏共识和循证医学证据,不同国家、不同地区、不同医院使用的PVP-I浓度有所差异。美国眼科学会(AAO)指南建议白内障术前结膜囊内使用5%的PVP-I,该指南警告不要使用更低浓度的PVP-I,但没有推荐具体的使用剂量和作用时间。欧洲白内障及屈光手术医师协会(ESCRS)指南建议白内障术前应用5%~10%的PVP-I持续至少3分钟。《我国白内障摘除手术后感染性眼内炎防治专家共识(2017年)》的讨论专家一致认为PVP-I结膜囊消毒是有效的白内障围术期预防感染的手段,建议使用1%~5%的PVP-I进行结膜囊消毒。现今的指南都建议使用浓度>1%的PVP-I,尽管观察到高浓度PVP-I的毒性,也多年没有做出改变。
PVP-I对病原体没有选择性[4],游离碘的强氧化作用会损伤眼组织,损伤呈浓度和时间依赖性。我们希望在保证结膜囊消毒效果的同时,尽可能的降低浓度或暴露时间,但适当的暴露时间是必不可少的。研究[16]表明,碘在稀释的溶液中解离度更高,稀释的PVP-I比高浓度的PVP-I起效更快,杀菌效果更好,0.1%的PVP-I中碘解离度最高,杀菌效果最好(图2)。而PVP-I浓度较高时,游离碘的含量较少,需要更长的暴露时间。Sauerbrei等[18]研究发现,PVP-I的浓度在0.008%~0.9%的浓度范围内显示出最合适的杀菌活性,PVP-I浓度从1%增加到10%会导致暴露时间延长,降低浓度则其杀菌活性也会下降。
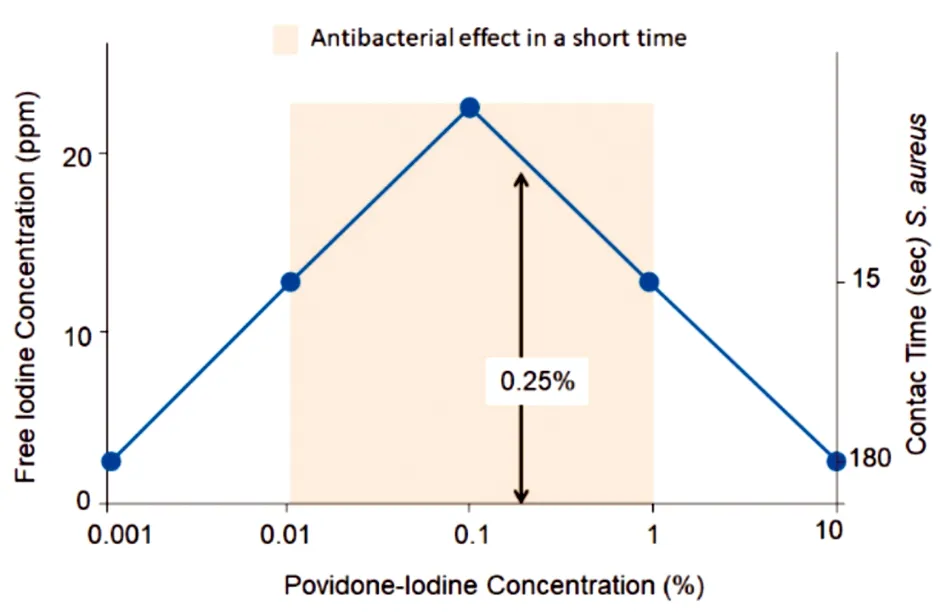
图2 聚维酮碘浓度、有效碘浓度和达到杀菌效果所需的暴露时间[16]。0.1%聚维酮碘的游离碘浓度为24 ppm,杀菌效果最好
由于碘在与细菌和有机物反应时被灭活,因此需要补充游离碘。当PVP-I浓度较高时,可以很容易地从周围充足的供应中补充游离碘,发挥作用的时间更长。然而,在低浓度的PVP-I中,可利用的碘量很少,杀菌效果不持久,必须反复使用才能保持效果[16]。手术过程中,结膜和眼睑的细菌可能通过切口进入眼内并引起感染[2],所以在术中使用低浓度的PVP-I多次冲洗可能是替代术前使用高浓度PVP-I进行一次结膜囊冲洗的方法,低浓度PVP-I有较高的杀菌活性,多次冲洗可以有效补充可利用碘,近些年已有许多对该方法的研究。Silas等[19]研究表明,1.0%的PVP-I应用3次,每次30 s,间隔2 min,与5.0%的PVP-I应用1次,在体外降低细菌数大致相同。Matsuura等[20]在术中使用0.33%的PVP-I冲洗眼表2次,分别在制作切口前和人工晶状体植入前,该研究认为及时的使用PVP-I冲洗可作为白内障手术中简单有效的辅助消毒步骤。Shimada等[11]提出在白内障手术中,应在手术开始、植入人工晶状体前和手术结束时彻底冲洗手术区域,并提出了Shimada技术(图3),该技术指在白内障手术期间每隔20~30 s用0.25%的PVP-I冲洗眼表,而不是用盐水冲洗[21]。Shimada等[11-22]评估了在日本白内障手术期间重复进行0.25%的PVP-I术前和术中表面冲洗后前房污染率,研究的实验组202只眼的前房污染率为0%。其团队又研究了在用0.025%的PVP-I冲洗眼表的同时进行白内障手术的有效性,也在100只眼中实现了0%的前房污染率。在这两项研究中,与平衡盐溶液冲洗对照组相比,使用稀释的PVP-I在术中多次冲洗眼表可以显著降低前房污染。PVP-I即使稀释到0.025%的低浓度,在术中多次冲洗也能有效减少前房的细菌污染。综上所述,低浓度PVP-I多次冲洗是一种简单、低成本的措施,有望成为预防眼内炎的一种方法[16],值得进一步研究和推广。
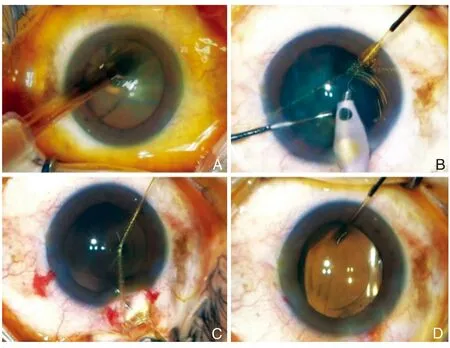
图3 在白内障手术期间用 0.25% 聚维酮碘冲洗眼表而不是用生理盐水(Shimada技术)[16]。A:放置开睑器后用 0.25% 聚维酮碘冲洗眼表;B:在冲洗角膜时,确保 0.25% 的聚维酮碘在结膜囊中积聚;C:由于 0.25% 聚维酮碘在 15 s 内即可显示出杀菌作用,因此在手术过程中每 20~30 s 冲洗1次;尤其在推注人工晶状体之前进行冲洗;D:在手术结束时也进行冲洗
我们知道,白内障手术后干眼症状的发生率和严重程度可能会增加。白内障手术要取得最佳效果,眼表健康状况非常重要。对于已经因糖尿病或干眼症导致角膜上皮细胞损伤的患者,应特别注意,尽量使用低浓度的PVP-I进行结膜囊的冲洗,避免术后干眼加重。Fan等[23]认为0.025-0.1%的PVP-I可用于因糖尿病或干眼症导致角膜上皮损伤的患者的眼表冲洗。他们发现应用0.05% PVP-I冲洗结膜囊30 s可有效减少结膜囊内细菌,可安全用于白内障术前结膜囊的消毒,同时还能减少眼表损伤,有利于眼表功能的恢复。最后应指出,对于PVP-I过敏的患者,可在皮肤上使用洗必泰,眼部使用PVP-I,或皮肤和眼睛上都使用洗必泰,但与使用PVP-I消毒相比,使用洗必泰消毒可能会增加患眼内炎的风险[24]。
四、展望
PVP-I的应用标准和毒性仍有待大量的研究,目前没有关于白内障手术期间用PVP-I反复冲洗眼表的术后眼内炎发生率的报道,还需进一步观察此方法预防术后眼内炎的效果,通过大样本的随机对照试验来评估最佳浓度和使用频率。
PVP-I目前已制成浓度为0.66%的滴眼液(IODIM®, Medivis),有研究[25]比较了以0.66%的PVP-I为基料的新配方与5%的PVP-I对不同细菌的体外杀菌效果。结果表明,0.66%稀释的制剂比5%的PVP-I制剂杀菌速度更快,能有效降低白内障手术患者眼表的总细菌载量[26],可能是目前白内障手术患者术前预防的一种有价值的抗菌辅助治疗,其在白内障手术中的应用有待进一步研究。
