细胞培养肉技术:研究进展与未来展望
2023-01-12关欣汪丹丹方佳华杨若青费卓成陈坚
关欣,汪丹丹,方佳华,杨若青,费卓成,陈坚*
(1 江南大学未来食品科学中心 江苏无锡214122 2 食品合成生物技术教育部工程研究中心 江苏无锡 214122)
1 细胞培养肉技术引领全球食品工业科技的革命浪潮
1931 年,英国前首相丘吉尔就曾憧憬:“在未来我们将摆脱为了吃鸡胸或鸡翅而饲养整只鸡”,近1 个世纪后,细胞培养肉技术诞生并迅速兴起,丘吉尔当初这个“狂野”的畅想成为现实[1]。如今,以细胞培养肉为代表的未来食品技术正在掀起一场食品工业科技的革命浪潮,同时推动全球蛋白质供应系统的颠覆性变革。
目前,全球主要发达国家和地区均将细胞培养肉列为重点研究方向并大力推进其产业化进程。2020 年,欧盟拨款270 万欧元启动Meat4all 项目进行细胞培养肉产业化技术研发,以色列创新局投资1 800 万美元支持“培养肉联盟”开展研究[2]。2021 年,美国塔夫茨大学创办细胞农业卓越中心并获得美国农业部1 000 万美元经费资助[3]。2022 年4 月,荷兰政府宣布投入6 000 万欧元资助细胞农业项目,这是至今为止全球在该领域最大的一笔公共基金[4]。在我国,2022 年3 月习总书记提出“大食物观”,随后国家发改委发布《“十四五”生物经济发展规划》,都强调了“发展生物技术,研发人造蛋白等新型食品”的重要意义[5]。国家和地方政府也提供了专项资金支持细胞培养肉的研发。中国工程院于2020 年和2022 年2 次立项开展细胞培养肉行业发展战略研究,2021 年国家科技部拨款2 000 余万元立项支持 “人造肉高效生物制造技术”重点研发项目,细胞培养肉是其中最主要的研究内容。此外,还有一些地方基金如上海高等研究院繁星科学基金,已连续2 年资助细胞培养肉研究项目,总经费超过4 000 万元。
在产业发展方面,目前全球培养肉相关初创企业超过100 家,融资总金额近6 亿美元,美国、荷兰、以色列的代表性企业均获得了上亿美元的融资。2021 年,已有两家细胞培养肉企业宣布建成细胞培养肉工厂,预估年产量超过40 万磅,已公布的最低成本约4 美元/100 g 培养鸡肉与植物蛋白混合产品,说明该领域头部企业已初步实现产业化。2022 年11 月,美国食品药品监督管理局(FDA)首次批准了细胞培养肉产品。美国将成为继新加坡之后又一允许销售细胞培养肉产品的国家。在我国,目前已有近10 家细胞培养肉初创企业成立,大多已获得千万元融资。2022 年3 月,我国联合新加坡、以色列等国的10 余家细胞培养肉企业,共同成立了“亚太细胞农业协会”,目的是通过提升与消费者的互动来普及培养肉的技术和影响力,也将与各界政府洽谈以促成培养肉在亚太地区的立法审批[6]。
同时,国内外已有一批大学和科研院所集中力量进行细胞培养肉创新研究,从细胞培养肉生产的各个环节开展基础理论和应用研究,不断提升其生产技术水平。本文以论文检索为基础,总结全球细胞培养肉领域主要研究机构和核心研究方向,并对生产关键技术的最新进展和面临的挑战进行分析,提出细胞培养肉未来重点攻关方向,以期为我国细胞培养肉技术发展提供借鉴。
2 细胞培养肉领域论文产出分析
在Web of science(WOS)数据库中以“TS=(cell -based meat * OR culture -meat * OR clean-meat * OR cell-meat * OR cultivatedmeat * OR cellular-meat * OR cultured-meat *OR cell-cultured-meat * OR in-vitro-meat)为关键词搜索到996 篇细胞培养肉相关领域的论文。图1 为近年来细胞培养肉文章发表情况,可以看出,近年来细胞培养肉相关文章发表日益增多,产业发展非常迅速,尤其近5 年,论文发表速度以每年50%左右的速度增长。从2017 年到现在,论文发表量增加约9 倍。细胞培养肉涉及多个研究领域,如图2 所示,主要涉及食品科学与技术,细胞农业,生物化学和分子生物学,营养饮食,环境学和生态学等领域。其中,细胞培养肉在食品科学和细胞农业领域发展迅速,相关研究占总研究论文比例分别约为29%和14.5%。在这两个领域,主要利用现代细胞生物学技术从动、植物中提取细胞并在体外进行培养,生产出所需农业产品和食品,后期利用食品加工工艺,使其生物构成、营养成分等品质与从动、植物本体上获得的产品类似。此外,还有一些论文进行细胞培养肉的可行性分析,包括细胞培养肉的环境生态影响、经济效益分析、消费者心理接受度等。可见,随着细胞培养肉技术的飞速发展,它带动了细胞农业、食品科学、营养饮食等热门研究领域的发展。

图1 细胞培养肉论文发表情况Fig.1 Publication of articles on cultured meat
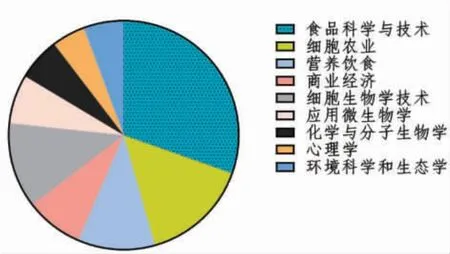
图2 细胞培养肉论文涉及的研究领域Fig.2 Research fields of cultured meat articles
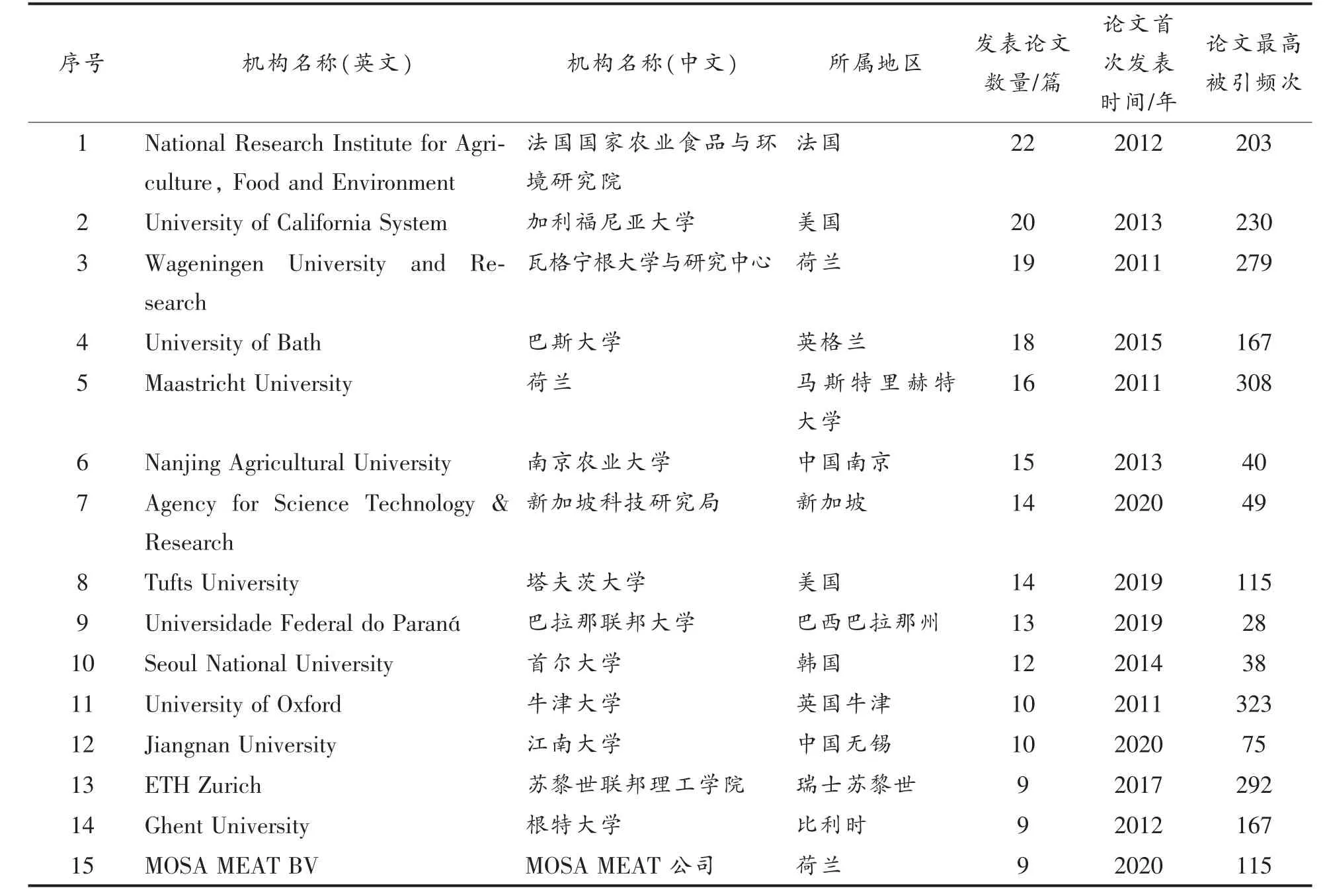
表1 从事细胞培养肉研究的国内外研究机构Table 1 Research institutions engaged in cultured meat research
3 细胞培养肉技术研究进展
3.1 种子细胞的分离提取
3.1.1 肌肉干细胞 肌肉干细胞(Muscle stem cells,MSCs)是一种具有自我更新能力和肌源性分化特性的细胞,也是制备细胞培养肉的主要种子细胞类型之一。在细胞培养肉的生产过程中,首先需要将肌肉干细胞从肌肉组织中分离出来,随后在体外进行细胞的大量增殖、诱导成肌分化,产生成熟的肌纤维,再经食品化加工过程制备出细胞培养肉。
肌肉干细胞可以通过酶消化法、组织块法、单根肌纤维法等方法获得[7-8],其中,酶消化法是目前最常用的肌肉干细胞提取方法。从动物体内获得新鲜的肌肉组织后,先通过物理破碎的方法使肌肉组织变为肉糜,再用蛋白酶消化使肌肉组织解离并释放细胞(图3),因此蛋白酶种类的选择和消化工艺条件的优化对肌肉干细胞的提取数量及活性至关重要。Choi 等[9]总结了多个物种肌肉组织消化所使用的蛋白酶,结果显示多种蛋白酶虽都具有消化肌肉组织的能力,如不同类型的胶原酶(Collagenase)、链霉蛋白酶(Pronase)、分散酶(Dispase)和胰酶(Trypsin)等,但消化效力显著不同且具有种间差异。睢梦华等[10]使用I 型胶原酶、胰蛋白酶,两步法消化山羊胎儿背长肌组织,获得了山羊胎儿肌肉干细胞;江南大学研究团队根据蛋白酶的作用机理系统设置了多种酶组合并进行研究[11],发现链霉蛋白酶(Pronase)与分散酶Ⅱ(Dispase Ⅱ)的全新酶组合能够高效消化猪肌肉组织,获得的细胞数量是现有报道的最高水平。

图3 肌肉干细胞分离纯化流程示意图Fig.3 Work flow of isolating and purifying muscle stem cells
使用酶消化法获得的肌肉干细胞通常混有其它种类细胞,如成纤维细胞、内皮细胞等,因此需要对获得的细胞悬液进行纯化。流式细胞分选是一种经典的细胞纯化方法,分选后的细胞几乎100%表达肌肉干细胞特定标志物Pax7,纯度极高[12]。然而,流式分选所需仪器及试剂价格昂贵且单次分选规模小、时间长,并不适合工业化的细胞培养肉生产。Benedetti 等[13]利用肌肉干细胞黏附性低的特性,将混合细胞置于冰上30 min,使肌肉干细胞脱落至上清中并转移上清重新培养,进而实现了低成本纯化肌肉干细胞。江南大学研究团队[11]探索了不同初始纯度对猪肌肉干细胞体外增殖和肌管形成能力的影响,并通过优化差速贴壁法建立高效、低成本的肌肉干细胞纯化方法,每克肌肉组织可以获得2.1×106个肌肉干细胞,适用于细胞培养肉工艺化生产。
3.1.2 间充质干细胞 间充质干细胞(Mesenchymal stem cells,MSCs)是一种基质细胞,具有自我更新和多向分化潜能。它可以从骨髓、脂肪和脐带中分离得到,并根据细胞来源被分为脂肪间充质干细胞(Adipose mesenchymal stem cells,AMSCs)、骨髓间充质干细胞(Bone marrow mesenchymal stem cells,BMSCs)和脐带间充质干细胞(Umbilical cord mesenchymal stem cells,UMSCs)。在体外培养过程中,间充质干细胞经诱导能够分化为软骨细胞、成骨细胞、成肌细胞和脂肪细胞等中胚层来源细胞,是一种优质的细胞培养肉种子细胞[14]。不同组织部位来源的间充质干细胞的分离方法也有所不同(图4)。骨髓间充质干细胞通常通过直接抽取骨髓液,再经密度梯度离心等纯化方法获得[15-16]。脐带间充质干细胞则通常使用酶消化法与组织块贴壁法进行分离。刘亭等[17]将人脐带切为1 mm2大小的组织块,贴壁培养7d后组织块周围长出梭形细胞,经鉴定成功获得了脐带间充质干细胞;许韧等[18]利用胶原酶、透明质酸酶和氯化钙溶液消化处理新生儿脐带,2 cm 的脐带可分离得到约4.2×105个间充质干细胞。

图4 间充质干细胞分离流程示意图Fig.4 Work flow of isolation of mesenchymal stem cells
脂肪间充质干细胞可从来源更为广泛、易得的脂肪组织中分离获得,是一种理想的培养肉种子细胞。其分离方法主要为酶消化法。张雅群等[19]采用I 型胶原酶和胰蛋白酶联合消化分离得到大鼠脂肪间充质干细胞,每mL 获得1.34×105个细胞;Yao 等[20]对脂肪组织使用机械力进行反复破碎,以10 mL/s 流速在两个10 mL 规格的注射器之间来回机械处理脂肪组织1 min,待脂肪组织呈乳状物后再使用胶原酶消化,每毫升脂肪组织可得到约9.9×104个细胞。
3.2 高效无血清培养基研制
3.2.1 干细胞增殖及功能调控化合物 培养基是细胞在体外培养一切营养物质的来源,高效、低成本培养基的研制是细胞培养肉工业化生产的先决条件。由于体、内外环境的巨大差异,通常情况下动物干细胞的体外增殖能力有限,且分化能力也会随体外培养时间的增加而大幅下降。因此,首先需要对各类型干细胞分裂增殖、成肌/成脂分化过程的关键调控因子以及相关信号通路进行解析,找到有效促进细胞增殖、特性维持、功能调控的化合物,这些化合物并非完全来自基础培养基或胎牛血清,可以利用高通量筛选的方法从天然活性化合物库、小分子化合物库中筛选得到。
目前,对于肌肉干细胞已有相关研究,多个研究团队报道了具有促进细胞增殖作用的化合物(表2)。Lei 等[21]得到促进猪肌肉干细胞体外长期增殖的细胞因子组合,可减少50%的胎牛血清使用量。Fang 等[22]使用价格低廉的食品级小分子化合物维生素C 促进猪肌肉干细胞体外增殖及成肌分化。Liu 等[23]利用小分子激活剂YAP 实现了高密度培养,减少了培养基的使用。Leng 等[24]通过体外添加花生四烯酸,促进了牛肌肉干细胞的增殖和成肌。

表2 肌肉干细胞增殖及功能调控化合物Table 2 Compounds that promote the proliferation of muscle stem cells
3.2.2 血清替代化合物 胎牛血清中含有丰富的细胞生长必需营养成分,对动物细胞,特别是干细胞体外存活和生长具有重要作用。然而,在细胞培养肉的生产过程中,使用胎牛血清不仅使得培养基成本大幅提高,并且违背了细胞培养肉避免动物屠宰的初衷,因此需对胎牛血清成分进行研究,建立化学成分的血清替代物成分库。目前已有多种组分可作为血清替代物,主要包括能源物质、激素、生长因子、蛋白质、蛋白水解物、氨基酸、维生素、微量元素、脂类、抗剪切保护剂等,详见表3。

表3 常见的血清替代物Table 3 Common serum substitutes
3.2.3 干细胞无血清培养基 在获得一系列促进干细胞增殖以及具有血清替代作用的化合物后,需针对特定的细胞类型,基于统计学方法进行多种化合物的复配研究,确定有效组合后再通过响应面分析等手段优化各化合物的使用浓度,最终开发出细胞类型特异性的无血清完全培养基。目前,已有研究团队成功研发出肌肉干细胞的无血清培养基用于细胞增殖或分化诱导,并发表相关论文或专利(表4)。

表4 肌肉干细胞无血清培养基研究总结Table 4 Summary of serum-free medium for muscle stem cells
3.3 大规模细胞培养体系
3.3.1 微载体材料及制备 随着种子细胞分离提取方法的改善,低成本细胞培养基的开发,细胞培养肉种子细胞的大规模培养将成为产业化核心技术之一。首先,因细胞培养肉的种子细胞多为贴壁细胞,故需要借助微载体进行培养,于反应器中进行大规模培养。微载体是一种固体细胞生长支持基质,通常为直径在微米级别的球体,球体表面或内部能使细胞贴附,主要用于生物反应器系统中贴壁细胞的生长[31]。与单层细胞培养相比,球体拥有更大的表面积与体积比,因此使用微载体可大幅提高细胞培养的密度。目前,已有多种类型的培养动物细胞,即哺乳动物、鸟类、鱼类和昆虫细胞通过微载体技术成功培养[32-34]。
制备微载体的生物材料大致可分为不可降解、可降解但不可食用、可食用3 种类型。早期微载体一般基于聚乳酸-羟基乙酸、聚羟乙基甲基丙烯酸酯、丙烯酰胺、聚苯乙烯和聚氨酯聚合物组成[35]。然而,这些高分子聚合物通常不可降解,也不可食用,在培养肉应用方面受到较大的限制,因此可食用微载体的研制对细胞培养肉具有重要意义。Park 等[36]以鱼明胶为材料,制备出具备输送营养物质能力的可食用微载体,成功使小鼠肌肉干细胞贴壁、增殖和分化,并培养出高细胞密度的肌肉干细胞片层,最终通过物理叠加和食品后加工的方式生产出细胞培养肉产品。Norris 等[37]使用油包水乳液作为明胶微粒子的模板,研制出具有凹槽拓扑结构、可伸缩性的可食用微载体,并利用该微载体培养C2C12 成肌细胞和牛肌肉卫星细胞,细胞成功增殖和分化产生肌肉微组织。随后,通过离心收集携带细胞的微载体制作成可烹调的肉饼,该肉饼在烹饪过程中形状得到较好地维持并能够正常褐变。
3.3.2 反应器放大工艺 随着细胞培养肉技术在实验室水平研究的逐步成熟,如何建立规模化技术体系成为细胞培养肉产业化的关键问题。在动物细胞大规模培养中,生物反应器是不可或缺的关键设备。生物反应器可以提供一个类似于体内环境的三维空间,并搭配探针或传感器能够自动检测内部环境并实时动态调整,从而实现大规模、高密度的动物细胞培养,提高细胞培养肉的产量。目前常用的生物反应器类型有搅拌式生物反应器、波浪式生物反应器及气升式生物反应器。其中,搅拌式生物反应器在生物行业内广泛应用,其优点在于应用工艺较为成熟,罐内传氧与传质较好,缺点是剪切力较大,可能会对细胞造成一定损伤[38]。此外,WAVE 波浪生物反应器也是细胞培养良好的设备,其采用非介入的波浪式摇动混合,避免了搅拌浆叶端和鼓泡对细胞的伤害,提供温和低剪切力、高溶氧的细胞培养微环境,然而,其需要配套价格较高的一次性反应袋,且培养规模通常限制在200 L 以内[39]。气升式生物反应器适用于较大规模的细胞培养,其液体湍动温和而均匀,剪切力相当小,对细胞的损伤较小,氧的传递效率高,然而,其在高密度培养时混合不够均匀[40]。可见,需要以细胞培养肉生产为目的进行生物反应器装备的选择、改良,以及控制参数的优化。
细胞大规模培养工艺的研发和建立需经历小试、中试、放大等过程,各个环节所使用的生物反应器类型和规模各不相同。生物反应器内部存在复杂的气、液两相或气、液、固3 相的流动、传递及反应过程,因此生物反应器的放大涉及生物特征、反应动力学、流体力学、传质传热、自动控制等跨学科复杂原理,研究过程十分复杂。通常基于小试及中试的试验数据,综合CFD 建模与仿真、大数据共享与分析、智能算法等技术手段,根据参数以及生物反应器和细胞系特性进行理性工艺放大。此外,通常将工艺控制系统设计成模块化形式,包含设备模型(Physical Model)和过程顺序控制模型(Procedural Model)。通过罐温控制模块、罐压控制模块、pH 控制模块、DO 溶氧控制模块、搅拌器控制模块等多种模块的自动化调节,可实现生物反应器内部环境的实时稳态,维持细胞的良好生长状态。Udomsom 等[41]开发了一种带有控制程序的可编程生物反应器和实时pH 监测的新型pH传感器,允许其每个组件自动操作,并利用该生物反应器实现了小鼠成纤维细胞的自动化培养,与常规细胞培养方法相比,细胞的增殖能力增强。
3.4 三维培养及组织塑形
三维塑形作为培养肉产品生产最重要的环节,是将大规模扩增得到的细胞接种于细胞支架上进行三维培养,使细胞分化形成细胞培养肉产品的过程。目前已有多种三维细胞培养及组织塑形技术可用于培养肉产品制备,包括固体支架或模具、3D 生物打印、静电纺丝和片层堆叠技术等(图5)。
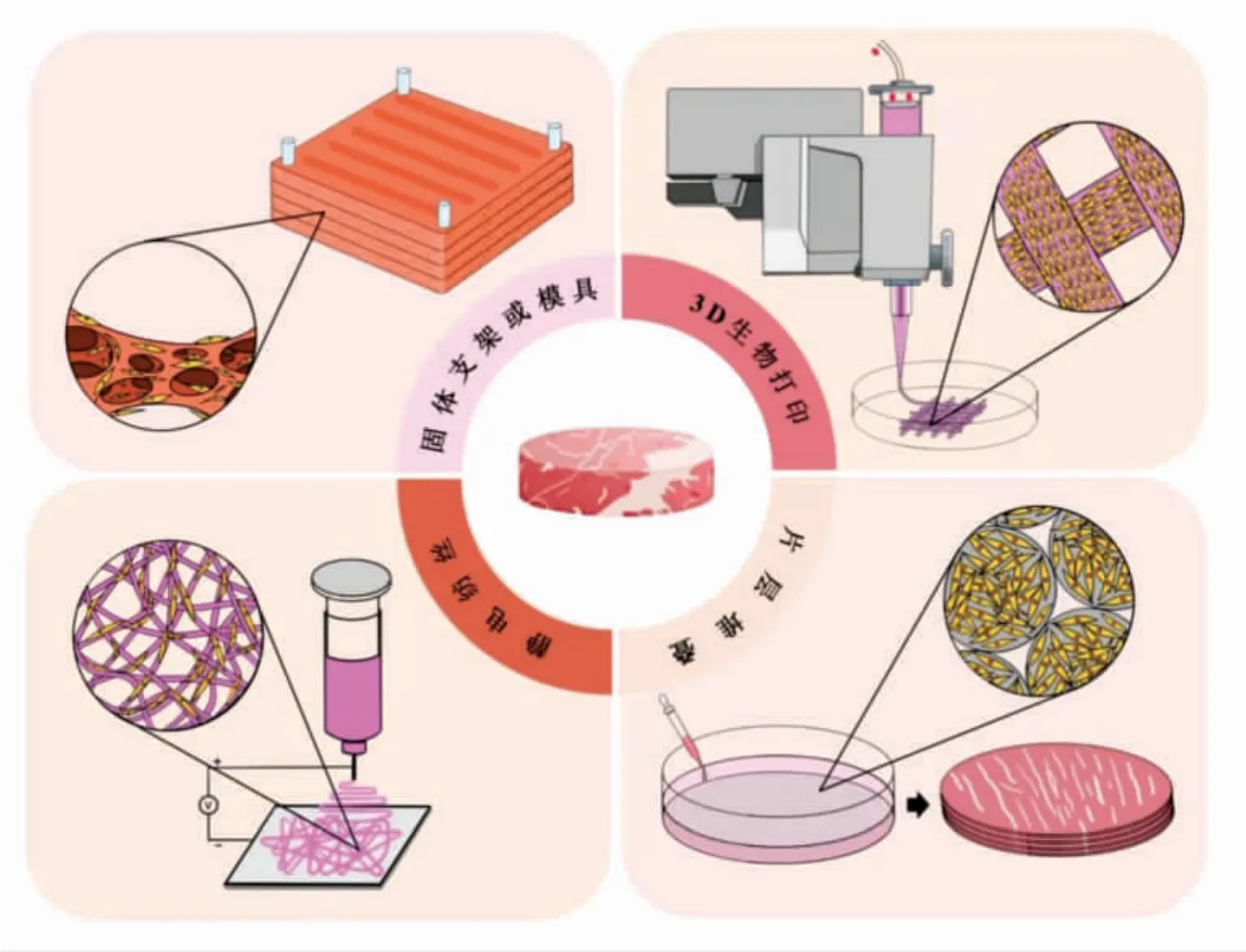
图5 培养肉三维塑形方式Fig.5 3D molding of cultured meat
3.4.1 固体支架或模具 固体支架或模具塑形及培养技术是将细胞接种于固体支架或模具中并进行三维培养,使细胞增殖分化进而形成肌纤维、脂肪等组织,再经加工获得块状细胞培养肉[42]。水凝胶由具有高细胞相容性的聚合物通过物理或化学方法进行交联制得,因其结构接近细胞外基质(Extracellular matrix,ECM),故可渗透细胞生长所需的营养素,是影响细胞三维培养过程的核心因素[43]。Zhu 等[44]设计了一种用于细胞培养肉生产的模具,并将猪肌肉干细胞与胶原蛋白水凝胶混合注入模具中塑形,经诱导分化培养获得网状猪肌肉组织。然而,水凝胶存在易降解且机械性能不足的缺陷,与之相比,植物蛋白支架具有稳定的海绵状结构,可为接种细胞的生长和分化提供所需的机械稳定性[45]。Ben-Arye 等[46]利用组织化植物蛋白(Textured vegetable protein,TVP)作为细胞支架进行成肌细胞的三维培养,研究表明TVP 支架具有支持细胞生长和细胞外基质沉积的作用,并促进肌肉组织的形成。
3.4.2 3D 生物打印 3D 生物打印塑形是利用3D 生物打印机的挤压式打印模式,将含细胞和非细胞成分的生物墨水构建为复杂组织,并经过长时间培养形成培养肉的塑形方式。打印产品的性能取决于生物墨水的生化特性、流变性等材料属性,生物墨水取材常为可食用的多糖或蛋白质组成的聚合物,比如胶原蛋白、明胶、丝素蛋白、纤连蛋白、角蛋白等[47],均具有良好的生物相容性。该类材料通常也具备合适的打印特性,即挤出性、细丝保真度和溶胶-凝胶转变性[48]。3D 生物打印塑形的优势在于可以调节样品形状和孔隙大小,精确地定位并分配细胞和非细胞成分[49],且允许多种生物墨水材料同时打印[50]。近年来,将3D 生物打印塑形应用于细胞培养肉塑形的案例层出不穷,如Kim 等[51]以纤维蛋白原、明胶、透明质酸和聚己内酯为生物墨水材料,与牛卫星细胞混合并通过3D 打印构建出牛骨骼肌组织;Oliveira 等[52]以结冷胶和乳清分离蛋白为生物墨水材料,与肌肉干细胞混合并通过3D 打印构建出可食用的培养肉产品。
3.4.3 静电纺丝 静电纺丝技术是利用静电作用力将明胶等高聚物溶液以一定流速挤出注射器针头形成微纳米级超细纤维,随后将细胞接种于超细纤维间隙并诱导分化为组织的塑形方式[53]。该超细纤维可支持细胞的黏附并为其提供氧气和营养素的输送间隙[54],且该纤维细丝排列一致,有助于促进肌肉纤维的形成。MacQueen 等[55]通过静电纺丝技术制备出明胶纤维细丝,并将兔成肌细胞和牛平滑肌细胞接种在明胶纤维细丝上,经长时间培养形成完整组织,并证明培养肉制品与真实肌肉具有类似的结构和机械特性。Apsite 等[56]以甲基丙烯酸海藻酸盐(AA-MA)和聚己内酯为纺丝原料制作出双层纤维支架,并成功接种骨骼肌细胞形成功能性肌肉组织。
3.4.4 片层堆叠 片层堆叠塑形技术是将细胞接种于微载体上,经增殖、诱导分化形成完整细胞片层,并通过多片层堆叠得到培养肉产品。该塑形方式节省了细胞消化步骤,无需去除用于细胞扩培的微载体,在细胞培养肉的工业化生产中具有明显优势。该方法使用的微载体需由可食用材料制成,如明胶、纤维素、交联葡聚糖、多聚半乳糖醛酸等[57],且表面覆盖胶原蛋白、纤连蛋白、层黏连蛋白等以促进细胞的黏附、增殖和分化[58]。首先将细胞接种于微载体上,培养形成具有高表面积/体积比的细胞片层,再将数十片细胞片层堆叠,形成整块细胞培养肉。Park 等[36]以明胶为原料,运用该塑形方式实现了培养肉的制备,并将培养肉产品与真实肉类进行比较,证明其质构特性与鸡胸肉相近。
4 细胞培养肉产业化面临的技术挑战
1)降低生产成本 因细胞培养肉的成本主要来自于培养基,故需从降低培养基的单位成本和减少培养基用量两方面着手攻关。在降低培养基单位成本方面,研制无血清培养基是首要环节;其次还需优化培养基组分及配比,以增强培养基的促增殖/分化效力,同时建立昂贵组分的微生物发酵法生产体系以降低成本。此外,需研发和建立高密度的细胞培养体系,减少培养基用量,这对降低培养肉的生产成本也起重要作用。
2)扩大生产规模 目前,虽然很多研究团队和企业都已实现小规模的细胞培养肉制备,但是工业规模的细胞培养肉生产仍具有挑战。随着生物反应器体积的不断扩大,为实现均匀混合将不断加大搅拌或通气速率,剪切力或气泡破裂导致的细胞损伤会更加严重,因此需要开发适用于细胞培养肉工业化生产的反应器装置并明确最佳的控制参数。此外,当细胞大量增殖后如何在反应器内创造一个适合细胞分化形成肌纤维/脂肪细胞的三维环境及营养传输方式也需进一步探讨。
3)提升风味品质 肉制品的风味取决于其中可溶性糖、游离氨基酸、游历脂肪酸以及挥发性风味物质的含量。从生理结构来看,真实肌肉组织含有肌肉细胞、脂肪细胞、成纤维细胞、血细胞等多种细胞类型,每种细胞都含有独特的化学成分,这些成分共同构成了肉的风味和营养品质。相比而言,大部分细胞培养肉产品由单种细胞和细胞支架、植物蛋白构成,组成和结构较为单一,呈味物质含量相对较少,因此尚需开发含有多种细胞类型的细胞培养肉产品,同时添加风味营养成分,从而提升细胞培养肉制品的风味品质。
5 细胞培养肉未来重点攻关方向
为进一步提高细胞培养肉生产效率,降低成本,提升产品风味与营养,推动细胞培养肉技术发展和产业化进程,未来细胞培养肉研究应聚焦以下4 个方面:
1)构建培养肉良种细胞资源库 选育畜、禽、水产动物优良品种,研发肌肉干细胞、间充质干细胞、成纤维细胞等多种细胞培养肉种子细胞的高效、低成本分离提取方法,探索安全、高效的细胞永生化技术;制定种子细胞鉴定和病原微生物检验标准,构建种类丰富、品质优良的种子细胞资源库,支撑细胞培养肉基础研究与应用。
2)深化组织发育机理基础研究 根据动物肌肉、脂肪等组织的胚胎及成体发育过程,从蛋白、非编码RNA、转录因子等多维度解析成肌/成脂命运决定因子;研究肌肉干细胞、间充质干细胞等的体内微环境的理化特性和细胞内、外信号传递过程,明确调控各类型细胞静息、激活、分裂等不同状态的分子机制,强化完善细胞培养肉基础科学理论。
3)建立无血清细胞培养技术体系 筛选及研究有效调控各类种子细胞增殖和分化的细胞因子、维生素、蛋白、活性肽、天然化合物等营养组分;分析细胞各发育阶段的营养偏好和代谢特点,构建促进种子细胞长期稳定增殖和支持肌纤维/脂肪高效产生的无血清培养技术体系,形成国际领先的细胞培养肉生产原创技术路线。
4)开发细胞培养肉智能制造系统及装备 研发细胞培养肉大规模生物反应器,借助计算流体力学、时空多尺度耦合仿真等技术建立生物过程多层级动态智能模型,实现细胞大规模培养的精准调控与理性放大;构建生物过程数字孪生系统,形成集成设计、仿真、管理的细胞培养肉制造过程全流程数字化技术平台,推进细胞培养肉的工业化发展。
