严重产后出血患者血小板输注的多变量预测模型*
2023-01-06姚丹丁虹娟余韦高明明俞兆儿贾瑞喆
姚丹 丁虹娟 余韦 高明明 俞兆儿 贾瑞喆
严重产后出血(postpartum hemorrhage,PPH)是指产妇24 h内持续失血>1 000 mL或伴有低血容量症状或体征[1-2],血小板具有重要的凝血功能,输注包括血小板在内的血液成分是抢救严重产后出血患者的重要手段。但血小板具有来源紧张、供给量少、保存困难等特点[3-4],各医院的血库非常规储备,需要时往往要到当地的中心血站临时调取,来回路途耗时长,给患者的抢救造成极大困难;然而产妇个体差异大,且血小板通常在脾脏有一些储备,因此如何能有预见性地提前准备血小板、掌握输注血小板的时机和量一直困扰着产科及输血科医生。虽然指南指出:急性出血时,血小板不能低于50×109/L;对于正在出血的患者,血小板低于75×109/L应输注血小板[5-6],但严重PPH时往往情况危急,很难适时把控此输注时机,所以探索可行的因严重PPH导致血小板严重降低的风险因素及血小板输注的多变量预测模型具有重要的临床意义。
本研究将回顾性分析严重PPH病例,通过分析严重PPH导致血小板严重降低的危险因素,建立血小板输注的多变量预测模型,从而能有预见性地提前准备血小板,并及时把控输注时机及剂量,为严重PPH时临床制定血小板输注方案提供依据。
资料与方法
1 一般资料 回顾分析2008年1月~2021年5月在南京医科大学附属妇产医院分娩的,发生严重PPH并成功救治的产妇,共计319例。严重PPH的诊断标准为2019年“产科患者血液管理NATA专家共识”[1]。排除标准:孕产妇合并原发性血液系统疾病、原发病凝血功能异常、肿瘤等疾病。本研究获得南京医科大学附属妇产医院伦理委员会批准(宁妇伦字[2021]KY-006)。
2 分组 严重PPH抢救过程中,如血小板计数<75×109/L,列入血小板严重降低[5-6],立即予以输注单采血小板1个治疗量。根据是否输注血小板,分为2组,血小板输注组(64人)及无血小板输注组(255人)。
3 方法 所有患者发生严重PPH时,均及时采取综合治疗措施,治疗方案按指南进行[1-2],包括:①支持治疗:吸氧、保暖、限制性晶体液复苏方案作为初始液体复苏策略;②针对产后出血的四大病因进行治疗;③及时手术止血:对于难治性产后出血,保守治疗无效,立即采取子宫动脉灌注栓塞术以及外科手术,必要时切除子宫;④输血治疗:根据血压、出血情况、血常规、血凝的检查结果,实施以目标为导向地输注红细胞悬液、血浆、血小板、冷沉淀及纤维蛋白原。
4 观察指标及预测因子
4.1 一般情况:记录产妇的年龄、身高、体重、体重指数(BMI)、分娩方式、妊娠合并症及并发症、抢救过程是否发生休克或弥散性血管内凝血(DIC)。
4.2 血细胞分析及凝血功能:分娩前的血细胞分析及凝血功能;自发生产后出血时,每2小时测一次血细胞分析及凝血功能至病情稳定;输血结束24 h左右复查血细胞分析及凝血功能。血细胞分析包括血红蛋白(Hb)、血小板计数(PLT)、红细胞比容(Hct),采用BC6800PLUS血细胞分析仪(深圳迈瑞生物医疗电子股份有限公司)检测。凝血功能包括:凝血酶原时间(PT)、国际标准化比值(INR)、活化部分凝血活酶时间(APTT)、纤维蛋白原(Fib)、D-二聚体(D-D)、抗凝血酶Ⅲ(ATⅢ)、纤维蛋白原降解产物(FDP),采用CS5100凝血分析仪(日本希森美康)检测。
4.3 出血及输血量:详细记录产妇产后的出血量、计算24 h出血量;大出血整个抢救过程中红细胞悬液、血浆、血小板的输注量,计算输注血小板前已输注红细胞悬液的总量。所有血液成分均来自南京市中心血站。
4.4 预测因子:年龄、BMI、分娩方式、妊娠合并症及并发症(包括:羊水栓塞、胎盘早剥、死胎、子痫前期、HELLP综合征、中重度肝功能异常(转氨酶升高≥3倍)、产后出血量、是否存在不易准确统计的隐性出血(包括腹腔内出血、腹壁下血肿、阴道壁血肿)、已输红细胞悬液的数量、分娩前的血小板计数。抢救期间的实验室指标具有延后性,未列入预测指标。
5 统计学处理 采用SPSS 26.0、GraphPad Prism 8.0及R 4.1.3对相关数据进行统计分析和作图。计量资料采用t检验,以表示;计数资料采用卡方检验或确切概率法,以n(%)表示。先应用单变量分析逐一比较预测因子,分类变量为使用卡方检验进行分析,连续变量分析采用独立样本t检验。多因素分析采用二元Logistic回归分析确定输注血小板的独立指标,应用R软件对输注血小板的独立指标建立诺莫图模型,即根据各个指标对输注血小板的影响权重赋分,并给出输注血小板的得分临界值。采用内部Bootstrap自测验证法对该模型进行内部验证,通过一致性指数(C指数)和校正曲线评价该模型的预测准确度和一致率,C-指数在0.5~0.7为准确度较低,0.7~0.9为准确度中等,高于0.9为高度准确。诺莫图模型的诊断效能通过绘制受试者工作特征曲线(receiver operation characteristic,ROC)并计算曲线下面积(area under curve,AUC)评估,并比较诺莫图模型与其他独立影响因素的诊断效能。P<0.05表示差异有统计学意义。
结 果
1 两组产妇分娩时一般情况、输血小板前的出血量、输血量及妊娠合并症比较 两组产妇的年龄、身高、体重、BMI、生理产/剖宫产人数,差异均无统计学意义。输血小板组的DIC的发生率、隐性出血、HELLP综合征、胎盘早剥的发生率明显高于未输血小板组;输血小板前的出血量、红细胞悬液、冷沉淀输注量明显高于未输血小板组;实验室指标:输血小板组分娩前PLT数量明显小于未输血小板组;输血小板前Hb明显降低,PT、APTT明显高于未输血小板组,差异具有统计学意义(P<0.05);两组间羊水栓塞、子痫前期、死胎、中重度肝功能异常的发生率及休克的发生率差异无统计学意义。(表中未输血小板组记录的出血量、输血量、实验室指标为严重PPH抢救期间的出血量、输血量及病情最严重时的实验室结果),见表1。
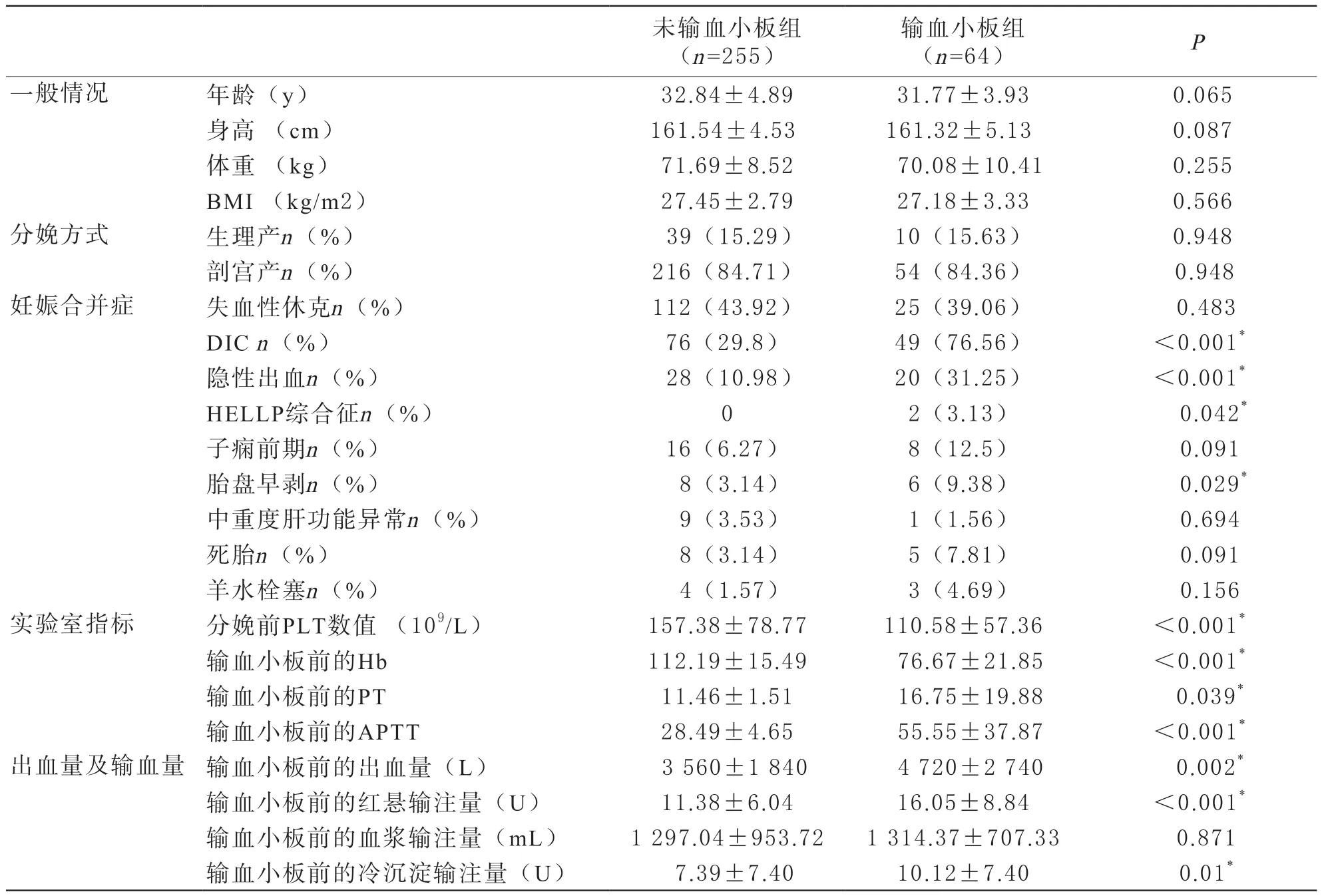
表1 产妇一般情况、妊娠合并症、输血小板前的出血量、输血量及实验室指标比较
2 引起血小板严重降低各原因的二元Logistic回归分析 将引起血小板严重降低(血小板计数<75×109/L)的各个原因作为自变量因素,进行二元Logistic回归分析(HELLP综合征人数太少,未列入分析),结果显示:输血小板前的出血量、输血小板前的红细胞悬液输注量、分娩前PLT数值、并发隐性出血、胎盘早剥、子痫前期、中重度肝功能异常为血小板严重降低的独立影响因素(P<0.1)。年龄、BMI、分娩方式、并发羊水栓塞、死胎对是否发生血小板严重降低无明显影响。(见图1)

图1 引起血小板严重降低各原因的二元logistics回归分析(*P<0.1)
2.1 应用诺莫图建立严重产后出血患者血小板输注的多变量预测模型:基于二元Logistics回归分析的结果,以及组合不同影响因素建立的模型对比的结果,应用R软件,我们最后将出血量、红悬输注量、分娩前PLT数值、隐性出血、子痫前期、胎盘早剥和中重度肝功能异常(P<0.1)纳入诺莫图分析,用于建立严重PPH患者血小板输注的多变量预测模型。诺莫图分析发现,并发症中,隐性出血及胎盘早剥的比重较大,其对于输血小板的影响更为重要(见图2)。根据诺莫图的结果,将各个因素划分等级来评分(见表2),方便临床计算总的评分。同时,由表3得知:以50%为割点,即患者的评分大于101分,意味着患者会输注血小板。经过内部Bootstrap自测验证法重复测量1 000次后进行的模型内部验证,该诺莫图模型的C指数为0.789>0.7,具有良好的预测准确度;校准曲线与平均曲线及理想曲线较为接近,平均误差为0.017,该模型对严重PPH输注血小板的预测具有良好的一致性和稳定性(见图3)。
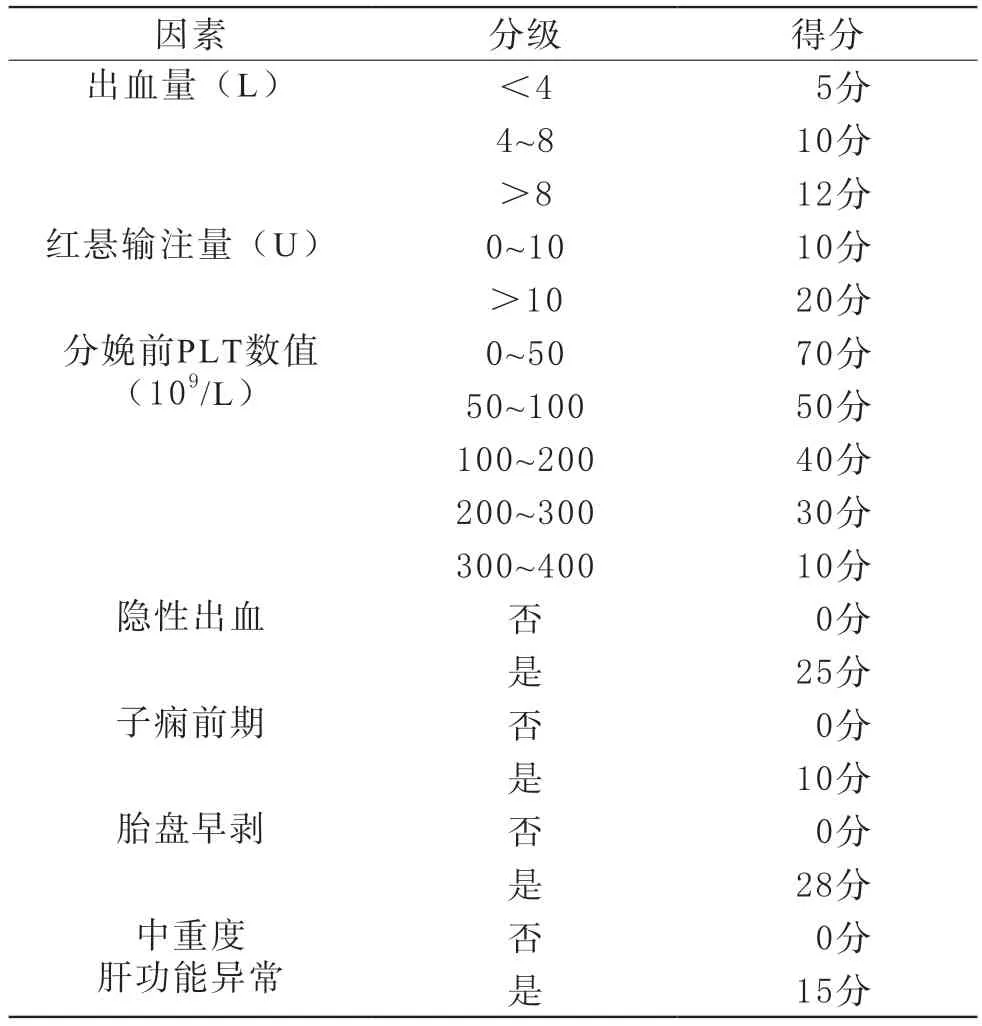
表2 各因素各级别评分

表3 总分与输注血小板发生率的对应情况

图2 应用诺莫图建立严重PPH患者血小板输注的多变量预测模型
2.2 ROC评估诺莫图预测严重产后出血患者输注血小板的预测效能:对诺莫图模型和各独立临床指标进行ROC曲线分析,研究结果现实诺莫图AUC值最高为0.789(95%CI为0.782~0.851)(见图4)。其他临床独立指标出血量、红细胞悬液输注量、分娩前PLT值、隐性出血、胎盘早剥、子痫前期、中重度肝功能异常的AUC分别为:0.631、0.689、0.518、0.611、0.641、0.531、0.529。

图4 诺莫图及各临床指标预测严重PPH患者血小板输注的ROC曲线
讨 论
血小板具有聚集、黏附、止血等功能,输注血小板一直是严重PPH并发血小板减少、血小板功能异常时止血的有效方式[7]。但血小板较其他血液成分来说具有来源紧张、供给量少、制备及保存困难等特点[3-4],各医院的血库常规不会储备血小板,往往是需要时到当地的中心血站临时调取,来回路途耗时长,给及时有效的输血抢救造成了极大困难。但庆幸的是并非每个严重PPH的患者都需要输注血小板,一个重要的原因是正常情况下约1/3数量的血小板储留于脾脏,未参与血液循环中,因此体内的血小板具有储备功能。根据指南建议[5-6],严重PPH时如血小板计数<75×109/L,立即予以输注血小板。那么哪些患者在发生严重PPH时易发生严重的血小板降低,需要立即输注血小板呢?也就是说哪些因素具有很好的预测性,在实验室结果出来之前就能预知可能发生血小板严重降低,从而提前准备血小板呢?
本研究就此问题建立了严重PPH时血小板输注的预测模型,通过对年龄、身高、体重、BMI、分娩方式、产后出血量、已输红细胞悬液的数量、分娩前的血小板计数、是否存在隐性出血(包括腹腔内出血、腹壁下血肿、阴道壁血肿)、妊娠合并症及并发症等因素进行了逐一的分析。妊娠合并症及并发症,我们选取了羊水栓塞、胎盘早剥、死胎、子痫前期、HELLP综合征、中重度肝功能异常这些易诱发DIC及血小板减少的病理妊娠。研究显示:产后出血量大、已输入红细胞悬液量多、分娩前PLT低、并发隐性出血、胎盘早剥、子痫前期、肝功能损害这些因素为血小板严重降低的独立影响因素,发生血小板计数快速下降到75×109/L以下的可能性大。进而基于二元Logistics回归分析的结果,以及组合不同影响因素建立的模型对比的结果,本研究最后将出血量、红细胞悬液输注量、分娩前PLT数值、隐性出血、子痫前期、胎盘早剥和中重度肝功能异常纳入诺莫图分析,用于建立严重PPH患者血小板输注的多变量预测模型。
本研究与FLINT等[8]通过多元逻辑回归分析建立心脏手术时血小板输注的风险预测工具的研究相似,其最优模型包含23个变量(P<0.001),如患心脏病感染性心内膜炎、近期心肌梗死等;其设计的Australian Cardiac Surgery Platelet Transfusion(ACSePT)风险预测评分工具包含九个变量,用于识别接受血小板输注的高风险患者。此外还有许多研究通过建立多变量统计模型来预测红细胞的输注。如TRENTINO等[9]的研究表明通过联合手术前的血红蛋白及手术方式建立的简单模型可以用于预测择期手术患者术中红细胞的输注(AUC=0.862)。
本研究应用的诺莫图能够可视化评估风险因素对于结局事件的影响,并能够通过累计得分量化结局事件的发生风险。本研究的风险因素包括:出血量、红细胞悬液输注量、分娩前PLT数值、隐性出血、子痫前期、胎盘早剥和中重度肝功能异常。根据患者实际情况,这些风险因素获得相应的分数,累计得分计算出总分,从而量化其发生风险。以50%为割点,即患者的评分大于101分,患者就会输注血小板。如某严重PPH患者,其出血量4 L、红细胞悬液输注量10 U、分娩前血小板为150×109/L,无其他并发症,按照表2其对应的得分分别为10分、10分、40分,累计总分60分,对应的风险为0.1,是不需要输血小板的。另一位严重PPH患者,其出血量2 L、红悬输注量3 U、分娩前血小板为100×109/L,存在隐性出血子痫前期、胎盘早剥、中重度肝功能异常的妊娠并发症,其得分分别为5分、10分、50分、25分、10分、28分、15,累计总分143分,对应的风险大于0.9,建议立即输注血小板。进而本研究通过内部曲线评价诺莫图预测效能,其一致性系数C-Index=0.789>0.7,一致性系数较高,诺莫图预测的符合程度较高。通过诺莫图曲线与平均曲线及理想曲线基本吻合,误差只有0.017,准确性较为可靠。
同时,ROC曲线也表明相比于单独应用严重PPH患者血小板输注的独立影响因素如出血量、红细胞悬液输注量、分娩前PLT数值、隐性出血、胎盘早剥和影响因素子痫前期和中重度肝功能异常来预测血小板输注(AUC值分别为0.631、0.689、0.518、0.611、0.641、0.531、0.529),多变量联合预测的效果更好(AUC=0.789),联合模型将明显提升血小板输注的预测精度与效能。
综上所述,本研究根据诺莫图建立严重PPH患者血小板输注的多变量预测模型,可根据患者出血量、红细胞悬液输注量、分娩前PLT数值、隐性出血、子痫前期、胎盘早剥和中重度肝功能异常这些因素预测风险,预测效能较高,可指导临床预见性地提前准备血小板,节省要血时间,为严重PPH时及时把控血小板输注时机、制定血小板输注方案提供依据,使抢救更加及时有效。
利益冲突所有作者均声明不存在利益冲突
