固相萃取/超高效液相色谱-串联质谱法同时测定水产养殖“非药品”投入品中37种禁限兽药
2023-01-05曼张兵吴花黄浩徐媛原
张 微,肖 曼张,兵吴,丹 钟 仕,花黄浩,*鹏,徐媛原,
(1.深圳市质量安全检验检测研究院,广东 深圳 518101;2.广东省市场监督管理局食用农产品监管重点实验室,广东 深圳 518101)
随着我国水产养殖行业的迅猛发展,水产行业对渔业投入品的需求越来越大,而目前对渔业“非药品”投入品的监管则有所缺失。“非药品”投入品的作用应为改良水产养殖环境,且不会造成养殖产品质量安全问题,但部分投入品却对养殖环境造成污染,给水产品安全及人类健康带来隐患[1-2]。目前,化学类水质底质改良剂、微生物制剂、中草药制剂、免疫增强剂等渔用非药品数量已远超正规兽药成为水产养殖第一大投入品[3-4],一些以“国标药品”为主成分的养殖投入品也被包装成“非药品”在市场上销售[5]。有研究报道了水产“非药品”致螃蟹大批量死亡[6]的事件,对国家产地水产品监控中发现的兽药残留阳性样品进行溯源也证实违禁药品来自“非药品”的使用[7]。针对当前存在的“非药品”成分不明、无生产技术及质量检测标准等问题,有必要建立一种快速、准确测定“非药品”投入品中多种禁限兽药残留的方法,以保障水产品质量安全,并进一步提升养殖投入品监管监测水平。
超高效液相色谱-串联质谱法因灵敏度高、准确度好、基质干扰小等优势,是复杂基质样品快速测定的首选[8-10]。在水产领域,现有研究大多是针对水产品中多种兽药残留的检测[11-14],对“非药品”投入品中兽药残留的研究较少。本研究针对基质复杂的投入品,重点从色谱条件、质谱条件、提取液、萃取方式等方面进行研究论证,最终采用PRiME-HLB固相萃取/超高效液相色谱-串联质谱法对“非药品”投入品中37种禁限兽药进行测定。此外,本研究还对市售的170份水产养殖投入品进行了分析检测,以期为监管部门提供数据参考,严防假劣投入品流入水产养殖领域。
1 实验部分
1.1 仪器、试剂与样品
Agilent 1290II超高效液相色谱串联AB SCIEX三重四极杆5500质谱仪(配备电喷雾离子源);PL602E百分之一电子天平;MTV-100多管旋涡混合仪;AS30600BDT超声波清洗仪;Sigma 3-30KS高速冷冻离心机;N-EVAP-24全自动氮吹仪;Waters PRiME-HLB固相萃取柱(6 mL,200 mg)。
乙腈、甲醇、甲酸、乙酸铵均为色谱纯;超纯水(Milli-Q超纯水仪制得),Mcllvaine-乙二胺四乙酸二钠(Mcllvaine-Na2EDTA)缓冲溶液(0.1 mol/L)。
分析标准品:磺胺类(磺胺嘧啶、磺胺噻唑、磺胺吡啶、磺胺甲基嘧啶、磺胺二甲基嘧啶、磺胺间甲氧嘧啶、磺胺甲噻二唑、磺胺对甲氧嘧啶、磺胺氯哒嗪、磺胺甲氧哒嗪、磺胺邻二甲氧嘧啶、磺胺间二甲氧嘧啶、磺胺甲基异唑、磺胺二甲异唑、磺胺喹啉、甲氧苄啶、磺胺苯吡唑),酰胺醇类(氯霉素、甲砜霉素、氟苯尼考),硝基咪唑类(羟基甲硝唑、甲硝唑、地美硝唑、洛硝哒唑、氯甲硝咪唑、苯硝咪唑、异丙硝唑、甲苯咪唑、5-羟基-甲苯咪唑、替硝唑、奥硝唑、羟基异丙硝唑),苯并咪唑类(氟苯达唑、芬苯达唑砜、噻苯哒唑、阿苯达唑砜),抗病毒类(金刚烷胺)(纯度≥92%,德国Dr.Ehrenstorfre公司)。
实际样品随机抽样于广东省各市水产养殖主要生产区水产药品销售点和互联网上经营的水产药品销售点。抽样品类包括底质改良剂、水质改良剂、消毒剂、杀菌杀虫和杀藻剂、中草药制剂等“非药品”共计170份。将固态、半固态样品充分均质后备用。
1.2 标准溶液配制
分别准确称取10.0 mg按纯度折算成100%质量的磺胺类、酰胺醇类、硝基咪唑类、苯并咪唑类、抗病毒类标准物质,用甲醇溶解并定容至10.0 mL,配制成1.00 mg/mL的单物质标准储备液。分别移取适量上述单物质标准储备液用甲醇稀释成适当质量浓度的混合标准工作液,-20℃下避光保存。
1.3 样品前处理
准确称取2.50 g(精确至0.01 g)均质试样于50 mL离心管内,加入10 mL 80%(体积分数)乙腈水(含0.2%甲酸)提取液和5 mL Mcllvaine-Na2EDTA缓冲溶液,置于多管旋涡混合仪上,以2 000 r/min涡旋振荡3 min,使用超声波清洗仪超声提取10 min后,用高速冷冻离心机以10 000 r/min离心5 min。准确吸取3.5 mL上清液直接过Waters PRiME-HLB固相萃取柱,保持1滴/s速度过柱。准确吸取收集好的滤液2.5 mL至5 mL带刻度离心管内,于40℃水浴下氮气吹至滤液少于0.5 mL,用复溶液将残留液定容至1.00 mL,涡旋振荡溶解残留物,过0.22 μm滤膜后上机测定。
1.4 仪器条件
1.4.1 液相色谱条件色谱柱:BEH C18(3.0 mm×100 mm,1.7 μm);柱温:40℃;流动相:A1为0.1%甲酸水溶液,A2为5 mmol/L乙酸铵水溶液,B为甲醇;流速:0.4 mL/min;进样量:5.00 μL。梯度洗脱程序见表1。

表1 流动相梯度洗脱程序Table 1 Gradient elution program of mobile phase
1.4.2 质谱条件离子源:电喷雾离子源;扫描方式:正/负离子模式;检测方式:多反应监测(MRM);电喷雾电压(IS):5.5 kV(正离子模式),-4.5 kV(负离子模式);离子源温度:550℃;气帘气压力(CUR):241.3 kPa;碰撞气压力(CAD):62.1 kPa;喷雾气(GS1)、辅助加热气压力(GS2):379.2 kPa。以子、母离子的丰度比和保留时间定性,以峰面积定量。各禁限兽药的质谱参数见表2。

表2 37种兽药的质谱参数Table 2 MS parameters of 37 veterinary drugs

(续表2)
2 结果与讨论
2.1 色谱条件的优化
为使色谱峰分离且获得良好峰形,提高目标化合物的灵敏度,实验对流动相体系进行了优化。由于在正离子模式下,向流动相中加入适量甲酸或乙酸铵可提高目标化合物离子化效率;而负离子模式下,加入甲酸会抑制目标化合物的离子化效率。因此,考察了0.1%甲酸水、5 mmol/L乙酸铵溶液、5 mmol/L乙酸铵溶液(含0.1%甲酸)与甲醇或乙腈的不同组合作为流动相时的分离效果。结果表明,以甲醇为有机相时,各目标化合物的响应均较乙腈时好,峰形更对称更尖锐。通过对比,实验最终确定2个最佳色谱条件:正离子模式采集时,磺胺类、硝基咪唑类、苯并咪唑类、抗病毒类的流动相体系为0.1%甲酸水溶液-甲醇;负离子模式采集时,酰胺醇类的流动相体系为5 mmol/L乙酸铵-甲醇。此时,各目标化合物间的分离效果最好,响应最高,峰形无拖尾,更对称。图1为空白加标(10.0 μg/kg)样品的MRM色谱图。
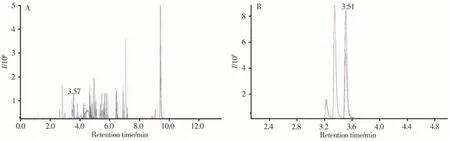
图1 空白加标(10.0 μg/kg)样品的MRM色谱图Fig.1 MRM chromatograms of a spiked(10.0 μg/kg)blank sample
2.2 质谱条件的优化
取各个药物的单标溶液(100 μg/L),以针泵注射方式单标进样,采用全扫描模式进行扫描,通过质荷比和各化合物的相对分子质量确定母离子,再对母离子进行打碎扫描获得各化合物的子离子信息,选取响应强度高的子离子作为定量离子和定性离子对。在多反应监测(MRM)模式下,优化各化合物的去簇电压和碰撞能量,结果见表2。
2.3 前处理方法的优化
2.3.1 提取溶剂的优化本实验对比了乙腈、酸化乙腈(含1%甲酸)、80%(体积分数,下同)乙腈水(含0.2%甲酸)、乙酸乙酯对37种目标物提取效率的影响。结果表明,乙酸乙酯对磺胺类药物的提取效率较低,乙腈对金刚烷胺的提取效率较低,酸化乙腈(含1%甲酸)和80%乙腈水(含0.2%甲酸)对目标物的提取效率无显著差异。从环保和节约资源的方面考虑,最终选取80%乙腈水(含0.2%甲酸)作为提取溶剂。
2.3.2 净化方法的优化水产养殖“非药品”基质成分较为复杂,净化效果对方法灵敏度有较大影响。QuEChERS法[15-16]与PRiME-HLB固相萃取柱法[17-18]各有优势,被广泛应用于兽药残留检测,本实验对比了这两种方法的净化效果。实验中采用的QuEChERS净化粉中含有50 mg C18、100 mg PSA和500 mg硫酸镁,采用的Waters PRiME-HLB柱是一款无需活化的固相萃取柱,与传统柱相比,省去了活化、淋洗、洗脱等步骤,大幅提高了检测效率。实验结果表明,采用QuEChERS法时目标化合物的平均回收率为56.6%~130%,其中磺胺甲氧哒嗪、磺胺二甲异唑、甲氧苄啶、甲砜霉素的平均回收率分别仅为56.6%、58.2%、60.5%、63.6%,氯苯达唑、甲苯咪唑的平均回收率均大于120%;而采用PRiME-HLB柱净化后,各目标化合物的平均回收率范围为71.6%~119%。最终选取Waters PRiMEHLB固相萃取柱进行净化。
2.4 方法学评价
2.4.1 线性范围与检出限以“非药品”投入品中37种禁限用兽药零检出的产品作为空白样品,添加一系列浓度的各物质标准溶液,制得系列加标样品,按“1.3”方法前处理后供超高效液相色谱-串联质谱测定,以各化合物定量离子的峰面积(Y)为纵坐标,质量浓度(X)为横坐标绘制标准曲线,各物质的线性方程、相关系数见表3。结果表明,各禁限兽药均呈现良好的线性关系,相关系数(r)均不小于0.991。根据信噪比(S/N)为3计算得到该方法检测各目标化合物的检出限(LOD),根据S/N=10计算得到该方法检测各目标化合物的定量下限(LOQ),得到LOD为0.156~1.94 μg/kg,LOQ为0.520~6.47 μg/kg,方法灵敏度较高。
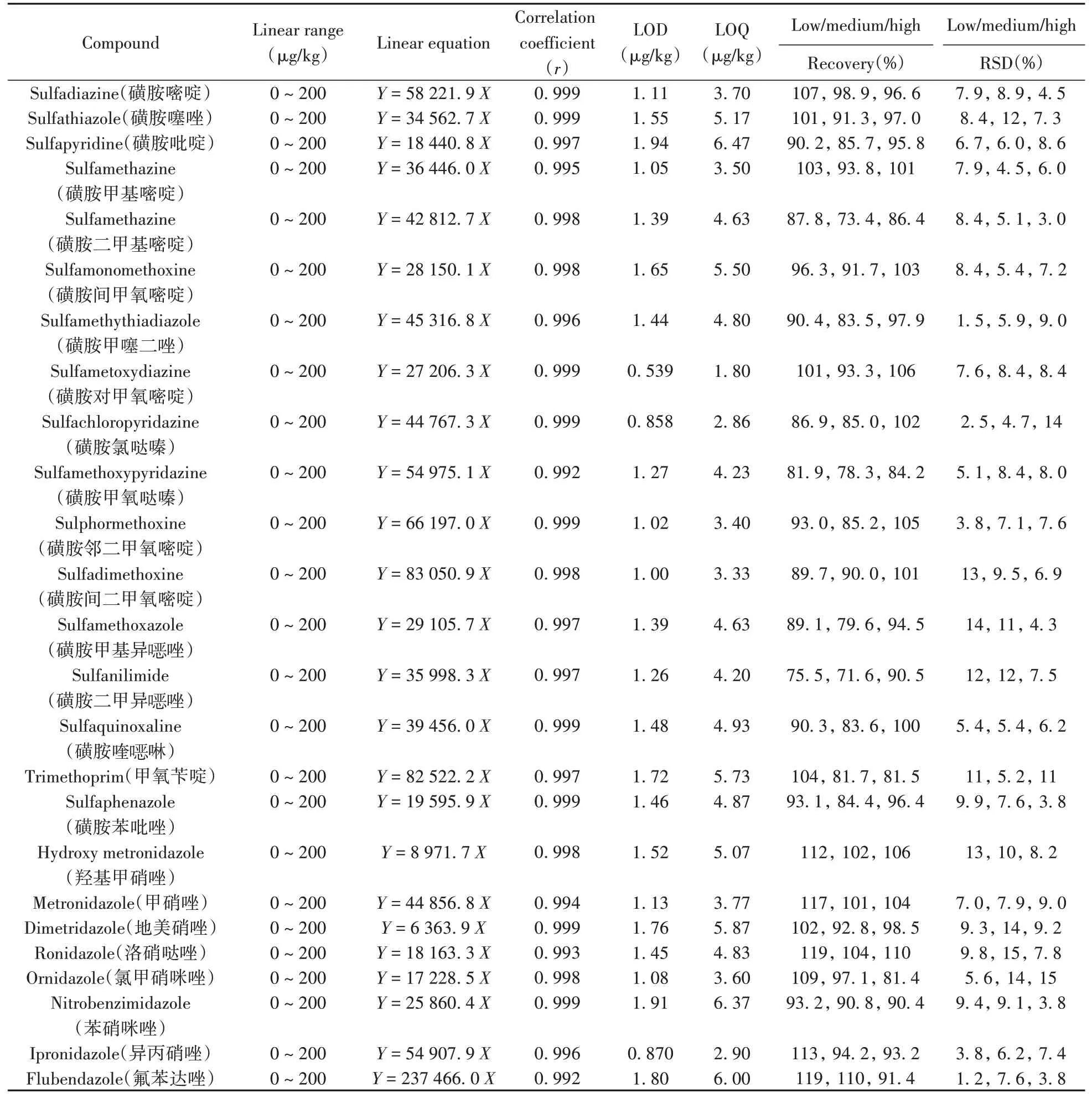
表3 37种兽药的线性关系、检出限、定量下限、加标回收率及相对标准偏差Table 3 Linear relationships,LODs,LOQs,spiked recoveries and relative standard deviations of 37 veterinary drugs
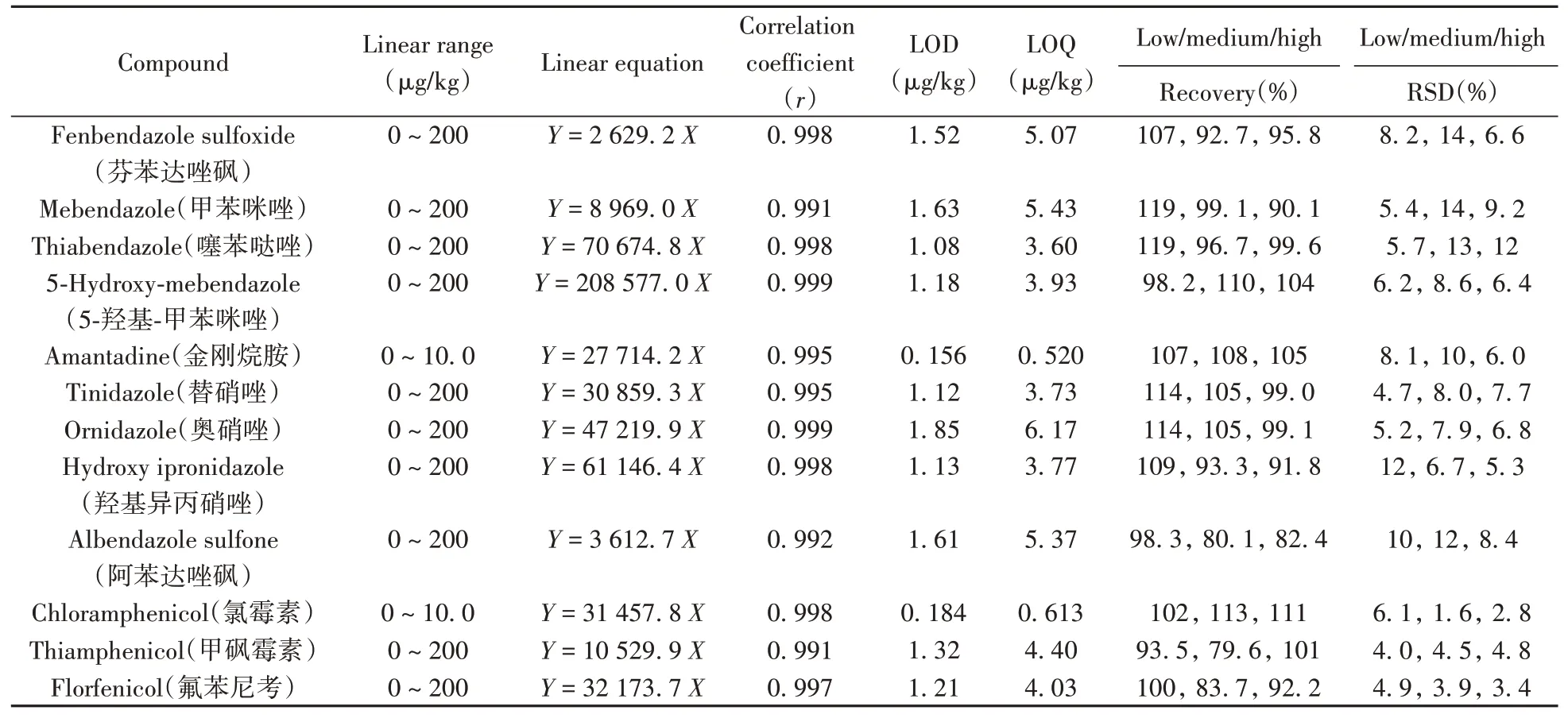
(续表3)
2.4.2 回收率及相对标准偏差对空白基质进行低、中、高3个水平的加标,进行回收率测定,除氯霉素、金刚烷胺的3个加标水平为1.00、2.00、6.00 μg/kg外,磺胺类、硝基咪唑类、苯并咪唑类、甲砜霉素、氟苯尼考的3个加标水平均为50.0、100、200 μg/kg,每个水平做6次平行,考察Waters PRiMEHLB固相萃取柱作为净化柱的回收率及相对标准偏差(RSD)。得到不同加标水平下的平均回收率为71.6%~119%,RSD为1.2%~15%。该方法的回收率及精密度良好,满足实验室质量控制的相关要求。
2.5 实际样品测定
对随机购买的170份水产养殖“非药品”(包括底质改良剂、水质改良剂、消毒剂、杀菌杀虫和杀藻剂、中草药制剂5类)开展检测,有32个产品检出药物,检出率为18.8%,上述5类药品的检出率分别为9.52%、15.4%、10.0%、23.3%、21.4%(图2)。其中中草药制剂中有10个产品同时检出多种磺胺类及酰胺醇类药物。从检出品类看,禁用抗病毒类药物金刚烷胺检出1次,限用兽药磺胺类药物(磺胺甲基异唑、磺胺间甲氧嘧啶、磺胺喹啉、磺胺嘧啶、甲氧苄啶)和酰胺醇类药物(氟苯尼考、甲砜霉素)为投入品中主要添加的风险物质,其含量范围为1.21~6.57×103μg/kg。各检出药物的具体名称、检出频次、检出含量范围见表4。结果表明,部分水产养殖投入品中存在非法添加兽药的情况,应加强监管。

表4 实际样品检测结果Table 4 Test results of practical samples
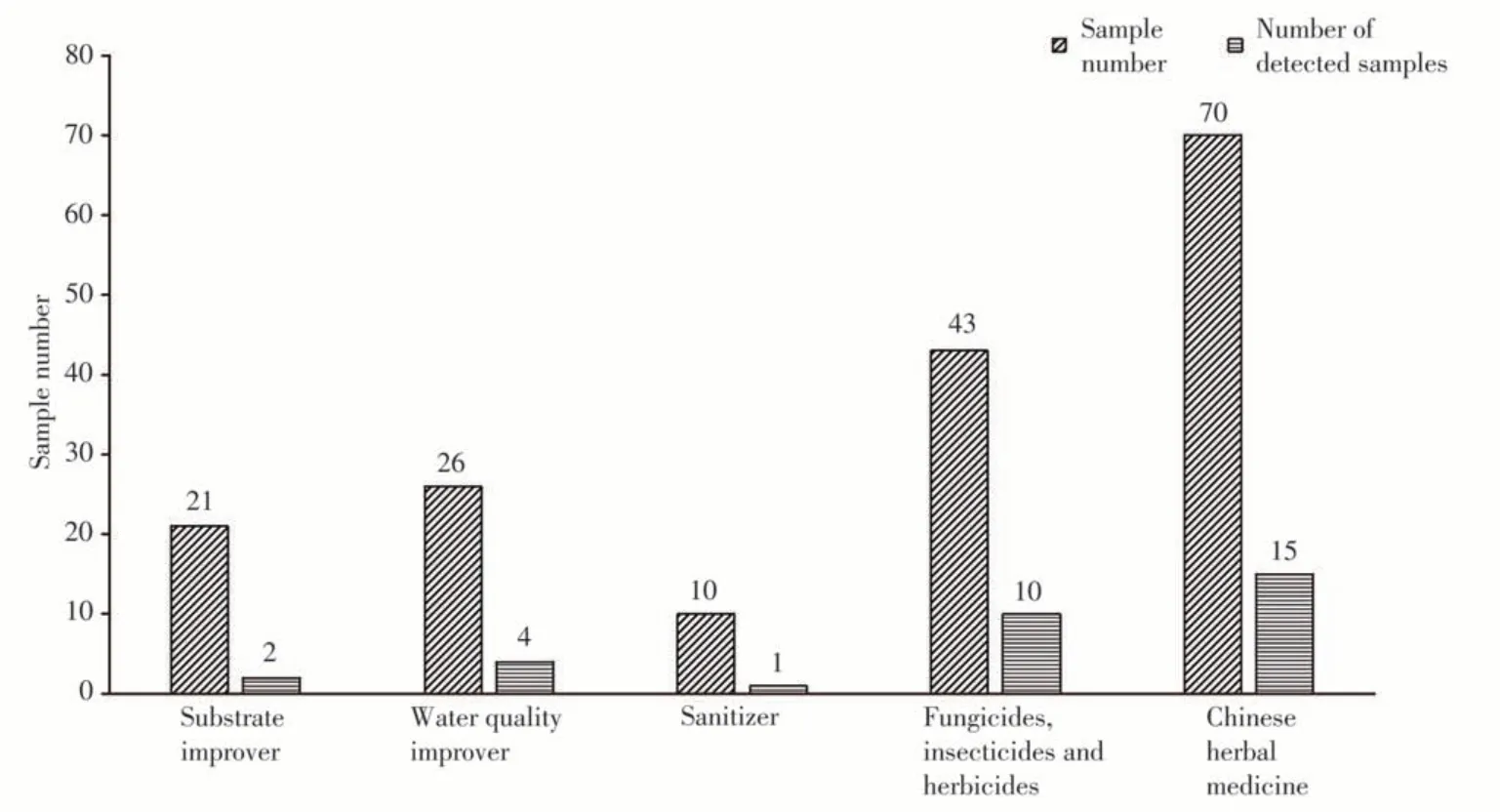
图2 不同类别“非药品”投入品的检出情况Fig.2 The detection of different types in“non-pharmaceutical”inputs
3 结论
本研究建立了固相萃取/超高效液相色谱-串联质谱测定水产养殖“非药品”投入品中37种禁限兽药(包括磺胺类、酰胺醇类、硝基咪唑类、苯并咪唑类、抗病毒类5类药物)残留的分析方法,实现了上述5类兽药残留的同时分析,大幅提高了检测效率。方法稳定性好,灵敏度、准确度高,可为“非药品”投入品的检测工作提供有力的技术支持。
