Ce改性的Rh-UiO-66-Zr催化剂对合成气制乙醇的影响
2023-01-04续开壮曹逢海李艳茹吴立志
续开壮 ,吕 倩 ,曹逢海 ,李艳茹 ,吴立志 ,谭 理
(福州大学 化学学院 分子催化与原位/表征研究所, 福建 福州 350108)
随着社会经济的持续发展,世界能源需求量不断提高,导致世界各国对化石燃料的需求也在不断的提升,但是化石能源储量有限以及在不合理的开发利用过程中会产生有毒有害气体污染环境。因此,寻找可替代化石能源的清洁能源就显得尤其的重要,除了风能、太阳能、潮汐能[1]等可再生能源外,乙醇作为一类清洁的可再生能源得到了世界各国的广泛关注,目前在医疗用品、食品饮料、有机原料、有机溶剂、汽车燃料等方面得到长足的应用。通常乙醇可以通过粮食发酵、合成气经甲醇(二甲醚)羰基化等方法制得。合成气直接合成乙醇由于其具有反应流程短等特点使其成为各国研究者一直关注的研究焦点。
在合成气制乙醇的工艺过程中,常用的催化剂主要分为Mo基催化剂、改性甲醇催化剂[2]、改性F-T催化剂[3]以及Rh基催化剂。其中,Rh催化剂对乙醇、乙酸、乙醛等C2含氧化合物具有较好的选择性而成为研究者关注的焦点。但目前关于Rh基催化剂在合成气制乙醇的生成机理中还存在着众多争议,其中为大多数研究人员所接受的是CO插入表面烷基键机理[4],一般认为合成气制乙醇的过程包括:在催化剂表面发生H2与CO的吸附;催化剂表面吸附的CO发生部分解离与加氢;未解离的CO插入到CHx中再加氢形成表面烯醇物种;表面烯醇物种加氢形成乙醇。但是Rh作为贵金属存在供应量不足的劣势导致其在商业化的过程中面临着很大的挑战,因此,探究Rh基催化剂的活性位点从而更好设计Rh基催化剂显得尤为重要。
在众多载体中金属有机骨架材料(MOFs)是一类由有机配体和金属离子通过自组装而成的排列有序的、多维的晶体材料。由于MOFs材料具有拓扑结构、较大的比表面积以及可以提供非常小的金属位点等固有的特殊性质,使得MOFs材料可以有效地控制负载金属的颗粒大小以及分散状态,并与负载金属产生强烈的相互作用[5]。因此,利用MOFs材料作为催化剂载体,可以更精准地构筑金属催化剂活性位点,研究其活性位点和构效关系。在众多的MOFs中,Zr基MOFs因其具有出色的结构稳定性[6,7]而广泛应用在酯化[8]、催化加氢[9]以及羟醛缩合[10]等催化反应中。Xue等[11]研究发现,将金属Rh和Mn负载在UiO-66上得到的催化剂对合成气制C2含氧化合物的催化性能较ZrO2[12]、SiO2[13]、TiO2[14,15]等多种传统载体的催化性能有很大提高。UiO-66的结构单元是由[Zr6O4(OH)4]金属节点和12个H2BDC配体连接而成[16],这就使得UiO-66的各个结构单元间连接紧密,相互作用较强,从而使UiO-66具有很高的稳定性,但这也使得它具有较少的配位点可供催化。要想解决这个问题可以采用引入具有更高配位数的路易斯酸金属去替代一个或多个Zr4+对UiO-66进行改性。
本研究以UiO-66为载体,制备了不同缺陷的负载金属Rh催化剂:Rh/UiO-66-Ce、Rh/UiO-66-Zr和Rh/UiO-66-ZrCe用以探究合成气制备乙醇的活性位点。研究发现在含C-O键产物中,随着金属Ce4+引入,Ce4+会替换 UiO-66-Zr的 [Zr6O4(OH)4]金属节点上的部分金属Zr4+,从而形成[Zr6-xCexO4(OH)4]金属节点,乙醇的活性位点数量显著提升。通过Rh/UiO-66-Ce、Rh/UiO-66-Zr和 Rh/UiO-66-ZrCe催化剂性能对比,揭示了[Zr6-xCexO4(OH)4]金属节点的形成对合成气制备乙醇活性位点的影响规律。
1 实验部分
1.1 实验原料
本实验所采用的试剂氯化锆(ZrCl4,≥99.9%)、氯化铑(III)水合物(RhCl3·xH2O,Rh 38.5%-42.5%)、对苯二甲酸(PTA,99%)、N,N-二甲基甲酰胺(DMF,>99.9%(GC))冰乙酸(CH3COOH,AR,99.5%)购买自阿拉丁试剂公司。硝酸铈铵((NH4)2Ce(NO3)6≥99.0%,AR(沪试))和无水乙醇(≥95.0%,CP(沪试))购买自国药试剂。
1.2 催化剂的制备
1.2.1 载体 UiO-66-Zr、UiO-66-Ce、UiO-66-ZrCe 的制备
UiO-66-ZrCe的合成方法是将硝酸铈铵(1.73 g)和氯化锆(0.74 g)按照 Zr∶Ce物质的量比为 1∶1 的比例溶解到置有15 mL的N,N-二甲基甲酰胺(DMF)中,然后在室温下搅拌20 min。另一个烧杯中将1 g对苯二甲酸溶解在68 mL N,N-二甲基甲酰胺(DMF)中搅拌30 min,然后将两个溶液混合后搅拌10 min,将其转移到100 mL聚四氟乙烯内衬的反应釜中,密封好后放入120 ℃预热的烘箱中,在120 ℃下维持24 h,待反应结束后取出放到水管下降至室温后取出。打开反应釜后,将产物转移到50 mL离心管中离心清洗,用30 mL N,N-二甲基甲酰胺(DMF)离心清洗三次,再用30 mL无水乙醇离心清洗三次,从而将样品中的N,N-二甲基甲酰胺(DMF)置换出来,最后将离心分离后的产物置于80 ℃的烘箱中过夜得到UiO-66-ZrCe黄白色粉末。
UiO-66-Ce和UiO-66-Zr的合成方法和UiO-66-ZrCe基本类似。
UiO-66-Ce的合成是将硝酸铈铵水溶液同对苯二甲酸的DMF溶液一块搅拌10 min,然后转移到200 mL聚四氟乙烯内衬的反应釜中进行后续的水热和离心清洗操作。
UiO-66-Zr的合成是将氯化锆溶解到N,N-二甲基甲酰胺(DMF)和调节剂冰乙酸中然后同对苯二甲酸的DMF溶液一块搅拌10 min,然后转移到100 mL聚四氟乙烯内衬的反应釜中进行后续的水热和离心清洗操作。
1.2.2 催化剂的制备
催化剂采用等体积浸渍法,将0.025 g三氯化铑配成1 mL的水溶液,然后缓慢滴加到1 g的载体中,边滴边搅拌,直到样品呈现出一种较稀的黏稠状态,室温下静置老化2 h,放入到80 ℃烘箱中过夜,最后将产物在马弗炉中于300 ℃下煅烧4 h得到催化剂。并分别在三种载体UiO-66-Ce、UiO-66-Zr和UiO-66-ZrCe上负载1%Rh,所得催化剂命名为Rh/UiO-66-Ce、Rh/UiO-66-Zr和Rh/UiO-66-ZrCe。
1.3 催化剂的表征
XRD测试采用的仪器是Rigaku SmartLab SE衍射仪,测试所用金属靶材为Cu靶(Cu Kα射线,λ = 0.15406 nm),测试所用电压为40 kV,电流为25 mA,在 5°-90° 对样品进行扫描,扫描速率为10(°)/min。
N2-BET采 用 美 国 Micromeritics ASAP 2020PLUS HD88氮气物理吸附仪,在温度77 K下测定催化剂的比表面积和孔结构,在测试前,将0.1 g样品在150 ℃真空氛围下脱气5 h。
H2-TPR采用配备有热导检测器(TCD)的美国Micromeritics Auto Chem Ⅱ的化学吸附分析仪,实验之前先将0.1 g催化剂在Ar氛围中300 ℃预处理2 h,降到室温后在10%H2/N2氛围下进行程序升温还原实验。
TG和DSC采用美国METTLER TOLEDO公司的TG/DSC 3 + 同步差热分析仪,实验前将30 mg催化剂放到坩埚中,然后在空气氛围下从室温一直升温到800 ℃测试。
拉曼光谱分析采用Thermo DXR2xi显微拉曼成像光谱仪进行测试,测试前先将催化剂在270 ℃下进行纯氢处理,然后取少量样品进行测试。
TEM在美国Thermo Scientific公司生产的型号为FEI Talos F200S G2场发射透射电子显微镜上进行测试。将待测试催化剂进行充分研磨,然后取少许催化剂放入乙醇中超声30 min,取上清液少量分多次滴加到Cu网上待自然晾干后取出进行样品测试。
原位漫反射傅里叶变换红外光谱研究采用美国的光谱仪Thermo Scientific Nicolet iS50 FT-IR进行原位分析测试,样品先在纯氢270 ℃下预处理2 h,然后降到250 ℃关掉氢气,打开Ar吹扫30 min采集背景,后通入流量 20 mL/min H2∶CO∶Ar为 16∶8∶1的合成气在1.2 MPa、250 ℃的反应中开始采集谱图进行分析。
XPS采用美国的Thermo Scientific公司生产的Thermo ESCALAB 250XI 仪器进行测试,以单色化Al靶(1486.6 eV)作为X射线激发源,采用284.6 eV的C 1s进行荷电校准后进行数据处理。
1.4 催化剂性能评价
催化剂反应性能评价在固定床反应器上进行。将40-60目催化剂颗粒与30-40目的石英砂(催化剂0.2 g,石英砂0.8 g)混合稀释后填装至反应器恒温段。反应开始前在270 ℃纯氢条件下预处理2 h,原料气采用H2∶CO∶Ar为16∶8∶1 的合成气,在285 ℃、3 MPa的条件下进行反应,通过配备有热导检测器(TCD)和火焰离子化检测器(FID)的在线HP-GC进行产物分析,反应后催化剂采用无水乙醇保护或在手套箱内封装后进行后续各项表征。
根据公式(1)和(2)计算CO转化率和产物的选择性。
CO转化率可用式(1)计算:
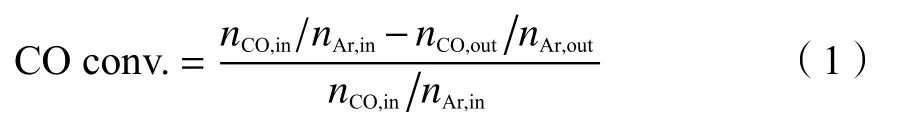
产物在所有含氧化合物中的选择性为:

式中,fi和Ri,m分别代表含氧化合物i的峰面积和含氧化合物i的碳摩尔响应。
2 结果与讨论
2.1 催化剂的结构分析
2.1.1 XRD分析
通过粉末X射线衍射(XRD)确定了所得材料的晶体结构,如图1和图2所示,分别为UiO-66-Ce、UiO-66-Zr和UiO-66-ZrCe三种载体材料以及Rh/UiO-66-Ce、Rh/UiO-66-Zr和 Rh/UiO-66-ZrCe催化剂的XRD谱图。从图1可以看出,UiO-66-Zr在 2θ 为 7.38° 、8.52° 、12.06° 、14.15° 和 14.78° 时表现出较强的衍射峰,分别归属于UiO-66-Zr载体的 (111)、(200)、(220)、(311)和 (222)晶面[17]。对于双金属UiO-66-ZrCe载体,观察到该载体的衍射峰整体向左移动1° ,这是由于较大半径的Ce4+(0.097 nm)部分替代了较小半径的Zr4+(0.084 nm),造成了Ce4+在[Zr6-xCexO4(OH)4]节点处晶格不匹配[18]。UiO-66-Ce的XRD谱图上,可以观察到在7.3° 、8.2° 、11.6° 、13.6° 、14.3° 处的具有明显的衍射峰,这些衍射峰分别归属于UiO-66-Ce载体上 (111)、(200)、(220)、(311)和 (222)晶面的特征衍射峰。此外,UiO-66-Ce载体相同晶面的衍射峰比UiO-66-Zr低,这是因为Ce4+(0.097 nm)的半径比Zr4+(0.084 nm)大。从图2可以观察到煅烧后的Rh/UiO-66-Zr和Rh/UiO-66-ZrCe催化剂与UiO-66-Zr和UiO-66-ZrCe载体的XRD衍射峰基本一致,这表明煅烧不会明显改变催化剂的金属有机骨架结构。而对于Rh/UiO-66-Ce催化剂来说,在300 ℃煅烧后,载体UiO-66-Ce的金属有机骨架已不复存在,其XRD谱图为CeO2的特征衍射峰,在 28.66° 、33.17° 、47.77° 和 56.57° 处的衍射峰,分别对应于 CeO2的 (111)、(200)、(311)和 (222)晶面[19],此结果与TG曲线相对应,说明此时材料中UiO-66-Ce晶体的热稳定性较差。在Rh/UiO-66-Ce、Rh/UiO-66-Zr和Rh/UiO-66-ZrCe催化剂的XRD谱图中并没有观察到金属Rh的衍射峰,这可能是因为金属Rh的负载量较低以及分散性良好。通过Scherrer方程计算的微晶尺寸为:UiO-66-Zr为31.99 nm,UiO-66-ZrCe为 52.74 nm,说明 Ce4+引入会导致晶体尺寸的增加[20]。
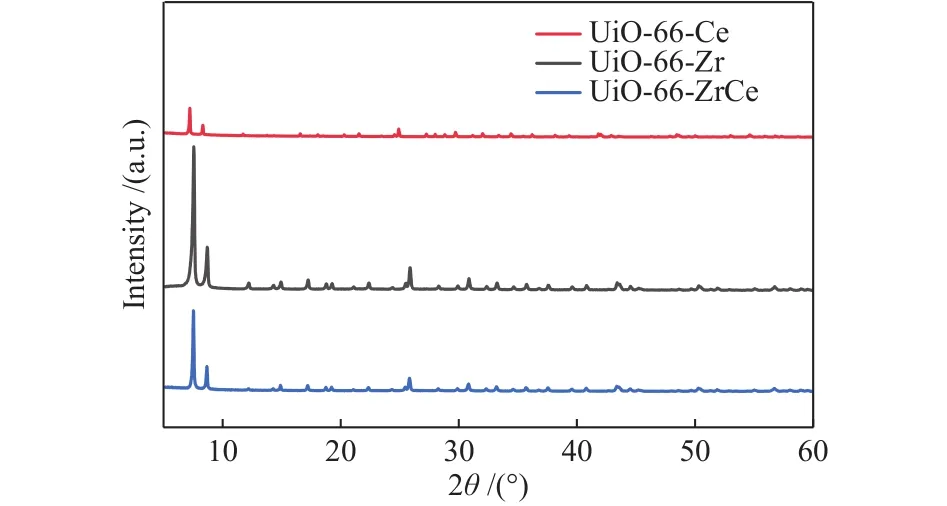
图1 不同载体的XRD谱图Figure 1 XRD patterns of different supports
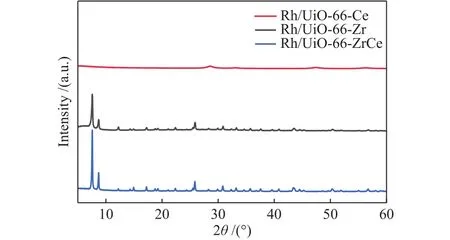
图2 不同催化剂在300 ℃煅烧后的XRD谱图Figure 2 XRD patterns of different catalysts after calcination at 300 ℃
2.1.2 N2吸附-脱附分析
图3是样品的N2吸附-脱附等温线。由图3可知,根据IUPAC分类可得,Rh/UiO-66-Ce、Rh/UiO-66-Zr和Rh/UiO-66-ZrCe催化剂均呈现为典型的IV型N2吸附-脱附等温线,同时呈现H3型回滞环,表明三种催化剂中均呈现介孔材料结构特性。催化剂的比表面积、孔容和平均孔径数据见表1。由图3可以看出,三种催化剂的滞后环大体类似,但Rh/UiO-66-Zr催化剂的滞后环的面积更大,这意味着催化剂的孔体积较大。而由Rh/UiO-66-ZrCe催化剂的吸附等温曲线以及表1可以看出,催化剂引入少量Ce4+之后,催化剂结构呈现出类似于Rh/UiO-66-Ce催化剂的孔径和孔体积,这表明,Ce4+的引入对催化剂结构具有一定的影响。由表1可知,Rh/UiO-66-Ce催化剂的比表面积最低,这是因为该催化剂经过煅烧后,[Ce6O4(OH)4]结点发生了结构塌陷,比表面积变小;Rh/UiO-66-Zr催化剂的比表面积较大,UiO-66-Zr中引入Ce4+使得Rh/UiO-66-ZrCe催化剂的比表面积降低。这可能是由于Ce在节点上不稳定,形成的[Zr6-xCexO4(OH)4]节点在焙烧温度下容易发生结构的裂解,从而暴露出表面缺陷[21]。
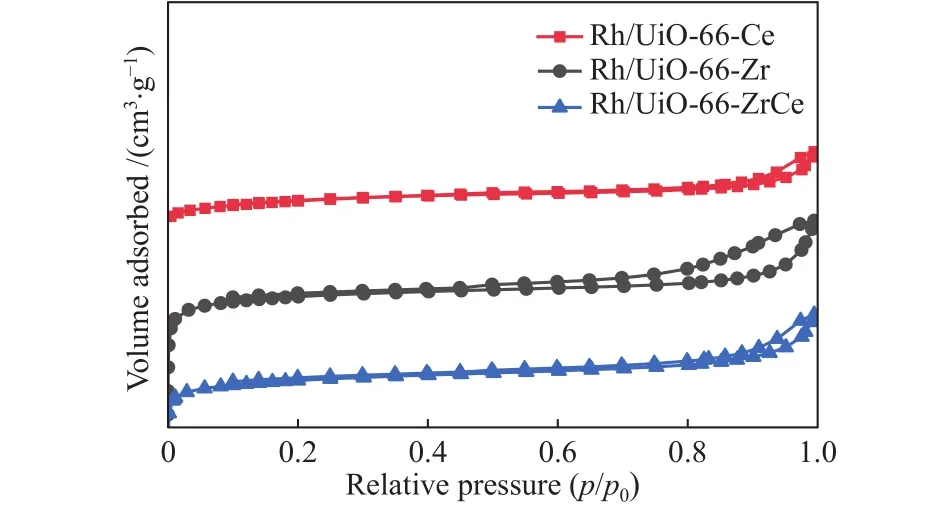
图3 不同催化剂的N2吸附-脱附等温线Figure 3 N2 adsorption and desorption isotherms of different catalysts
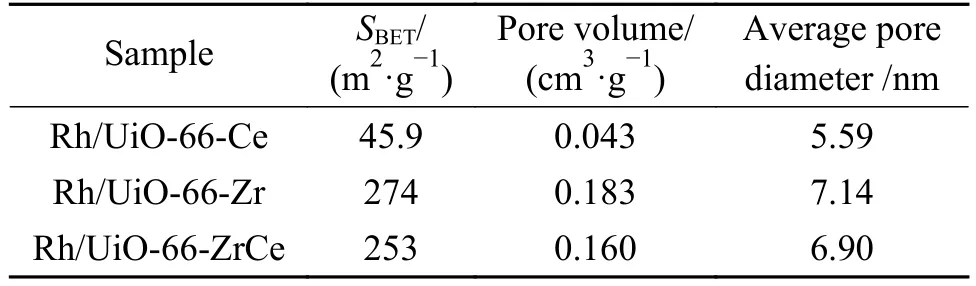
表1 不同催化剂的结构参数Table 1 Properties of different catalysts
2.1.3 热重分析TG
通过TG对材料的热稳定性进行评价,图4和图5分别为不同MOFs载体的Rh基催化剂的TG和DTG曲线。结果表明,三个催化剂均在100 ℃之前发生第一阶段的失重,这与催化剂表面物理吸附的水分的脱去有关。第二阶段催化剂表面发生脱羟基作用,使得少量水从催化剂表面流失。第三阶段发生了MOFs结构的降解[22],由图4可见,不同催化剂的降解温度不同,Rh/UiO-66-Zr的开始降解温度较高在464 ℃,Rh/UiO-66-Ce的降解温度最低(310 ℃),Rh/UiO-66-ZrCe 的降解温度为 374 ℃。三种催化剂中Rh/UiO-66-Zr最稳定,Rh/UiO-66-ZrCe次之,Rh/UiO-66-Ce最不稳定。可见Ce4+的引入使得MOFs的结构稳定性变差。与Rh/UiO-66-Zr相比,Rh/UiO-66-ZrCe的热稳定性较低,这是由于Ce部分替换掉了Zr,Ce4+的原子半径要比Zr4+原子大,同时Ce4+的金属有机框架节点不稳定。Lammert等[23]认为,UiO-66-ZrCe中Ce含量的增加对材料的热稳定性有一定负面影响。结合N2吸附-脱附分析以及XRD分析发现,Rh/UiO-66-ZrCe催化剂发生了类似于Rh/UiO-66-Ce结构的变化,UiO-66上Ce位点在300 ℃已经发生结构裂解,Rh/UiO-66-ZrCe催化剂上结合到[Zr6-xCexO4(OH)4]节点的Ce位点在煅烧时进一步裂解,催化剂稳定性变差,使得催化剂的比表面积、孔径、孔体积等结构性质发生了变化。

图4 不同催化剂的TG曲线Figure 4 TG curves of different catalysts
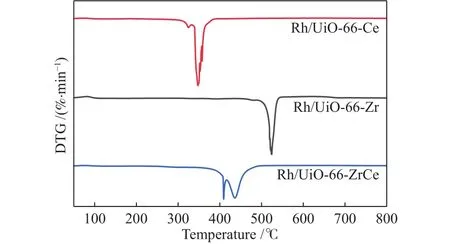
图5 不同催化剂的DTG曲线Figure 5 DTG curves of different catalysts
2.1.4 透射电镜TEM分析
图6为Rh/UiO-66-Ce、Rh/UiO-66-Zr和Rh/UiO-66-ZrCe催化剂在300 ℃煅烧后的TEM照片。如图6(b)所示,Rh/UiO-66-Zr催化剂呈现出标准的八面体结构,其表面光滑密实[24],这表明煅烧后UiO-66-Zr节点没有团聚,同时催化剂粒径约为270 nm。从图6(a)中可以发现,Rh/UiO-66-Ce催化剂表面不规则,结合XRD发现,UiO-66-Ce的骨架已经坍塌,Rh/UiO-66-Ce催化剂在煅烧时配体分解,八面体各面收缩,在XRD谱图中呈现出CeO2的衍射峰。而图6(c)中催化剂的形貌类似于图6(a),但是结合 XRD发现,Rh/UiO-66-ZrCe和 UiO-66-Zr的XRD谱图一致,这说明Rh/UiO-66-ZrCe催化剂金属有机骨架结构还保持一定的完整性,Rh/UiO-66-ZrCe催化剂引入的Ce4+分布于UiO-66-ZrCe表面,在煅烧条件下Rh/UiO-66-ZrCe催化剂表面的Ce4+发生配体分解,使得Rh/UiO-66-ZrCe催化剂表面粗糙呈现出类似于Rh/UiO-66-Ce催化剂的形貌。此外,所有的催化剂TEM照片中均没有观察到金属颗粒的出现,这表明金属在载体中分散均匀。
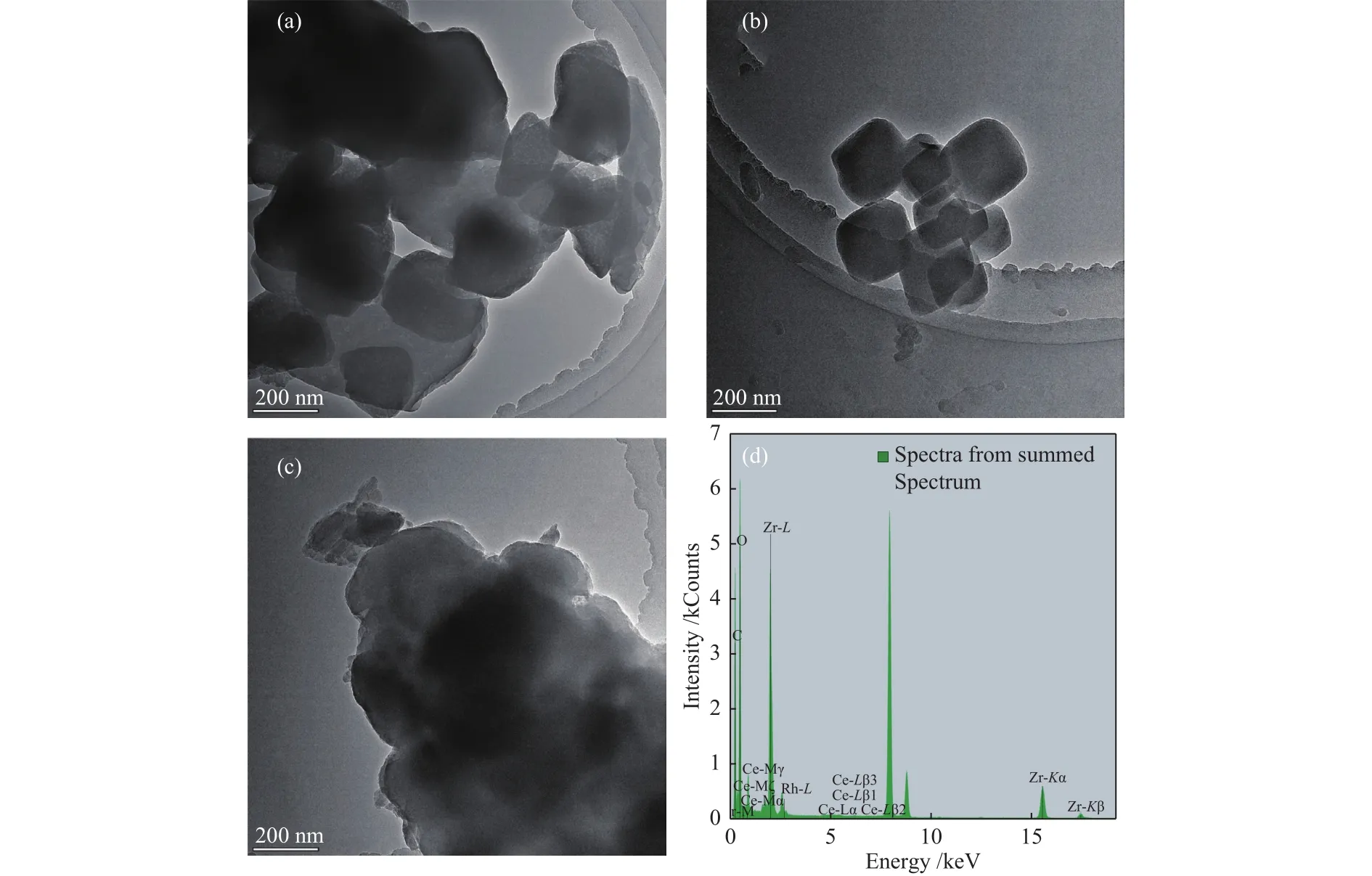
图6 催化剂在300 ℃煅烧后的TEM照片Figure 6 TEM images of the catalyst after calcination at 300 ℃
表2为催化剂Rh/UiO-66-ZrCe中的相对元素含量,从图6(d)和表2得到的EDS数据可以看出,Rh/UiO-66-ZrCe催化剂上Ce的引入量很少,原子分数只有0.05%,相比于元素Zr的原子分数12.92%来说比较微量。同时也给出了相对原子分数以及相对质量分数的误差,数值越大代表该数据的可信度越差,对于元素Zr和Ce的误差都在10%以下,表明元素相对含量存在很高的可信度。根据MOFs结构推测,Rh/UiO-66-ZrCe催化剂中的Ce存在于[Zr6-xCexO4(OH)4]节点上。

表2 催化剂Rh/UiO-66-ZrCe中的相对元素含量Table 2 Relative element content in the catalyst Rh/UiO-66-ZrCe
2.1.5 拉曼光谱分析
图7为催化剂Rh/UiO-66-Ce的拉曼光谱谱图,拉曼光谱显示出592和462 cm-1的特征峰,这是由缺陷诱导的D (592 cm-1)模式和F2g(462 cm-1)模式引起,这表明在UiO-66-Ce载体上具有丰富的缺陷位点[21]。但结合三种催化剂的XRD谱图、TG曲线以及H2-TPR曲线发现,Rh/UiO-66-Ce不稳定的结构使得催化剂上存在多种类型的Rh物种,塌陷的[Ce6O4(OH)4]节点使得分散在UiO-66-Ce上的Rh物种容易团聚;而在Rh/UiO-66-Zr和Rh/UiO-66-ZrCe催化剂上Rh物种较为单一,高分散的Rh物种可以被UiO-66-Zr载体稳定。而在Rh/UiO-66-ZrCe催化剂上,Ce4+作为一种缺陷位点被引入催化剂,在煅烧时UiO-66上与Ce结合的位点不稳定以及Ce4+的半径较大,使得Ce位点容易发生结构塌陷,形成[Zr6-xCexO4(OH)4]节点,从而引入缺陷位点[25]。这些结果证明,高度分散的Rh在UiO-66-Zr和UiO-66-ZrCe上分别形成了-(Zr-O)-Rh-(O-Zr)-和-(Zr-O)-Rh-(O-Ce)-位点。
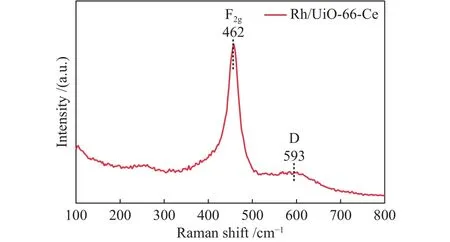
图7 催化剂Rh/UiO-66-Ce的Raman谱图Figure 7 Raman spectrum of the Rh/UiO-66-Ce catalyst
2.2 催化性能测试
图8为三种催化剂的CO转化率以及含氧化合物的选择性,本实验的研究是基于乙醇作为目标产物进行的,即通过目标产物选择性的变化研究有效乙醇活性位点。Rh/UiO-66-Ce、Rh/UiO-66-Zr和 Rh/UiO-66-ZrCe在 3 MPa、285 ℃ 的条件下进行CO加氢反应,CO的转化率都达到了20%以上,证明Rh基UiO-66型MOFs材料都具备不错的CO加氢能力。如图8所示,通过对比三种催化剂的CO转化率以及含氧化合物的选择性发现,催化剂Rh/UiO-66-ZrCe的催化性能最好,CO的转化率为36.51%,其次是催化剂Rh/UiO-66-Zr,CO的转化率为30.01%,催化性能最差的是催化剂Rh/UiO-66-Ce,CO的转化率仅为21.49%。对产物中乙醇的选择性进行比较后可以明显地看到催化剂Rh/UiO-66-ZrCe的乙醇在含氧化合物中选择性最高为49.72%,比催化剂Rh/UiO-66-Zr的33.18%以及催化剂Rh/UiO-66-Ce的28.3%要高出接近20%,并且乙醇在催化剂Rh/UiO-66-ZrCe的所有含氧化合物中选择性最高。在CO2的选择性上,可以看到催化剂Rh/UiO-66-Zr的CO2选择性最低,当金属Ce引入后CO2的选择性明显提高,这是由于Ce的引入导致解离后的CO形成的O物种插入CO增多导致的。由此可以得出在金属有机骨架UiO-66-Zr中掺入金属Ce以替代部分金属Zr节点对催化剂在合成气制备乙醇的过程中具有明显的促进作用,金属Ce的加入在一定程度上抑制了甲醇的生成,促进了乙醇的产生。
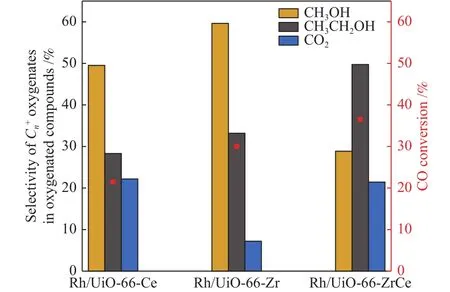
图8 不同催化剂的CO转化率和各含氧化合物在所有含氧化合物中的选择性Figure 8 CO conversion of different catalysts and the selectivity of each carbohydrate in all carbon oxides of different catalysts
2.3 催化剂化学性质分析
2.3.1 H2-TPR分析
图9为三种催化剂的H2-TPR谱图。通过程序升温还原分析了三种催化剂的还原性能,由于MOFs结构在高温条件的不稳定性,所以只观测了30-350 ℃的H2-TPR谱峰。如图9所示,其中Rh/UiO-66-Ce催化剂上第一个还原峰(94 ℃)归属于UiO-66-Ce上具有更好分散度的小颗粒的Rh物种的还原;第二个还原峰归属于较大块状颗粒Rh物种的还原;而第三个还原峰归属于载体与Rh物种之间具有的较强相互作用。而在Rh/UiO-66-Zr和Rh/UiO-66-ZrCe催化剂上,均未观察到分散Rh物种以及颗粒状Rh物种的还原,这可能是由于UiO-66-Zr上[Zr6O4(OH)4]节点与Rh具有相对更强的相互作用,而且UiO-66-Zr具有发达的孔道,Rh物种可以形成较好的分散。在三个样品中,Rh/UiO-66-Ce催化剂上的金属Rh与UiO-66-Ce载体存在多种不同形态相互作用形式,在H2-TPR谱图上呈现出三种不同的还原峰;而在Rh/UiO-66-Zr和Rh/UiO-66-ZrCe催化剂上Rh物种形式单一,并且具有单一形态的还原峰。相比于Rh/UiO-66-Zr催化剂的还原峰温度(290 ℃),Rh/UiO-66-ZrCe催化剂的还原峰温度较低(267 ℃),这是由于缺陷型Ce4+引入[Zr6O4(OH)4]节点替换部分Zr4+形成具有缺陷的[Zr6-xCexO4(OH)4]节点,催化剂表面形成了-(Zr-O)-Rh-(O-Ce)-位点,由于-(Zr-O)-与-(O-Ce)-和金属Rh的相互作用不同,降低了与Rh的相互作用强度,使得Rh/UiO-66-ZrCe的金属Rh物种的还原温度降低到267 ℃。
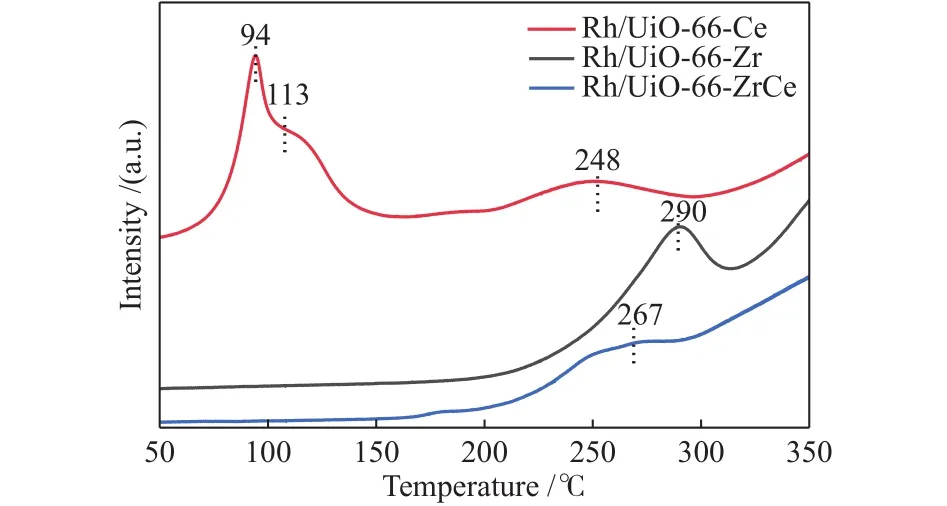
图9 不同催化剂的H2-TPR谱图Figure 9 H2-TPR profiles of different catalysts
2.3.2 XPS分析
使用X射线光电子能谱检测了催化剂表面的组成和化学状态,图10和表5分别为Rh/UiO-66-Zr和 Rh/UiO-66-ZrCe催化剂的 Rh 3d、O 1s、和Zr 3d轨道的详细峰拟合结果和定量结果,根据表5中各元素的定量结果可以确定有Ce4+被引入到了催化剂中。图10(a)和图10(b)为Rh/UiO-66-Zr和Rh/UiO-66-ZrCe催化剂的Rh 3d的XPS光谱谱图,其中,位于307.00和311.70 eV为金属Rh0的特征峰,位于308.60和313.30 eV为Rhv+的特征峰[26]。从表3Rh/UiO-66-Zr和Rh/UiO-66-ZrCe催化剂的Rh3 d XPS拟合结果可以发现,随着金属Ce4+的引入,催化剂上Rh0的含量增加并且Rhv+的含量减少,在Rh/UiO-66-Zr催化剂上形成的-(Zr-O)-Rh-(O-Zr)-位点,Rh物种与-(O-Zr)-物种的相互作用较强。相比于未引入Ce4+的Rh/UiO-66-Zr催化剂,Rh/UiO-66-ZrCe催化剂上形成了-(Zr-O)-Rh-(O-Ce)-位点,由于Rh与-(O-Zr)-位点的相互作用较强,而Rh与-(O-Ce)-位点的相互作用较弱,这种相互作用的势差有利于电子的高效率传输。图10(c)和图10(d)分别为Rh/UiO-66-Zr和Rh/UiO-66-ZrCe催化剂的O 1s的XPS光谱谱图,其中,位于530.10-530.20 eV为催化剂表面晶格氧(Oα)的特征峰,位于531.75-531.85 eV为催化剂表面吸附氧物种(Oβ)的特征峰[26]。通过图10(c)和图10(d)以及表4中的数据可以看出,微量Ce4+的引入对催化剂表面氧物种也有较大的影响,这有利于反应物种的吸附与活化,在反应过程中对催化反应中间体也有一定的稳定作用。
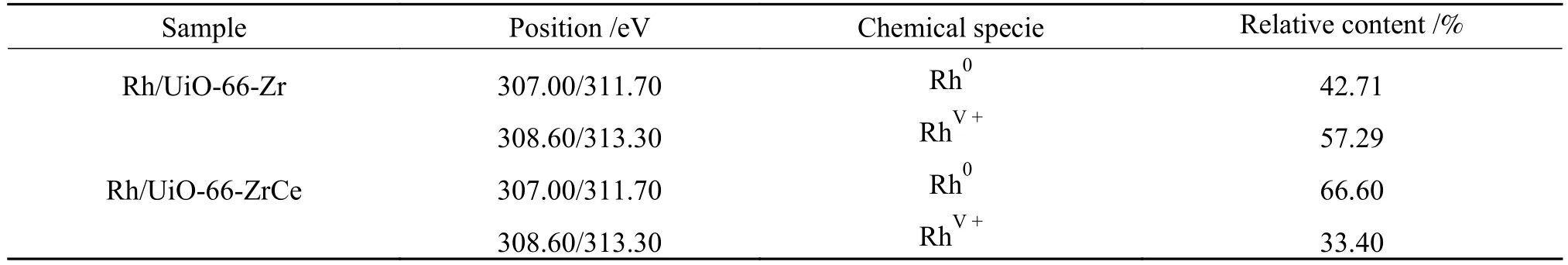
表3 催化剂Rh/UiO-66-Zr和Rh/UiO-66-ZrCe上Rh 3d的XPS谱图拟合Table 3 XPS spectrogram fitting results of Rh 3d on Rh/UiO-66-Zr and Rh/UiO-66-ZrCe
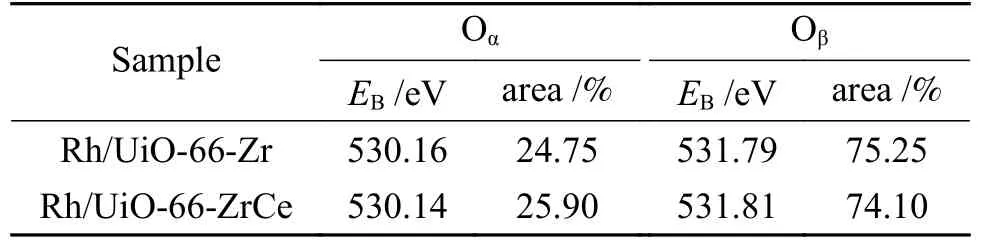
表4 催化剂上O 1s的XPS谱图拟合Table 4 XPS spectrogram fitting results of O 1s on Rh/UiO-66-Zr and Rh/UiO-66-ZrCe

表5 Rh基催化剂的XPS定量Table 5 XPS quantitative results of Rh-based catalysts

图10 不同催化剂的XPS光谱谱图Figure 10 XPS spectra of the catalysts
2.3.3 In-situ DRFITS光谱分析
图11是Rh/UiO-66-Ce、Rh/UiO-66-Zr和Rh/UiO-66-ZrCe的原位红外谱图。位于3018、2929、2857、1408和1305 cm-1处的特征红外吸收峰归属于-CH3或者-CH2的C-H红外振动吸收峰[27],从红外光谱中可以明显看出,相比于Rh/UiO-66-Zr和Rh/UiO-66-Ce催化剂,Rh/UiO-66-ZrCe催化剂位于1408 cm-1处的红外吸收峰明显增强,这意味着Rh/UiO-66-ZrCe催化剂能够稳定-CH3物种,这有利于乙醇的形成。位于1886 cm-1处的红外特征吸收峰为位于Rh物种上桥式吸附的CO[28]。同时位于1155、1132、1034 cm-1处的红外吸收峰归属于桥接和末端甲氧基(b-OCH3和 t-OCH3)[29],相比于 Rh/UiO-66-Zr催化剂,Ce4+的引入使得Rh/UiO-66-ZrCe催化剂上桥式吸附的CO和甲氧基吸附强度明显增强。同时位于1576 cm-1处的红外吸收峰归属于桥接的-HCOO*物种[27],相比与 Rh/UiO-66-Zr和 Rh/UiO-66-Ce催化剂,Rh/UiO-66-ZrCe催化剂上桥接的-HCOO*物种吸附强度明显降低。因此,由于Rh/UiO-66-Zr和Rh/UiO-66-ZrCe催化剂表面形成了-(Zr-O)-Rh-(O-Zr)-和-(Zr-O)-Rh-(O-Ce)-位点,使得催化剂对不同中间产物的吸附稳定性发生了变化,Rh/UiO-66-ZrCe催化剂上形成的-(Zr-O)-Rh-(O-Ce)-更有利于乙醇产生。
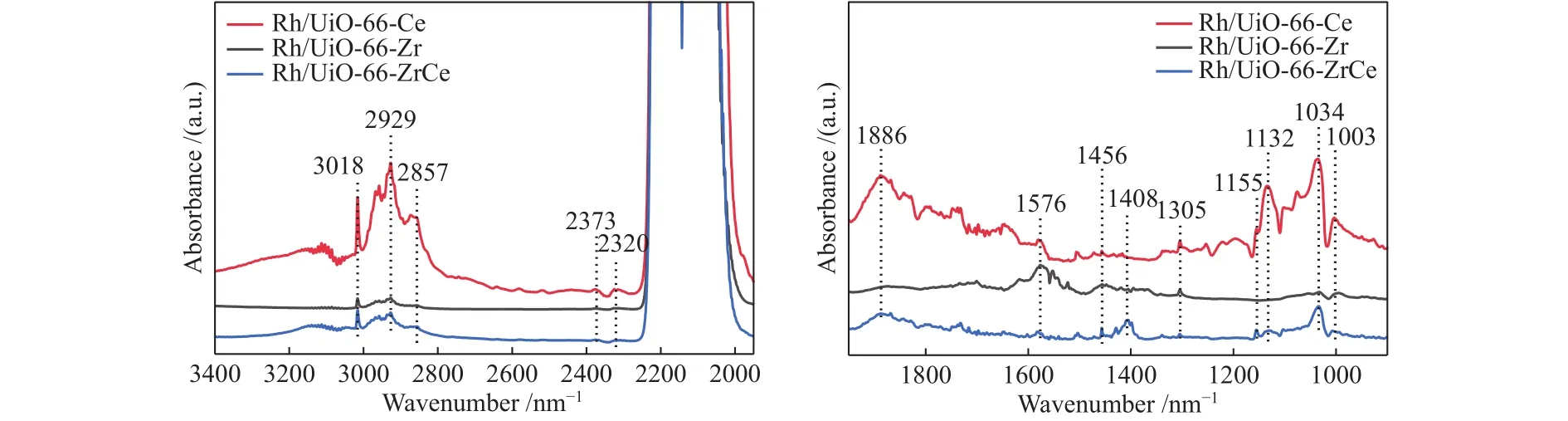
图11 三种催化剂在 250 ℃、1.2 MPa、原料气 H2∶CO∶Ar为 16∶8∶1的条件下的原位红外光谱谱图Figure 11 In-situ DRIFITS spectra of three catalysts under the conditions of 250 ℃ 1.2 MPa and the H2∶CO∶Ar ratio is 16∶8∶1
3 结 论
本研究以UiO-66为载体,制备了具有不同缺陷的 Rh基催化剂,Rh/UiO-66-Ce、Rh/UiO-66-Zr和Rh/UiO-66-ZrCe探究其合成气制备乙醇的活性位点。研究发现,在Rh/UiO-66-ZrCe催化剂上,随着金属Ce4+引入,可以替换掉UiO-66-Zr中的部分Zr金属节点形成[Zr6-xCexO4(OH)4],促进了CO加氢合成乙醇反应的催化性能。通过对Rh/UiO-66-Ce催化剂的表征及反应性能的研究,揭示了引入Ce4+可以创造出一种重要的缺陷位点,在这种形成的-(Zr-O)-Rh-(O-Ce)-位点上同时存在两种与Rh物种具有不同相互作用强度的-(Zr-O)-和-(O-Ce)-结构,从而导致-(Zr-O)-Rh-(O-Ce)-位点上形成一定的相互作用势差,有利于催化剂表面电子的高效传输,同时该催化剂还稳定了合成气制备乙醇的反应中间体,有利于乙醇的形成,增加了反应活性位点。本研究加深了对于乙醇合成中Rh催化剂真实活性位的理解,并可为更好的设计合成气制备乙醇催化剂提供一定指导。
