新一代国产自锁式经导管二尖瓣缘对缘修复系统KokaclipTM首次临床应用的研究结果
2023-01-04高建斌马米尔史青唐永研杨宏波潘家华张戈军骆志玲朱达潘湘斌
高建斌 马米尔 史青 唐永研 杨宏波 潘家华 张戈军 骆志玲 朱达 潘湘斌
二尖瓣疾病是最常见的瓣膜病变,既往体外循环心内直视手术是治疗二尖瓣病变的金标准,但其创伤较大,并不适用于高龄且外科手术高风险的二尖瓣病变患者,尤其是对心功能不全导致的功能性二尖瓣反流(functional mitral regurgitation,FMR)人群。据统计,美国中度及以上二尖瓣反流(mitral regurgitation,MR)患者达到250万人,而治疗率不足5%[1]。由于人口基数庞大,我国罹患二尖瓣疾病的人群达千万级,治疗需求同样巨大[2]。经导管二尖瓣缘对缘介入技术的问世填补了这一空白,凭借充分的临床研究证据,该技术已经相继被美国食品药品监督管理局(Food and Drug Administration,FDA)、我国国家药品监督管理局(National Medical Products Administration,NMPA)及欧盟CE认证用于外科手术高风险的退行性二尖瓣病变及经过最佳内科治疗仍然有症状的FMR患者[3-7]。2020年美国心脏病学会/美国心脏协会(American College of Cardiology/American Heart Association,ACC/AHA)瓣膜疾病指南[8]也明确了其为最优指南药物治疗下依旧有明确症状的FMR的Ⅱa类推荐,也是外科手术高危及不能行外科手术的退行性二尖瓣反流(degenerative mitral regurgitate,DMR)的Ⅱa类推荐。
进口医疗器械价格昂贵,作为人口大国及MR病变罹患人群大国,我国急需成熟的国产二尖瓣介入治疗器械,KokaclipTM是我国自主研发的新一代自锁式经导管二尖瓣缘对缘修复系统,该系统已经顺利完成慢性动物实验验证,具有完善的型式检测,且首例患者置入效果亦较为良好[9]。本研究以此为契机,报道该系统首次临床应用研究及随访结果。
1 对象与方法
1. 1 研究对象
本研究是前瞻性、单中心、单组观察的可行性临床研究,纳入2021年10月至2022年2月于云南省阜外心血管病医院行经导管二尖瓣缘对缘介入治疗的患者12例。纳入标准:(1)年龄>18岁;(2)超声心动图证实为中重度(3+)或重度(4+)MR,包括DMR患者和FMR患者;(3)经过最佳药物治疗无效且不能经外科手术治疗的FMR患者;(4)FMR患者左心室射血分数(lef t ventricular ejection f raction,LVEF)≥20%并≤50%,DMR患者需两位外科专家判定为外科手术禁忌或高危,建议参考标准为美国胸外科医师协会(Society of Thoracic Surgeons,STS)评分≥6%,或者存在其他高危因素,如虚弱、手术操作障碍及器官功能障碍等;(5)左心室收缩末期内径≤70 mm;(6)纽约心脏病协会(New York Heart Association,NYHA)心功能分级Ⅱ~Ⅳ级;(7)MR束来自二尖瓣A2/P2区;(8)受试者愿意并遵守方案要求和数据收集程序,能够理解试验的目的,本人或法定监护人自愿参加并签署知情同意书。排除标准:(1)4周内发生过急性心肌梗死。(2)合并中度以上的主动脉瓣狭窄或反流,或合并重度三尖瓣反流及狭窄。(3)未经治疗的严重冠状动脉狭窄,需血运重建,或需要进行其他心脏外科手术。(4)二尖瓣瓣口面积<4.0 cm2。(5)严重二尖瓣钙化。(6)瓣叶解剖结构不利于二尖瓣修复系统置入,表现为A2/P2区钙化,A2/P2区外存在明显反流。DMR患者瓣叶严重脱垂,瓣叶呈枷样改变且连枷宽度≥15 mm;FMR患者对合缘<2 mm,对合深度>11 mm。(7)既往有二尖瓣手术史,或置入过二尖瓣人工瓣膜,左心室辅助装置。(8)受试者存在已知或疑似左心房黏液瘤,或超声心动图显示存在心脏内血栓、赘生物、肿块。(9)过去3个月内有出血病史、活动性消化道溃疡,或过去6个月内发生过脑血管事件,或具有抗血小板制剂和抗凝剂治疗禁忌证,以及无法进行抗栓治疗等。本研究获得云南省阜外心血管病医院伦理委员会批准(批件号:2021-048-01)。所有患者均签署知情同意书。
1. 2 研究器械
本研究使用KokaclipTM经导管二尖瓣缘对缘修复系统,采用经典的经股静脉路径及具有调弯功能的三层鞘管输送系统,第一层引导导管外径为22 F,第二层器械输送鞘管拥有超过90°调弯度功能,并与第三层夹子操控手柄相连,不同于MitraClip,其输送系统引导导管和第二层输送鞘管之间可以互相转动,从而提供了更大的自由度,可以满足更多复杂的心内调弯状态(图1 A~B)。其独特设计的二尖瓣夹子采用不同于MitraClip的弹性自锁功能,夹子自然状态即为关闭状态,并具有弹性,从而可以降低瓣叶夹闭后的二尖瓣应力,也极大地增加了器械的锁定可靠性(图1 C~D)。同时其拥有二尖瓣瓣叶独立捕获功能,并具备四个型号的夹子设计(依据夹臂长宽径的不同分为四个型号,长短型号为臂长12 mm/9 mm,宽和非增宽型号夹臂宽度分别为4 mm/6 mm),从而适应更复杂的瓣膜解剖病变。

图1 KokaclipTM 经股静脉路径缘对缘二尖瓣修复系统工作原理 A~B.其采用具有调弯功能的三层鞘管输送系统设计,第一层引导导管外径为22 F,第二层器械输送鞘管拥有超过90°调弯度功能;C~D.独特设计的二尖瓣夹子采用不同于MitraClip 的弹性自锁功能,夹子自然状态即为关闭状态,从而有效达到瓣叶缘对缘修复的效果
1. 3 研究方法
患者术前采用经胸超声心动图(transthoracic echocardiography,TTE)及经食管超声心动图(trans esophageal echocardiography,TEE)评估瓣膜解剖形态及MR程度,并确定患者是否满足入排标准。手术过程患者全身麻醉,气管插管,建立中心静脉通道、动脉压力监测通道,植入临时起搏导线及安置体外除颤电极等,术中采用实时三维超声心动图及X线引导手术操作。
1. 3. 1 缘对缘瓣膜修复系统置入流程 手术采用经典经股静脉-房间隔路径,患者行股静脉穿刺,TEE引导下行房间隔穿刺,穿刺点位于房间隔后上方、距离二尖瓣环4.0~4.5 cm,穿刺完成后置入左心房导丝,超声引导下将22 F引导导管置入左心房,引导导管进入左心房1.5~2.0 cm,进行排气后,将缘对缘瓣膜修复输送系统通过引导导管置入左心房,在TEE实时引导下,将瓣膜夹准确置入病变目标区域(包括调整夹子轴向,进入左心室,捕获瓣叶,关闭瓣膜夹),超声心动图评估瓣膜夹置入效果满意,MR减轻程度满意,无明显狭窄且瓣膜夹稳定后释放瓣膜夹,撤离输送系统,采用TEE评估手术效果,如有必要,采用同样方式置入第二枚瓣膜夹。手术完成后,撤离输送系统及引导导管,关闭股静脉穿刺口。
1. 3. 2 术后管理 患者术后转入重症监护病房,行常规监护,维持内环境及水、电解质稳定,循环稳定,于术后早期(24 h内)拔出气管导管。密切监测血流动力学参数、心肌标志物、心电图、超声心动图、肾及各器官功能等指标,并记录相应参数及并发症发生情况。术后患者将继续按医嘱使用抗血小板或抗凝药物。
1. 3. 3 研究终点 主要终点为:术后30 d手术成功率(定义是指术后30 d无临床死亡、无本器械造成的二尖瓣瓣膜相关其他手术,超声心动图检测MR≤2+)。次要终点为:术后即刻手术技术成功,试验器械顺利置入并撤回输送系统,无手术死亡,无需任何紧急手术或二次干预,术后30 d全因死亡,心力衰竭再入院等。
1. 4 统计学分析
所有数据采用SPSS 20.0软件进行统计学分析。计量资料用均数±标准差(±s)表示。计数资料用[例(比)]表示。
2 结果
2. 1 12例患者术前临床基线资料(表1)

表1 12 例患者术前基线指标
本研究共收集资料完整且符合入排标准的患者12例。所有患者平均年龄(67.00±8.55)岁,其中男7例,平均身高(160.25±7.39)cm,平均体重(56.00±6.25)kg;NYHA心功能分级Ⅲ级10例,Ⅳ级2例。患者罹患包括慢性阻塞性肺疾病、心肌梗死、外周血管病变、高血压病、脑血管疾病、心房颤动、瓣膜手术史等多种并发症及高危因素。术前超声心动图确认DMR患者1例,FMR患者11例(其中Type Ⅰ型10例,Type Ⅲb型1例)[8];6例患者MR 4+,6例患者MR 3+,MR平均缩流颈宽度(7.68±2.73)mm,平均LVEF(39.1±10.7)%,平均左心室舒张末期内径(59.5±10.2)m m,平均左心室收缩末期内径(45.7±11.8)m m,左心房前后径(44.90±8.13)mm,平均二尖瓣瓣口面积(5.47±1.13)cm2,平均跨瓣压力阶差(1.08±0.29)mmHg(1 mmHg=0.133 kPa)。FMR患者平均对合缘高度(5.09±1.22)mm,对合深度(8.80±1.83)mm。术前平均N末端B型脑钠肽前体(amino-terminal probrain natriuretic peptide,NT-pr oBN P)(3 922±4 414)pg/ml(139~11 389 pg/ml)。
2. 2 12例患者围术期指标及术后30 d主要不良事件
所有患者均成功接受全身麻醉下经导管二尖瓣缘对缘修复,术后即刻技术成功率为100%,所有患者器械均顺利撤出,器械准确置入目标区域(A2/P2区),无围术期死亡及严重不良并发症发生,无紧急外科及介入治疗,其中11例患者均使用1枚二尖瓣夹子(型号长12 mm、宽6 mm),1例患者使用2枚二尖瓣夹子(型号长12 mm、宽6 mm及型号长9 mm、宽6 mm各1枚),术后即刻无MR ≥2+,手术操作时间(定义为可操控引导导管置入房间隔至输送系统撤回到可操控引导导管内)均<90 min,围术期并发症发生情况见表2。

表2 围术期至出院前指标及不良事件[例(比)]
12例患者术后恢复顺利,无严重肾功能不全、致残性卒中、心肌梗死等并发症发生。术后平均住院时间(5.30±1.77)d。术后30 d手术成功率100%,术后30 d随访结果提示无严重心血管临床并发症发生,包括心力衰竭再入院、死亡及器械相关(溶血、器械栓塞、血栓形成、器械断裂等)并发症。术后30 d超声心动图提示MR显著改善,3例患者MR 0,8例MR 1+,1例患者MR 2+(图2)。平均二尖瓣开口面积(3.09±0.70)cm2,平均跨瓣压力阶差(2.40±1.69)mmHg。平均LVEF(42.91±14.32)%,平均左心室舒张末期内径(57.08±12.62)mm(表3)。患者术后30 d状态良好,NYHA心功能分级显著改善,Ⅲ级4例,Ⅱ级6例,Ⅰ级2例(图3)。

图3 患者术前及30 d 随访心功能改善情况
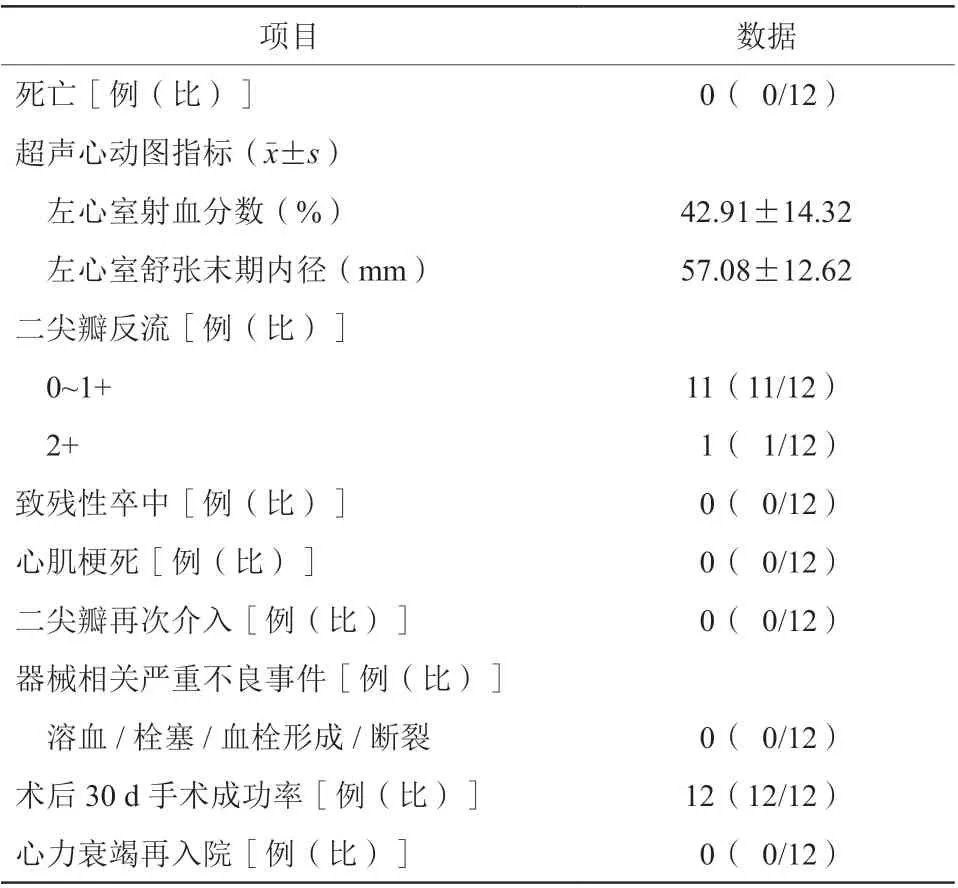
表3 术后30 d 指标及主要不良事件

图2 患者术前、术后及30 d 随访二尖瓣反流改善情况
3 讨论
二尖瓣病变病因相对复杂,根据病因大致可分为原发性和继发性两类,原发性MR为二尖瓣自身病变导致,在高龄患者中其主要构成为DMR。继发性MR指由二尖瓣以外的心脏病变导致的瓣膜病变,其主要为心室或心房功能不全导致的FMR。研究显示,FMR患者是MR患者的主要人群,占70%以上[1,10-11]。凭借EVEREST及COAPT系列研究提供的强有力循证医学证据[3-5],股静脉路径经导管缘对缘介入修复术(MitraClip)已经被美国FDA批准用于外科手术风险极高的DMR及内科最优药物治疗下依旧存在临床症状的FMR患者。
本文报道了首次采用我国自主研发的经股静脉路径缘对缘二尖瓣修复系统(KokaclipTM)的临床研究结果。研究主要纳入了FMR患者及部分DMR患者。研究结果提示,该类器械具有很好的安全性及有效性,围术期及术后30 d随访无严重器械相关不良事件,达到预期治疗结果。该系统在设计上具有一定的优势[9],包括了独特设计的二尖瓣夹子,其采用不同于MitraClip的弹性自锁功能,夹子自然状态即为关闭状态,并具有一定的弹性回缩,在确保夹子关闭锁定绝对可靠的前提下,还可以降低瓣叶夹闭后的二尖瓣应力,瓣叶捕获夹片具有独特的横排及竖排倒刺设计,可以确保稳定捕获瓣叶并分散瓣叶受力及防止夹合器脱落。此外,其拥有二尖瓣瓣叶独立捕获功能,且同时具备四个型号的夹子设计,从而能够适应更复杂的解剖病变,降低手术难度,尤其是长宽型号的夹子,使得绝大部分患者仅需一枚器械便可以达到治疗目的。其输送系统采用经典的三层输送系统设计以及更细的22 F引导导管,技术路径同经典的缘对缘二尖瓣修复器械类似,学习曲线可以相通,从而可以更快更好地使用该类器械治疗MR,为研究的顺利开展提供了坚实基础。
本研究主要纳入了经内科治疗无效的FMR患者(11例),虽然目前针对FMR的COAPT研究已经提示其显著的治疗效果,但MITRA-FR研究结果却为阴性,由于FMR疾病谱众多,包括了房性以及室性FMR,其中室性FMR又可分为缺血性和非缺血性,患者基础情况及瓣膜病变解剖特点均存在差异,其获益人群仍存在争议[12-14]。对于COAPT研究结果的深入分析提示,经导管缘对缘技术治疗FMR能够获益的患者需满足包括最佳药物治疗、MR较重(参考美国超声心动图学会的诊断标准)、左心室未显著增大、解剖合适等条件(即所谓不成比例MR患者)[15-16]。EVEREST系列研究[3-4]也推荐,对于FMR患者的选择需要满足二尖瓣瓣叶对合缘>2 mm,而对合深度<11 mm的标准,从而保证最佳的治疗效果。本研究对于FMR患者的选择也尽可能参考了上述相关研究,研究中FMR患者平均对合缘高度(5.09±1.22)mm,对合深度(8.80±1.83)mm,纳入患者MR平均缩流颈宽度达(7.68±2.73)mm,平均左心室舒张末期内径为(59.5±10.2)mm,从而一定程度上保证了患者的手术效果。研究结果也提示,MR程度降低,NYHA心功能分级改善,进一步证实了手术的良好效果。
本研究作为早期探索性研究存在一定的局限性,其样本量较小、随访时间较短,且纳入了包括DMR及FMR的患者人群,目前研究结果仅能对器械的可行性及安全性进行初步验证,未来大规模法规注册临床研究将为该类产品的临床应用提供更加充分的临床证据。
利益冲突所有作者均声明不存在利益冲突
