利用Lactobacillus kisonensis发酵藜麦-黑燕麦复合谷物富集多酚及黄酮的工艺优化
2023-01-03钟苓玥宋立华
聂 攀,吕 玮,陆 军,钟苓玥,吴 艳,宋立华,
(1.上海交通大学农业与生物学院,上海 200240;2.国家半干旱农业工程技术研究中心,河北石家庄 050011;3.中国科学院上海植物逆境生物学研究中心,上海 201602)
与常规主食谷物稻米和小麦相比,藜麦富含优质蛋白、脂肪酸、维生素、膳食纤维、皂苷和多酚等功能性成分,还含有一般谷物缺乏的限制性氨基酸赖氨酸[1-2];黑色燕麦作为有色谷物,除β-葡聚糖外,还含有花青素等多酚类物质[3-4]。因此,藜麦与黑燕麦均具有改善人体健康、预防慢性疾病的潜在价值[5-6],可用于功能性谷物食品的开发。
全谷物藜麦和黑燕麦中虽含有一定量多酚物质,但其通常与麸皮细胞壁基质组分相连,难以以可溶形式进入人体血液循环实现其活性,造成生物利用率低[7]。研究表明,谷物经微生物发酵后,不但可使细胞壁基质降解,促进酚类物质的释放,还能改善天然谷物的某些不足(如蛋白消化率和矿物质生物利用率低,含有植酸等抗营养因子,保质期较短、适口性和口感差等),赋予谷物更好的感官品质[8-9]。目前在藜麦的发酵加工方面,有研究利用干酪乳杆菌发酵藜麦,使游离酚增加而结合酚减少,总酚含量显著增加[10];邢慧雅[11]利用乳酸菌发酵白藜麦,当接种量为2%、发酵时间为10 h时,藜麦发酵浓浆中多酚含量较发酵前提高18.5%,但黄酮含量较发酵前降低54.6%;韩林等[12]利用酵母菌发酵藜麦,接种量1.7%、料液比1:1.6(g/mL)、发酵时间80 h,发酵后藜麦总酚含量是未发酵的2倍。在利用微生物发酵燕麦富集多酚或黄酮类物质的研究方面,崔江明等[13]利用根霉菌发酵燕麦,使多酚和黄酮含量分别提高46.7%和56.9%;刘燕[14]分别利用红曲霉与枯草芽孢杆菌发酵燕麦,总多酚和总黄酮含量分别是未发酵燕麦的30.2倍和8.3倍。但利用藜麦和黑燕麦进行复合谷物发酵,在充分利用两种谷物营养价值的同时,有效富集多酚和黄酮成分的相关研究较少。
本研究以藜麦与黑燕麦为原料,采用植物乳杆菌发酵,以多酚含量和黄酮含量为响应值,先利用单因素实验明确原料比(藜麦:黑燕麦)、液料比、接种量和发酵时间等发酵工艺参数的优化范围,然后采用响应面法建立优化的发酵工艺,为功能性发酵全谷物食品的开发提供新思路。
1 材料与方法
1.1 材料与仪器
藜麦 青海省海西蒙古族藏族自治州境东部乌兰县(青藜一号);黑燕麦(也称有壳燕麦(A. sativaL.)、皮燕麦) 青海海东互助土族自治县,所用原料均为当年新采收样品;植物乳杆菌(Lactobacillus kisonensis,Watanabe et al. 2009,JCM15041) 由华东理工大学生物反应器工程国家重点实验室馈赠;无水乙醇、福林酚、三氯化铝、碳酸钠、乙酸钾(均为分析纯) 国药集团化学试剂有限公司;95%芦丁、没食子酸(均为分析纯)、耐高温α-淀粉酶(10 U/g)上海阿拉丁生化科技股份有限公司;MRS肉汤培养基配方(g/L):蛋白胨10.0 g,牛肉粉8.0 g,酵母粉4.0 g,葡萄糖20.0 g,磷酸氢二钾2.0 g,柠檬酸氢二铵2.0 g,乙酸钠5.0 g,硫酸镁0.2 g,硫酸锰0.04 g,吐温80 1.0 mL,pH6.5±0.2(25 ℃) 上海盛思生化科技有限公司。取本品52.3 g,用1000 mL蒸馏水,加热至完全溶解,121 ℃高压灭菌20 min。
THC型数控超声波仪 济宁天华超声电子仪器有限公司;DR-3000系列酶标分析仪 无锡华卫德朗仪器有限公司;Legend Micro17高速离心机 德国Thermo Fisher公司;LRH-150培养箱 上海一恒科学仪器有限公司;THE01504B ATC手持糖度计深圳市雅戈科技有限公司。
1.2 实验方法
1.2.1 藜麦与黑燕麦复合谷物发酵工艺流程 复合谷物发酵工艺流程如下:

预处理:藜麦、黑燕麦→清理杂质→粉碎→过筛(80目)→4 ℃保存备用。
复合谷物(藜麦-黑燕麦)酶解液培养基配制:将经粉碎处理的藜麦粉和黑燕麦粉按照不同质量配比混合,然后按照不同料液比加入纯水搅拌混匀,用1 mol/L 盐酸调节pH至6.5,加热升温至70 ℃时加入耐高温α-淀粉酶10 U/g,保温40 min,并以糖度计检测糖度值达到12%为酶解终点,于120 ℃灭菌20 min,灭菌后冷却备用。
菌种活化:从保存Lactobacillus kisonensis菌种的甘油管中吸取30 μL菌液,加入到1.4 mL MRS液体培养基中,混匀,于30 ℃培养箱中培养16 h活化。
接种与发酵:将活化菌株(8.7×108CFU/mL)稀释至1.0×108CFU/mL,按照一定体积比接种到灭菌后的藜麦-黑燕麦复合全谷物培养基中,混合均匀,于30 ℃恒温培养箱中密封避光发酵,即得到发酵原液。
1.2.2 单因素实验
1.2.2.1 原料比(藜麦与黑燕麦)的优化 根据预实验,固定液料比为7:1(mL/g)、接种量3%、发酵时间36 h、发酵温度30 ℃,研究不同藜麦与黑燕麦配比(5:1、3:1、1:1、1:3、1:5)(g/g)对发酵谷物多酚和黄酮含量的影响。同时设置藜麦组(Q)和黑燕麦组(BO)作为对照,其单独发酵工艺条件同上述复合谷物。
1.2.2.2 液料比的优化 固定藜麦与黑燕麦配比为1:1(g/g)、接种量3%、发酵时间36 h、发酵温度30 ℃,研究不同液料比(3:1、5:1、7:1、9:1、11:1)(mL/g)对发酵谷物多酚和黄酮含量的影响。
1.2.2.3 接种量的优化 固定藜麦与黑燕麦配比1:1(g/g)、液料比7:1(mL/g)、发酵时间36 h、发酵温度30 ℃,研究不同接种量(0%、1%、2%、3%、5%、7%)对发酵谷物多酚和黄酮含量的影响。
1.2.2.4 发酵时间的优化 固定藜麦与黑燕麦配比1:1(g/g)、液料比7:1(mL/g)、接种量3%、发酵温度30 ℃,研究不同发酵时间(12、24、36、48、60 h)对发酵谷物多酚和黄酮含量的影响。
1.2.3 响应面试验 在1.2.2中单因素实验的基础上,采用Box-Behnken模型的中心组合试验设计原理对藜麦与黑燕麦复合谷物发酵工艺进行优化,以原料比(藜麦:黑燕麦)、液料比、接种量和发酵时间作为自变量,设计四因素三水平响应面试验,并以多酚和黄酮含量为响应值(如表1)。

表 1 响应面试验设计表Table 1 Horizontal coding table of response surface factors
1.2.4 藜麦和黑燕麦复合谷物发酵与单独发酵富集效果的比较 采用1.2.3中优化后的发酵工艺制备藜麦-黑燕麦复合谷物,并采用相同的发酵工艺制得藜麦发酵物和黑燕麦发酵物,比较藜麦-黑燕麦复合谷物发酵物与单独发酵(藜麦发酵物和黑燕麦发酵物)中多酚和黄酮含量差异。
1.2.5 多酚的检测 采用Folin-Ciocalteu比色法[15]:取混匀发酵液0.200 g,加入1.8 mL 70%乙醇溶液,涡旋混匀后超声(200 W、30 ℃)提取30 min,4000 r/min离心10 min后取上清液0.1 mL,加入0.2 mL福林酚试剂、0.6 mL碳酸钠溶液(8%)和0.1 mL蒸馏水,漩涡混匀,30 ℃下避光静置1 h后在760 nm波长处测定吸光度;以没食子酸为标准品,测得工作曲线线性方程为:y=3.1517x+0.0544,R2=0.9962,以没食子酸当量(mg/100 g)计算多酚含量,同时做空白对照。注:如有沉淀则在8000 r/min下离心5 min后取上清液进行吸光度测定。
1.2.6 黄酮的检测 参考董晶等[16]的方法:取混匀发酵液0.200 g,加入1.0 mL 80%乙醇溶液,漩涡混匀后超声(200W、45 ℃)提取40 min,4000 r/min离心10 min后取上清液0.5 mL,加入0.2 mL三氯化铝溶液(0.1 mol/L)、0.3 mL乙酸钾溶液(1 mol/L),涡旋混匀,避光静置30 min后在405 nm下测定吸光度;以芦丁为标准品,测得工作曲线线性方程为:y=6.7009x+0.0417,R2=0.9992,以芦丁当量(mg/100 g)计算黄酮含量,同时做空白对照。
1.3 数据处理
采用单因素方差分析(one-way ANOVA)通过LSD多重比较检测各组平均值之间的差异(SPSS Statistics 21),并分别以P<0.05和P<0.01作为差异显著和极显著的判断标准。应用GraphPad Prism 8.2.1软件作图,所有数据均以“平均值±标准差”的形式表示。

图 1 原料比(藜麦:黑燕麦)对发酵复合谷物中多酚和黄酮含量的影响Fig.1 Effect of raw material ratio (quinoa:black oat) on polyphenols and flavonoids contents after fermentation
2 结果与分析
2.1 单因素实验
2.1.1 原料比(藜麦:黑燕麦)对发酵复合谷物中多酚和黄酮含量的影响 图1为原料比(藜麦:黑燕麦)对发酵复合谷物中多酚和黄酮含量的影响。当复合谷物原料比为1:3和1:5(g/g)时,多酚含量显著高于其他比例组和藜麦与黑燕麦单独发酵组(P<0.05);原料比为1:5(g/g)时,黄酮含量显著高于其他比例组和藜麦与黑燕麦单独发酵组(P<0.05)。原料比为1:3和1:5(g/g)可使多酚和黄酮含量分别达到最大值。这可能是因为合适比例的复合谷物其营养成分组成更均衡,可为乳酸菌的生长和多酚类次级代谢产物的合成提供足够的营养支持;生长良好的植物乳杆菌能产生丰富的复合分解酶系[17-18],有利于多酚和黄酮物质的释放,从而使发酵后复合谷物中多酚和黄酮含量升高。可见,与单独发酵藜麦或黑燕麦相比,合理比例的复合谷物发酵可更有利于多酚和黄酮含量富集。因此,本研究选取原料比(藜麦:黑燕麦)1:1、1:3、1:5(g/g)作为响应面优化试验的水平。
2.1.2 液料比对发酵复合谷物中多酚和黄酮含量的影响 图2所示为液料比对发酵复合谷物多酚和黄酮含量的影响。总体上来看,当液料比≤7:1(mL/g)时,多酚物质和黄酮物质随着液料比的增加而提高;液料比为7:1(mL/g)时,二者均显著富集,达到最大值(P<0.05),分别为285.4和211.9 mg/100 g;当液料比>7:1时,多酚和黄酮含量则均呈下降趋势,与已有部分研究结果相一致[12,19]。液料比较低(≤5:1(mL/g))时,发酵基质黏度增大,影响传质效率,从而影响发酵菌的生长和多酚及黄酮等次级代谢产物的合成[19-20];液料比过高(≥9:1(mL/g))时,过多的水分稀释了培养基中营养物质的浓度,微生物也不能充分利用谷物中的营养物质,从而影响多酚和黄酮的合成[19]。可见,只有适宜的液料比(7:1(mL/g))才可为乳酸菌的生长繁殖提供良好的发酵环境,从而有利于多酚和黄酮物质富集。因此,本研究选取液料比5:1、7:1、9:1(mL/g)作为响应面优化试验的水平。

图 2 液料比对发酵复合谷物中多酚和黄酮含量的影响Fig.2 Effect of liquid-solid ratio on polyphenols and flavonoids contents after fermentation
2.1.3 接种量对发酵复合谷物中多酚和黄酮含量的影响 由图3可知,发酵后多酚及黄酮含量均显著高于未发酵组。微生物能以芳香氨基酸(如酪氨酸和苯丙氨酸)为前体物质,在酶的作用下异源合成多酚和黄酮等次级代谢产物[21];此外,微生物代谢过程中产生的多种酶会导致谷物细胞壁降解,也有利于多酚和黄酮物质的释放[22-24],使得发酵后谷物多酚和黄酮得以富集。但发酵工艺不同,富集效果有所不同。本研究发现不同接种量对藜麦-黑燕麦发酵复合谷物中多酚和黄酮富集效果有一定影响:随着接种量的增加,多酚和黄酮含量总体呈先上升后下降趋势,两者都在5%接种量下达到最大值,变化趋势同已有研究结果基本一致[25-26]。这是因为在适宜的接种量(1%~5%)下,液体培养基能为发酵菌的生长提供足够底物,发酵比较充分,产酶效果好,有利于多酚和黄酮次级代谢产物的累积;而当接种量增加至7%时,由于发酵菌数量较多,导致培养基不能满足其生长所需的原料,促进酒精和酸等产物的累积,反而限制多酚及黄酮类产物的合成[27]。因此,本研究选取接种量3%、5%、7%作为响应面优化试验的水平。

图 3 接种量对发酵复合谷物中多酚和黄酮含量的影响Fig.3 Effect of inoculation amount on polyphenols and flavonoids contents after fermentation
2.1.4 发酵时间对发酵复合谷物中多酚和黄酮含量的影响 从图4可以看出,发酵时间对发酵复合谷物中多酚和黄酮含量也存在一定影响。发酵时间在12~60 h范围内,多酚含量先上升后下降,发酵至36 h达到最大值(P<0.05),但与发酵24 h差别不大,继续延长发酵时间,多酚含量反而显著降低(P<0.05)。类似地,发酵时间在12~48 h范围内时黄酮含量呈上升趋势,发酵至48 h黄酮含量最高,继续发酵黄酮含量反而下降,与已有研究结果相一致[28-30]。

图 4 发酵时间对发酵复合谷物中多酚和黄酮含量的影响Fig.4 Effect of fermentation time on polyphenols and flavonoids contents after fermentation

图 5 各发酵工艺参数交互作用对藜麦-黑燕麦发酵后多酚富集效果的影响Fig.5 Effects of interaction of fermentation parameters on polyphenol enrichment after fermentation of quinoa and black oat
发酵初期,多酚含量(发酵0~12 h)和黄酮含量(发酵0~24 h)较低,这是因为在较短的发酵时间内乳酸菌生长不充足,复合谷物中的营养物质未被充分利用,导致发酵不充分;而随着发酵时间的延长,微生物得以生长繁殖,分泌的酶增加,促进多酚和黄酮等次级代谢产物的形成;到发酵后期(发酵超过48 h),多酚和黄酮含量反而降低,这是因为乳酸菌的生长进入了衰亡期,由于部分发酵菌种死亡,细胞内的多种酶被释放出来,造成多酚、黄酮氧化、消化或降解[19-20,31]。因此,本研究选取发酵时间24、36、48 h作为响应面优化试验的水平。
2.2 响应面优化藜麦-黑燕麦复合谷物发酵工艺
2.2.1 响应面优化试验结果 利用软件Design-Expert设计响应面试验,对藜麦-黑燕麦复合谷物发酵工艺参数进行优化,以原料比(藜麦:黑燕麦)、液料比、接种量和发酵时间这四个因素作为自变量,以多酚(Y1)和黄酮含量(Y2)为响应值,建立藜麦-黑燕麦复合谷物的优化发酵工艺,试验设计及结果如表2所示。

表 2 响应面试验设计及结果Table 2 Response surface experiment design and results
2.2.2 响应面模型建立与方差分析 多酚富集效果回归模型方差分析结果如表3所示。从表3可以看出该模型显著性检验P<0.01,且失拟项(表示所用模型与实验拟合的程度)P值为0.1194>0.05,差异不显著;模型的决定系数R2=0.9533,校正决定系数R2Adj=0.9065,模型的变异系数CV=0.7509%,进一步说明该模型具有很好的稳定性,实际值与预测值具有较好的拟合相关性。综上,该模型对藜麦-黑燕麦复合谷物发酵物中多酚富集效果分析具有实际应用价值。
由表3可知,该模型一次项A原料比(藜麦:黑燕麦)、B液料比、C接种量和D发酵时间对复合谷物发酵多酚富集作用的影响均为显著水平(P<0.05);二次项四个因素的影响均达到极显著水平(P<0.01);各因素对响应值的影响并不是简单的线性关系。由F值可以确定,各因素对复合谷物多酚含量影响的重要顺序依次为:原料比(藜麦:黑燕麦,A)>发酵时间(D)>液料比(B)>接种量(C)。通过Design-Expert软件对复合谷物多酚含量进行回归模型拟合,得到复合谷物发酵液多酚含量(Y1)与原料比、液料比、接种量、发酵时间之间的多元二次回归模拟方程:


表 3 多酚富集效果回归模型方差分析Table 3 Variance analysis of regression model (polyphenols)
黄酮富集效果回归模型方差分析结果如表4所示。从表4可以看出该模型显著性检验P<0.01,且失拟项(表示所用模型与实验拟合的程度)P值为0.0822>0.05,差异不显著;模型的决定系数R2=0.9535,校正决定系数R2Adj=0.9070,变异系数CV=0.7482%,进一步说明该模型具有较好的稳定性,实际值与预测值具有较好的拟合相关性。综上,该模型对藜麦-黑燕麦复合谷物发酵物中黄酮富集效果分析具有实际应用价值。
由表4可知,一次项中A原料比(藜麦:黑燕麦)、B液料比、C接种量和D发酵时间这四个因素对复合谷物黄酮富集作用的影响均为极显著水平(P<0.01)。二次项中除了发酵时间外,其余三个因素对响应值(Y2)的影响均达到极显著水平(P<0.01)。交互项中CD项对响应值(Y2)具有显著影响(P<0.05)。根据F值可以判断,各因素对复合谷物黄酮含量的影响次序为:接种量(C)>原料比(藜麦:黑燕麦,A)>发酵时间(D)>液料比(B)。通过Design-Expert软件对复合谷物黄酮含量进行回归模型拟合,得到复合谷物发酵液黄酮含量(Y2)与原料比、液料比、接种量、发酵时间之间的多元二次回归模拟方程:
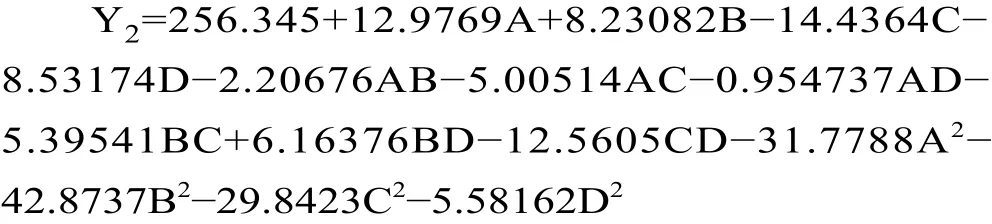

表 4 黄酮富集效果回归模型方差分析Table 4 Regression model variance analysis (flavonoids)
2.2.3 各因素间的交互作用对复合谷物发酵后多酚及黄酮富集效果的影响
2.2.3.1 各因素交互作用对复合谷物发酵后多酚含量的影响 图5a~图5f为各因素交互作用对复合谷物发酵后多酚含量影响的响应面图。从图中可看出,响应面均呈现比较陡峭的山丘状曲面且存在极大值,说明原料比(藜麦:黑燕麦)、液料比、接种量和发酵时间对复合谷物中多酚富集效果均有影响,与方差分析结果一致;根据图5a、5d、5e和5f所示,液料比分别与原料比、接种量、发酵时间的交互及发酵时间与接种量交互等高线呈近椭圆状,表明其交互作用对复合发酵谷物富集多酚有一定影响,但影响不显著(P>0.05)。
2.2.3.2 各因素对复合谷物中黄酮含量的交互影响
各因素交互作用对黄酮含量的影响如图6a~图6f所示。其中原料比与液料比、接种量及发酵时间和液料比与接种量及发酵时间之间的交互作用对黄酮富集效果影响不显著(P>0.05)。从图6f可以看出,接种量的坡面较陡峭且发酵时间的曲线不平滑,两者间的等高线呈椭圆状,其交互作用对复合谷物发酵后黄酮的富集效果影响显著(P<0.05),黄酮含量随接种量增加呈先上升后下降趋势,表明回归方程存在极大值。提示本研究中对于黄酮的富集,在相同发酵菌种条件下,原料比和液料比直接影响到发酵时间,进而影响到接种量,而接种量和发酵时间可显著影响黄酮次级代谢产物的富集。
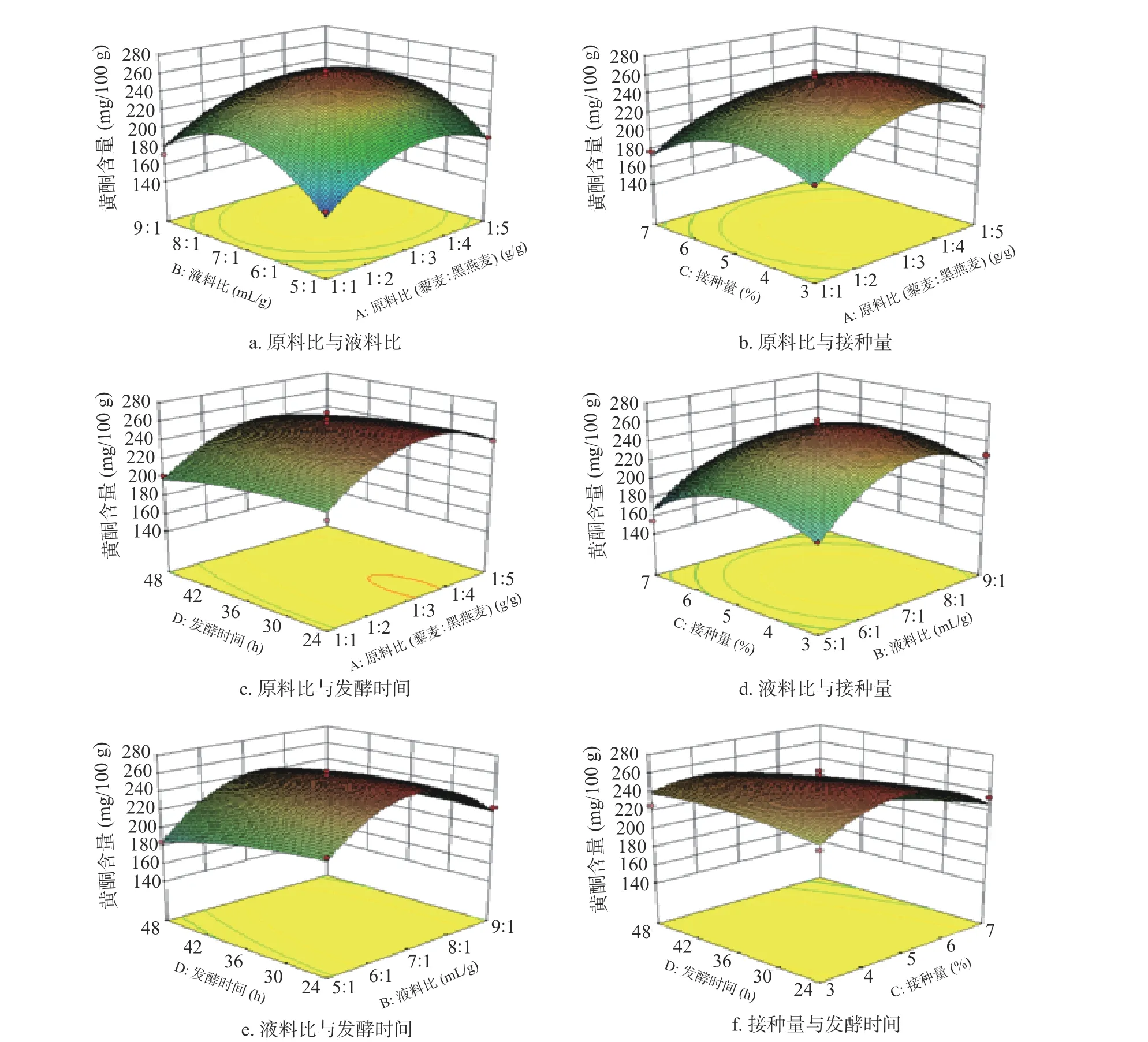
图 6 各发酵工艺参数交互作用对藜麦-黑燕麦发酵后黄酮富集效果的影响Fig.6 Effects of interaction of fermentation parameters on flavonoids enrichment after fermentation of quinoa and black oat
本研究通过分析藜麦和黑燕麦复合谷物发酵工艺优化过程中各因素及交互作用对多酚和黄酮富集效果的影响,表明对于不同次级代谢产物,各交互作用影响程度有所不同,其具体机制尚有待于进一步阐明。
2.3 藜麦-黑燕麦复合优化发酵工艺条件的确定
藜麦与黑燕麦复合谷物发酵优化的工艺参数如下:原料比(藜麦:黑燕麦)1:3.357(g/g)、液料比7.490:1(mL/g)、接种量4.927%、发酵时间36.467 h。在此工艺条件下发酵后多酚和黄酮含量预测值分别为299.4和257.3 mg/100 g。验证实验中考虑到实际加工条件,将发酵工艺调整为原料比(藜麦:黑燕麦)1:3.4(g/g)、液料比7.5:1(mL/g)、接种量4.9%、发酵时间36.5 h。经验证,在该条件下,复合谷物发酵液中多酚和黄酮含量分别为295.3和256.3 mg/100 g(表5),RSD分别为0.99%和0.27%,预测值与实际值相近,说明本次所建立的响应面模型对藜麦-黑燕麦复合谷物发酵有效富集多酚和黄酮具有较好的实际应用价值。
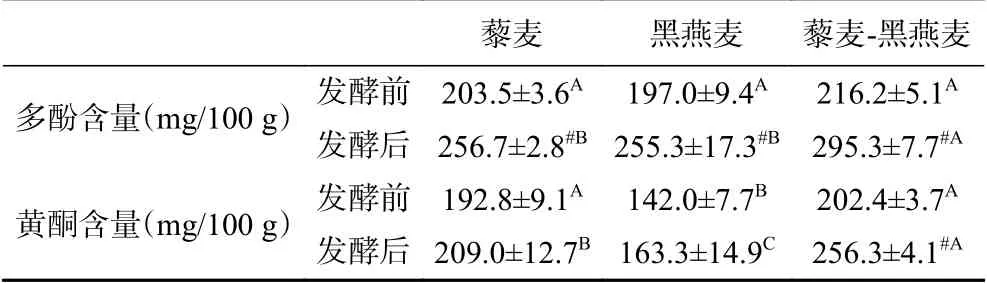
表 5 藜麦-黑燕麦复合谷物发酵与两谷物单独发酵后多酚和黄酮富集效果对比Table 5 Comparison of polyphenol and flavonoid enrichment effect between quinoa-black oat complex grain fermentation and two grains fermentation alone
2.4 藜麦和黑燕麦复合谷物发酵与单独发酵多酚和黄酮富集效果的比较
与单独发酵藜麦和黑燕麦相比,藜麦-黑燕麦复合谷物发酵能使多酚含量分别提高15.04%、15.67%(P<0.05),黄酮含量分别提高了22.63%、56.95%(P<0.05)。此外,与各自对应的未发酵组相比,藜麦、黑燕麦、藜麦-黑燕麦组合发酵后多酚含量分别提高了26.14%、29.59%和36.59%(P<0.05),藜麦-黑燕麦复合谷物发酵组黄酮含量显著提高了26.63%(P<0.05);而藜麦、黑燕麦单独发酵前后黄酮含量差异不显著(P>0.05)。上述说明藜麦-黑燕麦复合谷物发酵较两种谷物单独发酵可显著改善多酚和黄酮的富集效果(如表5所示)。这可能是因为藜麦-黑燕麦复合谷物基质营养成分组成较单一组分丰富,能为植物乳杆菌生长提供更适宜的营养支持,良好的生长环境促进次级代谢产物合成相关酶及蛋白的表达,有利于多酚类和黄酮类物质的合成代谢,但具体机制尚有待于深入研究。
3 结论
本文以藜麦与黑燕麦为原料,利用植物乳杆菌发进行复合谷物发酵,建立可有效富集谷物多酚及其组分黄酮的优化发酵工艺条件。实验结果表明,复合谷物配比(藜麦:黑燕麦)、液料比、接种量和发酵时间对多酚和黄酮的富集均具有显著影响。藜麦-黑燕麦复合谷物发酵的最优工艺条件为:原料比(藜麦:黑燕麦)1:3.4(g/g)、液料比7.5:1(mL/g)、Lactobacillus kisonensis接种量4.9%、发酵时间36.5 h。在该条件下藜麦与黑燕麦复合谷物中多酚和黄酮含量可达
295.3和256.3 mg/100 g,均显著高于两种谷物各自单独发酵后多酚和黄酮含量(P<0.05)。本研究为利用全谷物复合发酵富集抗氧化活性成分、开发健康发酵谷物食品提供可参考的理论依据。但复合谷物发酵后多酚类物质的具体组成及含量、风味成分的变化规律等理化特性、以及发酵复合谷物食品的安全性和健康作用等尚值得广泛深入的研究。此外谷物和发酵菌种不同,发酵工艺参数及其对功能性次级代谢产物的富集作用影响有所不同,其机制也有待于进一步研究。
