氢氧化镁改性纤维素制备及对Cu(Ⅱ)的吸附
2022-12-30管彬伟赵建海任小雨
管彬伟,赵建海,任小雨
(a.天津城建大学 环境与市政工程学院;b.天津市水质科学与技术重点实验室,天津 300384)
近年来,由于冶炼、采矿、化工等工业的快速发展,重金属污染日益严重,被重金属废水污染的水体往往给人类和水生动植物带来严重影响[1].每天都有大量有毒污染物,如重金属离子铜、镉、铅、砷、汞等排放到水体中,对各类生物的毒性浓度均高于允许值[2].根据世界卫生组织提出的限值,工业废水中Cu(II)的允许限值为1 mg/L[3].Cu(II)是一种低成本的金属离子,其用途广泛,是工业排放中最大的污染物,因此从废水中降解或去除Cu(II)对于水环境保护非常重要[4].
目前,去除铜离子的方法有如下几种:反渗透法、离子交换法、化学沉淀法、气浮法、电解法、吸附法和膜分离法等[5].化学沉淀法和吸附法是去除废水中铜离子最常用的方法[6-7].吸附法是对低浓度废水进行净化的最具成本效益和环境可持续的方法之一,从无机改性材料到来自各种生物质的天然活性炭等众多材料已被成功用于去除染料、重金属离子、有机污染物等[8].虽然这些材料具有一定的去除效率,同时也存在许多缺点,例如吸附剂的来源、环境可持续性、成本效率、再生能力和来源可再生性[9].这就迫使研究人员进一步研究新型吸附剂弥补以上缺点.因此,纤维素等天然可再生资源的开发吸引了人们的关注[10].
纤维素是一种低成本、低污染的吸附剂,纤维素吸附剂有粉末状、颗粒状和球状[11-12].纤维素作为吸附剂具有价格低廉、无毒安全、不会造成环境污染等优点[13-14].氢氧化镁具有很强的吸附能力,在酸性废水中和、土壤pH值调节等环保领域得到越来越多的应用,可用于去除重金属离子、氨氮和有机废水,但单独使用处理效果不显著;同样单独用纤维素作吸附剂时,其吸附容量小,选择性低,去除废水效果不够理想[15-16].为了使纤维素达到所预期的吸附性能,需要对其进行改性,因此本实验采用“浸渍-共沉淀”的方法在纤维素上原位负载氢氧化镁,制备出氢氧化镁改性纤维素吸附剂.利用改性吸附剂对对铜离子进行吸附研究,重点探讨改性吸附剂的制备条件及材料特性分析.
1 实验部分
1.1 试剂与仪器
实验所用纤维素由上海誉宇科技有限公司生产,并通过GB/T 19001—2014质量体系认证.本实验所用试剂均为分析纯试剂(AR),实验所用药品及厂家如下:MgCl2·6H2O(天津光复)、NaOH(天津风船)、HCl(上海泰坦)、CuSO4(天津科威)、HNO3(北京南固新光).
实验中所用仪器的型号及厂家如表1所示.

表1 实验仪器清单
1.2 氢氧化镁改性纤维素(Mg(OH)2-CM)改性材料的制备
(1)取一定量的纤维素,浸泡在稀盐酸中进行预处理,过滤并干燥以后备用.
(2)用去离子水配制一定浓度的氯化镁溶液100 mL,与3 g预处理的纤维素一起放入250 mL锥形瓶中,将锥形瓶放入恒温水浴振荡器中,使氯化镁与纤维素充分反应.
(3)用真空过滤器从氯化镁溶液中分离出负载镁离子的纤维素,将分离出的Mg-CM干燥,然后转至250 mL锥形瓶中.
(4)配制一定浓度的氢氧化钠溶液,通过蠕动泵泵入锥形瓶中,同时将锥形瓶置于磁力搅拌器上搅拌,恒温水浴控制温度,使氢氧化钠和氯化镁在纤维素上原位生成氢氧化镁.
(5)将反应制得的氢氧化镁改性纤维素改性材料在真空过滤器下用蒸馏水反复洗涤,直至滤液中的pH值基本稳定在同一值,取出沉淀物,100℃烘干后研磨备用.
1.3 吸附实验
将100 mL质量浓度为50 mg/L、pH值为5的铜离子溶液加入不同的250 mL锥形瓶中,并分别加入0.2 g不同制备条件下的氢氧化镁改性纤维素.在一定温度下进行静态吸附实验.用10 mL注射器取其上清液,经0.45 μm微孔滤膜过滤后,利用火焰原子吸收法测Cu2+的浓度.
为了确定不同制备条件下制备出的改性材料对铜离子的吸附效果,用火焰原子吸收法测量其中Cu2+的浓度并计算吸附剂的平衡吸附量,平衡吸附量计算公式如下:

式中:qe为平衡吸附量(mg/g);c0为初始浓度(mg/L);ce为平衡浓度(mg/L);V为溶液的体积(L);M为吸附剂的质量(g).
1.4 材料的表征
(1)测定改性材料中氢氧化镁的负载量.氢氧化镁的负载量的测定采用酸提取法[17].取载有氢氧化镁改性纤维素的材料1 g,将其放入盛有100 mL pH=1盐酸的250 mL锥形瓶中,置于恒温水浴振荡器中,25℃振荡10 h,通过针管式过滤器过滤,用离子色谱法测定镁离子含量.氢氧化镁的负载量由下式计算:

(2)氢氧化镁在改性材料中的稳定性.进行氢氧化镁负载在纤维素上的稳定性试验,以了解改性吸附材料的稳定性能.将100 mL去离子水的pH值分别调节为3、4、5、6、7,放入250 mL锥形瓶中,然后加入1 g氢氧化镁改性纤维素改性材料置于锥形瓶,并在25℃恒温水浴振荡器振荡3 h,利用离子色谱法测定镁离子含量,并以此计算氢氧化镁的溶解率.
(3)材料物性分析.对吸附材料进行了FTIR、SEM、BET和XRD表征分析.
2 结果与讨论
2.1 制备条件对氢氧化镁改性纤维素吸附性能的影响
2.1.1 氯化镁浓度对改性纤维素吸附性能的影响
选用浓度为0.75 mol/L的氢氧化钠溶液50 mL,在反应温度为25℃、反应时间为60 min时,探讨不同氯化镁浓度对改性纤维素吸附性能的影响,并且氯化镁浸泡纤维素的温度在后续实验中一直保持40℃,氯化镁浸泡纤维素的时间在后续实验中一直保持120 min;吸附条件也保持恒定,吸附时间为80 min,吸附温度为25℃,铜离子溶液初始浓度为50 mg/L,溶液pH值为5,吸附剂投加量为200 mg,结果如图1所示.

图1 氯化镁溶液浓度对改性纤维素吸附性能的影响
由图1可以看出,制备Mg(OH)2-CM吸附剂所用氯化镁溶液浓度较低时,对铜离子仍具有吸附效果,是因为氢氧化镁本身具有吸附性,当氯化镁浓度由0.2 mol/L增加至1.0 mol/L,铜离子吸附量由17.0 mg/g增加至18.16 mg/g,这是由于氢氧化镁负载于纤维素上,氢氧化镁和纤维素都具有吸附性能,两者结合可发挥协同作用,以优化其吸附性能.当氯化镁溶液的浓度超过1.0 mol/L时,吸附量开始下降,这是因为氢氧化镁颗粒随氯化镁浓度的增加在纤维素内部结构中逐渐形成,降低了比表面积,导致吸附量下降[18].因此1.0 mol/L是制备改性吸附材料的最佳氯化镁浓度.
2.1.2 氢氧化钠浓度对改性纤维素吸附性能的影响
选用浓度为1.0 mol/L的氯化镁溶液100 mL,在反应温度为25℃、反应时间为60 min时,探讨不同氢氧化钠浓度对改性纤维素吸附性能的影响,结果如图2所示.

图2 氢氧化钠溶液浓度对改性纤维素吸附性能的影响
由图2可以看出,随着氢氧化钠溶液浓度的增加,吸附剂对溶液中铜离子的吸附能力在一定范围内增加,这是由于Mg(OH)2-CM吸附剂协同发挥氢氧化镁和纤维素共同的吸附作用吸附铜离子,而在制备氢氧化镁过程中,氢氧化钠溶液的浓度变化,会影响氢氧化镁颗粒的大小和形态,进而影响改性吸附剂的吸附效果[19].当氢氧化钠浓度为1.25 mol/L时其吸附量达到最大.随后开始下降,这是OH-浓度的不同,会使镁离子和氢氧根离子的配比不同,影响氢氧化镁颗粒的形状,因此将氢氧化钠溶液浓度为1.25 mol/L作为后续实验制备最佳条件.
2.1.3 反应温度对改性纤维素吸附性能的影响
选用浓度为1.0 mol/L的氯化镁溶液100 mL,在氢氧化钠浓度为1.25 mol/L的条件下,探究反应温度对改性纤维素吸附效果的影响,结果如图3所示.
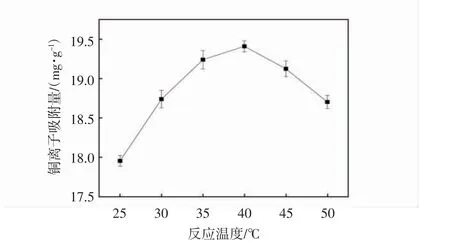
图3 反应温度对改性纤维素吸附性能的影响
由图3可以看出,温度从25℃上升到40℃,铜离子吸附量从17.95 mg/g增加到19.41 mg/g,从40℃到50℃,铜离子吸附量从19.41 mg/g下降18.62 mg/g.随着材料制备温度的升高,Mg(OH)2-CM吸附剂对铜离子的去除率逐渐升高然后逐渐下降,但铜吸附量的下降幅度不大.材料制备过程中的温度会影响氢氧化镁的形状和尺寸[19].低温有助于产生晶核,过饱和度大,形成小尺寸的产物,从而有更多小粒径氢氧化镁负载于纤维素上;温度升高有利于晶体的生长,导致氢氧化镁粒径增大,并且温度升高有利于化学反应的进行,但是纤维素的承载能力有限,氢氧化镁粒径大,会堵塞纤维素的孔隙,从而影响吸附效果.因此选择40℃作为最佳的反应温度.
2.1.4 反应时间对改性纤维素吸附性能的影响
选用浓度为1.0 mol/L的氯化镁溶液100 mL,氢氧化钠浓度为1.25 mol/L、反应温度为40℃的条件下,探究反应时间对改性纤维素吸附效果的影响,结果如图4所示.

图4 反应时间改性纤维素吸附性能的影响
由图4可以看出,时间从20 min到100 min,铜离子吸附量从18.04 mg/g增加到20.14 mg/g,反应时间从100 min到140 min,铜离子吸附量逐渐稳定.随着反应时间的增加,Mg(OH)2-CM吸附剂对铜离子的吸附量逐渐增加,到反应时间为100 min时铜离子的吸附量保持稳定,铜离子的吸附量随着时间增加而快速上升是由于氢氧化钠与氯化镁得到充分反应生成氢氧化镁,但随着反应时间的增加,氢氧化镁已经负载于纤维素上不再增加,之后趋于稳定,因此选择100 min作为最佳的反应时间.
2.2 氢氧化镁改性纤维素改性材料的表征
2.2.1 氢氧化镁负载量的测试
不同氯化镁浓度时改性纤维素的氢氧化镁负载量,结果如表2所示.随着氯化镁浓度的升高,氢氧化镁负载量逐渐增大.氯化镁浓度为1.0 mol/L时,氢氧化镁负载量达到9.77%.继续增大镁离子浓度,吸附量下降.这是因为过高的负载量会使纤维素的孔隙被氢氧化镁堵塞,降低对废水中Cu2+的吸附效率[20].因此,最优氯化镁浓度为1.0 mol/L,此时氢氧化镁负载量为9.77%.由此可得,氯化镁溶液浓度是材料中氢氧化镁的负载量的主要影响因素.

表2 不同氯化镁浓度时改性纤维素的氢氧化镁负载量
2.2.2 氢氧化镁在改性材料中的稳定性
对改性纤维素中的氢氧化镁进行稳定性测试,使用在最佳制备条件下的氢氧化镁改性纤维素,结果如表3所示.由表3可见,随着pH值的不断增大,氢氧化镁的溶出率也逐渐降低,但总体来说溶出率的大小满足吸附剂的吸附条件[21].

表3 不同pH条件下氢氧化镁的溶出率
2.2.3 扫描电镜分析
图5为未改性纤维素和氢氧化镁改性纤维素的扫描电镜表征图.由图5(a)可见,未改性纤维素的表面形貌不规则,但相对较为光滑;氢氧化镁改性过的纤维素(图5b)表面粗糙,露出不规则的密集针状外观,由于在纤维素的表面和层间结构中生成了氢氧化镁,使纤维素的结构发生了改变,改性后纤维素的这些变化均利于吸附反应的进行.

图5 CM和Mg(OH)2-CM的SEM图
2.2.4 X射线衍射分析
图6为CM和Mg(OH)2-CM的XRD图谱.图6显示,纤维素和改性纤维素上均有明显的衍射峰,衍射角为14.9°、16.8°和22.9°分别对应纤维素(110)、(110)和(200)晶面衍射峰[22],Mg(OH)2-CM与CM的主要衍射峰基本相同,说明纤维素的主要结构未被破坏,从XRD图谱可知,在37.96°、50.78°和58.64°处分别出现了特征衍射峰,与标准卡片GBPDS07-0239J相匹配[23],对应于六方晶型氢氧化镁(101)、(102)、(110),说明成功制备了氢氧化镁改性纤维素复合吸附材料.

图6 原纤维素和改性纤维素的XRD图谱
2.2.5 比表面积和孔容测试
氢氧化镁改性前后纤维素的比表面积及孔体积参数如表4所示.由表4可知,Mg(OH)2-CM的比表面积发生了变化,由1.773 m2/g增至80.786 m2/g,总孔容积比未改性纤维素有所增加,这是因为改性后生成了颗粒较小的氢氧化镁,填充了纤维素的夹层和表面,从而增加了纤维素的比表面积和孔容.平均孔径也比未改性纤维素增大,这可能是由于部分新生成的氢氧化镁负载在纤维素表面,堵塞了改性纤维素的微孔,另外的氢氧化造成中孔数量增加[31].

表4 吸附剂的比表面积及孔体积参数
2.2.6 FTIR表征
为了进一步证明氢氧化镁是否成功负载在纤维素表面,用红外表征从官能团的角度对改性前后两种纤维素进行分析对比,图7为改性前后纤维素的红外光谱图.由图7可知,在2 878 cm-1处的吸收峰为甲基和亚甲基上的C—H键伸缩振动引起,在1 641 cm-1处有吸收峰,归因于水分子中H—OH的伸缩振动和O—H的弯曲振动[24-25].羟基的伸缩振动频率一般出现在3 700~3 000 cm-1区间,在3 699 cm-1处的吸收峰主要是自由基O—H的伸缩振动产生的,与未改性纤维素(图中b)相比,改性纤维素(图中a)在3 699 cm-1和1 432 cm-1处出现了新的吸收峰,为氢氧化镁的特征吸收峰[26-29].由此可知,改性纤维素仍保留原有大部分氨基和羟基等基团,同时氢氧化镁成功负载于纤维素上.
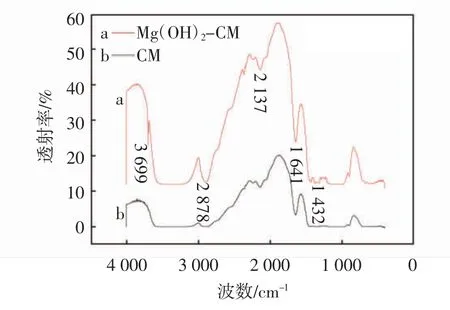
图7 纤维素和改性纤维素红外光谱分析
2.3 吸附性能研究
当吸附温度为45℃、溶液pH值为5时,用五水硫酸铜分别配制100 mL、50 mg/L的Cu2+溶液置于250 mL的锥形瓶中,投加2种吸附剂各200 mg,研究不同时间2种吸附剂的吸附性能,并分别于30、60、90、120、150、180、210 min时取出锥形瓶,取上清液用针头滤器过滤,稀释相应倍数至火焰原子收光谱仪检测范围,测定滤液中Cu2+浓度.改性前后纤维素在不同吸附时间下对铜离子吸附量的影响如图8所示.

图8 不同吸附时间下2种吸附剂吸附铜离子的对比
由图8可知,Mg(OH)2-CM和CM对溶液中铜离子都有吸附能力,但在同一吸附时间下,Mg(OH)2-CM对Cu2+的吸附能力明显高于CM,吸附时间达到150min时,Mg(OH)2-CM对Cu2+的吸附量达到22.89 mg/g,而此时CM对Cu2+的吸附量为13.59 mg/g,Mg(OH)2-CM对Cu2+的吸附量是CM对Cu2+的吸附量的1.65倍,说明改性后的纤维素的吸附性能增强.李振等[30]采用Mg(OH)2对天然硅藻土进行改性,并应用于处理含Cd2+废水,结果表明,改性材料具有粒径小、晶型好、结晶度高、分布比较均匀、孔道结构良好的特点,最佳条件下改性硅藻土对Cd2+的去除率(90.2%)为原土的7.6倍.这说明利用氢氧化镁改性天然吸附材料作为吸附剂可以大大提高对重金属废水的吸附能力,因此对天然吸附材料的无机改性有着很大的发展前景.
3 结论
(1)作者采用浸渍-共沉淀的方法制备了改性材料Mg(OH)2-CM,确定了最佳制备条件:氯化镁浓度为1.0mol/L,氢氧化钠浓度为1.25 mol/L,反应温度为40℃,反应时间为100 min.
(2)对改性纤维素进行了FTIR、SEM、BET和XRD的表征,结果表明,氢氧化镁成功地负载于纤维素上.纤维素表面的微观特性被改变,作者制备的改性纤维素较原来的纤维素比表面积和总孔容积都有所增加.
(3)通过吸附实验得出,通过最佳制备条件Mg(OH)2-CM整体比CM对铜离子的吸附性能强,Mg(OH)2-CM对铜离子的平衡吸附量为22.89 mg/g.
