机器人及腹腔镜胃癌根治术后胰瘘发生的影响因素分析
2022-12-29张小磊江志伟王刚潘华峰王海锋江晓晖吴金东
张小磊,江志伟,王刚,潘华峰,王海锋,江晓晖,吴金东
1.南通大学附属肿瘤医院胃肠外科,江苏 南通 226000;2.江苏省中医院普外科,江苏 南京 210004
胃癌是常见的恶性肿瘤之一,全世界每年有超百万的新发病例,我国胃癌死亡率居恶性肿瘤第3位[1]。在我国主要是以进展期胃癌为主,D2根治术作为非晚期胃癌的标准手术方式已成为共识[2-3]。目前手术方式主要有开放手术、腹腔镜手术和机器人手术,然而作为胃癌的主要治疗方式,手术后近期并发症的发生率仍较高。有研究显示随着近年来腹腔镜胃癌手术的开展,胰瘘的发生呈现上升趋势[4]。胃癌术后胰瘘有时后果严重,可导致大出血、腹腔感染、水电解质紊乱、多脏器功能衰竭,甚至死亡[5],这种恶性级联反应值得胃外科临床医师格外重视。本文通过分析胃癌病人的临床资料,探讨胰瘘发生的相关影响因素,以期为临床预防和治疗胰瘘提供一定的参考依据。
资料与方法
一、一般资料
收集2018年6月至2022年6月江苏省中医院普外科由同一组医师行胃癌根治术的病人的临床资料。纳入标准:(1)行机器人或腹腔镜胃癌根治术;(2)术后病理确诊为胃腺癌。排除标准:(1)复发性胃癌手术;(2)联合胰腺或脾切除术;(3)急诊手术;(4)相关医学资料不全的病人。最终本研究共纳入符合标准的病人386例。本研究通过江苏省中医院伦理委员会批准(批件号:2021NL-167-02),所有病人术前均签署知情同意书。
二、研究方法
围手术期参照加速术后康复(ERAS)流程处理[6],根据术前胃镜、腹部增强CT及术中探查结果决定手术方式及切除范围。淋巴结清扫均严格按D2淋巴结标准清扫。所有病例手术者均有机器人及腹腔镜胃癌根治术100例以上操作经验。
三、观察指标及胰瘘诊断标准
记录所有病人的年龄、性别、体质量指数(BMI)、糖尿病史、高血压史、腹部手术史、新辅助治疗史、肿瘤位置、手术方式、切除范围、淋巴结清扫数目、术中出血量、总手术时间、肿瘤分期等。
胰瘘的评价标准:本研究中胰瘘的诊断主要依据国际胰腺外科研究小组(ISGPS)发布的2017版胰瘘定义及分级系统[7]。术后第3天后腹腔引流液淀粉酶值大于血清淀粉酶正常值上限的3倍即可诊断为胰瘘。
四、统计学分析

结 果
一、胃癌病人术后胰瘘的发生情况
符合入组的病人共386例,其中男性225例,女性161例,年龄(64.8±8.8)岁,BMI为(23.6±2.5) kg/m2。本研究386例病人中符合胰瘘标准的病人共64例,术后胰瘘发生率为16.6%(64/386),生化漏的发生率为13.5%(52/386),B级瘘的发生率为3.1%(12/386),无C级瘘发生。所有胰瘘病人经预防或治疗性生长抑素、充分引流、抗感染及营养支持治疗后均得到治愈,无行二次手术治疗病例。
二、胃癌病人术后胰瘘的影响因素分析
单因素分析结果显示:胃癌术后胰瘘与病人性别、BMI、腹部手术史、新辅助治疗史、手术方式、淋巴结清扫数目、总手术时间及肿瘤分期有关(P<0.05),而与年龄、糖尿病史、高血压史、肿瘤位置、切除范围及术中出血量无关(P>0.05),见表1。将单因素分析中有统计学差异的因素纳入二元Logistic回归多因素分析模型进行分析,结果显示:BMI、新辅助治疗史、手术方式、淋巴结清扫数目、总手术时间及肿瘤分期是胃癌术后胰瘘的独立影响因素(P<0.05),见表2。
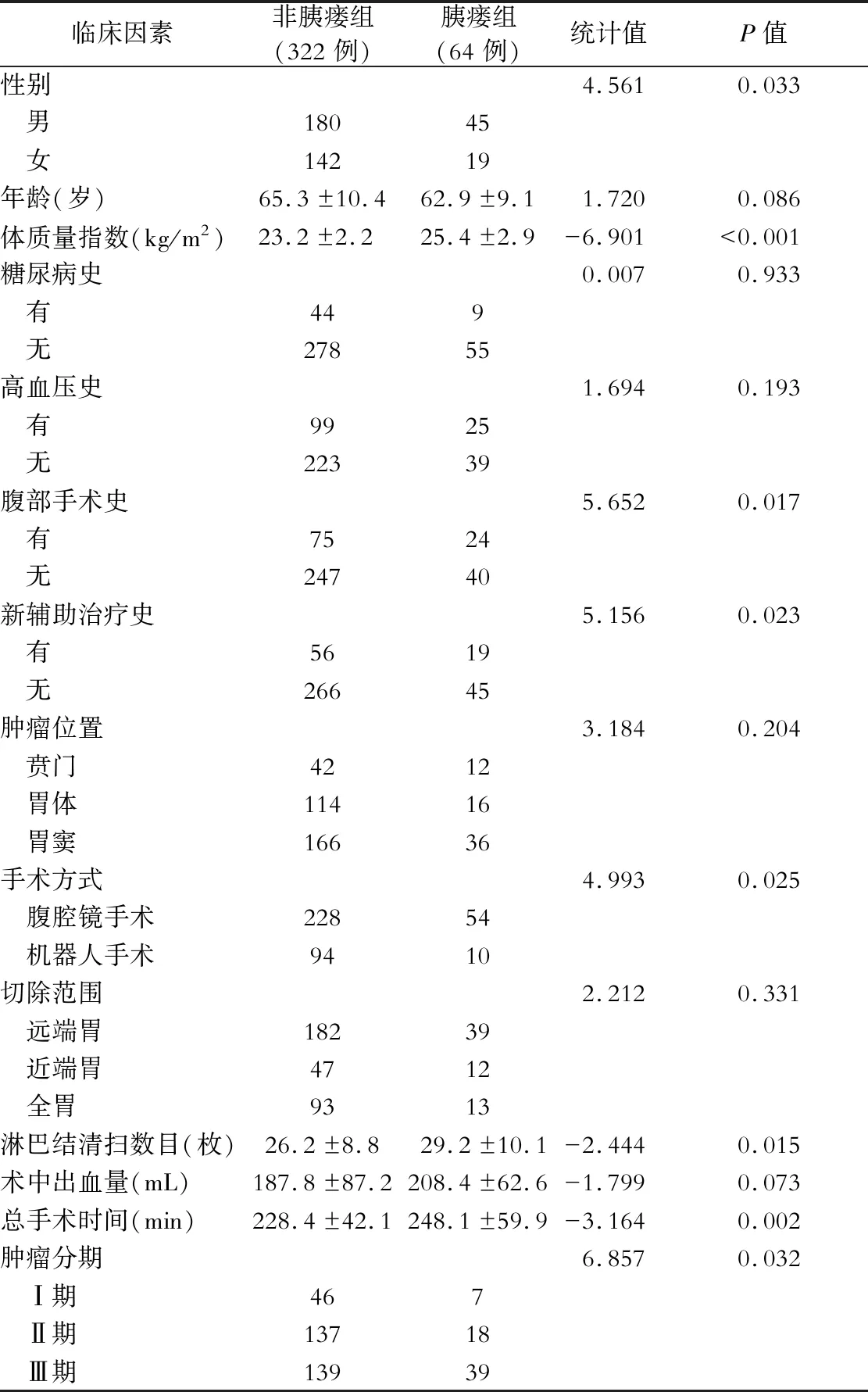
表1 胃癌病人术后胰瘘发生的单因素分析
讨 论
术后并发症被认为是评价外科手术质量的重要指标,其发生直接延长病人住院时间,增加住院费用,甚至对其长期生存和预后产生不良影响[8],因此对于并发症应以早期预防、早期治疗为主。胰瘘作为胃癌术后的并发症之一,其造成的恶性级联反应后果有时较为严重。目前关于胃癌术后胰瘘的诊断标准主要有两种,一种是Clavien-Dindo分级诊断标准[9],一种是国际胰瘘研究小组(ISGPF)诊断标准[7]。前者将胰瘘分为5大类7小类,临床上以Ⅱ、Ⅲa级胰瘘最为常见,后者于2017年更新发布了新的标准,将原版中A级胰瘘改名为生化漏,B级和C级胰瘘也重新进行了严格定义。近年来关于胃癌术后胰瘘发生的研究显示,其发生率为3.7%~20.7%,B级胰瘘发生率为1.1%~5.4%,C级胰瘘发生率为0.4%~6.5%[10-12]。不同的医疗中心胰瘘发生率差异较大,因此研究本中心的发生率及其影响因素具有一定的临床指导意义。本研究结果显示胃癌手术后胰瘘发生率为16.6%(64/386),生化漏的发生率为13.5%(52/386),B级瘘的发生率为3.1%(12/386),无C级瘘发生,与文献报道相符合。胃癌术后胰瘘的发生主要与3类因素有关:病人全身因素、手术因素以及胰腺本身因素[13]。其发生主要与术中在胰腺周围行淋巴结清扫时胰腺受到的直接损伤、热损伤以及钝性损伤有关。本研究结果显示BMI、新辅助治疗史、淋巴结清扫数目、手术方式、总手术时间及肿瘤分期是胃癌根治术后胰瘘发生的独立影响因素。
肥胖病人内脏脂肪含量较高,胰腺肥厚饱满,增大淋巴结清扫的难度,尤其在清扫第6、10组淋巴结时易误将胰头或胰尾组织当成脂肪组织而损伤,增加胰瘘的发生[14-15],本研究结果显示术后发生胰瘘的病人BMI较高(P<0.05)。也有研究表明在衡量肥胖的指标上,内脏脂肪面积比BMI对胰瘘的发生更有预测价值[16]。此外,有研究显示有新辅助治疗史者更易发生胰瘘,可能与化疗药使胰腺周围脂肪组织变性导致胰腺周围层次难以辨认有关,增加术中胰腺损伤可能[17-18]。

表2 胃癌病人术后胰瘘发生的多因素分析
当肿瘤TNM分期较晚,胃后壁肿瘤与胰腺粘连,甚至外侵胰腺前被膜,胃周淋巴结尤其是幽门区和胰腺上缘淋巴结出现转移时,术中分离肿瘤与胰腺粘连、剥离胰腺被膜、清扫胰周淋巴结、游离十二指肠起始部等操作均会增加胰腺损伤的可能,引起胰瘘发生[19]。本研究结果与前述相符,当肿瘤病期偏晚时术后易并发胰瘘(P<0.05)。此外手术时间延长也增加胰瘘的发生,腔镜器械长时间的牵拉或压迫胰腺会导致胰腺腺泡破裂从而引起胰瘘,因此术中减少接触胰腺可降低胰瘘的发生[20-21]。“T”型纱布条垫压胰腺或者牵拉胰腺下缘结肠系膜暴露胰腺上缘,避免直接牵拉压迫胰腺,均可减少胰瘘的发生。
已有多个临床试验证实了腹腔镜技术在早期和进展期胃癌治疗中的安全有效性[11,22-23]。其中中国的CLASS-01、韩国的KLASS-01研究显示腹腔镜与开放手术后胰瘘发生率相当[22-23]。而日本Hiki教授的研究数据表明腹腔镜远端胃手术后胰瘘发生率高于开腹手术[24]。与之相反的是我国一项多中心前瞻性研究[12]显示腹腔镜的镜头放大作用提高了术中的精细解剖,减少对胰腺的损伤,减少了术后胰瘘的发生。各方研究结果的差异可能与研究人群、肿瘤部位、肿瘤分期以及入组的胰瘘诊断标准不同有关。本研究显示腹腔镜胃癌术后胰瘘的发生率为19.1%(54/282),无C级瘘发生,与大宗研究的发生率相似,但因同时期开腹手术较少,未行腹腔镜与开腹手术的比较。
此外,多个研究[25-26]证实了机器人胃癌手术在近期效果与远期预后方面,与腹腔镜手术相似甚至更有优势,尤其表现在学习曲线、淋巴结清扫、手术精准度、狭窄空间操作等方面。本研究中所有机器人手术均采用第四代达芬奇Xi系统完成,其提供了更多的图像视野,更大的活动范围[27]。本研究发现机器人胃癌手术比腹腔镜手术减少胰瘘的发生(9.6%比19.1%,P<0.05),与Suda等[28]、Seo等[29]的研究结论相似。机器人手术减少胃癌术后胰瘘发生的原因考虑有:(1)机器人手术系统的三维空间成像较腹腔镜的二维平面更接近于开腹直视下手术,10~15倍三维立体景深效果,能准确识别胰腺边界,辨别局部微小解剖结构间隙,稳定无震颤的机械臂使得操作解剖更精细;(2)不同于腹腔镜手术中助手需两手各持抓钳,机器人2号、3号臂的使用,降低腹腔镜对助手的配合依赖[30],在清扫第7、8a、9、12a及11p组淋巴结时,助手可双手操作吸引器或抓钳借助纱布条稳定压迫胰腺表面从而保持合适的张力[31],或仅牵拉胰腺下缘结肠系膜进行暴露[32],减少对胰腺的损伤;(3)灵活的机器手腕器械使得在行胰腺上缘淋巴结清扫时,能更方便抓提组织,减少超声刀对胰腺的压迫损伤[31]及热损伤。
本研究为单中心回顾性研究,样本量偏少,所选的胰瘘相关因素不全面,具有一定的局限性,期望在后续进行前瞻性多中心研究,增加样本量,加入内脏脂肪面积[16]、胰腺至肝总动脉距离[33]、胰腺表面与主动脉的垂直距离[34]等数值相关因素指标。
综上所述,胃癌术后胰瘘是临床医师需要关心的问题,尤其当病人BMI较高、有新辅助治疗史、肿瘤分期偏晚时,术前应预估手术难度,术中操作轻柔,精细解剖,术后及时观察,一旦发生胰瘘,应积极处理。此外在具有机器人操作系统的医疗中心,应充分发挥机器人的优势,减少胃癌术后胰瘘的发生。
利益冲突所有作者均声明不存在利益冲突
