沉淀pH对共沉淀制备ZnCr2O4及其合成气一步法制烯烃反应性能的影响
2022-12-27尚蕴山袁德林邢爱华
尚蕴山,李 民,韦 慧,袁德林,刘 华,刘 意,邢爱华
(1.北京低碳清洁能源研究院,北京 102211;2.神华包头煤化工有限责任公司,内蒙古 包头 014060)
金属氧化物-分子筛(OX-ZEO)双功能催化剂用于催化合成气(CO+H2)一步法直接制取低碳烯烃(乙烯、丙烯及丁烯)近年来受到了广泛关注[1-5]。该技术路线将传统的甲醇合成与甲醇制烯烃(MTO)反应耦合,从原理上突破了费托合成产物服从Anderson-Schulz-Flory(ASF)分布的限制,低碳烯烃选择性达到80%以上[6-8],是一条极具发展前景的低碳烯烃生产技术路线。
双功能催化剂上的反应过程是一个串联反应:CO在金属氧化物活性位上活化,接着加氢生成含氧中间体,然后该中间体进入相邻分子筛的孔道转化生成乙烯、丙烯等目标产物[5,9]。金属氧化物不仅可以促使合成气形成含氧化合物中间体,同时也可以催化烯烃等中间体加氢生成烷烃,这使得金属氧化物与分子筛之间的距离(也称“紧密程度”)对CO转化率以及产物选择性均有显著的影响[10-13]。CHENG等[9]发现,C2=~C4=选择性随着金属氧化物与分子筛之间“亲密性”的增加而逐渐降低。JⅠAO等[14]研究发现,将金属氧化物与分子筛以20~40 目颗粒均匀混合时,CO转化率约为17%,C2=~C4=选择性为80%;如果采用上下分层装填或者多层交替装填,CO转化率为4%~10%,C2=~C4=选择性为54%~65%。ZEČEVⅠĆ等[15]研究发现,双功能催化剂活性位点的过度紧密接触反而不利于烃类的加氢裂化。综上所述,金属氧化物与分子筛之间“亲密性”越高,对中间体生成的拉动效应越强,对CO的转化越有利。目前,大部分关于“亲密性”的研究是通过设计不同混合模型以在大范围内对其进行调控,如分层装填,颗粒混合装填等;而小范围内调控“亲密性”,探究其对反应性能的影响鲜见系统性报道,特别是介观尺寸粉末混合下金属氧化物与分子筛“亲密性”的研究最为少见。
ZnCr2O4基催化剂是一种常用的低碳醇合成催化剂[2,16]。近年来,由于其在烯烃、芳烃生成反应中表现出良好的稳定性而被广泛应用于CO/CO2加氢直接制烯烃、芳烃等反应中[2]。目前,关于ZnCr2O4在合成气直接制取低碳烯烃/芳烃方面的研究主要集中在反应机理探索、改性或与不同拓扑结构的分子筛组合以及高选择性获得不同目标产物[1-2]这3方面。FU等[17]研究表明,在ZnCr2O4/ZSM-5催化的合成气一步法制芳烃反应中,CO转化率、芳烃选择性以及芳烃时空收率随着ZnCr2O4的晶粒尺寸的降低而增加。鲜有学者将ZnCr2O4的沉淀参数与双功能催化剂性能进行关联。本研究通过调节共沉淀法制备ZnCr2O4过程中的沉淀pH,制备不同粒径、聚集态的ZnCr2O4,采用XRD、H2-TPR、N2吸/脱附和EDS等表征方式研究沉淀pH对金属氧化物粒径、晶相等物化性质以及金属氧化物与分子筛“亲密性”的影响,采用小型固定床微型反应器评价双功能催化剂的反应性能,研究沉淀pH对双功能催化剂上CO转化率、C2=~C4=选择性的影响规律。
1 实验部分
1.1 实验试剂
实 验 所 用 试 剂Zn(NO3)2•6H2O(分 析 纯)、Cr(NO3)3•9H2O(分析纯)和(NH4)2CO3(分析纯)均购自国药集团化学试剂公司;拟薄水铝石(Al2O3,质量分数为72%,铝源)购自中铝山东公司;三乙胺(99.0%,模板剂)和H3PO4(质量分数为85%,磷源)购自阿拉丁试剂(上海)有限公司;硅溶胶(质量分数为30%,硅源)购自青岛海洋化工厂;石英砂(20~40 目)购自天津市光复科技发展有限公司。H2(99.99%)、合成气(φ(CO) = 45%,φ(H2) = 45%,φ(N2) = 10%)均购自北京氦普公司。
1.2 催化剂制备
采 用 共 沉 淀 法 制 备ZnCr2O4:0.375 mol Zn(NO3)2·6H2O和 0.500 mol的Cr(NO3)3·9H2O溶于去离子水中,制备成浓度为0.5 mol/L混合溶液M。再称取1.100 mol的(NH4)2CO3固体分别配制浓度为0.45 mol/L、0.50 mol/L、0.60 mol/L 和 0.63 mol/L 的水溶液(沉淀剂B),将混合溶液M与沉淀剂B通过蠕动泵同时滴加到配有机械搅拌和pH计的三口瓶中,水浴保持沉淀温度在70 °C,通过控制沉淀剂的滴加速度,控制沉淀pH分别为5.5~6.0、6.0~6.5、6.5~7.0 以及 7.5~8.5。滴加完成后,70 °C下继续老化3 h;抽滤,滤饼用去离子水洗涤至中性后转移到干燥箱中,90 °C干燥 12 h制得前躯体,根据沉淀pH的不同,分别命名前躯体为P-5.5、P-6.0、P-6.5和P-7.5。将上述前躯体转移至马弗炉中,350 °C焙烧4 h制得金属氧化物,根据沉淀pH的不同,分别命名金属氧化物为S-5.5、S-6.0、S-6.5 和S-7.5。
SAPO-34分子筛参考文献[18]中的方法(水热法)制备:H3PO4、拟薄水铝石、硅溶胶和三乙胺(TEA)按照n(Al2O3):n(P2O5):n(SiO2):n(TEA):n(H2O) =1.00:0.95:0.10:3.50:75.00配料。所制备的SAPO-34分子筛在马弗炉中 650 °C焙烧 5 h,制得H-SAPO-34分子筛。
双功能催化剂制备方法:将H-SAPO-34分子筛粉末与ZnCr2O4粉末按照质量比1:1在研钵中充分研磨混合均匀,压片、破碎,筛分20~40 目颗粒,制得双功能催化剂,根据复配的金属氧化物不同,命名为BS-x,如与S-5.5制备的双功能催化剂为BS-5.5。
1.3 表征方法
X射线粉末衍射(XRD)表征在Bruker D8 Advance型衍射仪上进行。测试条件:X射线辐射源为Cu Kα(γ= 0.154184 nm),管电压 40 kV,管电流 40 mA,采集步长为 4 (°)/min,采集范围为 5°~90°。
SEM测试在美国FEⅠ公司Nova Nano SEM 450型扫描电镜仪上进行。扫描电压3 kV。同时使用Super Oxford X-Max 100 TLE分析系统记录EDS光谱,扫描电压 20 kV。
H2程序升温还原(H2-TPR)实验在AutoChem HP 2950 型吸附仪仪上进行。将 100 mg样品装入U型石英管中,在 150 °C下用N2吹扫 90 min,然后冷却至 50 °C,加上冷阱,转换气路为 5%H2/Ar(25 mL/min),稳定后,开始还原,以 10 °C/min由 50 °C加热到 800 °C,记录TCD信号。
N2吸/脱附在美国麦克仪器公司ASAP2460型物理吸附仪上进行测试。测试前样品在300 °C真空下处理3 h,采用BET模型计算得到总比表面积。采用t-plot方法,计算相对压力为0.99的单点脱附孔体积得到总孔体积,孔径分布使用BJH模型。
1.4 催化剂评价方法
采用小型固定床微型反应器(ϕ12 mm × 20 mm)进行合成气一步法制烯烃反应评价。将1.0 g双功能催化剂(20~40 目,2.0 g石英砂稀释)装入内径为8 mm的石英管中,置于反应管中,上端使用耐高温“O”型圈密封。首先将双功能催化剂进行预处理(400 °C,99.99%H2还原 8 h,流速 15 mL/min),预处理结束后,保持温度不变,气切换为合成气,使用前经过活性炭(粒径5 mm)的净化罐脱除气体中羰基铁、羰基镍等杂质,待系统压力升至2 MPa,记录反应开始时间点。
反应尾气管线-自动切换阀-气相色谱之间的所有管线均配有电加热伴热,保证所有组分以气态的形式进入色谱,伴热带温度为160 °C。采用安捷伦7890B气相色谱进行全组分在线分析,烃类经HP-PLOT Q(50.00 m × 0.53 mm)毛细管色谱柱进行分离,FⅠD检测器检测;CO、CO2和N2经过q柱和 5A分子筛柱串联进行分离,TCD检测器检测。所有尾气产物均采用外标法测量,产物分析根据下列公式进行[17]:

式中,XCO为CO转化率,%;xCO,in和xCO,out分别为进口和出口CO物质的量分数,%。


式中,Si为各产物的选择性,%;ai是烃类分子的碳原子数;xi,out是烃类分子在色谱中物质的量分数,%。
2 结果与讨论
2.1 金属氧化物的结构分析
图1为不同沉淀pH共沉淀法制备的前躯体(图1(a))和金属氧化物(图1(b))的XRD谱图。
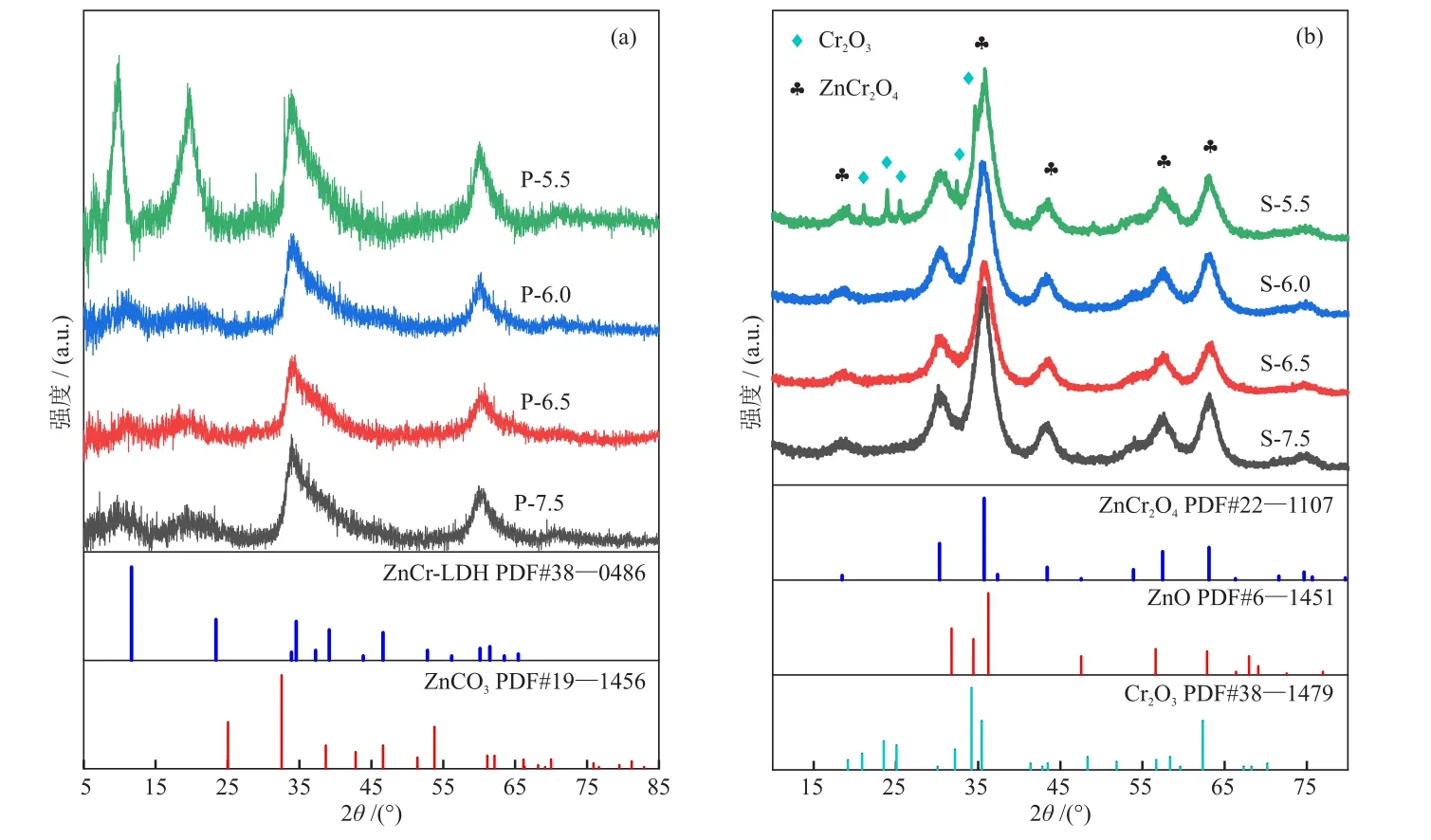
图1 不同沉淀pH下制备的前躯体(a)和金属氧化物(b)的XRD谱图Fig.1 XRD patterns of precursors (a) and metal oxides (b) prepared at different precipitation pH
不同沉淀pH下制备的前躯体为类水滑石衍射峰,衍射峰强度均较低,推断沉淀过程属于非晶沉淀。350 °C焙烧后,S-5.5 在 2θ为 30.3°、35.7°、43.4°、57.5°和63.1°的衍射峰归属于ZnCr2O4的特征峰外(PDF#22—1107)[20],2θ为 23.92°、25.02°和 34.88°有明显的Cr2O3衍射峰(PDF#38—1479)[21]。这表明沉淀pH在5.5~6.0时,由于沉淀剂剂量不足,导致Zn2+、Cr3+和Al3+无法充分的共沉淀,部分Cr3+发生异步沉淀。在S-6.0、S-6.5和S-7.5这3种样品的XRD衍射峰中无其它杂晶相衍射峰,均为典型的ZnCr2O4尖晶石结构。根据文献[22]报道,共沉淀法制备催化剂的过程中,通常酸性溶液过饱和度低,会形成组分分布不均的大颗粒沉淀;而碱性溶液过饱和度高,形成的沉淀组分分布均匀、颗粒小。
图2为4种金属氧化物的SEM照片,S-5.5和S-7.5的二次粒子均为不规则形状堆积的粒子,粒子大小不一,尺寸范围在1~100 μm,推测这些颗粒主要通过物理研磨形成。S-6.0为颗粒聚集的颗粒,二次粒子的粒径为10~20 μm。S-6.5不同形状的多孔团聚体,颗粒内含有丰富的介孔和大孔结构。

图2 4种金属氧化物的SEM照片((a)~(d))及其局部放大图((e)~(h))Fig.2 SEM images ((a)~(d)) and local enlargements ((e)~(h)) of four metal oxides
2.2 金属氧化物的织构性质
图3为4种金属氧化物的N2吸/脱附实验结果。S-5.5 在p/p0= 0.42 处出现了明显的H2 型滞后环,而S-6.0、S-6.5 和S-7.5 均在p/p0= 0.45 处出现了H3 型滞后环。S-6.5在p/p0= 0.80后出现吸附曲线的突变说明体系中存在较大的晶间中孔。孔径分布显示,S-5.5在 4.5 nm处有一个峰;S-6.0则在 6.4 nm和36.8 nm处呈现两个明显的峰;S-7.5的孔径分布主要在4.3 nm处,42.0 nm处还显示出一个相对较弱的宽峰。
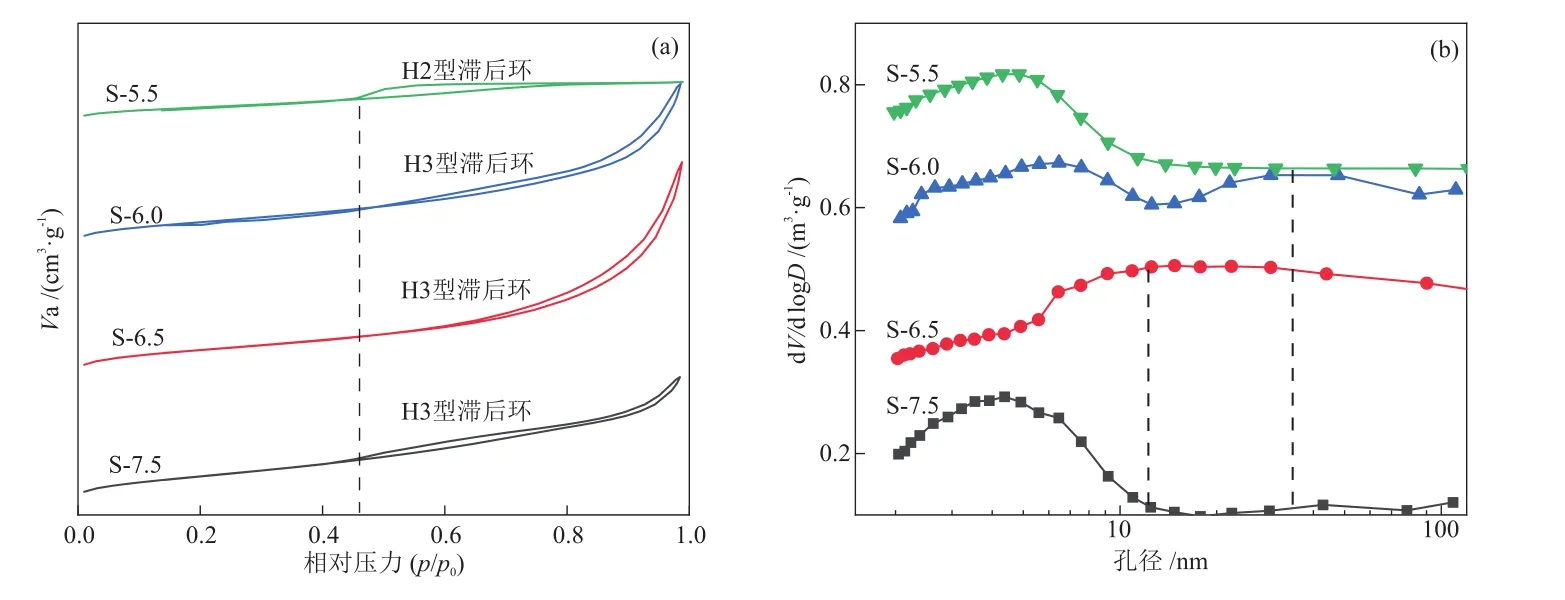
图3 4种金属氧化物的N2吸/脱附曲线(a)和孔径分布(b)Fig.3 N2 adsorption/desorption isotherms (a) and pore diameter distribution (b) of four metal oxides
表1为4种金属氧化物的N2低温物理吸附数据。随着沉淀pH的增加,金属氧化物的比表面积逐渐增加,S-5.5、S-6.0、S-6.5和S-7.5的比表面积依次为 103 m2/g、168 m2/g、173 m2/g和 185 m2/g,这与XRD计算得出的晶粒尺寸变化规律相一致,晶粒越小,比表面积越大。S-5.5、S-6.0、S-6.5和S-7.5的总孔容依次为 0.09 cm3/g、0.38 cm3/g、0.47 cm3/g和 0.29 cm3/g。金属氧化物平均粒径(根据谢乐公式计算)随着沉淀pH的增加,金属氧化物的粒径由15.88 nm(S-5.5)逐渐减小至8.98 nm(S-7.5)。由此可知,沉淀pH显著影响金属氧化物的织构性质。文献研究[22]发现,沉淀的形成一般经过晶核形成和粒子长大或聚集两个过程。当晶核生成速率远远大于晶核增长速率时,大量的晶核会聚集成细小的无定形颗粒,形成非晶形沉淀甚至胶体(非晶沉淀),这种沉淀脱水焙烧后会形成紧密聚集的金属氧化物。相反,当成核速率与粒子增长速率匹配时,金属氧化物粒子在吸附团聚的过程中会形成多孔结构,脱水后这些孔结构可以继续保留。
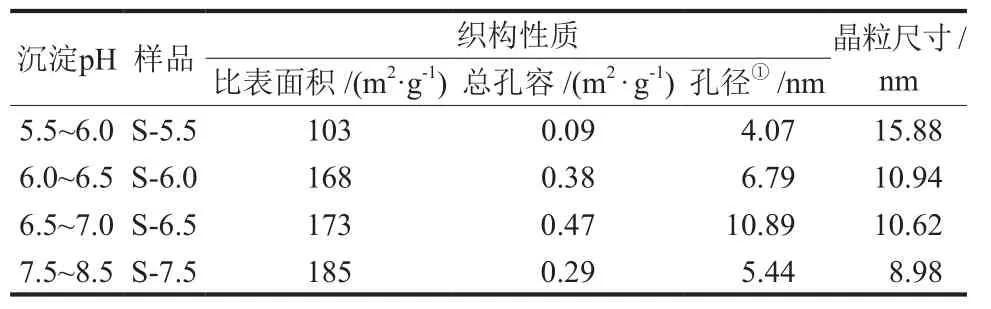
表1 4种金属氧化物的织构性质和晶粒尺寸Table 1 Texture properties and pore diameter of four metal oxides
2.3 金属氧化物的可还原性
图4为4种金属氧化物的H2-TPR吸/脱附曲线。
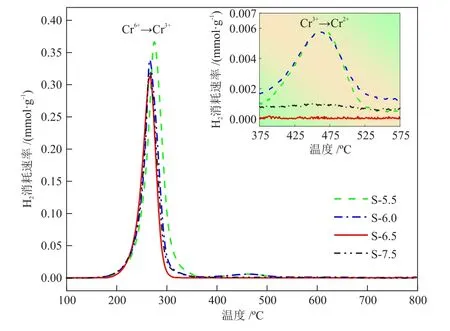
图4 4种金属氧化物的H2-TPR曲线Fig.4 H2-TPR curves of four metal oxides
200~320 °C之间有一个明显的还原峰,归属于Cr6+→Cr3+的还原过程;ZnCr2O4尖晶石Cr3+在焙烧过程中会被过度氧化而形成Cr6+[23]。除此之外,S-5.5和S-6.0在465 °C处还显示出一个小的还原峰,归属于Cr3+→Cr2+的还原峰,而S-6.5和S-7.5并没有该还原峰,这表明,沉淀pH在5.5~6.5时,制备的金属氧化物中夹杂了少量的Cr2O3,这与S-5.5样品的XRD谱图中发现存在Cr2O3相吻合,而S-6.0的XRD谱图中无Cr2O3的衍射峰,这可能是由于提高沉淀pH生成的Cr2O3相反而较少。除此之外,随着沉淀pH的增加,所得样品的还原峰中心温度逐渐向低温方向移动,这是由于催化剂中的晶粒减小,比表面积增大(表1),使得催化剂更容易被还原[24]。
2.4 双功能催化剂的催化反应性能
在相同的反应条件下,考察双功能催化剂在合成气一步法制烯烃反应行为,评价结果如图5所示。由图5 可知,反应条件为 400 °C、2 MPa,GHSV= 6000~7500 mL/(h∙g)时,4 种双功能催化剂的CO转化率明显不同,BS-6.5上具有最高的CO转化率,约为25.00%。由N2吸/脱附结果可知,S-6.5的比表面积大于S-5.5和S-6.0,更大的比表面积有利于暴露更多的活性位点,有利于CO转化。然而,BS-6.5上CO转化率却高于具有更大比表面积BS-7.5,这一“反常”现象可以从金属氧化物与分子筛的“亲密性”角度解释。尽管本文中ZnCr2O4与SAPO-34分子筛均采用粉末混合,但是由于ZnCr2O4的聚集态、分散性不同,导致粉末混合过程与两组分的混合程度也不同,即“亲密性”也不同。
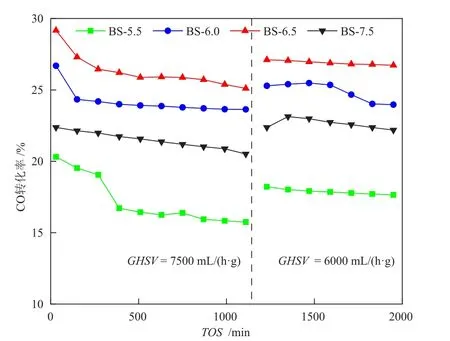
图5 4种双功能催化剂的CO转化率对比Fig.5 Comparison of CO conversion rate of four bifunctional catalysts
为此,通过测定双功能催化剂表面的元素分布(EDS),选择SAPO-34(P和Si)与ZnCr2O4(Zn和Cr)专有的元素来描述双功能催化剂的“亲密性”,结果如图6所示。4种双功能催化剂颗粒表面的元素分布存在明显差异,BS-5.5和BS-7.5表面的Zn存在明显的“集中”现象,而BS-6.5表面的Zn分散性明显高于其他3个样品,该结果反映出BS-6.5中,SAPO-34分子筛与ZnCr2O4具有最好“亲密性”。为此推测,由于S-6.5疏松的结构使其在物理混合过程中容易“破碎”成更小的粒子,使其与SAPO-34分子筛充分混合,二者具有更好的“亲密性”;而S-7.5由于质地坚硬,在混合过程中难以通过物理研磨而破碎为更小的粒子,导致金属氧化物与分子筛之间的距离增加,“亲密性”降低。从热力学角度讲,金属氧化物与分子筛“亲密性”越高,越有利于中间体进入分子筛孔道,消除高温下CHxO(x= 2,4)生成的热力学障碍,促进CO转化[10]。而CHxO中间体如果不能及时进入分子筛孔道,在扩散过程中会加氢生成甲烷[23]。当GHSV降低至 6000 mL/(h∙g)时,CO转化率均增加,BS-6.5上依然显示了最高的CO转化率,约为27.00%。
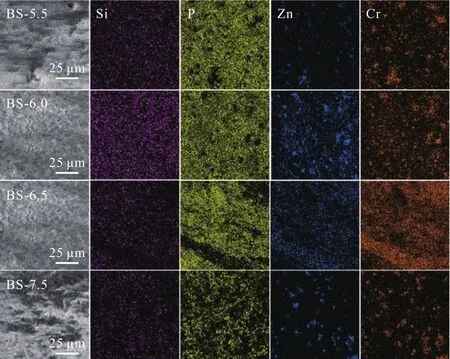
图6 4种双功能催化剂的EDS谱图与元素分布Fig.6 EDS mapping and element distribution of four bifunctional catalysts
4种双功能催化剂的产物选择性如图7所示(反应条件为 400 °C,2 MPa),为便于比较,图中同时给出了CO和CO2转化率变化情况。BS-6.0上CO转化率21.98%,C2=~C4=选择性75.71%,在所有样品中最高。而BS-6.5具有最高CO转化率25.00%,但是C2=~C4=选择性则为74.04%。从EDS谱图可知,BS-6.5中ZnCr2O4与SAPO-34分子筛具有更好的“亲密性”,金属氧化物与分子筛之间的距离最短,但是并未表现出最高的C2=~C4=选择性。这可能是由于ZnCr2O4与SAPO-34分子筛之间越近,在分子筛周围的金属氧化物表面解离的活性H就会更容易溢流到分子筛孔道内,增强分子筛的酸性,进而增强分子筛的裂解能力,从选择性的角度,可能并非二者越近越好。关于这一点,研究人员在Co/SiO2与Pd/Beta双功能体系以及Pt-Y分子筛-Al2O3双功能体系中均发现并非两活性组分距离越近越好[15,24-25],例如颗粒混合的Co/SiO2与Pd/Beta反而比粉末混合时表现出更高的异构烷烃选择性[25]。
当反应空速由7500 mL/(h∙g)降低到6000 mL/(h∙g)时,4种双功能催化剂上的C2=~C4=选择性为75.25%~76.30%,C2=~C4=选择性之间的差异缩小(图7(b))。综上所述,沉淀pH主要影响双功能催化剂两活性组分之间的“亲密性”,进而影响CO的转化率,而对C2=~C4=选择性的影响相对较小。
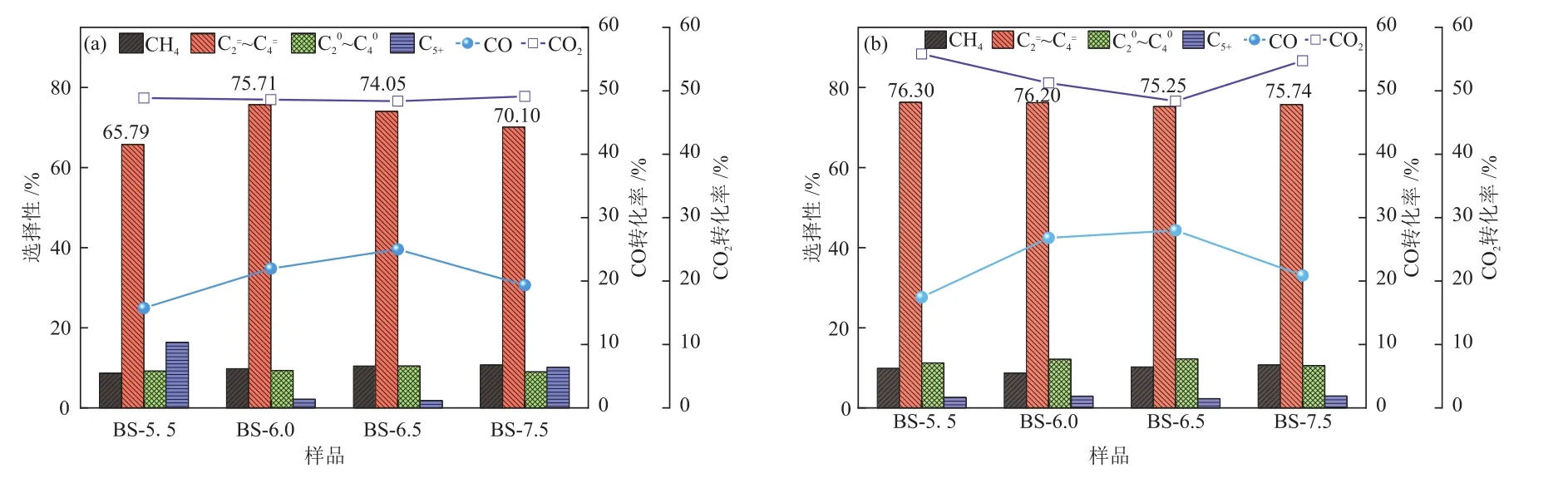
图7 4 种双功能催化剂的产物选择性对比:GHSV = 7500 mL/(h·g) (a),GHSV = 6000 mL/(h·g) (b)Fig.7 Comparison of product selectivity of four bifunctional catalysts: GHSV = 7500 mL/(h ·g) (a), GHSV = 6000 mL/(h ·g) (b)
3 结论
本文研究了共沉淀法制备ZnCr2O4过程中沉淀pH对ZnCr2O4结构、晶粒尺寸、孔结构以及团聚形态等物化性质的影响,然后与SAPO-34分子筛复合制备了一系列ZnCr2O4/SAPO-34双功能催化剂,评价了其对合成气一步法制烯烃反应性能的影响,得到以下结论。
(1)调节沉淀pH对ZnCr2O4的晶相、晶粒尺寸、团聚态、比表面积以及还原温度等产生了显著影响。随着沉淀pH的增加,金属氧化物粒径逐渐减小,比表面积逐渐增加。
(2)诸多因素中,沉淀pH对金属氧化物的团聚态的影响是造成双功能催化剂活性中心“亲密性”差异的主要因素。在pH = 6.5~7.0条件下制得的ZnCr2O4与SAPO-34分子筛混合更加充分,二者之间距离最短,耦合相应最强,因此双功能催化剂在合成气一步法制烯烃反应中具有最高的CO转化率(25.00%),C2=~C4=选择性为74.05%。
后续研究需要进一步考察双功能催化剂在实际还原和反应过程中的ZnCr2O4结构变化、元素迁移等情况,探究金属氧化物表明氧空位浓度变化、表面元素比例、化学态等与CO转化率、C2=~C4=选择性影响机制,建立更加完整的反应构效关系。
