中国临床试验注册中心急性肺损伤/ 急性呼吸窘迫综合征项目特征分析
2022-12-25陈一凡曾燕鹏
陈一凡 李 雁 郭 楠 刘 锦 曾燕鹏 陈 瑜
北京中医药大学东直门医院急诊科,北京 100700
急性肺损伤/急性呼吸窘迫综合征(acute lung injury/acute respiratory distress syndrome,ALI/ARDS)是由各种肺内外因素引发的急性、进行性加重的弥漫性炎症性肺损伤,临床主要表现为呼吸窘迫及进行性、顽固性低氧血症[1]。自2012 年柏林定义取消ALI 概念,而以氧合指数(oxygenation index,OI)划分轻、中、重度ARDS[2]以来,其诊断标准仍处于不断修正完善的过程[3]。2015、2017 年国际上则又根据儿童及新生儿特点分别制定并发布了儿童急性呼吸窘迫综合征(pediatric acute respiratory distress syndrome,pARDS)、新生儿急性呼吸窘迫综合征(neonatal acute respiratory distress syndrome,nARDS)的诊断标准[4-5],与成人ARDS 相区别。ARDS 临床试验随之陆续开展,根据“实施地注册”原则[6],临床试验项目在我国开展者于2007 年后均应在中国临床试验注册中心(Chinese Clinical Trial Registry,ChiCTR)进行注册。此作为推动临床试验透明化、提高临床试验质量及安全性的重要举措之一[7],注册登记也日益受到临床研究人员关注,其对保障临床试验安全性、提升研究质量具有重要意义,也可为未来研究方向提供参考。
1 资料与方法
1.1 资料来源
以“急性肺损伤”“ALI”“急性呼吸窘迫综合征”“ARDS”为检索词,检索ChiCTR 自建库至2021 年6 月30 日注册的所有项目。
1.2 纳入及排除标准
1.2.1 纳入标准 在ChiCTR 登记的注册信息中明确干预对象为ALI/ARDS。
1.2.2 排除标准①重复注册;②未提交伦理批件。
1.3 资料采集
根据纳入及排除标准筛选符合条件的项目,录入项目注册信息。随机对照试验(randomized controlled trial,RCT)参考改良的Jadad 评分量表[8-9]条目进行质量评价。
1.4 统计学方法
由2 名研究者独立筛选,经交叉核对后,进行频数、频率统计及图表绘制。
2 结果
2.1 注册项目概况
共得注册项目96 项,约占2021 年6 月30 日前ChiCTR 总注册试验数量(47 103 项)的0.20%。除3 项未明确指出研究对象的年龄范围,其余93 项中涉及18 岁以下人群的共27 项(29.03%),包含pARDS、nARDS 临床试验12 项(12.90%)。
2.2 项目注册年度
注册最早者为2008 年12 月31 日注册的《经无创正压通气吸入肺腔通气液对急性肺损伤干预的多中心随机对照研究》。此后,相关项目注册数量逐步上升,截至2021 年6 月30 日已有14 项相关研究进行注册。见图1。

图1 注册时间及数量统计图
2.3 主要研究单位地区分布
全国18 个省份/直辖市均已组织开展该领域相关项目,以山东、上海为主要研究单位的项目居多,分别有12 项(各占12.50%)。见表1。

表1 主研单位地区分布
2.4 研究单位数量
以76 项单中心试验为主(79.17%),除3 项仅描述为“多中心试验”而未明确中心数量的注册项目外,以《肺表面活性物质治疗婴幼儿中重度急性呼吸窘迫综合征的临床研究》及《西维来司他钠治疗ARDS 患者有效性及安全性多中心临床研究》为实施单位数量最多的两个项目,均涉及12 所参与单位。
2.5 研究类型
包括42 项干预性研究、46 项观察性研究、4 项诊断试验、3 项基础科学研究及1 项预后研究,最多者为随机平行对照试验数量。见表2。

表2 纳入研究类型
2.6 研究样本量
除4 项未说明样本量外,其他92 项共预计招募样本23 310 例,包含干预性研究5 312 例(样本量:9~620 例)、观察性研究17 288 例(样本量:25~5 000 例)、诊断试验340 例(样本量:90~150 例)、基础科学研究340 例(样本量:60~200 例)、预后研究30 例。见图2。

图2 注册项目样本量统计情况
2.7 RCT 质量评价
根据改良的Jadad 评分量表条目对41 项RCT 随机序列的产生、随机化隐藏、盲法使用情况进行质量评价。见表3。
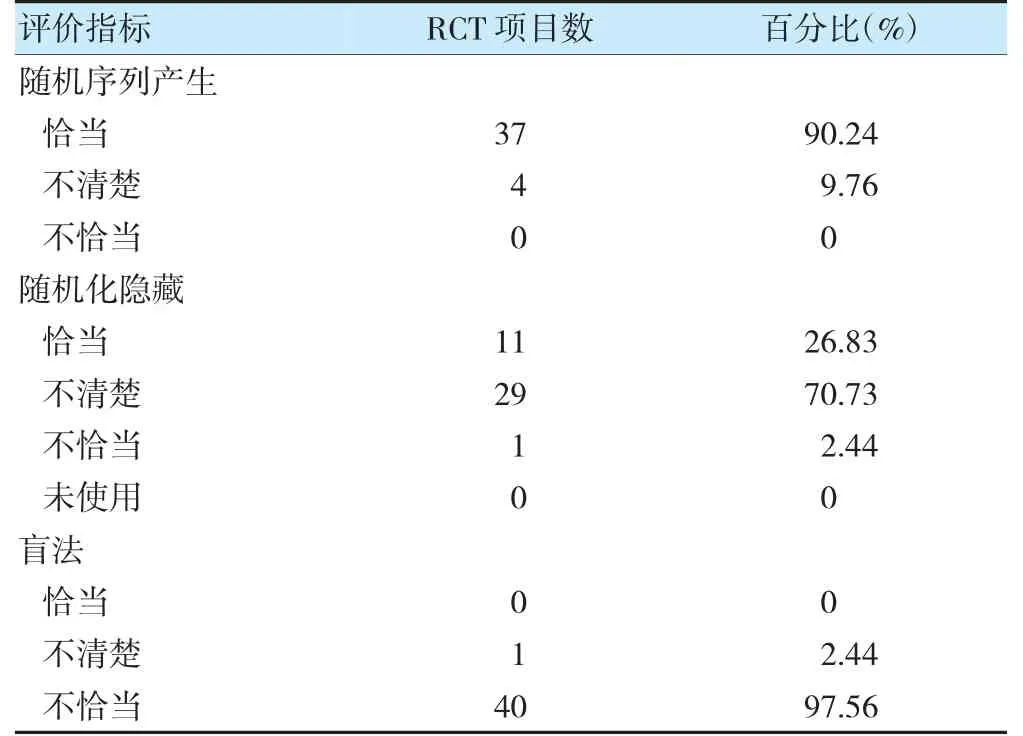
表3 纳入RCT 质量评价
2.8 病因或合并其他疾病
对ALI/ARDS 发病原因或合并其他疾病做出描述者共44 项,出现2 次及以上的主要包括脓毒症、外科手术后、外伤或创伤、主动脉夹层、体外循环术后、感染性休克等。
2.9 干预措施
①中西医结合治疗:6 项前瞻性RCT 分别采用通腑泻肺法、疏风解毒胶囊、电针、宣白承气汤、复苏合剂(温肾潜阳法)、血必净注射液结合西医治疗干预。②西药治疗:以乌司他丁(4 项)、西维来司他钠(2 项)干预较多。③西医非药物治疗:以俯卧位通气(5 项)、体外膜式氧合、无创通气、人脐带间充质干细胞、呼吸末正压(各3 项)及连续性血液滤过、经鼻高流量氧疗(各2 项)干预较多。④4 项pARDS、nARDS 相关试验:分别采用肺表面活性物质、穿心莲内酯磺化物、甲泼尼龙及血液滤过干预。
2.10 标本采集与指标观测
76 项试验指出需采集患者标本,其中仅取血液标本的项目57 项,仅取支气管肺泡灌洗液(bronchoalveolar lavage fluid,BALF)标本的项目2 项,兼取血液与BALF 标本的项目14 项,另有取唾液、痰液及口腔分泌物标本者。观测结局指标中出现频次较高的指标见表4,评分量表类指标除表4 中所列3 项外,其余仅出现1 次故未列出。

表4 高频观测结局指标
3 讨论
3.1 注册数量趋增,质量尚需加强
与2008—2017 年每年注册数量比较,2018 年以后,每年在ChiCTR 注册的ALI/ARDS 项目皆超过10 项,这与国内学者临床试验注册登记的意识日益加强及2017 年起美国临床试验注册中心不再直接接受不在美国进行的临床试验项目注册,指出仅在中国实施的临床试验应在ChiCTR 注册[6]有关。注册质量方面,除未提交伦理审查批件的项目外,尚存在研究对象年龄范围、样本量、研究单位数量等信息缺失问题。针对干预性RCT,随机序列产生方面,有4 项研究仅描述“随机”,但未明确具体方法;随机化分配隐藏方面,仅26.83%的项目采用了能使临床医生和受试者无法预知分配序列的恰当措施,70.73%仅说明随机序列生成法而未说明随机分配隐藏法,不恰当的方法则体现为由临床医生进行随机分配,不能避免分组的可预测性;盲法使用方面,仅有1 项研究表明为“双盲”试验,且未在注册信息中明确其实施方法,其余40 项均未说明盲法的使用情况。同时,就研究单位数量而言,79.17%的单中心试验仍占据多数,而在20.83%的多中心试验中,涉及5 所及以上研究单位共同开展临床试验的项目仅有6 项;主要研究单位所在地也具有不均衡性,多处于医疗及经济条件较为发达的地区。因此,亟须以优势地区带动其他区域协同发展,开展多中心、大样本量临床试验,以便研究结论获取更高质量的临床证据支持。
3.2 发病原因复杂,干预措施多样
ARDS 的发病原因一般可分为肺内源性和外源性因素。有研究指出,不同病因引发的ARDS 在多方面存在差异,且针对ARDS 原发病的治疗常决定患者的预后[10-11]。本研究发现,44 个项目涉及的发病原因或合并病中,除作为ARDS 主要病因的脓毒症[12]外,其他病原体感染、创伤、外科术后、胰腺炎等病因也受到研究者关注。目前尚无针对ARDS 的特效治疗手段,除积极治疗原发病外,仍以限制潮气量与呼吸末正压[13]的保护性肺通气策略、俯卧位通气等呼吸支持治疗作为具有较高级别证据支持的主要干预措施[14]。药物治疗方面则包括对抗炎药、肺泡表面活性物质、抗凝或纤溶药、抗氧化药及神经肌肉阻断剂等临床应用研究[15]。本研究显示,注册项目包含初步应用非常规药物作为干预手段的临床试验,同时还对通气策略的优化完善及新型通气设备的使用、体外膜式氧合应用时间与方式等非药物疗法开展更细化的研究。中西医结合治疗在降低病死率、改善临床表现及炎症指标等方面也体现出良好的应用潜力[26],注册项目现主要针对ARDS 患者辨证施予中药复方,但项目数量仍偏少。随着越来越多临床及实验研究同时证实中医药可有效干预ARDS[17-18],中西医结合干预在防治ARDS 方面可能发挥的效果及机制值得进一步研究。
3.3 结局指标丰富,核心指标待建
研究发现,当前研究者关注的结局指标与Porter’s结局层次[19]描述的三层结构具有较高的契合性,如住院生存率、7 天生存率等与第一层第一级的“生存率”相对应;症状改善度、生命体征、氧合指数与舒适度评分、临床状态评分等指标与第一层第二级的“达到或维持健康或恢复程度”相对应;机械通气时间、疾病临床改善所需时间等指标与第二层第一级的“恢复时间”相对应;镇痛剂使用量、血管活性药物用量等指标与第二层第二级的“治疗过程”相对应;肝肾功能、心肺功能及影像学的定期监测等指标则与第三层“健康可持续性”相对应。统计分析显示,现有注册项目更多关注于第一层第一级“生存率”与第二层“恢复过程”,对第一层第二级“达到或维持健康或恢复程度”与第三层“健康可持续性”的关注稍显不足。另外,自2010 年“有效性试验核心结局测量”组织成立及倡议提出以来,为规避同类疾病的临床试验在选择、测量与报告等环节异质性大、选择性报告偏倚风险、规范性不强及同类研究不能合并造成资源浪费等问题,核心指标集(core outcome set,COS)的研制与应用研究进入快速发展阶段[20-21]。本研究发现,注册项目中仅出现1 次的结局指标多达124 种,势必不利于高质量循证医学证据的产生。检索COS 研究公开注册平台发现,关于ARDS 的COS 研究仍罕见。而关于结局指标的框架建设及具有中医特色的结局指标在COS 中亦未充分体现[22-23]。因此,规范构建相关COS 尚具有较大的研究空间。
综上所述,鉴于ARDS 复杂的发病原因及尚待完善的诊疗方式,ARDS 临床试验仍将不断增加,研究者的注册意识及试验设计、数据管理与注册信息填写质量均亟须进一步提升,从而促进负责人做好试验顶层设计,助力临床试验透明化,减少发表偏倚及不必要的重复试验,获取高质量的循证依据[24-26],为ARDS的临床诊疗及研究进展提供更多帮助。
