塑料药物包装材料可提取物全景分析方法概述
2022-12-21图尔荪托合提托合提萨伊普孙兆增韩建勋宋薇魏海燕肖进进
图尔荪托合提·托合提萨伊普,孙兆增,韩建勋,2,宋薇,魏海燕,肖进进
塑料药物包装材料可提取物全景分析方法概述
图尔荪托合提·托合提萨伊普1,孙兆增1,韩建勋1,2,宋薇1,魏海燕1,肖进进1
(1.谱尼测试集团股份限公司,北京 100095;2.谱尼测试集团北京检验认证研究院有限公司,北京 100095)
对国内常用的塑料药物包材的挥发性、半挥发性、非挥发性物质及金属元素等提取物质的检测和分析方法进行总结,为塑料药物包材可提取物质全景分析和安全性评价提供参考。通过检索国内外相关文献,对塑料药物包材中不同可提取物的分析方法进行总结和归纳。目前,国内塑料药物包材日益更新,但可提取物的分析手段单一、检测分析方法不全面,缺乏相应的数据库。药物包材的相容性研究在国内起步不久。针对目前存在的塑料包材可提取物的分析手段单一、不全面,缺乏相应的数据库等问题,现阶段亟需构建分辨率和灵敏度高、特异性强、筛查范围广的方法,对药物包材可提取物质进行全景分析,减少因包材安全性不良引起的医疗事故。
塑料药物包材;包材相容性;可提取物;色谱质谱联用
塑料药物包材具有密度小、质量轻、力学性能强等特点,广泛用于各种药物的储藏、运输等方面。我国“化学药品注射剂与塑料包装材料相容性研究技术指导原则”和美国食品药品监督管理总局(FDA)明确规定,药物包装系统一方面为药品提供保护,以满足其预期的安全性和有效性;另一方面应与药品具有良好的相容性。相容性是指“包装系统与内容物的相互作用不足以使药物制剂或包装发生不可接受的改变”,这相互作用主要体现在3个方面:药物包装材料吸附或吸收药物成分,降低药物有效性;药物包材成分迁移到药物中,污染药物或降解药物活性物质,从而降低药物效果;药物在贮藏过程包材或药物颜色发生变化,从而影响药物有效性[1]。当药物制剂与包材直接接触时,药物制剂与包材之间发生吸附、吸收、渗透、浸出及提取等相互作用[2],从而影响药物的治疗效果,甚至可能会污染药物,对患者带来潜在的危害,特别是注射类药物,其给药方式是直接接触血液,属于高风险制剂,因此其包装的相容性(主要是塑料包装)更是要引起高度重视。因此,近年来药物制剂与塑料包材的相容性研究已成为一项新兴的研究领域,在国内外引起了不小的重视。
1 塑料包材可提取物和溶出物
药物生产、储藏及运输过程中可能会产生一些杂质,而塑料包材中添加了聚合引发剂、催化剂、塑化剂、抗氧化剂等多种添加剂。这些添加剂与塑料包材主要成分并不是通过化学键结合,因此受到特殊的外界环境因素时,容易分解产生一些物质[3]。此外,有些注射类药物制剂灌装到输液袋之后,进行高温灭菌,在此过程中,塑料包材可能会发生物理化学反应,产生一些未知物[4]。如邻苯二甲酸盐是常添加于塑料包材的增塑剂之一[5]。有文献显示,邻苯二甲酸盐进入人体,即使在低浓度也会影响内分泌系统和生殖系统的正常代谢功能,导致内分泌失调[6]。抗氧化剂、增塑剂及防老剂2–巯基苯并噻唑,常检测到于吸入的鼻用药物中。有研究表明,2–巯基苯并噻唑具有致癌的潜在风险[7]。而这些物质以可提取物或溶出物的形式出现于药物制剂中(见图1)。
随着塑料包材的更新换代,目前市场提倡使用聚乙烯(Polyethylene,PE)、聚丙烯(Polypropylene,PP)等非PVC材质的塑料包材,并要求添加于这些包材的抗氧化剂种类不超过3种,总量不得超过0.3%,因此,目前大多数研究主要集中于这些抗氧化剂(Irganox1010、Irganox1076、Irganox168)或增塑剂(邻苯二甲酸酯类)含量的测定上[6]。但有些注射类药物灌装之后进行高温灭菌,在此情况下包材成分与药物制剂发生反应,可能产生一些未知物。此外,包材中还存在本身掺杂于抗氧化剂或增塑剂的一些杂质[8]。前期,对医疗系统上常用的非PVC输液软袋、输液瓶及PVC输液袋挥发性和半挥发性成分全面提取,且鉴定成分。结果发现,除了上述提到的抗氧化剂和增塑剂之外,还鉴定了不少反应中间体、掺杂于抗氧化剂2046的杂质7,9–二叔丁基–1–氧杂螺[4.5]十二烯–2,8–二酮(CAS:82304–66–3)以及一些未知物。通过SwissADME等在线毒理学评估系统,初步评估了7,9–二叔丁基–1–氧杂螺[4.5]十二烯–2,8–二酮的毒理学特性,发现该杂质具有一定的毒性(该内容还未发表)。可见,目前包材安全性评价方面不止要关注特定的已知化合物,也要关注可能存在于包材添加剂的杂质、药物贮藏或灌装过程中出现的杂质或反应副产物。
包材相容性研究过程有确定包材、分析包材组分、提取包材中可提取物,鉴定及评估其安全性、开展迁移试验、对溶出物(浸出物)的安全性进行评估、评价包材相容性等六大步骤(见图2)[9]。确定好研究对象之后,充分了解包材组成成分,通过可提取物的种类、含量及潜在的风险,对其安全性进行评价。在此过程中提取试验至关重要,可提取物的评估结果决定是否进行后续的迁移试验[10],因此,塑料包材用于药物包装之前,使用合适的提取溶剂在高温、强酸、强碱、高压等苛刻的条件下对塑料包材可提取物进行提取,全面分析其种类,测定含量,对可提取物进行全景分析,针对不同的可提取物建立特定的提取和分析方法,评估其潜在风险,以指导后续开展的迁移试验[11]。
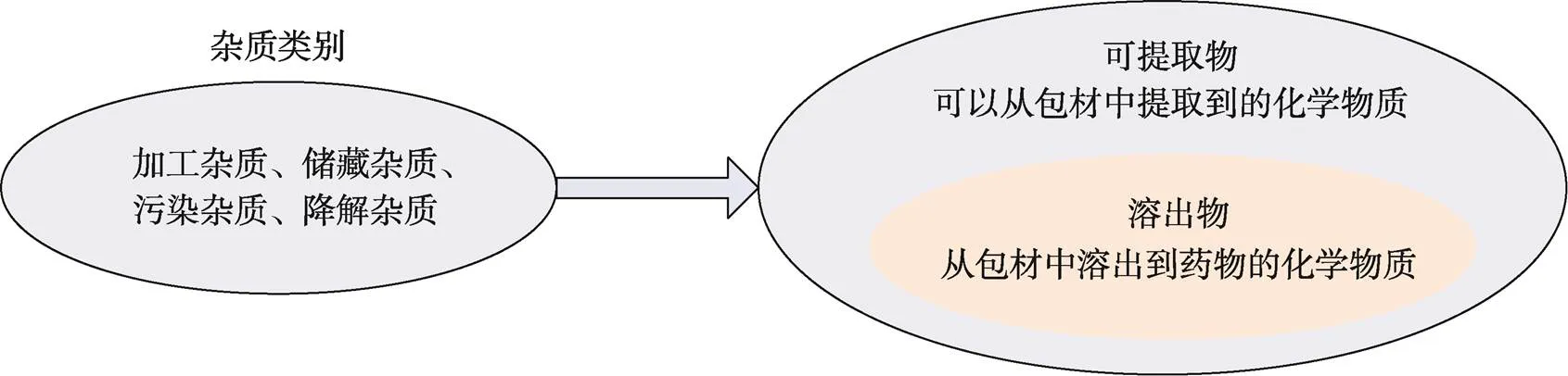
图1 杂质、溶出物和可提取物之间的关系

图2 包材相容性研究过程
2 塑料包装材料可提取物分析方法
2.1 塑料包装材料可提取物的提取
因药物制剂的物理、化学特性的不同,其储藏环境也不同,有些药物制剂本身需要储存于弱酸性或弱碱性等特殊环境,以维持其药物活性[12]。如蛋白类药物制剂,其本身具有弱酸性或弱碱性,因此这类药物需要储存于酸性或碱性环境,以防止蛋白类药物制剂中的活性成分在未使用前就发生变性而降低药物功效。虽然在临床中大多数的药物制剂都是以水为溶剂的亲水性药物,但有些药物是亲油性的,如脂溶性维生素。这些亲油性药物活性成分需要一些乙醇、甘油、丙二醇等亲油性溶剂的辅助溶解才能用于临床输液中,但这些非极性溶剂的引入对药包材来说是一项极大的挑战,可能会增大药物包装中小分子物质的溶出以及增加它们的迁移量[13]。塑料包材中添加剂的种类繁杂,含量较低,其中有些添加剂表现出极端的遗传毒性、肝毒性或致畸性等[14]。包材相容性研究领域的知名研究者Jenke等[15-16]试图汇总大量此类化合物的毒理学信息,但其中许多还没有可用的毒理学数据。此外,因技术保密问题,多数厂家不会完全公开包材全部的成分信息,因此,采用合适的前处理方法,全面提取可提取物至关重要[17]。
目前报道的可提取物质提取方法有超声波辅助提取、索氏提取、微波辅助提取、亚临界提取和超临界提取等[18](见图3)。
超声波辅助提取法通过超声波机械效应和热效应加快分子运动,促进溶剂对待测样品的穿透能力,从而加速溶剂对目标化合物的提取[19]。该提取方法操作简单、成本低,同时可以分析多个样品。但单次提取率不高,需要多次重复提取,因此提取过程耗时,且需要进一步的样品净化操作(如旋蒸、复溶等)。
索氏提取法利用溶剂回流和虹吸原理,使被分析的固体样品每次被提取时跟冷凝回流下的纯溶剂接触,在反复提取的过程,目标物质被提取出来,因此索氏提取法的提取率较高。索氏提取法所需的有机溶剂的用量大,一定的萃取时间内溶剂的回流次数有限,因此所需要的萃取时间较长。此外,提取介质为水溶液时,由于水的沸点较高,回流提取则过于苛刻,可能导致某些有机可提取物发生进一步的降解[4]。
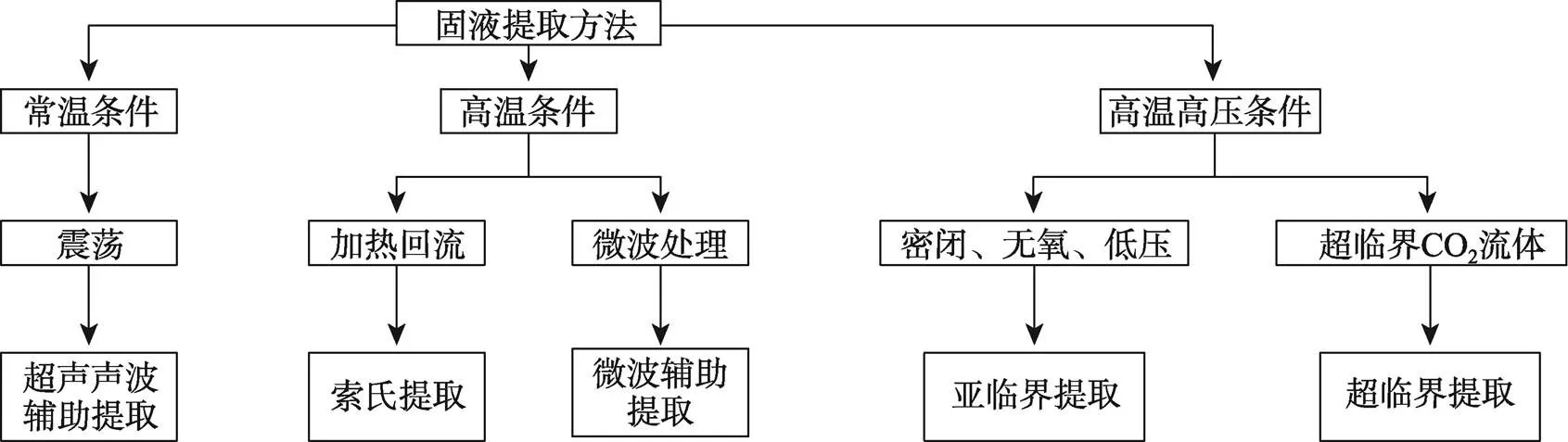
图3 包材可提取物质提取方法
微波辅助提取法通过微波场中各种物料吸收微波能力的差异,使提取体系中的某些组分选择性加热,从而物质内部产生能量差,被提取物质得到足够的动力从体系中分离。微波辅助提取法具有设备简单、适用范围广、提取效率高、重现性好等特点[20],但微波的热效应,使体系的温度升高,可能会降解包材中的部分可提取物质。
亚临界萃取是利用亚临界流体作为萃取剂,在密闭、无氧、低压的压力容器内使物料与溶剂充分接触,使固体物料中的脂溶性成分转移到液态的提取溶剂中,再通过减压蒸发的过程将溶剂与目标物分离。超临界流体萃取法主要利用超临界CO2作为提取剂,通过改变温度和压力改变提取溶剂的性质从而提高提取效率。上述2种方法与传统的超声波辅助提取方法、索氏提取方法相比,具有更加快速、自动化程度更高等特点[21]。但对设备要求较高、较昂贵。
针对塑料包材,美国药典<1663、1665>[22-23]规定,提取温度不超过40 ℃,提取时间为1~21 d。由此可见,上述五种提取方法中超声波辅助提取方法比较适合塑料药物包材可提取物质的提取。通常,以pH=2.5的酸性缓冲溶液,pH=9.5的碱性缓冲溶液及异丙醇水溶液(体积比为1∶1)为模拟提取剂(表1)[4],开展不同周期的加速试验[24]。模拟加速试验结束之后,用二氯甲烷借助超声波辅助提取法,把可提取物质提取出来,旋蒸、复溶、再上机鉴定。
虽然上述方法常用于塑料包材可提取物质的提取,但模拟提取试验周期有待进一步优化。以输液袋为例,输液袋由袋体、袋头、袋尾及输液导管等组成。目前为止,针对包材不同部位的模拟提取试验周期的优化方面鲜有研究,因此,以可提取物质种类和相对含量为参考指标,对模拟提取试验周期进行优化是目前需要解决的问题之一。
2.2 塑料包装材料可提取物分析
在制药工业包装材料和输送系统中塑料包材的使用日益增加,随之塑料包材和所添加的添加剂的种类也增加,导致了各种提取物和溶出物种类的广泛。这些物质根据其浓度和毒理学特性,对患者带来潜在的安全风险,因此,可提取物和溶出物的定性定量分析对验证药品安全性至关重要,近年来已得到监管机构越来越多的重视[25]。由于,塑料包材中的可提取物质种类繁杂,而单一的分析方法无法满足其可提取物质的全景分析要求,因此,根据可提取物性质的不同,如挥发性、半挥发性、非挥发性、金属元素及无机阴离子等,通过非靶向和靶向的方式进行定性、定量分析(见图4)[26]。通常,包材可提取物质成分是未知的,在此情况下采用非靶向分析方法进行筛查,之后对鉴定物质的毒理学特性进行分析。若有存在安全隐患的物质,如有致癌或诱变效应的硝胺类、2–巯基–苯并噻唑、多环芳烃等,针对这些物质进行靶向分析,即用该化合物的标准品用外标法进行定性定量,再结合安全阈值评价该包材的安全性[27]。若研究者目的是寻找抗氧化剂、增塑剂、润滑剂等特定物质,则对这类物质也进行靶向分析,如图4所示的脂肪酸类、聚乙二醇等是目前常用的润滑剂。
可提取物质的分析手段比较多,有传统的核磁共振(Nuclear Magnetic Resonance, NMR))和红外光谱法(Infrared Spectrometry, IR),主要用于添加剂的定性分析[17]。Cherif等[28]利用核磁共振分析方法,鉴定了聚乳酸(Polylactic Acid, PLA)材质的包材中的几种抗氧化剂和光稳定剂,Gratia等[29]利用红外光谱法快速鉴定塑料包装中的添加剂Irganox B215。随着分析需求的提高,一些特异性强、分辨率高、分析速度快的气相色谱法(Gas Chromatography, GC)、气相色谱质谱联用法(Gas Chromatography–Mass Spectrometry, GC–MS)、高效液相色谱法(High Performance Liquid Chromatography, HPLC)、高效液相色谱质谱法(High Performance Liquid Chromatography–Mass Spectrometry, HPLC–MS)、超高效液相色谱–四级杆–飞行时间质谱联用法(Ultra–Performance Liquid Chromatography–Quadrupole Time–of–Flight–Mass Spectrometry, UPLC–QTOF–MS)等检测手段应运而生(表2)[30]。
表1 可提取物模拟提取环境及选择依据

Tab.1 Simulated extraction environment and selection basis of extractables
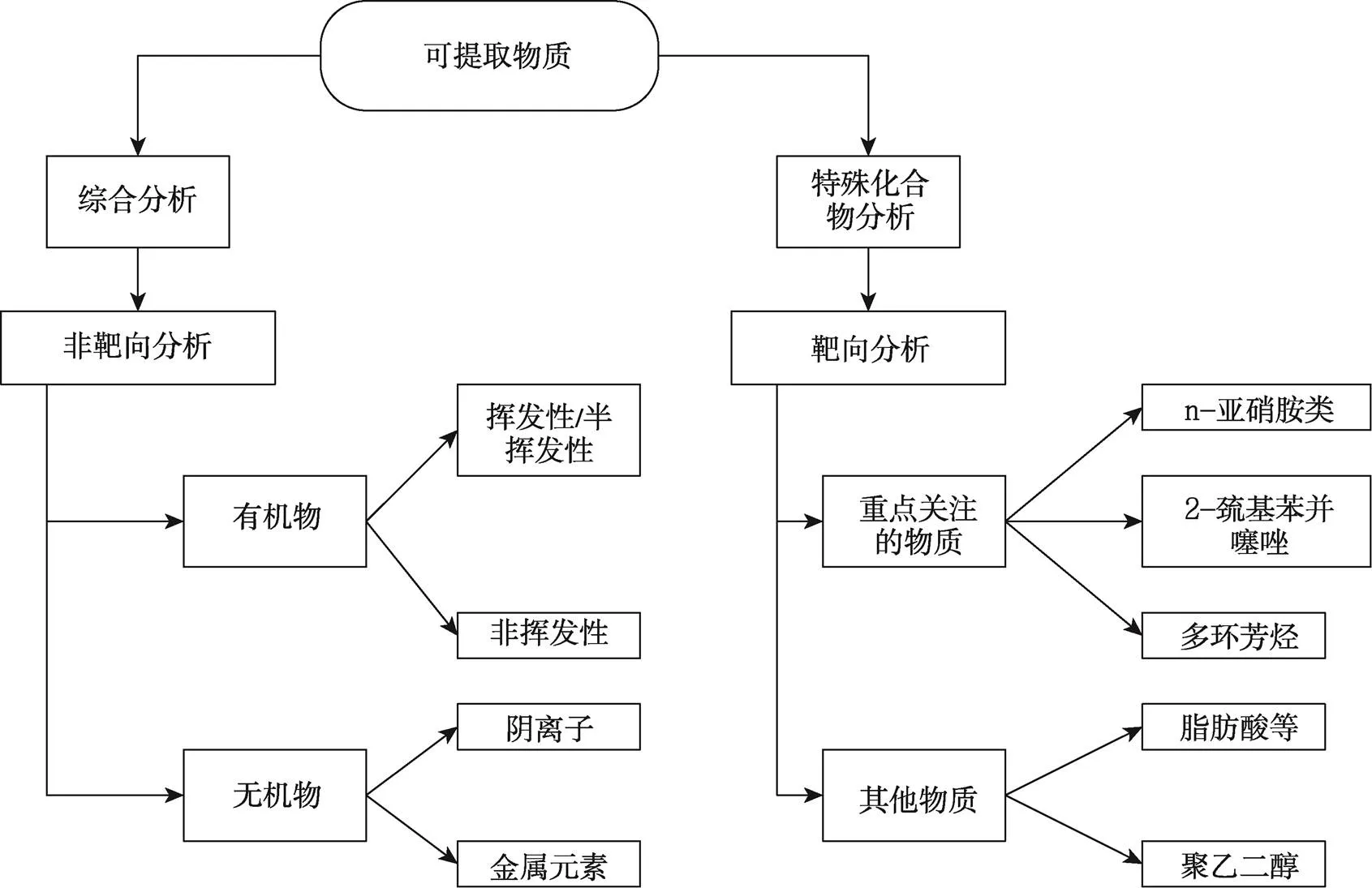
图4 可提取物分析思路
表2 可提取物的检测方法

Tab.2 Methods for detection of extractables
在化合物结构鉴定中,色谱–质谱联用技术因其高灵敏度和特异性而成为首选。气相色谱质谱联用(GC–MS)技术由于70 eV下EI质谱的可重复性,建立了基于计算机的质谱库(NIST数据库),目前普遍使用于挥发性和半挥发性未知化合物的鉴定[31]。通过GC–MS鉴定未知化合物的基本流程见图5[25]。若实验目的为对包材提取物进行全景分析,则采用非靶向分析方法,综合分析实验测出来的保留指数与NIST库上的保留指数大小、NIST库上显示的可能性(Probability)大小,以及质谱图与检测的物质质谱图匹配度等3个因素,再定性未知物。若实验目的为分析具体的物质,如抗氧化剂、增塑剂等,则通过外标法进行靶向分析,并根据保留时间和峰面积比例,对目标物质进行定性定量(见图5)。Zdravkovic等[32]采用GC–MS方法分析了药品包材中的31种半挥发性化合物。Fekete等[33]采用GC–MS的方法,检测了输液软袋中挥发性化合物。Jenke等[30]通过GC–MS,HPLC–DAD–MS及ICP–MS的方法,对滴眼液瓶中的可提取物(挥发性、半挥发性、非挥发性及金属元素)进行全景分析。
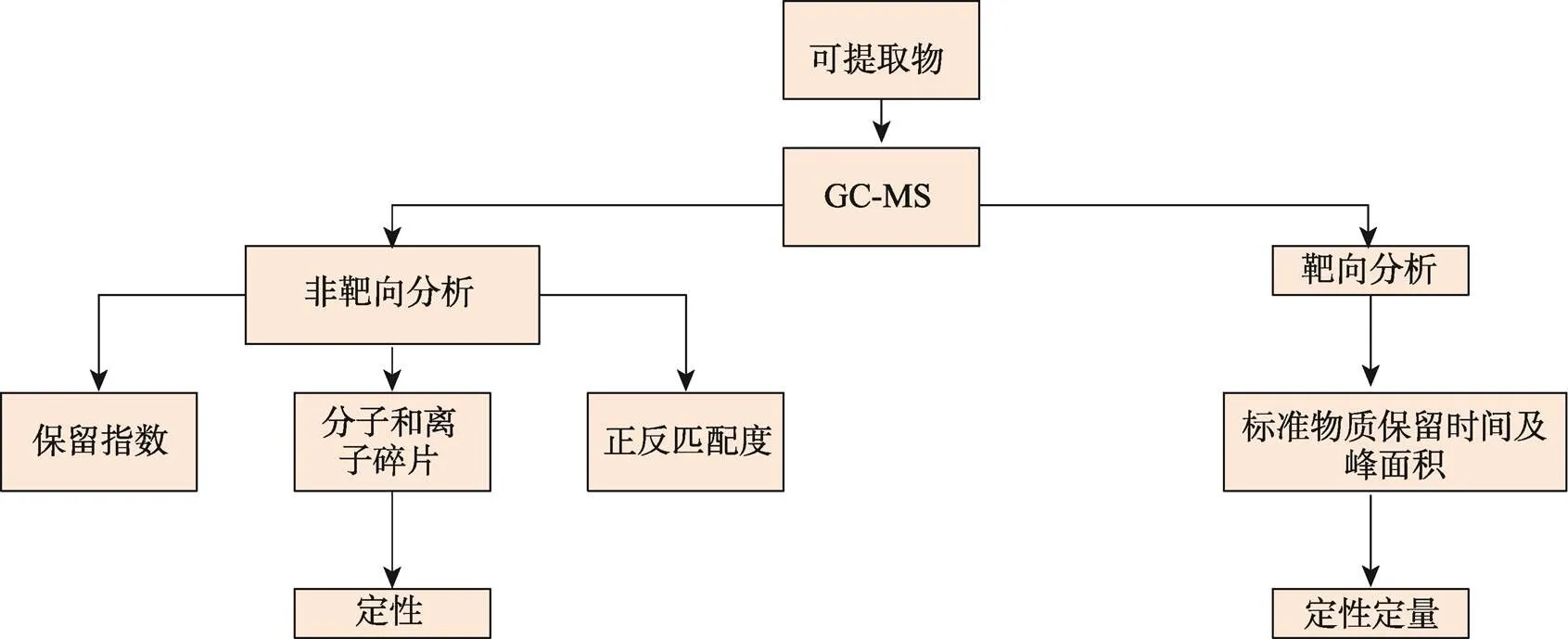
图5 可提取物中挥发性和半挥发性物质的GC–MS分析流程
液相色谱质谱联用(LC–MS)技术具有良好的色谱分离效果和质谱的高分辨率、高灵敏度、重现性佳、方法稳定、结果准确可靠等特点。因此,成为复杂样品分析时优先选择的分析技术,近年来常用于包材中迁移到食品和药物的微量物质的分析[34]。应旭辉等[35]采用液质联用技术分析葡萄糖注射液输液袋中烷醇酰胺类浸出物。结果显示,从6个厂家收集的12批葡萄糖注射液中鉴定出10种主要的烷醇酰胺类浸出物,浸出物质量浓度为1.1~41.1 μg/mL,烷醇酰胺类浸出物迁移率大多在90% 以上。岳志华等[36]通过LC–MS技术研究了异丙托溴铵气雾剂药包材的药物相容性。结果发现,异丙托溴铵气雾剂中有效成分含量降低,而检测出了两种未知杂质,分别为添加于塑料包材的抗氧剂BHT和2246。
虽然LC–MS技术有检测范围广、分离效果好、灵敏度高等特点,但不同的仪器公司的质谱设计有一定的差异,设置参数存在一些差异,在这种情况下相同的电离模式下,各个离子的丰度比也有差异,LC–MS筛查库的统一具有一定难度,目前还没有商业化的用于LC–MS筛查化合物的基础数据库,因此,用LC–MS确定未知化合物需要建立相应的数据库[37]。UPLC–QTOF–MS方法具有较高的分离效率和高分辨率,在目标化合物的筛选方面表现良好,当UPLC–QTOF–MS方法用于数据库检索时,可进一步提高未知化合物的鉴定效率。Zhang等[38]用UPLC–QTOF–MS的方法,在MSE模式下进行数据采集,建立了174种用于塑料包材的聚合物添加剂在UNIFI在线添加剂筛查谱库中能搜到的标准质谱库(建库流程见图6),且对从塑料包装中迁移到疫苗的溶出物进行全面筛查,确定了疫苗包材特有的4种添加剂,同时发现了一种未知化合物,并借助该化合物的碎片离子以及ChemSpider网站上的相关信息,确定了该未知化合物,该化合物为2–羟基间环己烷甲酸甲酯(也是一种塑化剂)。
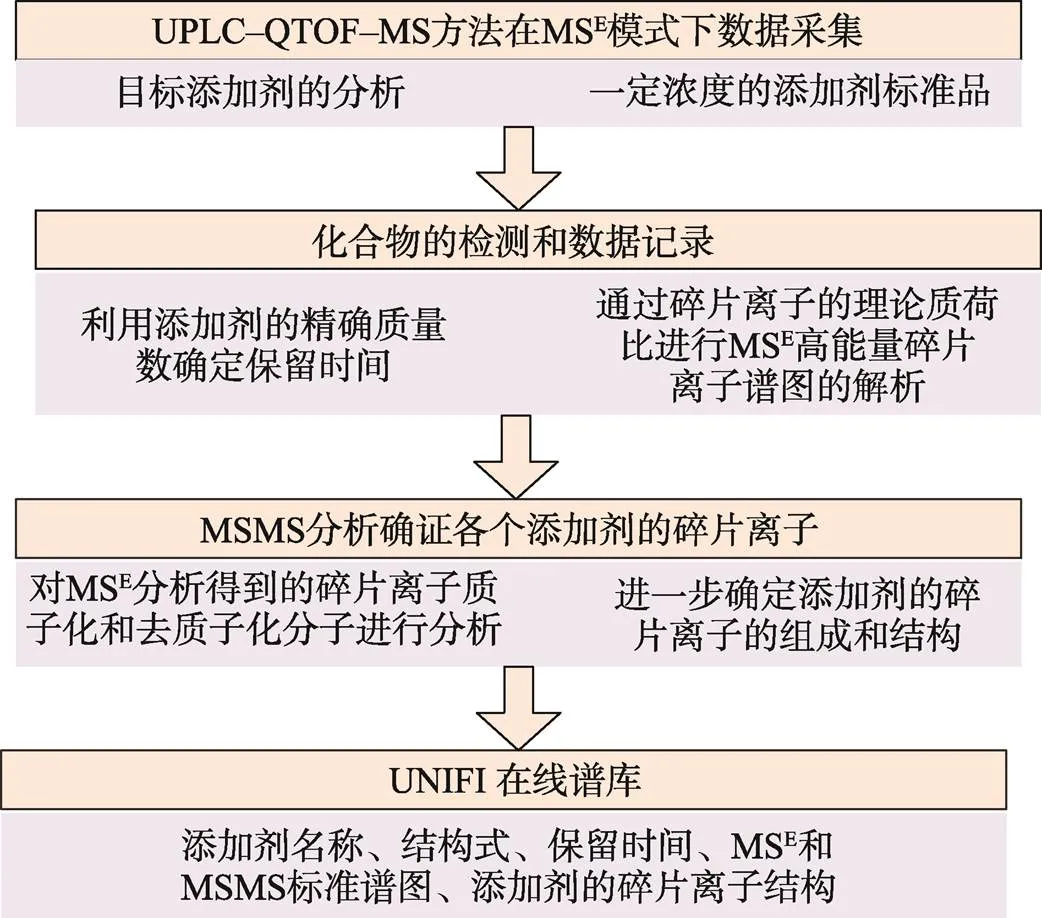
图6 UPLC–QTOF–MS的方法建立数据库的具体流程
2.3 塑料包装材料可提取物数据库建立概况及展望
据文献报道,塑料包材添加剂种类多大200多种,包括低分子量的挥发性和高分子量的非挥发性物质[39]。目前,通过已有的NIST在线数据库,可鉴定挥发性和半挥发性物质,而针对非挥发性物质,目前美国AB SCIEX公司中国分公司(SCIEX中国)、上海微谱科技有限公司建立了药包材可提取物质相关的数据库、但只限于公司内部使用。Zhang等[38]建立了174种聚合物添加剂UPLC–QTOF–MS谱库。该数据库具有精确质量数检索,质谱图检索及分子式检索等多种检索方式,通过UNIFI在线添加剂筛查普库,对包材可提取物质(迁移物质)进行筛查和鉴定。
综上,目前药物塑料包材可提取物质相关的数据库建立比较缺乏,根据所查阅的文献,对建立数据库方面提出2点的建议:针对挥发性或半挥发性成分,通过文献统计学,汇总国内外文献报道的包材挥发性物质,并将它列入相关包材数据库中;针对非挥发性成分,基于前人的研究方法结合文献统计学,继续丰富原有的数据库,增加物质类别,针对不同检测仪器建立相应的数据库。
3 结语
塑料药物包材中可提取物质的鉴定,并对其安全性评估对确保患者生命安全至关重要。要了解可提取物对药品治疗效果和患者的影响,就需要对可提取物进行全景分析、并进行毒理学评价。而塑料包材是用途广泛,含有多种添加剂的复杂体系,目前针对塑料包材可提取物质的研究方法比较单一,大多数研究主要集中于抗氧化剂、塑化剂、引发剂等某一类物质类别的鉴定和其安全性评价上,缺乏全景分析,尤其是建立相应数据库方面具有比较大的研究空间。基于此,文中提出建议如下。
1)包材可提取物质提取方面:优化现有的模拟提取试验周期,将同一类别的塑料包材的试验周期尽可能统一。
2)包材迁移物质的分析方面:将目标物质不要仅限于国家市场监督管理总局指出的抗氧化剂、塑化剂等几类物质,扩大目标物质的范围,做到全面提取、全面分析、并采用SwissADME、AI Lab等在线毒理学评估系统初步评估鉴定的迁移物质的毒理学特性,若有必要后期开展毒理学实验,分析其潜在的危害。
3)促进相关数据库的建立,为PVC(聚氯乙烯)、PP(聚丙烯)、PE(聚乙烯)及PLA(聚乳酸)等不同材质的药物包材成分和迁移物质的鉴定提供基础数据库。
[1] 蒋煜, 马玉楠, 霍秀敏, 等. 《化学药品注射剂与塑料包装材料相容性研究技术指导原则》解读——提取迁移试验方法设计[J]. 中国新药杂志, 2014, 23(15): 1738-1742.
JIANG Yu, MA Yu-nan, HUO Xiu-min, et al. Interpretation of the Guidance of Compatibility Study of Injections and Plastic Packaging Materials-Extract and Migration Study Design[J]. Chinese Journal of New Drugs, 2014, 23(15): 1738-1742.
[2] 方旻, 梁伊琳, 谢新艺, 等. 药品包装与药品的相容性研究进展[J]. 中国包装, 2018, 38(7): 78-81.
FANG Min, LIANG Yi-lin, XIE Xin-yi, et al. Research Progress of Drug Packaging and Drug Compatibility[J]. China Packaging, 2018, 38(7): 78-81.
[3] UBEDA S, et al. Migration Studies and Toxicity Evaluation of Cyclic Polyesters Oligomers from Food Packaging Adhesives[J]. Food Chemistry, 2020, 311: 125918.
[4] CUADROS-RODRÍGUEZ L, LAZÚEN-MUROS M, RUIZ-SAMBLÁS C, et al. Leachables from Plastic Materials in Contact with Drugs. State of the Art and Review of Current Analytical Approaches[J]. International Journal of Pharmaceutics, 2020, 583: 119332.
[5] HERMABESSIERE L. Occurrence and Effects of Plastic Additives on Marine Environments and Organisms: A Review[J]. Chemosphere, 2017, 182: 781-793.
[6] 朱玲风. 食品药品包装材料中抗氧化剂毒理学研究[D]. 长沙: 中南林业科技大学, 2013: 12-23.
ZHU Ling-feng. A Toxicological Security Study of the Antioxidant in the Food and Pharmaceutical Packaging Materials[D]. Changsha: Central South University of Forestry & Technology, 2013: 12-23.
[7] 黄梓为, 方旻, 谢新艺. 2-巯基苯并噻唑在注射用丹曲林钠中的迁移试验及其评估[J]. 广东化工, 2021, 48(15): 23-25.
HUANG Zi-wei, FANG Min, XIE Xin-yi. The Determination and Migration Result of 2-MBT in the Dantrolene Sodium[J]. Guangdong Chemical Industry, 2021, 48(15): 23-25, 17.
[8] PAN Chang-kang, et al. Strategy for Identification of Leachables in Packaged Pharmaceutical Liquid Formulations[J]. Journal of Pharmaceutical and Biomedical Analysis, 2008, 46(3): 520-527.
[9] 崔萍. 化学药品注射剂中三种亚剂型模型药物与包装材料的相容性研究[D]. 南京: 南京工业大学, 2016: 20-45.
CUI Ping. Study on Compatibility of Three Sub-Dosage Model Drugs and Packaging Materials in Chemical Injection[D]. Nanjing: Nanjing University of Technology, 2016: 20-45.
[10] JENKE D. Compatibility of pharmaceutical products and contact materials safety considerations associated with extractables and leachables[M]. Hoboken, NJ: John Wiley, 2009: 252-261.
[11] JENKE D, et al. Evaluation of the Chemical Compatibility of Plastic Contact Materials and Pharmaceutical Products; Safety Considerations Related to Extractables and Leachables[J]. Journal of Pharmaceutical Sciences, 2007, 96(10): 2566-2581.
[12] 庄劲聪. 多层共挤聚乙烯输液袋中可提取物和溶出物的安全性研究[D]. 北京: 北京化工大学, 2018: 15-32.
ZHUANG Jin-cong. Research on Safety of Extractables and Leachables of Multi-Layer Co-Extrusion Polyethylene Infusion Bags[D]. Beijing: Beijing University of Chemical Technology, 2018: 15-32.
[13] LEGRAND P, et al. Development of an HPLC/UV Method for the Evaluation of Extractables and Leachables in Plastic: Application to a Plastic-Packaged Calcium Gluconate Glucoheptonate Solution[J]. Journal of Pharmaceutical and Biomedical Analysis, 2018, 155: 298-305.
[14] BALL D J, NORWOOD D L, STULTS C L M, et al. Leachables and Extractables Handbook: Safety Evaluation, Qualification, and Best Practices Applied to Inhalation Drug Products[M]. Hoboken, NJ, USA: John Wiley & Sons, Inc., 2012.
[15] JENKE D. Safety Risk Categorization of Organic Extractables Associated with Polymers Used in Packaging, Delivery and Manufacturing Systems for Parenteral Drug Products[J]. Pharmaceutical Research, 2015, 32(3): 1105-1127.
[16] JENKE D, CARLSON T. A Compilation of Safety Impact Information for Extractables Associated with Materials Used in Pharmaceutical Packaging, Delivery, Administration, and Manufacturing Systems[J]. PDA Journal of Pharmaceutical Science and Technology, 2014, 68(5): 407-455.
[17] 张云. 基于色谱质谱技术的食药塑料包装材料中添加剂的分析及其迁移行为的研究[D]. 北京: 北京化工大学, 2017: 9-42.
ZHANG Yun. Analysis and Migration of Polymer Additives in Plastic Packagings for Food and Drugsbased on Chromatography and Mass Sepctrometry Technologies[D]. Beijing: Beijing University of Chemical Technology, 2017: 9-42.
[18] BESTWICK D, COLTON R. Extractables and Leachables from Single-Use Disposables[J]. BioprocessInternational, 2009, 62(3): 88-94..
[19] MORETA C, TENA M T. Determination of Plastic Additives in Packaging by Liquid Chromatography Coupled to High Resolution Mass Spectrometry[J]. Journal of Chromatography A, 2015, 1414: 77-87.
[20] STONE T E. An Overview of Risk-Assessment Strategies for Extractables and Leachables[J]. Biopharm International, 2012, 25(1): 39-45.
[21] ARIAS M, PENICHET I, YSAMBERTT F, et al. Fast Supercritical Fluid Extraction of Low- and High-Density Polyethylene Additives: Comparison with Conventional Reflux and Automatic Soxhlet Extraction[J]. The Journal of Supercritical Fluids, 2009, 50(1): 22-28.
[22] USP. Plastic Components and Systems Used to Manufacture Pharmaceutical Drug Products (1665) [M]. Rockville: United States Pharmacopeia, 2019: 1-12.
[23] USP. Assessment of Extractables Associated with Pharmaceutical Packaging/Delivery Systems (1663) [M]. Rockville: United States Pharmacopeia, 2017: 3-17.
[24] QI Li, LIU J, RONK M, et al. A Holistic Approach of Extractables and Leachables Assessment of Rubber Stoppered Glass Vial Systems for Biotechnology Products[J]. Journal of Pharmaceutical Sciences, 2021, 110(11): 3580-3593.
[25] SINGH G, DL B, CL B, et al. Analytical Challenges and Recent Advances in the Identification and Quantitation of Extractables and Leachables in Pharmaceutical and Medical Products[J]. TrAC Trends in Analytical Chemistry, 2021, 141: 116286.
[26] GÖRÖG S. Critical Review of Reports on Impurity and Degradation Product Profiling in the last Decade[J]. TrAC Trends in Analytical Chemistry, 2018, 101: 2-16.
[27] MOYER K L, SCULL J R, RUBERTO M. Extractables and Leachables[M]. Specification of Drug Substances and Products. Amsterdam: Elsevier, 2020: 535-557.
[28] CHERIF L M, et al. Characterization of Plastic Packaging Additives: Food Contact, Stability and Toxicity[J]. Arabian Journal of Chemistry, 2017, 10: S1938-S1954.
[29] GRATIA A, et al. A Comprehensive NMR Methodology to Assess the Composition of Biobased and Biodegradable Polymers in Contact with Food[J]. Analytica Chimica Acta, 2015, 853: 477-485.
[30] JENKE D, EGERT T, HENDRICKER A, et al. Simulated Leaching (Migration) Study for a Model Container-Closure System Applicable to Parenteral and Ophthalmic Drug Products[J]. PDA Journal of Pharmaceutical Science and Technology, 2017, 71(2): 68-87.
[31] DEMPSTER A J. A New Method of Positive Ray Analysis[J]. Physical Review, 1918, 11(4): 316-325.
[32] ZDRAVKOVIC S A Solid Phase Extraction in Tandem with GC/MS for the Determination of Semi-Volatile Organic Substances Extracted from Pharmaceutical Packaging/Delivery Systems via Aqueous Solvent Systems[J]. Journal of Pharmaceutical and Biomedical Analysis, 2015, 112: 126-138.
[33] FEKETE Z, RÓFUSZ T, ANGYAL V, et al. Gas Chromatographic-Mass Spectrometric Analysis and Subsequent Quality Improvement of Plastic Infusion Packaging Materials[J]. Journal of Pharmaceutical and Biomedical Analysis, 2014, 97: 111-115.
[34] 郭子立. 基于液质联用技术的猫须草多组分分析与酚类成分的药代动力学研究[D]. 杭州: 浙江工业大学, 2020: 8-12.
GUO Zi-li. Multicomponent Analysis of Orthosiphon Stamineus Benth. by LC-MS Technologies and Pharmacokinetics of Phenols[D]. Hangzhou: Zhejiang University of Technology, 2020: 8-12.
[35] 应旭辉, 张育乐, 鲁梦霞, 等. 基于液质联用技术分析葡萄糖注射液包装材料中烷醇酰胺类浸出物[J]. 中国药品标准, 2018, 19(1): 68-76.
YING Xu-hui, ZHANG Yu-le, LU Meng-xia, et al. Analysis of Alkanolamide Leachables from Packaging Materials of Glucose Injection by LC-MS Method[J]. Drug Standards of China, 2018, 19(1): 68-76.
[36] 岳志华, 沈甸甸, 胡昌勤. 异丙托溴铵气雾剂药包材和药物相容性研究[J]. 药学学报, 2010, 45(8): 1035-1038.
YUE Zhi-hua, SHEN Dian-dian, HU Chang-qin. The Compatibility between Packing Material and Ipratropium Bromide Aerosol[J]. Acta Pharmaceutica Sinica, 2010, 45(8): 1035-1038.
[37] 马之攀, 任理顺, 侯军. 液质联用仪最佳校准条件选择分析[J]. 品牌与标准化, 2021(6): 25-26.
MA Zhi-pan, REN Li-shun, HOU Jun. Selection and Analysis of Optimum Calibration Conditions for LC-MS[J]. Brand & Standardization, 2021(6): 25-26.
[38] ZHANG Yun, SUN Shu-qi, XING Xue-bin, et al. Detection and Identification of Leachables in Vaccine from Plastic Packaging Materials Using UPLC-QTOF MS with Self-Built Polymer Additives Library[J]. Analytical Chemistry, 2016, 88(13): 6749-6757.
[39] ZIMMERMANN L, AD A, CV B, et al. Are Bioplastics and Plant-Based Materials Safer than Conventional Plastics?Toxicity and Chemical Composition[J]. Environment International, 2020, 145: 106066.
Overview of Comprehensive Analysis of Extractables from Plastic Pharmaceutical Packaging Materials
TUERSUNTUOHETI Tuohetisayipu1,SUN Zhao-zeng1,HAN Jian-xun1,2,SONG Wei1,Wei Hai-yan1,XIAO Jin-jin1
(1. Pony Testing International Group Co., Ltd., Beijing 100095, China; 2. Beijing Academy of Inspection and Certification Co., Ltd., Pony Testing International Group, Beijing 100095, China)
The work aims to summarize the detection and analysis methods for the extractables, including volatile, semi-volatile, non-volatile substances and metal elements form plastic pharmaceutical packaging materials to provide reference for panoramic analysis and safety evaluation of the extractables of plastic pharmaceutical packaging materials. By searching the relevant publications at home and abroad, the analysis methods of different extractables in plastic pharmaceutical packaging materials were summarized. At present, plastic pharmaceutical packaging materials in our country are updated day by day, but the analysis method is fairly single to comprehensively analysis the extractables of plastic pharmaceutical packaging materials. Especially, the database about the extractables has not been established. The research on compatibility of pharmaceutical packaging materials has just started. In allusion to the aforementioned problems, it is urgent to build a method with high resolution, sensitivity, specificity and wide range of screening to have an overall analysis on the extractables of plastic pharmaceutical packaging materials and reduce medical safety issues caused by the plastic pharmaceutical packaging materials.
plastic pharmaceutical packaging materials; combability of packaging materials; extractables; combination of chromatography-mass spectrometry
TB484.3
A
1001-3563(2022)23-0182-09
10.19554/j.cnki.1001-3563.2022.23.022
2022−03−09
科技服务品牌机构发展(20220467097);2022年度北京市博士后基金(2022–ZZ–053)
托合提萨伊普·图尔荪托合提(1987—),女,博士,主要研究方向农产品加工与储藏,医药包材安全性评价。
韩建勋(1983—),博士,副研究员,主要研究方向为药品质量与安全控制。
责任编辑:曾钰婵
