基于新处方工艺的尿素乳膏长期稳定性考察*
2022-12-20朱欣然沈佩亚胡恩实
朱欣然 ,闫 希 ,沈佩亚 ,胡恩实 ,程 钢 △
(1. 中国药科大学药学院,江苏 南京 211198; 2. 安徽医科大学第一附属医院药剂科·国家中医药管理局中药化学三级实验室,安徽 合肥 230022; 3. 中国药科大学中药学院,江苏 南京 211198)
尿素乳膏是皮肤科常用非处方药,主要成分为尿素,可使角质蛋白溶解变性,增进角质层的水合作用,从而使皮肤柔软,防止干裂,同时具有抗菌和止痒作用[1]。目前,主药含量为15%的制剂市场无销售,仍依靠医院自制制剂满足市场需求。安徽医科大学第一附属医院自制尿素乳膏的最早处方来源于《安徽省医院制剂规范:1999 年版》[2]140,处方为油包水(W/O)型乳膏,但有效期短,随存放时间的延长外观性状易改变,涂布延展性差等。20世纪80年代改基质为水包油(O/W)型,采用混合共融法配制,即取制备乳膏基质的所有成分置同一容器中,加热熔化至80~90 ℃,然后加入尿素,搅拌成型,油相、水相无需分开配制,步骤简单,但成品在贮存期的稳定性差,易失水变粗,析出结晶和干粉,有效期仅为6个月。参考文献并结合多次试验结果,最终确定参照《安徽省医院制剂规范:1999 版》中复方二氧化钛乳膏处方[2]151,以 O/ W 型为乳膏基质,采用混合乳化剂,并增加单硬脂酸甘油酯为稳定剂,拟提高制剂的稳定性。本研究中考察了新旧处方制剂的外观性状和物理稳定性,以及新处方留样制剂12 个月的稳定性,为处方、配制工艺和产品有效期的确立提供参考。现报道如下。
1 仪器与试药
1.1 仪器
Agilent1200 型高效液相色谱仪(美国Agilent 公司),包括 G1310A 型四元泵、G1314BVWD 型紫外检测器、手动进样器、Agilent1200 色谱工作站、DT-230A 型柱温箱;BT25S 型电子天平(赛多利斯科学仪器< 北京>有限公司,精度为十万分之一);FA2004 型电子天平(上海精科天平公司,精度为万分之一);BiosaferSB-3200 DT-6L 型超声清洗仪(南京赛飞生物科技有限公司,功率为180 W,频率为40 kHz);SPX-150B-Z型生化培养箱(上海博讯实业有限公司);XL-3型霉菌培养箱(上海虹浦仪器厂);DM6B 型正置双目生物显微镜(德国Leica公司)。
1.2 试药
尿素乳膏(医院制剂,新处方制剂批号分别为20201104,20201109,20201112;旧处方制剂批号为20201125);尿素对照品(北京盛世康普化工技术研究院,批号为#S14A8134007,纯度100%);胰酪大豆胨琼脂培养基(批号为20181221 - 00),沙氏葡萄糖琼脂培养基(批号为20180129 - 00),胰酪大豆胨液体培养基(批号为20181218-00),甘露醇氯化钠琼脂培养基(批号20180122 - 00),十六烷三甲基溴化铵培养基(批号为20180415 - 00),均购自杭州微生物试剂有限公司;乙腈(美国Tedia 公司,批号为20125104);灭菌注射用水(四川科伦药业股份有限公司,批号为M21011101A,规格为每支500 mL)。
2 方法与结果
2.1 尿素乳膏制备
取白凡士林30 g、单甘酯50 g、液体石蜡65 g、硬脂酸150 g 作为油相,取纯化水400 g、甘油100 g、十二烷基硫酸钠2 g、三乙醇胺2 g、羟苯乙酯1 g 作为水相,分别加热至85 ℃,在搅拌过程中将油相缓缓加入水相中,形成初乳,继续搅拌,使温度降至70~75 ℃,同时取约100 g 纯化水,加热至 70 ℃,加入尿素 150 g 使溶解,继续加热至70 ℃,将尿素溶液缓缓加入初乳中,边加边搅拌,持续搅拌至冷凝,即得。按以上处方和配制工艺制备3 批(批号分别为20201104,20201109,20201112)尿素乳膏,每批200盒,每盒装量50 g。
2.2 尿素含量测定
2.2.1 色谱条件[3]
色谱柱:Zorbax NH2柱(250 mm × 4.6 mm,5 μm);流动相:乙腈 - 水(90∶10,V/V);流速:1.0 mL/min;检测波长:190 nm;柱温:25 ℃;进样量:10 μL。
2.2.2 溶液制备
取尿素对照品30.7 mg,精密称定,置50 mL棕色容量瓶中,加流动相溶解并定容,摇匀,即得质量浓度为0.614 mg/mL 的对照品贮备液;取 5 mL,置 10 mL 容量瓶中,用流动相稀释并定容,摇匀,即得质量浓度为0.307 mg/ mL 的对照品溶液。取样品(批号20201104)0.5 g,精密称定,置50 mL 烧杯中,加流动相20 mL,水浴加热使溶解,放至室温,冰浴30 min,滤过,滤液转移至50 mL 棕色容量瓶中,放至室温,用流动相稀释并定容,摇匀;精密吸取2 mL,置10 mL 容量瓶中,以流动相稀释并定容,摇匀,即得供试品溶液。按处方比例制备不含尿素的空白基质乳膏,按供试品溶液制备方法制备阴性对照品溶液。
2.2.3 方法学考察
专属性考察:精密吸取2.2.2 项下对照品溶液、供试品溶液、阴性对照品溶液各10 μL,按2.2.1项下色谱条件进样分析,记录色谱图。结果供试品溶液色谱图中尿素的保留时间约为7.04 min,色谱峰峰形良好,阴性对照无干扰。色谱图见图1。
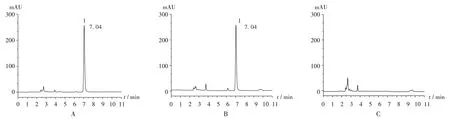
图1 高效液相色谱图Fig.1 HPLC chromatograms
线性关系考察:精密吸取2.2.2项下对照品贮备液0.2,0.5,1.0,2.0,3.0,4.0,5.0 mL,置5 mL容量瓶中,加流动相稀释并定容,摇匀,按2.2.1 项下色谱条件进样分析。以质量浓度(X,μg/mL)为横坐标、峰面积(Y)为纵坐标进行线性回归,得回归方程Y = 6.328 6X+84.936(r=0.999 7,n=7)。结果表明,对照品溶液质量浓度在61.4~614.0 μg/mL 范围内与峰面积线性关系良好。
检测限与定量限确定:精密吸取2.2.2项下对照品贮备液适量,加流动相逐级稀释,按2.2.1 项下色谱条件进样分析,以3 倍信噪比(S/N)的质量浓度为检测限,10 倍S/N的质量浓度为定量限。结果检测限为8.94 μg/mL,定量限为29.80 μg/mL。
精密度试验:精密吸取2.2.2 项下对照品溶液(质量浓度为0.307 mg/mL)10 μL,按2.2.1项下色谱条件连续进样测定3 d,每天重复测定6 次,记录峰面积。结果日内精密度试验结果的RSD为0.61%(n= 6),日间精密度试验结果的RSD为1.42%(n=18),表明仪器精密度良好。
稳定性试验:精密吸取2.2.2 项下同一批(批号20201104)供试品溶液10 μL,配制完成后分别于室温放置 0,2,4,6,8,10,12 h 时进样测定。结果峰面积的RSD为0.51%(n=7),表明供试品溶液室温下放置12 h内稳定性良好。
重复性试验:取样品(批号为20201104)适量,按2.2.2 项下方法平行制备供试品溶液6 份,分别进样测定,以外标法计算尿素的标示百分含量。结果平均含量为100.33%,RSD为0.75%(n=6),表明方法重复性良好。
加样回收试验:取已知含量的样品(批号20201104)0.5 g,精密称定,置烧杯中,加20 mL 流动相,水浴加热至溶解,冰浴30 min,抽滤,定容至50 mL 棕色容量瓶中,摇匀。精密吸取1 mL,置10 mL 容量瓶中,共9份,分别精密加入对照品贮备液2.0,2.5,3.0 mL,各3 份,分别稀释并定容,摇匀,进样测定,计算回收率。结果见表1。
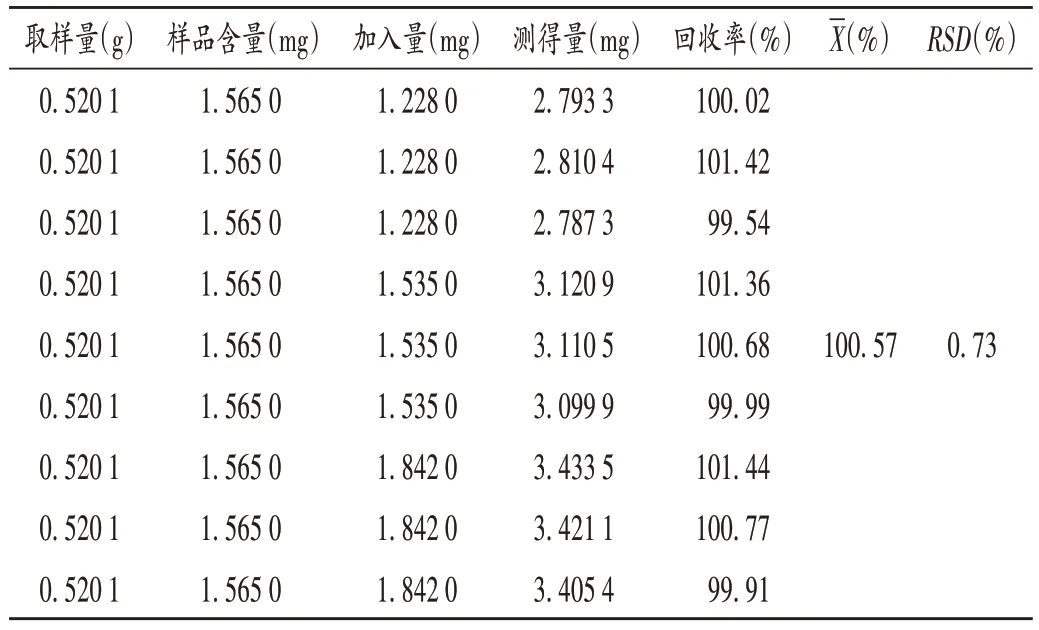
表1 加样回收试验结果(n=9)Tab.1 Results of the recovery test(n=9)
2.2.4 样品含量测定
取3批(批号分别为20201104,20201109,20201112)样品各适量,精密称定,按2.2.2 项下方法制备供试品溶液,按2.2.1 项下色谱条件进样测定,以外标法计算尿素的标示百分含量。结果3批样品的尿素含量分别为99.66%,97.71%,97.53%。
2.3 长期稳定性考察
长期稳定性考察在接近药品实际贮存条件下进行,为药品的最佳贮存条件、制订药品有效期提供依据。根据2020 年版《中国药典(四部)》通则9001 规定,设计常温(25±2)℃铝塑膜封口加盖、常温未封口直接加盖、冷藏(5±3)℃铝塑膜封口加盖、冷藏未封口直接加盖4 组,每组取 3 批采用市售包装,于制备后 0,3,6,9,12 个月末取样,重点考察其性状、粒度、装量、含量、微生物限度[4]457的变化。
性状:新处方样品质地均匀、细腻,稠度适宜,易于涂布,在皮肤上具有良好的涂布延展性和滞留性,无变色、酸败、变硬、油水分离等变质现象。12 个月观察期内,各组均未出现酸败、异臭、变色、分层等现象,但常温未封口组出现了较明显的发粗干燥现象,涂布延展性下降,部分留样旋盖附近有少量结晶粉末析出。
粒度:取样品少许,置载玻片上,加少许注射用水拌匀[5],涂抹薄层面积等同于盖玻片面积,共3片,覆上盖玻片,轻压使颗粒分布均匀,按2020 年版《中国药典(四部)》通则0982粒度与粒度分布测定法第一法(显微镜法)检视[4]145,应无凝聚现象,并不得检出50 μm 及以上的粒子。结果各组样品12 个月观察期内均未出现粒径超过50 μm及以上的粒子。
装量:灌装前,分别称量空包装盒质量、灌装后称量总质量,二者之差即为样品的初始装量(0 个月),按规定条件贮存,分别于制备后0,3,6,9,12 个月末称量总质量,并与初始总质量比较,求得装量变化。结果见表2。可见,12个月观察期内,各组尿素乳膏的装量在各考察时间点均有不同程度的减少,按减少量由高到低排序为常温未封口>冷藏未封口>常温封口>冷藏封口,常温未封口组批间和批内差异均较大,其他各组批间和批内差异小。其中,常温未封口组样品(批号为20201112)12 个月末装量减少接近5%,达到不合格临界值[4]138,而冷藏封口组各批号样品在整个观察期内装量基本不变。表明是否经铝塑膜封口是影响尿素乳膏装量变化的关键因素,尿素乳膏装量减少的主要原因为水分挥发,铝塑膜具有良好的水汽阻隔性,能有效减少因药品水分挥发和/或空气中水分侵入导致的装量变化。考虑到在实际使用中铝塑膜均为撕开状态,密封性能下降,为有效延长药品的有效期,推荐贮存方式为拆封前常温贮存,无需冷藏,拆封后冷藏贮存。
表2 不同贮存条件下尿素乳膏12个月装量变化(,g,n=6)Tab.2 Changes of deliverable volume of urea cream prepara⁃tions under the different conditions for 12 months(,g,n=6)

表2 不同贮存条件下尿素乳膏12个月装量变化(,g,n=6)Tab.2 Changes of deliverable volume of urea cream prepara⁃tions under the different conditions for 12 months(,g,n=6)
装量变化贮存条件 批号 初始装量常温封口常温未封口冷藏封口冷藏未封口20201104 20201109 20201112 20201104 20201109 20201112 20201104 20201109 20201112 20201104 20201109 20201112 55.16±3.17 54.79±1.18 50.70±2.15 54.01±2.10 55.44±4.18 55.10±1.06 55.89±3.84 55.60±3.97 51.47±3.01 56.00±2.28 54.16±4.58 54.58±1.01 3个月末-0.03±0.01-0.03±0.01-0.02±0.01-0.43±0.23-0.64±0.32-0.95±0.78 0.00±0.02 0.00±0.01-0.01±0.01-0.08±0.03-0.10±0.09-0.13±0.05 6个月末-0.04±0.01-0.04±0.01-0.03±0.01-0.69±0.36-1.07±0.53-1.48±1.13 0.02±0.03 0.01±0.01-0.01±0.02-0.16±0.03-0.22±0.17-0.18±0.07 9个月末-0.01±0.01-0.01±0.01 0.00±0.01-0.92±0.42-1.46±0.65-2.11±1.68-0.01±0.02-0.01±0.02-0.02±0.03-0.38±0.17-0.39±0.26-0.29±0.11 12个月末-0.06±0.01-0.07±0.01-0.05±0.01-1.20±0.43-1.69±0.62-2.55±1.74-0.02±0.01-0.01±0.02-0.01±0.02-0.41±0.10-0.46±0.28-0.33±0.12
含量:依据尿素乳膏质量标准,本制剂含尿素(H2NCONH2)应为标示量(g/g)的90.0%~110.0%[6]。分别于0,3,6,9,12 个月末按 2.2.1 项下色谱条件测定以上4 组尿素乳膏制剂中尿素的含量。结果见表3。可见,12 个月观察期内,各批样品有效成分含量均呈增加趋势,按增加程度由高到低排序为常温未封口> 冷藏未封口>常温封口>冷藏封口,批间差异较小。增加程度与装量变化相对应,即装量减少越多,含量增加越多,同样由水分挥发所致。尽管4 组各批次尿素乳膏有效成分含量均在90.0%~110.0%之间,符合药品质量标准,但水分挥发可导致膏体变性,影响涂布延展性等。故推荐的存方式仍为拆封前常温贮存,无需冷藏,拆封后冷藏贮存。
表3 不同贮存条件下尿素乳膏12个月含量测定结果(,%,n=3)Tab.3 Results of the content determination of urea in urea cream preparations under different conditions for 12 months(,%,n=3)
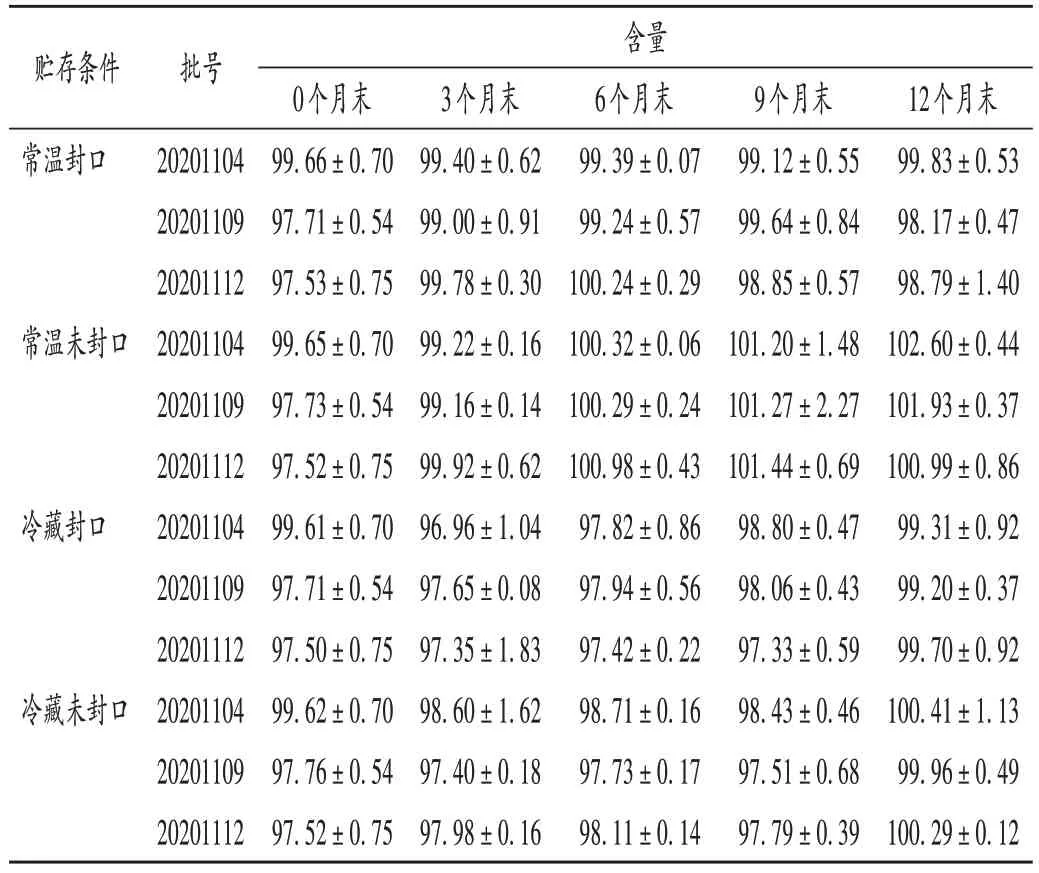
表3 不同贮存条件下尿素乳膏12个月含量测定结果(,%,n=3)Tab.3 Results of the content determination of urea in urea cream preparations under different conditions for 12 months(,%,n=3)
含量贮存条件 批号常温封口常温未封口冷藏封口冷藏未封口20201104 20201109 20201112 20201104 20201109 20201112 20201104 20201109 20201112 20201104 20201109 20201112 0个月末99.66±0.70 97.71±0.54 97.53±0.75 99.65±0.70 97.73±0.54 97.52±0.75 99.61±0.70 97.71±0.54 97.50±0.75 99.62±0.70 97.76±0.54 97.52±0.75 3个月末99.40±0.62 99.00±0.91 99.78±0.30 99.22±0.16 99.16±0.14 99.92±0.62 96.96±1.04 97.65±0.08 97.35±1.83 98.60±1.62 97.40±0.18 97.98±0.16 6个月末99.39±0.07 99.24±0.57 100.24±0.29 100.32±0.06 100.29±0.24 100.98±0.43 97.82±0.86 97.94±0.56 97.42±0.22 98.71±0.16 97.73±0.17 98.11±0.14 9个月末99.12±0.55 99.64±0.84 98.85±0.57 101.20±1.48 101.27±2.27 101.44±0.69 98.80±0.47 98.06±0.43 97.33±0.59 98.43±0.46 97.51±0.68 97.79±0.39 12个月末99.83±0.53 98.17±0.47 98.79±1.40 102.60±0.44 101.93±0.37 100.99±0.86 99.31±0.92 99.20±0.37 99.70±0.92 100.41±1.13 99.96±0.49 100.29±0.12
微生物限度:取样品10 g,加无菌5%聚山梨酯80溶液(45 ℃保温)至100 mL,混匀,制成1∶10 供试液。取1∶10 供试液按平皿法进行需氧菌、霉菌和酵母菌总数的计数,采用常规法分别进行金黄色葡萄球菌、铜绿假单胞菌的检查,按2020 年版《中国药典》四部通则1105与通则 1106[4]161检查应符合规定。分别于 0,3,6,12 个月末取样进行微生物限度检查,结果3 批(批号分别为20201104,20201109,20201112)样品的需氧菌、霉菌和酵母菌菌落计数均低于10 cfu/g,均未检出金黄色葡萄球菌、铜绿假单胞菌。可见,3 批常温未封口组乳膏剂在12个月内微生物限度合格,因该贮存方式相对其他3种方式更易染菌,进而可推断4 种贮存方式在12 个月考察期内均可满足制剂微生物限度要求。
2.4 新处方工艺与原处方制剂稳定性比较
2.4.1 处方与配制工艺
原处方与新处方成分组成见表4。
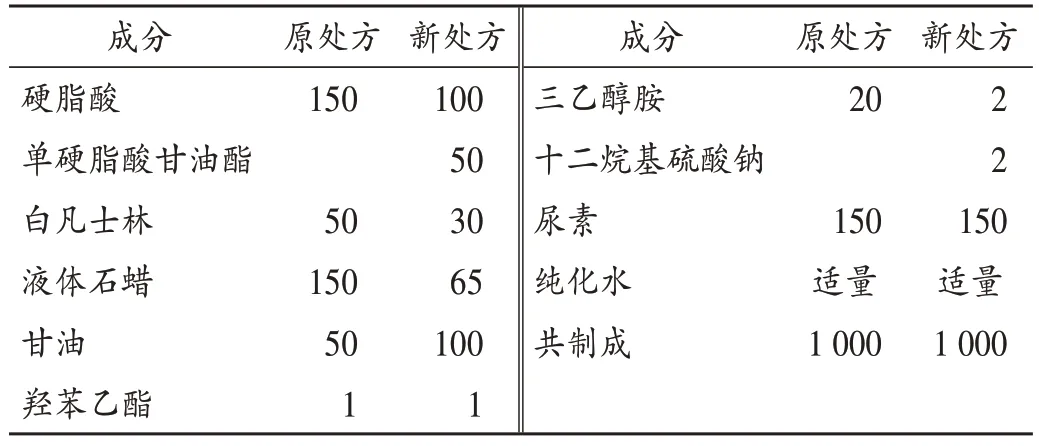
表4 尿素乳膏处方(g)Tab.4 Prescriptions of the urea cream preparations(g)
原处方采用混合共融法配制,步骤简单,但加入尿素后会使膏体变粗,必须放置20 h 以上再搅拌,才能使膏体细腻。究其原因,一是使用单一乳化剂(三乙醇胺与硬脂酸反应生成的一价皂硬脂酸三乙醇胺)乳化效果差,加入尿素时必须快速搅拌,而搅拌过快又会将尿素溶解时产生的气泡带入膏体,使乳膏失去细腻光泽感[7];二是尿素占比较大,其溶解时大量吸热会使体系温度快速降低,导致乳膏凝固、膏体变粗。
新处方采用油相加入水相法,使用混合乳化剂(十二烷基硫酸钠和三乙醇胺与硬脂酸反应生成一价皂,提高了乳膏剂的稳定性[8];处方中增加了单硬脂酸甘油酯作为稳定剂和增稠剂,兼有一定乳化作用。初乳形成后加入温度(70 ℃)与之相近的尿素溶液,不需加大搅拌速度,膏体一次成型,避免了因温度骤降而使膏体变粗。此外,按新处方制备的乳膏剂降温后即可灌装,缩短了配制时间,同时也减少了放置过程中微生物污染的可能性。故新处方成品优于原处方。
2.4.2 稳定性比较
性状:观察原处方(批号为20201125)与新处方样品(批号为20201104)0,3,6,12个月末的性状。结果0个月末时,二者性状差异不明显;3 个月末时,原处方乳膏可见增粗;6 个月末时,原处方乳膏已有尿素结晶和基质细粉析出,颜色由亮白变为暗白,光滑度、细腻度均下降,但新处方乳膏仍保持细腻、光滑、易涂布的性状。
粒度:取常温未封口组的原处方样品(批号为20201125)与新处方样品(批号为20201104),按2020年版《中国药典(四部)》通则0982粒度与粒度分布测定法第一法(显微镜法)检视[4]145,于显微镜下观察,每个样品量取并记录乳粒粒径各100 个,求得各样品乳粒粒度[7,9]。结果显示,原处方乳膏的乳粒粒径大小不稳定,随着时间的延长,乳粒粒径呈增大趋势(3~6 μm);而新处方乳膏的乳粒粒径小于原处方,且大小均一稳定(1.8~1.9 μm),粒径在12 个月观察期内变化不大。可见,新处方乳膏更加细腻,储存稳定性明显提高。
含量与装量:取常温未封口组的原处方样品(批号为20201125),分别于0,6,12 个月末测定含量和装量,结果含量分别为101.22%,104.64%,109.20%,装量分别为50.44,46.91,43.22 g,虽未超出上限(110%),但12个月末的装量已不合格,故原处方样品稳定性差,有效期仅为6 个月。新处方样品在12 个月考察期内均合格,稳定性好。
3 讨论
3.1 含量测定方法选择
尿素乳膏的质量标准源自2020年版《中国药典(四部)》[4]138,含量测定采用的是显色后紫外 -可见分光光度法,即对二甲氨基苯甲醛与尿素反应生成黄色的对二甲氨基苯缩脲衍生物后,于420 nm 波长处测定衍生物吸光度,计算出尿素含量。属间接测定,易受温度、避光时间、操作人员熟练程度的影响,且显色剂二甲氨基苯甲醛溶液于420 nm 波长处有较大吸收,导致样品测定误差增大[10]。检验发现,该方法重复性差,准确度低,不能准确反映乳膏剂的真实含量。故本试验中参考文献[3,11],采用高效液相色谱法测定尿素乳膏的含量。
尿素含有2 个氨基,是小分子极性化合物,采用普通C18柱的保留较弱,尿素出峰快,混杂在溶剂峰中,难以分离。有研究报道,尿素含量测定采用的色谱柱有氨基柱[3,11]、亲水色谱柱Xbridge Amide[12]、阳离子交换色谱柱Zorbax 300SCX[13]等,其中氨基柱最常见、使用较多,其氨基键合相为极性固定相,可有效地延长尿素的保留时间。故本试验中采用氨基柱。
预试验中,比较了多种流动相,包括乙腈-水(90∶10,V/V),乙腈 -0.1%磷酸溶液(90∶10,V/V),乙腈 - 甲醇 - 水(89∶10∶1,V/V/V),发现乙腈 - 水(90∶10,V/V)已可满足较好的峰形、分离度和理论板数,不必采用更复杂的流动相,故以此为流动相。曾比较190 nm和200 nm测定波长,发现190 nm 波长处较200 nm 波长处的响应值高,故选择190 nm 为检测波长。曾比较甲醇、乙醇、水和乙腈-水(90∶10,V/V)分别加热溶解提取,发现甲醇溶解会产生较大溶剂峰,造成基线不平;乙醇溶解会导致尿素峰拖尾;水溶解会造成油性基质无法除去,过滤时吸附尿素使测定值减小;采用流动相溶解最好,乳膏基质干扰小,没有溶剂峰,基线平稳。故选择乙腈- 水(90∶10,V/V)为提取溶剂。
3.2 新处方乳膏稳定性考察结果分析
文献[14]研究表明,导致乳膏性质改变的主要因素是水分的散失。12 个月观察期内,从性状上看,常温未封口组出现较明显的发粗、干燥现象,部分留样旋盖附近有少量结晶粉末析出;装量减失按由高到低排序为常温未封口> 冷藏未封口> 常温封口> 冷藏封口,含量增加按由高到低排序为常温未封口> 冷藏未封口> 常温封口> 冷藏封口,增加程度与装量变化相对应,即装量减少越多,含量增加越多。
依据2020年版《中国药典》最低装量检查法“20~50 g固体、半固体每个容器的装量不得少于标示装量的95%,即不得减少标示量的5%”。常温未封口组样品(批号为20201112)第12 个月装量减少接近5%,为不合格品,而冷藏封口组各批号样品在整个观察期内装量基本不变。可见,是否经铝塑膜封口是影响尿素乳膏稳定性的关键因素,而封口状态下是否冷藏对尿素乳膏稳定性的影响不大。为延长其有效期,应尽量减少水分散失,推荐贮存方式为拆封前常温贮存,无需冷藏,拆封后冷藏贮存。
新处方为混合乳化剂,采用分别加热配制的方法,配制方法为将内相加入外相的逆相转型法[15],不需转相,转型后细腻度佳,无颗粒感。本研究中性状对比、粒度检查、耐热试验、耐寒试验、离心试验等物理稳定性研究结果表明,新处方乳膏稳定性好,乳粒的粒径明显小于原处方,膏体洁白细腻,有光泽,无粗糙感,具有适宜的黏稠度和涂布延展性,久置不分层,无结晶析出。综合考察试验结果和临床治疗需求,最终选择新处方工艺投入生产。医院制剂的特点是批量小、批次多、周转快、有效期一般在1 年内,故本试验中暂考察了12 个月的稳定性。结果表明,新处方制剂的有效期可延长至12 个月,为使结论更可靠,还需进一步考察18~24 个月的稳定性。目前,本试验中采用的尿素乳膏市售包装为聚乙烯塑料盒,未来可更换为铝塑复合管、铝制软管等再进行试验,以寻找最佳包装方式和贮藏条件。
