ANCA相关性血管炎合并膜性肾病伴亚急性肾小管间质损伤1例
2022-12-20胡文慧居红格
胡文慧,张 伟,2,居红格,2
(1.包头医学院,内蒙古包头 014040;2.包头医学院第一附属医院病理科)
相关性血管炎(associated vasculitis ,AAV)是一组血清中检测到抗中性粒细胞胞浆抗体(antineutrophil cytoplasmic antibody ,ANCA)为特点的系统性血管炎,主要累及肺和肾脏,病理特点为小血管全层的炎症、坏死、伴或不伴肉芽肿形成[1]。膜性肾病(membranous nephropathy ,MN)则是肾病综合征最常见的病理类型,二者同时发生的案例较少,易被忽略而延误治疗。笔者通过报道1例AAV合并MN伴亚急性肾小管间质损伤案例并查阅相关文献,旨在学习此类疾病的临床病理表现及用药指南,为医务人员的诊疗提供相关证据并制定更有效的治疗方案。
1 临床资料
1.1基本病史 患者女性,46岁,主诉血肌酐高1个月,于2021年10月7日以“肾功能不全”收入我院。病史:患者1个月前体检无明显诱因发现血肌酐高(163 μmol/L),偶有尿中泡沫增多,后就诊于包钢医院,查24 h尿蛋白定量3.06 g,白蛋白36 g/L,ANA 1∶160(+),PANCA+(1∶32),MPO+,抗SSA抗体+,抗RO-52抗体+;肾脏彩超示双肾实质质地轻度改变,血红蛋白98 g/L,未系统治疗,自动出院。患者自病发以来精神状态一般,食欲一般,睡眠良好,大小便正常,体力情况良好,体重无明显变化。既往史:否认肝炎、结核、疟疾病史,否认高血压、心脏病史,否认糖尿病、脑血管疾病、精神病史,否认手术、外伤、输血史,否认食物、药物过敏史,预防接种史不详。
1.2查体 体温36.5 ℃,脉搏80次/min,呼吸20次/min,血压120/80 mmHg,发育正常,营养良好,正常面容,表情自如,自主体位,神志清楚,合作;心前区无隆起,心尖搏动正常,心浊音界正常,心率80次/min,律齐,各瓣膜听诊区未闻及杂音,无心包摩擦音;双肺呼吸音清晰,未闻及干湿啰音,无胸膜摩擦音;腹平坦,无腹壁静脉曲张,腹部柔软,无压痛、反跳痛,腹部无包块;肝脾未触及,Murphy氏征阴性,肾脏无叩击痛,无移动性浊音;肠鸣音正常,3次/min;双下肢不肿。
1.3辅助检查 (1)血常规:白细胞4.85×109/L, 红细胞3.51×1012/L↓, 血红蛋白111 g/L↓,血小板317×109/L;(2)肝功:白蛋白44.6 g/L, 谷丙转氨酶13 U/L, 谷草转氨酶18 U/L, 肌酸激酶44 U/L, 肌酸激酶同工酶9.9 U/L, 尿素10.5 mmol/L↑,肌酐159 umol/L↑,尿酸354 umol/L,二氧化碳20.5 mmol/L,葡萄糖5.0 mmol/L,钾4.26 mmol/L,钠140.0 mmol/L,氯107.5 mmol/L,钙2.44 mmol/L,磷1.33 mmol/L,镁0.86 mmol/L;(3)甲功三项:促甲状腺激素测定0.30 mIU/L↓,游离三碘甲状原氨酸2.34 pg/mL,游离甲状腺素18.09 pmol/L;(4)甲状旁腺激素测定:103.30 pg/mL↑。入院第2天行尿液相差分析:尿蛋白定性+++,RBC数满视野/(40×10),尿RBC约30 %大小均一,形态基本正常;约70 %RBC大小不等,变形呈面包圈、靶形、虫蛀、花环、影子细胞;尿本周蛋白定性检查为阴性,血κ-轻链8.47 g/L,血λ-轻链7.12 g/L, 尿κ-轻链17.60 mg/dL↑,尿λ-轻链714.60 mg/dL↑,血清游离轻链比值1.19。
1.4病理诊断 经皮肾穿刺活检。免疫荧光:6个肾小球,IgG(+~++)、IgM(+)、C3 (+~++)、C1q(+)、κ链(+++)、λ链(+++);毛细血管袢颗粒状沉积(图1),IgA(-)、FRA(-)。光镜:送检肾穿刺组织包括肾皮质及髓质,可见25个肾小球,其中1个肾小球缺血性硬化,其余肾小球系膜细胞和基质轻度节段性增生,基底膜轻度增厚,上皮下、基底膜内、内皮下、系膜区可见少量嗜复红蛋白沉积,可见毛细血管袢节段纤维素样坏死,局灶足细胞增生,3个小细胞性新月体,2个小细胞纤维性新月体,3个细胞性新月体,肾小管上皮细胞空泡及颗粒变性,多灶状萎缩,少量红细胞管型,肾间质多灶状淋巴-单核细胞浸润伴轻度纤维化,小动脉管壁明显增厚,管腔狭窄(图2-5)。电镜:检测到1个肾小球,毛细血管内皮细胞明显空泡变性,个别管腔内可见红细胞聚集,节段性内皮细胞增生,毛细血管开放,肾小囊壁层增厚、分层,壁层细胞空泡变性,无明显增生;基底膜轻度不规则增厚,厚度300~800 nm;脏层上皮细胞肿胀、空泡变性,足突弥漫融合;系膜细胞和基质增生;上皮下、基底膜内、内皮下、系膜区电子致密物沉积;肾小管上皮细胞空泡变性,部分肾小管基底膜增厚,上皮细胞脱落;肾间质水肿伴少量炎症细胞浸润;个别毛细血管管腔内见红细胞聚集(图6)。诊断 ANCA相关性血管炎合并膜性肾病伴亚急性肾小管间质损伤。

图1 A-F 免疫复合物呈细颗粒沉积于毛细血管袢 (免疫荧光×200)

图2 肾小球(HE染色×40)
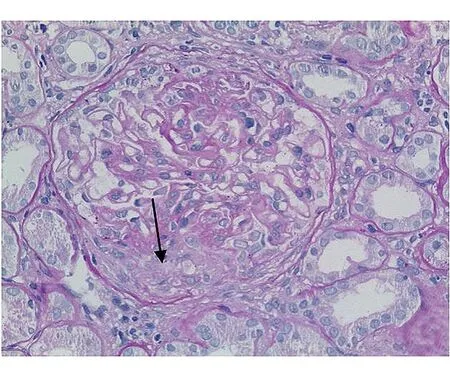
图3 小细胞性新月体形成(PAS染色×400)
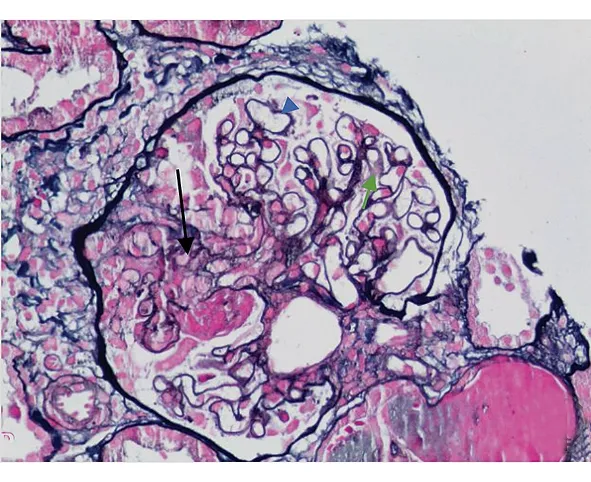
图4 蓝色箭头示钉突形成,黑色箭头示小细胞性新月体形成,绿色箭头示基底膜空泡变性(Masson染色+PASM染色×400)

图5 毛细血管袢嗜复红蛋白沉积(Masson染色×400)
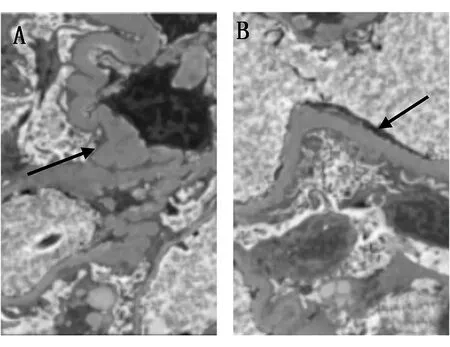
图6 A-B电镜 基底膜不规则增厚,内皮下电子致密物沉积(×5000)
1.5诊治经过 患者血肌酐高病史>1个月,血常规明确存在贫血,完善肾脏彩超明确双肾实质质地轻度改变,且存在基础疾病高血压,故考虑慢性肾脏病可能性大。患者无发热、恶心、呕吐、腹泻容量不足等肾前性因素;既往无特殊药物口服史,不考虑药物加重肾脏损害;患者无尿量明显减少,无中断尿,不考虑肾后梗阻所致肾脏加重。患者无皮肤瘀点、瘀斑,无光过敏,无球结膜充血水肿,无关节疼痛、骨痛,无听力、视力下降,无口干、牙齿片状脱落,完善抗核抗体、ANCA除外继发性肾病,患者感染指标、传染指标阴性。初步诊断:(1)肾功能不全原因待查;(2)肾性贫血可能。治疗上降尿蛋白、保护肾功能对症治疗。随后加做PANCA+,MPO+,诊断考虑ANCA相关性小血管炎、小血管炎肾损害,加用糖皮质激素甲泼尼龙40 mg。患者住院期间,多次发现血压升高150/100 mmHg,后行肾穿刺活检术,病理结合临床最终诊断:ANCA相关性小血管炎、小血管炎肾损害、AAV合并MN伴亚急性肾小管间质损伤、慢性肾脏病3期、肾性贫血、高血压2级。继续原有激素40 mg静点,复查肾功能、24小时尿蛋白定量,加用环磷酰胺50 mg/次,每日2次。经治疗,患者病情平稳,蛋白尿由治疗前3.06 g/24h下降到治疗后的2.26 g/24h,肌酐由163 μmol/L降至119 μmol/L。肾功能明显好转,后康复出院,嘱患者院外避免劳累、感染,避免肾毒性药物的使用,正规糖皮质激素联合免疫抑制剂口服,2周后门诊随诊。
2 讨论
MN是中老年人常见肾脏病理类型,是典型的免疫复合物沉积所致肾炎,免疫荧光显示IgG和C3特征性颗粒状沉积。此患者上皮下、基底膜内、内皮下、系膜区均颗粒状沉积免疫复合物IgG,而AAV多致寡免疫复合物型新月体性肾小球肾炎。该患者无肺部疾病,无免疫系统疾病,临床无特异性表现,只初始血肌酐升高,最终通过血液检查、肾穿刺活检结合临床症状确诊。此病例同时合并肾间质多灶状淋巴细胞、单核细胞浸润,轻度纤维化,小动脉管壁明显增厚,管腔狭窄。
从1993年发现至今,AAV与MN同时发生的案例仍属少见,组合机制尚不明确。在动物模型中证实,ANCA本身无直接损伤肾小球的能力,但是当感染等因素导致中性粒细胞脱颗粒,整合到毛细血管壁并释放多种蛋白水解酶,可能是导致肾小球毛细血管袢受损的原因之一[2]。与此同时,中性粒细胞死亡时形成的中性粒细胞胞外陷阱(neutrophil extracellular traps,NETs)也对血管内皮细胞造成伤害,还可激活补体旁路途径,这与疾病的活动性相关[3]。C3在肾脏沉积与毛细血管增生具有相关性,是肾脏预后不良的指标之一[3]。髓过氧化物酶(MPO)和蛋白酶3(PR3)作为ANCA的两种主要抗原,多出现在AAV血清中,又以MPO型常见,本例为MPO阳性。通过双重免疫荧光和免疫电镜检查,发现AAV伴MN的患者基底膜内共同存在MPO和IgG,推测激活的中性粒细胞释放的MPO可能与肾小球细胞在基底膜结合,从而诱导免疫复合物沉积[4]。Kanahara 等[4]认为免疫复合物在MN初始阶段已在原位形成,随后被ANCA阳性中性粒细胞释放的溶酶体破坏。禹丹等[5]提示MN和AAV的同时发生可能只是偶然的,因为它们在病理上没有关系,一起发生的频率也太低。此外,M型磷脂酶A2受体(PLA2R)为特发性MN的典型抗原,而AAV合并MN的PLA2R沉积率低于特发性MN。特发性MN有典型IgG4沉积,而AAV合并MN以IgG2、IgG3沉积为主,因此考虑两种疾病发生机制有一定相关性。此病例没有进行PLA2R及IgG分型检查。
肾小管间质损伤多发生在肾小球和血管损伤后,多为继发性。本例患者肾小管间质损伤需与MN及药物所致损伤相鉴别。该患者在入我院治疗前未系统性服用药物,故排除药物损伤肾功能致间质损伤;单纯MN以肾小球损伤显著,肾小管间质损伤率低,而在AAV肾病中多数患者伴肾小管间质损伤,因此考虑为血管损伤后的继发事件[6]。董蕾等[7]认为肾小管间质损伤与其周围毛细血管内皮细胞CD34部分丢失有关。谷胱甘肽转移酶、肾脏损伤分子-1(KIM-1)和中性粒细胞明胶酶相关脂质运载蛋白(NGAL)等是肾小管间质损伤的主要标志物;血肌酐、尿素氮的水平,尿液中的一些蛋白质,例如α1微球蛋白和尿β2微球蛋白均与间质损伤程度相关[8]。表皮生长因子(EGF)作为肾小管的主要营养因子,是肾小管间质损伤的特异性标志物。在AAV中,尿中EGF降低与肾小管间质损伤程度及患者预后相关。此外,补体途径选择性标志物Bb和补体调节蛋白CD46也与肾小管萎缩程度相关[6]。因此,Bulanov等[6]认为肾小管间质萎缩和/或纤维化,是不良预后的指标之一。
本病目前无标准治疗方案,多以新月体性肾炎治疗为主,经学习相关资料发现多个指南推荐使用激素联合环磷酰胺(Cyclophosphamide, CTX)方案,必要时行血浆置换,经积极治疗后,仍有部分患者病情继续恶化、治愈率较低。有研究[9]显示血浆置换对本病的短期疗效好、长期疗效无明显优势。预后不仅取决于AAV本身,还取决于肾脏损害程度和靶向药物的副作用,肌酐水平愈高则预后越差。鉴于CYC一定的毒副作用,利妥昔单抗(Rituximab, RTX)在AAV的治疗中获得了有力的循证医学支持,并被纳入现行指南,在合并肾损伤患者中,RTX方案更具有优势。同时,补体C5a受体抑制剂作为新型生物制剂,有望成为最有前景的治疗药物[10]。
3 结论
AAV致不同类型肾炎病例报道常见,病情进展快,预后差,但是合并MN者少见,目前发病机制仍不明确。本例患者无其他系统疾病临床症状,易被忽略。作者报道此病例,希望为临床医务工作者提供相关医学证据,为制定更有效的诊断及治疗方案提供参考。
