血清AgRP、IL-28A在慢性阻塞性肺疾病合并肺动脉高压中的表达及临床意义
2022-12-19仇海兵葛红庭胡中英
孙 艳,仇海兵,葛红庭,胡中英
慢性阻塞性肺疾病(chronic obstructive pulmonary disease, COPD)是呼吸系统常见疾病,全球范围内患病数达3亿人,每年死亡例数达300万例,严重威胁人类健康[1]。COPD时缺氧导致肺动脉重构,平滑肌细胞增殖及凋亡失衡,可导致肺动脉高压(pulmonary hypertension, PH)形成。PH是COPD的重要并发症,可引起右心衰竭,导致COPD患者预后不良。虽然心漂浮导管是目前COPD患者合并PH诊断的金标准,但具有一定的创伤性。因此,寻找非侵入性的能够早期诊断COPD合并PH,同时能反映PH严重程度的血清学指标具有重要临床意义。刺鼠基因相关蛋白(AgRP)基因编码黑皮质素受体3的拮抗因子,通过黑皮质素受体调节下丘脑对摄食行为的控制[2]。研究发现,COPD合并PH患者血清AgRP表达水平下调,可能是新的COPD患者预后相关血清标志物[3]。白细胞介素-28A(IL-28A)基因位于19q13.2,编码蛋白作为一种细胞因子,能与异二聚体型Ⅱ类细胞因子受体相互作用,与呼吸系统疾病关系密切[4-5]。研究表明,鼻病毒感染后能够诱导气道上皮细胞中IL-28A等细胞因子表达水平升高,通过加重气道炎症及氧化应激,促进COPD的疾病进展[6]。本研究通过检测COPD合并PH患者血清AgRP及IL-28A水平,探讨二者与疾病严重程度、肺功能及炎性因子的关系。
1 资料与方法
1.1一般资料 将2019年1月—2021年1月我院诊治的COPD合并PH 122例设为PH组。纳入标准:COPD诊断符合《慢性阻塞性肺疾病诊治指南(2013年修订版)》[7]中诊断标准;PH诊断符合《中国肺高血压诊断和治疗指南2018》[8]诊断标准;年龄18~80岁;患者及家属对本研究知情并签署同意书。排除标准:合并哮喘、肺栓塞等其他肺部疾病;严重的长期高血压、主动脉瓣关闭不全、风湿性心脏病及先天性心脏病等导致的PH;伴有严重肝肾功能障碍;临床资料不完整;妊娠期或哺乳期妇女。根据多普勒超声心动图检测肺动脉收缩压(PAP),分为轻度组(PAP为40~50 mmHg)50例、中度组(PAP为50~70 mmHg)41例、重度组(PAP>70 mmHg)31例。选取同期诊治的单纯COPD 66例为对照组,均符合《慢性阻塞性肺疾病诊治指南(2013年修订版)》[7]中的诊断标准,且多普勒超声心动图检测PAP<40 mmHg。本研究经本院医学伦理委员会审核批准。
1.2血清AgRP、IL-28A及炎性因子检测 取所有研究对象静脉血5 ml,3000 r/min离心5 min,分离上层血清。采用酶联免疫吸附试验(ELISA)检测血清AgRP、IL-28A及肿瘤坏死因子-α(TNF-α)、白细胞介素-6(IL-6)水平。人AgRP ELISA试剂盒购自北京诺为生物公司;人IL-28A ELISA试剂盒购自上海康朗生物科技公司;TNF-α、IL-6 ELISA试剂盒均购自北京索莱宝公司。应用Colorimetric Microplate Reader酶标仪检测。试验步骤按照相应的试剂盒说明书进行操作,每个样本检测3次,结果取平均值。
1.3资料收集 收集所有患者性别、年龄、体质量指数等一般资料。收集入院后心率、收缩压及舒张压、血肌酐、血尿酸、空腹血糖、C反应蛋白(CRP)、总胆固醇、三酰甘油及血气分析指标[动脉血氧分压(PaO2)、二氧化碳分压(PaCO2)]等。所有患者入院后48 h内均进行肺功能检测,采用飞利浦IE33型超声诊断仪(频率2.5~3.75 Hz)检测PAP。
2 结果
2.1一般资料及血清AgRP、IL-28A水平比较 2组年龄﹑性别、体质量指数、吸烟史、空腹血糖、血肌酐、总胆固醇、三酰甘油、心率、收缩压、舒张压比较差异均无统计学意义(P>0.05)。PH组PAP、PaCO2、TNF-α、CRP、IL-6、IL-28A水平高于对照组,而PaO2、AgRP水平低于对照组(P<0.01)。见表1。

表1 2组COPD一般资料及血清AgRP、IL-28A水平比较
2.2不同病情COPD合并PH患者血清AgRP、IL-28A水平、肺功能及炎症指标比较 COPD合并PH患者中,重度组IL-28A、PAP、PaCO2、TNF-α、CRP和IL-6高于中度组和轻度组,而血清AgRP、PaO2水平低于中度组和轻度组(P<0.05);中度组IL-28A、PAP、PaCO2、TNF-α、CRP和IL-6高于轻度组,而血清AgRP、PaO2水平低于轻度组(P<0.05)。见表2。

表2 不同病情COPD合并PH患者血清AgRP、IL-28A水平、肺功能及炎症指标比较
2.3血清AgRP、IL-28A水平与肺功能及炎症指标的相关性 血清AgRP与PAP、PaCO2、TNF-α、CRP、IL-6呈负相关,与PaO2呈正相关(P<0.01);血清IL-28A与PAP、PaCO2、TNF-α、CRP、IL-6呈正相关,与PaO2呈负相关(P<0.01)。见表3。

表3 COPD合并PH患者血清AgRP、IL-28A水平与肺功能及炎症指标的相关性
2.4影响COPD发生PH的多因素Logistic回归分析 以COPD患者是否合并PH为因变量,以AgRP、IL-28A、PAP、PaO2、PaCO2、TNF-α、CRP、IL-6为自变量,行多因素Logistic回归分析结果显示,血清AgRP、IL-28A是COPD发生PH的独立危险因素(P<0.01)。分别把PAP、PaO2、PaCO2、TNF-α、CRP、IL-6带入模型校正后,结果显示,AgRP、IL-28A仍然是COPD患者发生PH的独立影响因素(P<0.01)。见表4。
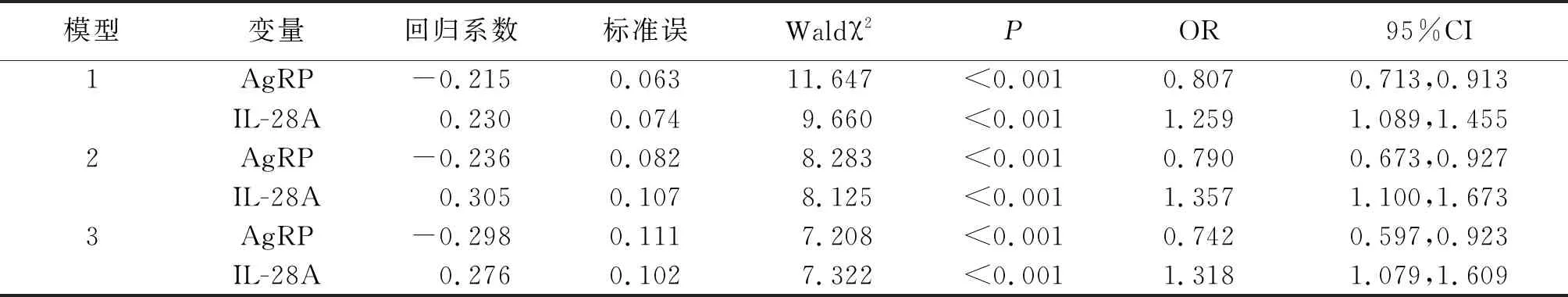
表4 COPD发生PH的危险因素多因素Logistic回归分析
2.5血清AgRP、IL-28A及二者联合对COPD合并PH的诊断价值 绘制血清AgRP、IL-28A及二者联合对诊断COPD合并PH的ROC曲线,二者联合检测时的曲线下面积(AUC)高于血清AgRP、IL-28A单独检测(P<0.01)。见表5,图1。
3 讨论
COPD的病理生理学特点是持续气流受限,肺泡通气不足导致缺氧,二氧化碳蓄积,进而引起肺血管重构,PH形成。合并PH的COPD患者右心负荷增大,右心功能障碍及肺血流量减少,患者心血管疾病和脑卒中的发生率和病死率明显升高。目前临床对于COPD合并PH的诊断主要根据患者临床症状、实验室及超声等检查,但患者临床主要表现为呼吸困难、气短等非特异性症状,早期诊断困难,多数患者确诊时病情已处于中重度,增加了患者的治疗难度。因此,深入研究COPD合并PH的机制,寻找能够早期诊断并反映病情程度的血清标志物,具有较大的临床意义。

表5 血清AgRP、IL-28A及二者联合对COPD合并PH的诊断价值

图1 血清AgRP、IL-28A及二者联合诊断COPD合并PH的ROC曲线
AgRP编码基因位于人类16号染色体,生理条件下,弓状核内的AgRP神经元可分泌产生AgRP,能够通过拮抗黑皮质素受体,抑制黑素细胞刺激激素的释放,促进机体食物摄入并抑制能量消耗[9]。近年来发现,AgRP能够通过调节细胞能量代谢,影响TNF-α等炎性因子的产生,调控炎症反应,与炎症、高血压等疾病关系密切[10-11]。本研究中,COPD合并PH患者血清AgRP表达水平明显降低,提示AgRP可能参与COPD合并PH的疾病发生过程。与ZHANG等[3]研究结果一致。AgRP表达降低的机制可能与COPD合并PH患者炎性因子的调控有关。研究表明,TNF-α、IL-6及IL-1β等促炎因子能够抑制神经细胞AgRP的分泌,进而导致患者急性炎症状态时厌食的发生[12]。本研究中也证实,COPD合并PH患者血清AgRP水平与TNF-α、CRP、IL-6呈负相关,提示机体炎症状态越重,对AgRP表达的抑制作用更明显。此外,COPD合并PH患者血清AgRP水平与肺功能有关,提示AgRP水平降低有助于反映患者肺功能障碍程度。有研究表明,AgRP能够抑制血管内皮细胞中过氧化物的产生,抑制半胱氨酸天冬氨酸蛋白水解酶1诱导的细胞凋亡[13]。因此,AgRP的表达水平降低可能通过促进肺血管内皮细胞功能障碍,诱导肺血管平滑肌细胞的代谢及增殖等过程,促进PH的形成,最终导致COPD合并PH的疾病进展。本研究中,血清AgRP与PAP呈负相关,且是影响COPD合并PH发生的危险因素。研究表明,血清AgRP降低能够激活Toll样受体4,促进下游Jacus激酶的磷酸化,激活炎症反应通路,导致大量活性氧及环氧合酶2的产生,最终导致肺血管重塑及PH的形成[14-15]。
IL-28A编码基因位于19q13.2,又称为IFN-λ,属于Ⅲ型干扰素,能够通过结合IL-28受体1,参与病毒感染过程中的免疫调节[16]。近年来发现,COPD患者往往存在鼻病毒感染,鼻病毒感染的气道上皮细胞的IL-28A等细胞因子表达增加[6],并通过促进氧化应激及病毒感染相关基因的表达,参与COPD的发生。本研究中,COPD合并PH患者血清IL-28A表达显著升高,其原因可能是COPD患者常存在病毒或细菌感染,病原体感染不仅诱导肺上皮细胞中IL-28A的表达,还能够促进单核巨噬细胞中IL-28A的分泌[17]。本研究中,COPD合并PH患者血清IL-28A水平与PAP呈正相关,提示血清IL-28A水平有助于反映PH的严重程度。分析其机制,IL-28A作为Ⅲ型干扰素,能够选择性的作用于肺上皮细胞表面的IL-28受体,通过激活Jacus相关激酶1,促进信号转导和转录活化因子1/2及下游IL-6等促炎因子的表达[18],而炎症反应和低氧进一步导致内皮细胞功能障碍,促进肺血管平滑肌细胞的收缩和增殖,肺血管重塑,促进COPD患者PH的疾病进展。此外,IL-28A水平较高患者,肺通气功能下降也更明显,加重肺组织缺氧及肺血管内皮细胞损伤,促进COPD患者PH的发生发展。本研究发现,IL-28A与TNF-α、CRP、IL-6呈正相关,亦证实IL-28A可能通过促进促炎因子的产生,加重COPD合并PH患者的炎症反应。有学者在动物实验中发现,敲低气道上皮细胞中生长分化因子15的表达,能够抑制IL-28A的表达,增强机体抗病毒免疫反应,抑制感染性颗粒释放,减轻COPD合并PH的疾病严重程度[19]。本研究中,血清IL-28A是影响COPD合并PH发生的独立危险因素,提示检测IL-28A水平有助于评估COPD合并PH发生的风险。ROC曲线分析发现,血清AgRP、IL-28A水平联合检测对COPD合并PH具有较高的诊断效能,表明联合检测可作为评估COPD患者合并PH的重要指标。临床上对于血清AgRP、IL-28A水平较高的COPD患者,应警惕合并PH的风险,予以积极早期诊断并及时干预治疗,以改善COPD合并PH患者的临床预后。
综上所述,COPD合并PH患者血清AgRP降低,IL-28A升高,是COPD合并PH发生的独立危险因素。血清AgRP、IL-28A表达与COPD合并PH患者疾病严重程度、肺功能状况及TNF-α、CRP、IL-6有关,共同参与COPD合并PH的疾病过程。血清AgRP、IL-28A联合检测对COPD合并PH具有较高的诊断效能。但本研究也存在不足之处,因样本量有限,未对研究对象进行分层分析,有待今后扩大样本量,并设计严格的临床试验进一步研究。
