克唑替尼胶囊联合NP方案治疗晚期非小细胞肺癌的效果及对血清NSE、CEA、Cyfra21-1水平的影响
2022-12-19钱伟玲吴沙沙赵红梅
钱伟玲,吴沙沙,赵红梅,徐 硕
非小细胞肺癌(non-small-cell lung cancer, NSCLC)是肺癌常见类型,占全部肺癌的75%~85%,具有发病率高、病死率高等特点[1-2]。NSCLC发病隐匿,早期缺乏典型症状,60%~80%的患者就诊时已错失手术根治机会[3-4]。NP化疗方案(顺铂联合注射用酒石酸长春瑞滨)是目前临床治疗中晚期NSCLC患者的重要方案,可一定程度改善患者生存质量,但疾病控制效果仍不甚理想[5-6]。近年来,针对不同靶点的个体化治疗逐渐应用于临床。间变性淋巴瘤激酶-酪氨酸激酶抑制剂(ALK-TKI)——克唑替尼胶囊于2013年获得NMPA批准用于治疗局部晚期或转移性NSCLC患者,该药可选择性抑制病灶部位棘皮动物微管相关蛋白样4(EML4)-间变淋巴瘤激酶(ALK)融合基因,从而发挥抗肿瘤作用[7]。但有研究显示,由于ALK基因拷贝数扩增、ALK激酶区域二次突变、合并或继发其他基因突变和旁路激活等因素影响,多数患者在应用克唑替尼胶囊治疗10~12个月后会产生耐药性,从而影响整体治疗效果[8]。化疗的主要作用之一是能广泛对抗体内肿瘤细胞,但常规化疗总有效率偏低,而ALK-TKI、化疗联合方案是否能进一步提升疾病控制效果,尚无定论。本研究采用NP方案联合克唑替尼胶囊治疗晚期NSCLC患者,并从肿瘤标志物变化方面量化评估治疗效果。现报告如下。
1 资料与方法
1.1一般资料 选取我院2018年10月—2021年2月收治的NSCLC 62例。纳入标准:均符合NSCLC诊断标准[9],经荧光原位杂交(FISH)检测确认为EML4-ALK阳性;病理分期为ⅢB~Ⅳ期;经CT检查发现有可测量病灶;预计生存期≥3个月;卡氏(KPS)评分>70分,可耐受化疗、靶向治疗;未接受过抗肿瘤治疗;治疗前检查血常规、心肝肾功能及骨髓造血功能正常;患者及家属签署同意书。排除标准:脑转移;合并肺气肿、肺间质纤维化、活动性肺结核、肺炎等肺部疾病;存在严重的全身性或系统性疾病;合并其他恶性肿瘤;治疗期间采取其他抗肿瘤措施;存在精神障碍影响治疗或效果评价者。62例按化疗方法分为观察组和对照组各31例。2组性别、年龄、体质量指数(BMI)等方面比较差异无统计学意义(P>0.05),具有可比性。见表1。本研究经我院伦理委员会审批通过。
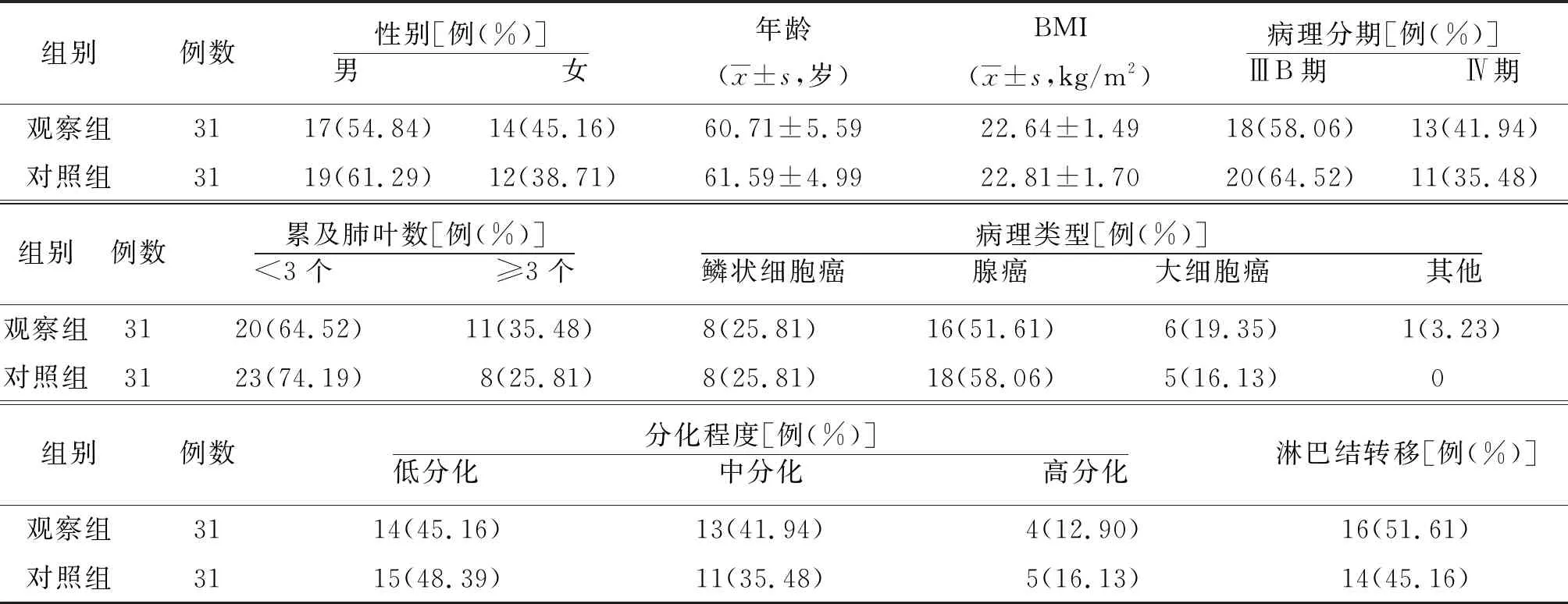
表1 2组晚期NSCLC一般资料比较
1.2方法 对照组采用克唑替尼胶囊(PFIZER EUROPE MA EEIG,批准文号H20171009)250 mg口服,2/d。观察组采用NP方案联合克唑替尼胶囊治疗,克唑替尼胶囊治疗方法与对照组相同。NP方案治疗:静脉滴注注射用酒石酸长春瑞滨(海南通用康力制药有限公司,国药准字H20040477)25 mg/m2,d1、d8;静脉滴注注射用顺铂(齐鲁制药有限公司,国药准字H37021358)25 mg/m2,d1~d3。化疗前应用昂丹司琼预防呕吐,应用奥美拉唑保护胃黏膜。3周为一个治疗周期,治疗期间每3周进行一次血常规、肝肾功能、视力检查,治疗2个周期进行影像学检查,评价效果。
1.3观察指标
1.3.1临床效果:参照实体肿瘤疗效评判标准RECIST1.1[10]分为疾病进展(PD)、稳定(SD)、部分缓解(PR)、完全缓解(CR),以SD、PR、CR计算疾病控制率(DCR)。
1.3.2EML4-ALK阳性率:治疗2个周期后评价。EML4-ALK阳性率评价标准[11]:活检取标本,石蜡切片、脱蜡等预处理,依次实施蛋白酶处理、变性、杂交、细胞核染色,荧光显微镜(200×)随机读取肿瘤细胞50个,若视野内红绿信号间隔2个信号直径或出现单独红色信号即为阳性细胞,阳性细胞计数<5个为阴性,>25个为阳性。若阳性细胞计数5~25个则再读取50个细胞,100个细胞中共计阳性细胞>15个则为阳性,否则为阴性。
1.3.3肿瘤标志物水平:分别于治疗前、治疗2个周期后检测肿瘤标志物水平,并计算差值。检测方法:采集空腹外周静脉血3 ml,离心10 min,半径为8 cm,转速为3500 r/min,取血清,采用电化学发光法检测神经元特异性烯醇化酶(NSE)、癌胚抗原(CEA)、细胞角蛋白19可溶性片段(Cyfra21-1)水平,并比较不同疗效分级患者ΔNSE、ΔCEA、ΔCyfra21-1。分析血清肿瘤标志物差值与疗效的相关性。
1.3.4生存质量:提高为治疗2个周期后KPS评分比治疗前增加≥10分;稳定为治疗2个周期后KPS评分增加或降低<10分;下降为治疗2个周期后KPS评分比治疗前降低≥10分。
1.3.5毒副反应发生率:治疗2个周期后参照CTCAE4.0版[12]评价毒副反应发生情况。
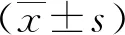
2 结果
2.1临床疗效 观察组PD低于对照组,DCR高于对照组,差异有统计学意义(P<0.05)。见表2。

表2 2组晚期NSCLC临床疗效比较[例(%)]
2.2EML4-ALK阳性率 治疗2个周期后,观察组EML4-ALK阳性1例(3.23%),对照组阳性8例(25.81%)。治疗2个周期后,观察组EML4-ALK阳性率低于对照组,差异有统计学意义(P<0.05)。
2.3血清肿瘤标志物水平 2组治疗前血清NSE、CEA、Cyfra21-1水平比较差异无统计学意义(P>0.05);治疗2个周期后,2组血清NSE、CEA、Cyfra21-1水平均低于治疗前,观察组低于对照组,且观察组ΔNSE、ΔCEA、ΔCyfra21-1小于对照组(P<0.05)。见表3。
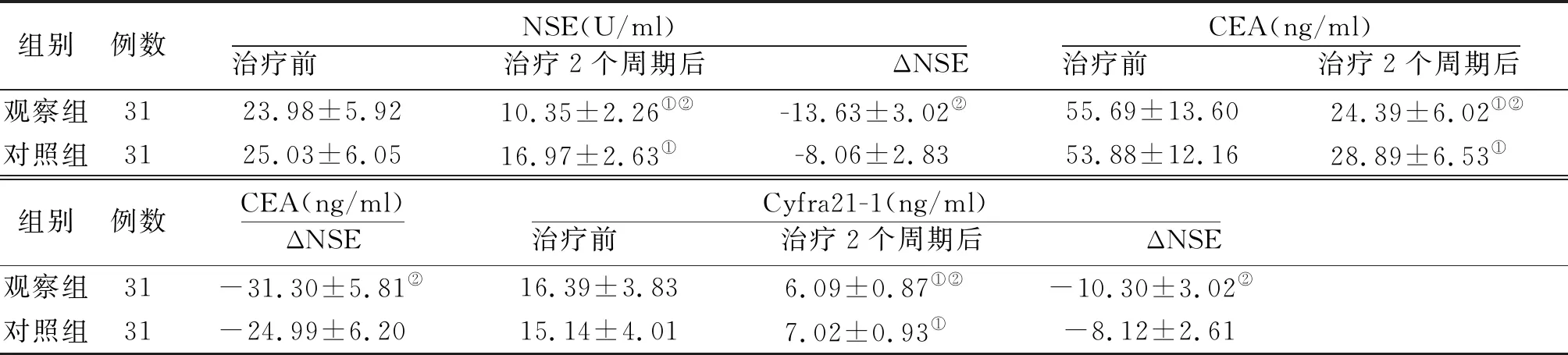
表3 2组晚期NSCLC治疗前后血清肿瘤标志物水平比较
2.4不同疗效分级患者ΔNSE、ΔCEA、ΔCyfra21-1 不同疗效分级患者ΔNSE、ΔCEA、ΔCyfra21-1比较差异有统计学意义(P<0.01);随疗效增加,ΔNSE、ΔCEA、ΔCyfra21-1呈降低趋势,差异有统计学意义(P<0.05)。见表4。

表4 不同疗效分级晚期NSCLC患者ΔNSE、ΔCEA、ΔCyfra21-1比较
2.5治疗前后血清肿瘤标志物差值与临床疗效的相关性 ΔNSE、ΔCEA、ΔCyfra21-1与临床疗效呈负相关(r=-0.611、-0.648、-0.432,P<0.05)。见图1~3。
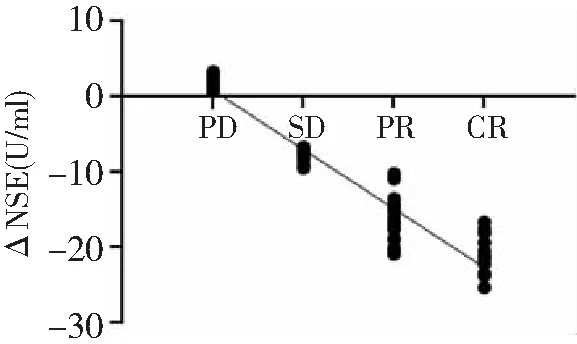
图1 ΔNSE与晚期NSCLC临床疗效的相关性
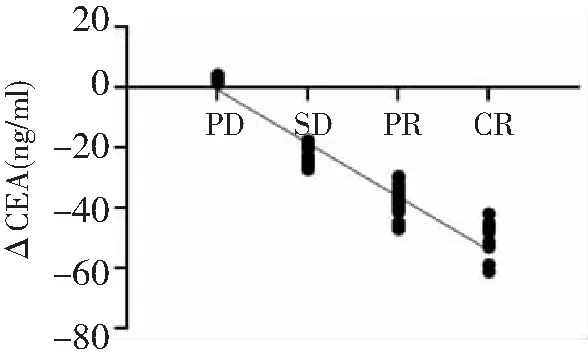
图2 ΔCEA与晚期NSCLC临床疗效的相关性
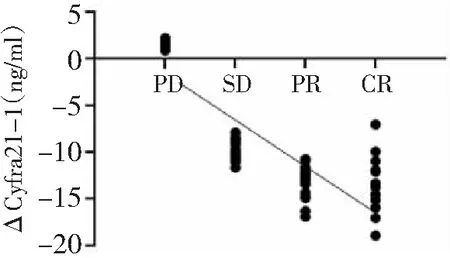
图3 ΔCyfra21-1与晚期NSCLC临床疗效的相关性
2.6生存质量 观察组生存质量优于对照组(P<0.05)。见表5。
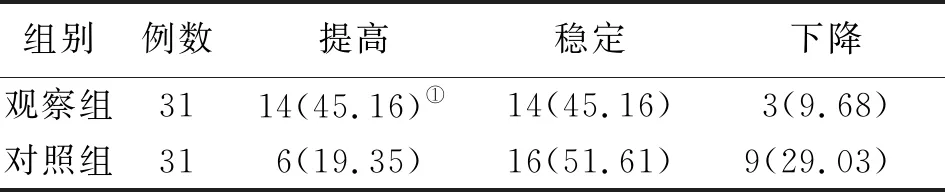
表5 2组晚期NSCLC生存质量比较[例(%)]
2.7毒副反应 2组毒副反应均以Ⅰ~Ⅱ级为主,患者可耐受,经对症治疗后缓解,未出现病死患者。2组骨髓抑制、恶心呕吐、肝功能异常、腹泻、皮疹、视觉异常发生率比较差异无统计学意义(P>0.05)。见表6。
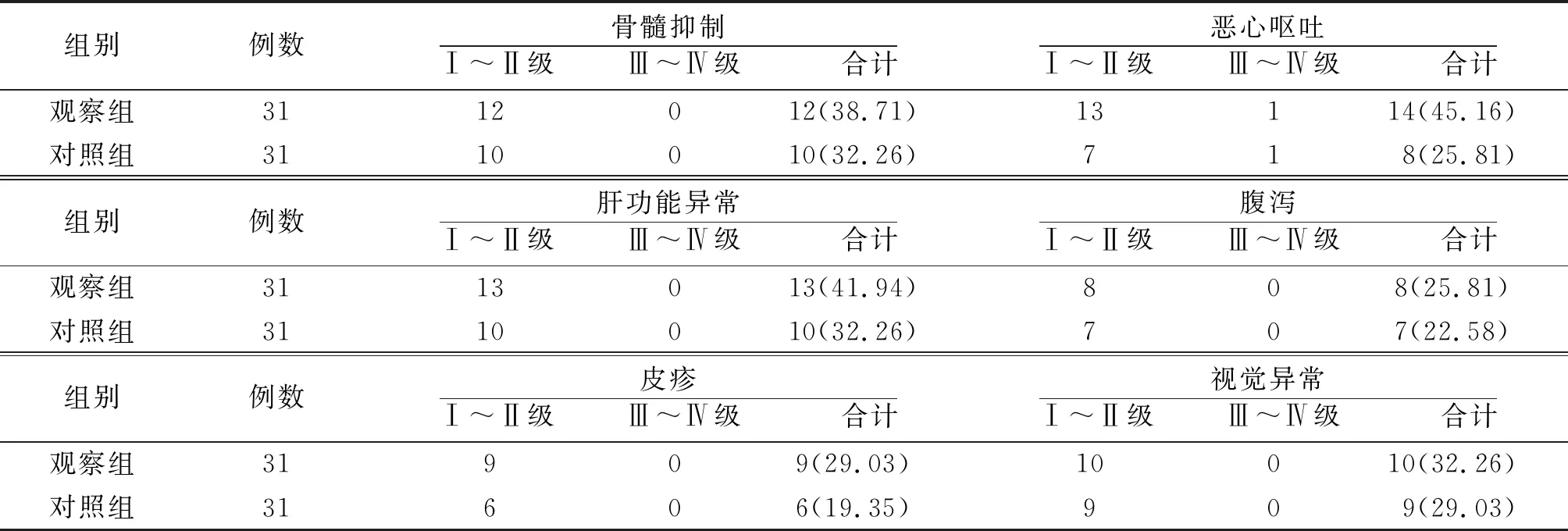
表6 2组晚期NSCLC毒副反应发生情况比较[例(%)]
3 讨论
靶向治疗因可通过蛋白水平或基因转录对细胞增殖、分化进行调控,从而促进肿瘤细胞凋亡[13]。ALK是一种受体酪氨酸激酶,可激活多种底物分子形成信号转导网络。最新指南推荐含特征性ALK融合癌基因的晚期或转移性NSCLC,应首先采用ALK抑制剂治疗[14]。ALK基因与EML4基因倒位融合后形成EML4-ALK融合基因,2个EML4-ALK分子的激酶区可结合EML4细胞外的螺旋结构,形成稳固的二聚体,促使酪氨酸激酶持续活化,引起下游的信号传导转录激活因子、磷脂酰肌醇-3-激酶、丝裂原活化蛋白激酶、蛋白激酶B等异常活化,诱导正常的细胞癌变,从而参与肿瘤的发生、发展[15]。NSCLC患者ALK基因阳性率为3.3%~6.1%,以EML4-ALK融合基因最常见[16]。克唑替尼胶囊是第一代ALK-TKI,可有效结合c-Met、ALK、ROS1等多靶点驱动基因,尤其对EML4-ALK融合基因阳性表达的肿瘤细胞作用效果显著,可通过干扰基因转录水平,减慢G1/S期跨越速度,延长细胞增殖周期,从而控制病情进展[17]。翟中武和杨艳[18]研究指出,克唑替尼胶囊治疗EML4-ALK阳性晚期NSCLC客观缓解率达50.00%,高于多西他赛化疗。本研究也发现,单纯克唑替尼胶囊治疗的NSCLC患者DCR达67.74%,效果良好。但随着ALK-TKI在临床的广泛应用,相继有报道显示,部分NSCLC患者存在ALK-TKI耐药性[19-20]。
有研究显示,与单独化疗方案治疗NSCLC患者相比,化疗方案与克唑替尼胶囊联合治疗DCR显著提高,可有效改善患者预后[21]。NP方案中顺铂是肺癌化疗的常用药物之一,其与肿瘤细胞DNA结合后可形成交叉链,有效抑制肿瘤细胞DNA复制、合成,且可通过与蛋白交联影响其生物功能,诱导细胞凋亡;注射用酒石酸长春瑞滨是一种半合成长春花生物碱,可特异性作用于肿瘤细胞,阻滞微管形成,从而干扰细胞有丝分裂过程,使其停滞在有丝分裂中期,进而阻止肿瘤细胞增殖[22-23]。赵景娟等[24]研究指出,晚期NSCLC患者采用NP方案治疗客观缓解率达46.4%,效果良好,且毒副反应可耐受。本研究结果显示,观察组DCR高于对照组。分析其原因:克唑替尼胶囊通过竞争性结合异常活化的ALK激酶的ATP位点,阻滞ATP结合异常活化的ALK激酶,抑制二者形成的结合物磷酸化,降低ALK激酶活性,抑制下游信号通路激活,从而发挥抗肿瘤作用[25];克唑替尼与顺铂、注射用酒石酸长春瑞滨的抗肿瘤途径各异,可协同抑制肿瘤细胞增殖,进一步提高治疗效果[26]。本研究还发现,观察组EML4-ALK阳性率低于对照组,分析原因为克唑替尼胶囊以EML4-ALK为作用靶点,且化疗具有广泛抗肿瘤作用,进一步证实联合治疗的有效性。
检测肿瘤标志物水平是诊断恶性肿瘤、评价预后的重要手段,与影像学检查相比,具有更高的敏感性。NSE、CEA、Cyfra21-1均为肺癌诊断常用标志物,其中CEA是一种细胞黏附分子,在多种恶性肿瘤中均呈现出异常高表达,但在不同病理分期NSCLC患者中表达均有差异,其动态变化情况可用于评估患者病情程度、治疗效果[27-30];Cyfra21-1主要分布于层状或鳞状上皮等正常组织表面,当层状或鳞状上皮组织发生恶变,其会被激活的蛋白酶降解并释放入血,致血清水平异常升高,在肺癌患者诊断中具有较高特异性[31-33];NSE是存在于神经细胞及神经元的糖酵解酶,但神经元受损或神经细胞破裂时,血清NSE水平会异常升高,已有多项研究显示,NSCLC患者NSE呈异常高表达,其水平可反映患者病情变化,并对疗效评估、指导临床治疗具有重要意义[34-37]。本研究结果发现,治疗2个周期后,2组血清NSE、CEA、Cyfra21-1水平均呈降低趋势,观察组降低幅度更大,证实克唑替尼胶囊联合NP方案更有助于降低NSCLC肿瘤标志物水平,可能是因为,顺铂、注射用酒石酸长春瑞滨可有效抑制肿瘤细胞增殖,减轻肿瘤负荷;克唑替尼胶囊可通过抑制EML4-ALK促使下游NOTCH信号通路中Bcl-2、Bax等细胞凋亡蛋白表达,促使肿瘤细胞凋亡,联合应用进一步降低循环血中肿瘤代谢产物水平。本研究结果显示,ΔNSE、ΔCEA、ΔCyfra21-1与疗效呈负相关,表明临床可结合肿瘤标志物变化幅度评估治疗效果。此外,本研究中观察组生存质量优于对照组,主要与联合治疗抗肿瘤效果更显著有关。安全性方面,2组毒副反应均以Ⅰ~Ⅱ级为主,患者可耐受,经对症治疗后缓解,未出现病死患者,2组毒副反应发生率比较差异无统计学意义,提示联合治疗安全性较高。
综上所述,ALK-TKI联合NP方案应用于晚期NSCLC患者,疗效显著,可有效降低EML4-ALK阳性、肿瘤标志物水平,提高生存质量,且安全性高。但联合方案是否可延迟克唑替尼胶囊的耐药性,仍需更多研究进一步探明。
