纳米CaO2激发餐厨垃圾碳组分合成水凝胶及溶胀性能分析
2022-12-15李亚林刘蕾关明玥孙猛李柳婷毛瑞月何海洋
李亚林,刘蕾,关明玥,孙猛,李柳婷,毛瑞月,何海洋
(河南工程学院环境与生物工程学院,河南 郑州 451191)
随着经济发展和人民生活水平的提高以及生活方式的转变,城市餐饮业日益繁荣,餐厨垃圾的产生量也快速增长[1]。据统计数据显示,截止到2020年我国餐厨垃圾的总量近1.28亿吨,但处理量不足总产量的20%,处理效率很低。2021 年10 月国务院印发的《2030 年前碳达峰行动方案》中要求“大力推进生活垃圾减量化资源化”“探索适合我国厨余垃圾特性的资源化利用技术”。
餐厨垃圾具有有机质含量高、含水量大、营养丰富等特点,具有很高的回收价值[2]。目前,常规的餐厨垃圾处置及资源化技术包括填埋、焚烧发电、好氧堆肥和厌氧发酵等[3-6],其中厌氧发酵和好氧堆肥因其具备能源化优势,已经成为餐厨垃圾资源化利用的主流技术[7]。这两种技术均是以降解为原理,最终从餐厨垃圾中获得CH4、H2、有机酸等小分子物质资源或进一步转化为腐殖质,然而在这样的过程中餐厨垃圾中的含碳组分利用率不高,造成资源的浪费,也增加了碳组分释放到环境中的概率。
我国餐厨垃圾的主要成分为淀粉、纤维素、蛋白质等大分子物质,这些物质中含有丰富的—COOH、—OH、C==C等特征官能团,具有发生自由基聚合反应的特性,利用这一特性可以将餐厨垃圾的主要成分聚合交联进而向更大分子物质转化[8-9],实现餐厨垃圾中含碳组分的回收与增值化利用。
基于此,本文以餐厨垃圾为原料,利用具有高效反应性和良好分散性的自制纳米CaO2作为氧化剂,激发餐厨垃圾中的碳组分,尿素作为改性剂,丙烯酰胺作为单体,N,N'-亚甲基双丙烯酰胺作为交联剂,过硫酸钠作为引发剂,通过自由基聚合交联反应合成水凝胶,探讨了不同制备条件对水凝胶溶胀性能的影响,并尝试建立了水凝胶的溶胀动力学模型,在此基础上通过SEM、XRD、FTIR 和TGA 对水凝胶的形貌、结构、热稳定性等进行表征,分析了水凝胶的溶胀机理,为餐厨垃圾的高增值化利用提供了一种思路。
1 实验部分
1.1 实验材料
实验中所用的餐厨垃圾取自于新郑市某高校学生餐厅,经分拣出塑料、骨头、一次性筷子等杂物后得到,主要成分为大米、面食、蔬菜、油水等。餐厨垃圾取回后放置在4℃的冰箱中保存,实验前将其取出,放至室温后添加适量的去离子水,保证餐厨垃圾与去离子水的质量体积比为1∶4,全部加入至破壁机中打碎混合均匀,之后将混合均匀的浆液过0.150mm(100 目)尼龙筛,过筛后的餐厨浆液(food waste slurry,FWS)待用,FWS 的基本性质见表1。

表1 餐厨垃圾浆液的基本性质
实验中制备水凝胶使用的CaO2为自制,粒度为45~300nm,纯度为79.13%[10],丙烯酰胺(acrylamide,AM)、N,N'-亚甲基双丙烯酰胺(N,N'-methylene bisacrylamide,MBA)、过硫酸钠(sodium persulfate,SPS)、尿素(urea)均为分析纯。
1.2 水凝胶的制备原理及流程
水凝胶的制备原理及流程如图1所示,水凝胶的制备主要是利用交联法和自由基聚合法,基本原理如下。
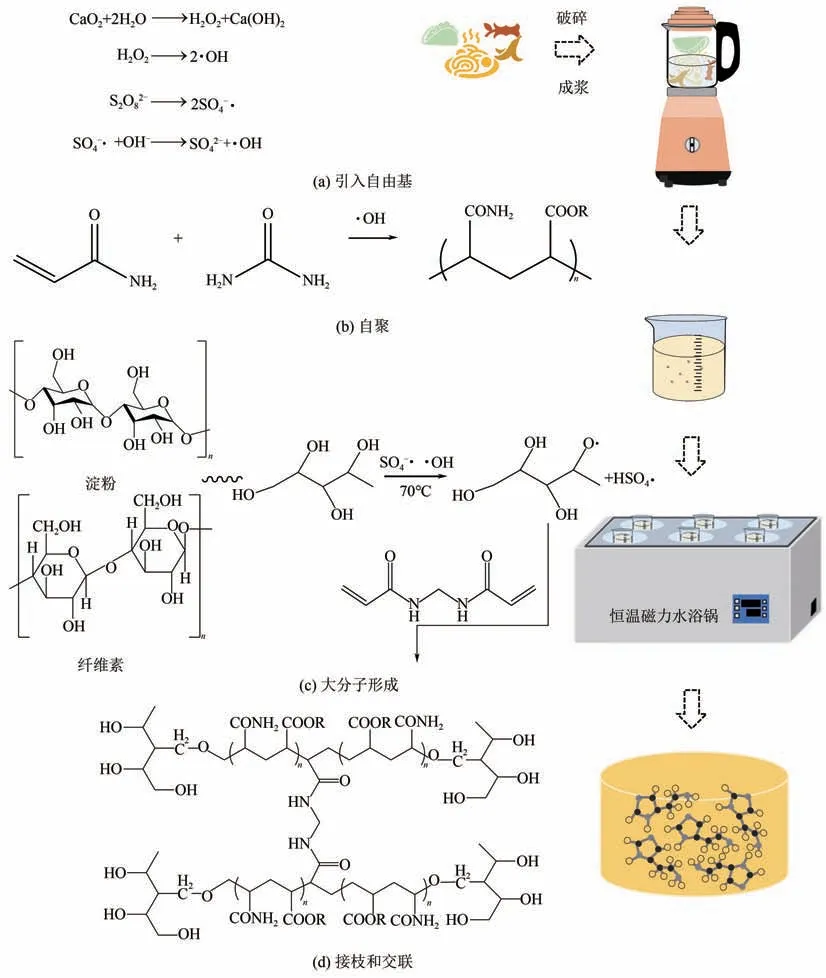
图1 凝胶的制备原理及流程
(1)利用CaO2引入自由基·OH,·OH 的强氧化作用可以促使餐厨垃圾中有机组分的释放和分解,为单体与其接枝共聚提供更多反应位点,形成更为致密的三维网络[11-12],另外,SPS 作为引发剂在70℃条件下热分解,生成·SO-4,进一步产生更多的·OH。
(2) 尿素中含有的—COO 发生质子化形成—COOH,—COOH 与—NH₂[13]以及丙烯酰胺上的—CONH2易形成氢键[14],起到物理交联的作用。
(3)从淀粉、纤维素等主链的—OH 中提取氢原子,进而形成活性—OR。
(4)AM作为单体被活性自由基引发,C==C双键打开并嫁接在淀粉或纤维素主链上,形成接枝共聚物。
(5)MBA 作为交联剂促进支链交联形成水凝胶的网状结构。
(6)多种组分聚合最终形成水凝胶。
水凝胶制备流程如下:取定量预处理的餐厨垃圾浆液于烧杯中,烧杯置于70℃恒温磁力水浴锅(HH-M6,江苏科析仪器有限公司)中搅拌进行预热[15],预热15min后加入CaO2,搅拌5min后加入尿素,再搅拌10min 后加入AM,之后搅拌10min 后加入MBA,再继续搅拌1min 后加入SPS,维持反应直至形成固相凝胶。
1.3 水凝胶溶胀性能的测定
将水凝胶置于真空冷冻干燥机(LGJ-10,北京悦诚嘉业科技有限公司)中干燥24h后,取部分干燥后的凝胶用尼龙布包裹完全浸泡在规格均为5cm×5cm×5cm 的正方体亚克力盒中,注入去离子水完全覆盖水凝胶,在人工气候箱(BIC-300 型,上海博讯实业有限公司医疗设备厂)中以恒定的温度(25℃)和湿度(55%)进行溶胀,每隔12h 将水凝胶取出置于300目的尼龙筛网上控水1min后用分析天平称取水凝胶质量,测定结束后重新将水凝胶放回亚克力盒中,重复上述过程,溶胀108h 后不同条件下制备的水凝胶在吸水过程中完全碎裂,且质量变化较小,故以108h作为溶胀测定的终点,定义此时凝胶的溶胀率作为终点平衡溶胀率,每个时间取3 个平行样,结果取平均值,计算如式(1)所示[16]。

1.4 水凝胶的微观表征及热重分析
为了探究水凝胶的溶胀机理及其热稳定性,将餐厨垃圾原料和制得的水凝胶在真空冷冻干燥机中干燥后,使用扫描电子显微镜(scanning electron microscope,SEM)(Quanta 250型,捷克FEI公司)分别对其进行表征。使用同步热分析仪(STA449 F3 型,德国Netzsch 公司)对样品进行TGA 分析,升温速率为30℃/min。
2 结果与讨论
2.1 水凝胶制备条件对其溶胀率的影响
2.1.1 尿素用量对水凝胶溶胀率的影响
量取50mL 的FWS,控制CaO2的用量为0.60g,改变尿素的加入量,单体AM 用量为2.00g,交联剂MBA用量为0.14g,引发剂SPS用量为0.36g,制得水凝胶,测定其溶胀性能,结果如图2所示。
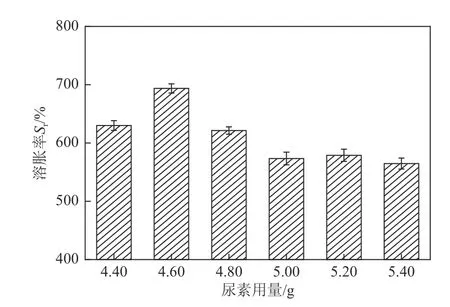
图2 尿素用量对水凝胶溶胀率的影响
由图2 分析,随着尿素加入量的增加,Sr呈现出先升高后降低的趋势。因为在尿素加入量较少时,尿素中含有的—COOR、—CONH2与淀粉、纤维素中的—OH 更易发生缩合反应而非基团间的交联反应,但是—COOR、—CONH2与—OH间的交联反应是水凝胶形成网状结构的主要诱因[17],而这种网状结构决定了水凝胶的吸水能力,因此尿素加入量的增加可以显著提升水凝胶的溶胀性能,在尿素加入量为4.60g时,Sr达到最大值693.66%。之后继续增加尿素的用量,Sr出现下降趋势,因为一方面,尿素加入量增加会使体系中—CONH2的保有量激增,—CONH2自身官能团缩聚概率增加,同时形成较大的空间位阻[18],淀粉、纤维素等大分子主链上的自由基聚合反应受到影响,水凝胶的溶胀性能下降;另一方面,当尿素加入量过多时,过量未参与反应的尿素晶体会包裹内嵌在水凝胶内部的三维网状结构中,同时亲水基团与水之间存在氢键作用[19],导致水凝胶内部被束缚,水分较难被吸收。
2.1.2 引发剂用量对水凝胶溶胀率的影响
量取50mL 的FWS,控制CaO2的用量为0.60g,尿素的用量为4.60g,单体AM 用量为2.00g,交联剂MBA 用量为0.14g,改变引发剂SPS 的加入量,制得水凝胶,测定其溶胀性能,结果如图3所示。
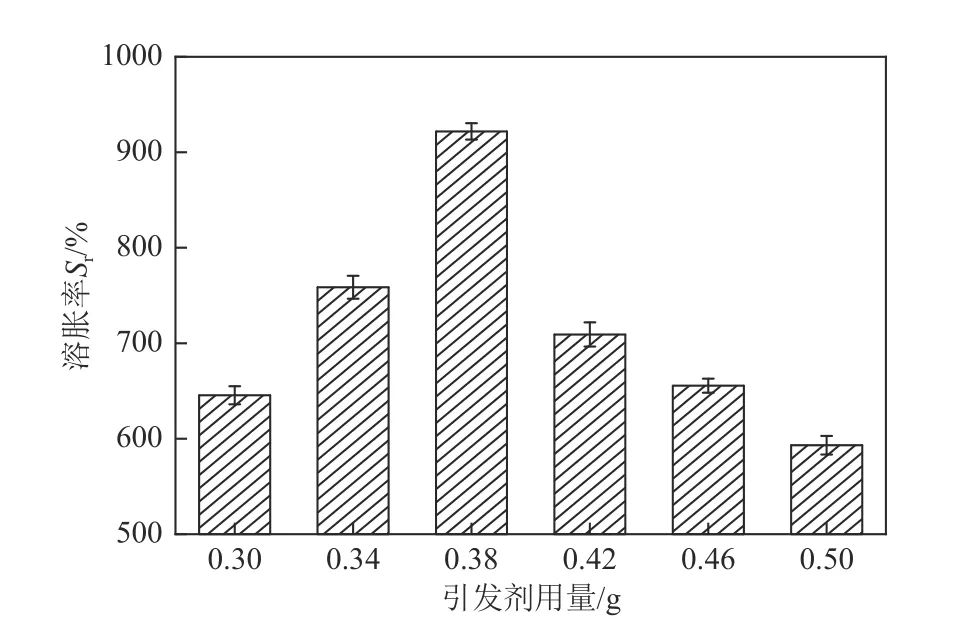
图3 引发剂用量对水凝胶溶胀率的影响
由图3 分析,随着SPS 加入量的增加,Sr同样呈现出先升后降的趋势,当SPS加入量为0.38g时,Sr达到最大值,为921.87%。因为SPS 在一定聚合温度下可发生热分解,如式(2)和式(3)所示[20]。
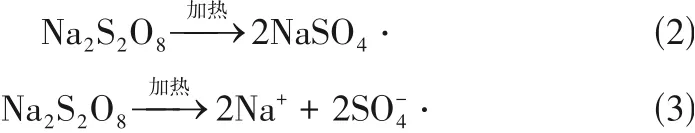
作为产生自由基聚合反应的活性中心物质,SPS一方面影响着聚合反应速率,另一方面影响聚合物的相对分子质量[21],SPS 加入量越大,反应体系中的·SO4-越多,·SO4-可以引发AM 与餐厨垃圾主要成分的接枝共聚反应及AM的自聚,在交联剂的作用下,发生交联反应;而当SPS的加入突破一定量时,反应的活性中心激增,共聚和自聚反应的速率提升[22],此时链终止反应概率增加,水凝胶聚合物的相对分子量下降,凝胶主链缩短导致溶胀性能下降。
2.1.3 单体用量对水凝胶溶胀率的影响
量取50mL 的FWS,控制CaO2的用量为0.60g,尿素的用量为4.60g,改变单体AM 的加入量,交联剂MBA 用量为0.14g,引发剂SPS 用量为0.38g,制得水凝胶,测定其溶胀性能,结果如图4所示。
由图4 分析,随着单体AM 加入量的增加,Sr总体呈现出升高后再降低的趋势,在单体用量为2.80g 时,Sr达到最大值1131.04%。在合成中随着体系中单体加入量的增加,水凝胶的交联程度上升,形成的网络结构更加稳定;单体的持续增加会使水凝胶的交联程度进一步得到提升,此时凝胶高分子链会受到已形成的网络结构的限制,新的网络结构构建受到约束,网络的壁厚也会增加[23],网络孔隙变小,水凝胶的延展性受到限制,溶胀性能下降。

图4 单体用量对水凝胶溶胀率的影响
2.1.4 CaO2用量对水凝胶溶胀率的影响
量取50mL的FWS,改变CaO2的加入量,控制尿素用量为4.60g,单体AM 用量为2.80g,交联剂MBA 用量为0.14g,引发剂SPS 用量为0.38g,制得水凝胶,测定其溶胀性能,结果如图5所示。
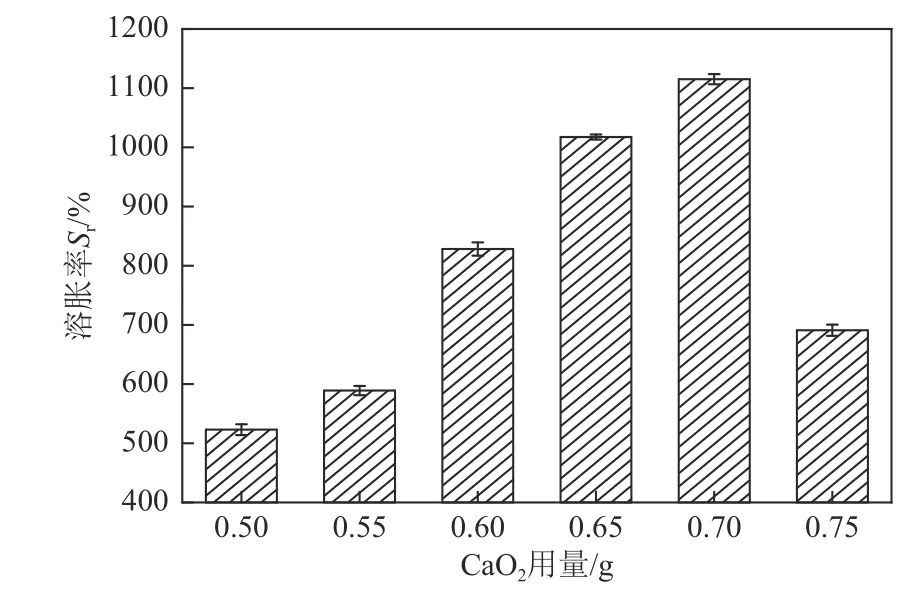
图5 CaO2用量对水凝胶溶胀率的影响
由图5分析,CaO2加入量对Sr有较大影响,当CaO2用量为0.70g时,Sr达到最大值,为1115.24%。当CaO2用量小于0.70g时,随着CaO2加入量的增加Sr逐渐升高,CaO2与水会发生式(4)中的反应[11]。

H2O2结构中HO—OH 中的O—O 键不稳定,易断裂,形成·OH;同时SPS产生的·SO4-会与式(4)中产生的OH-发生式(5)中的反应[12]。
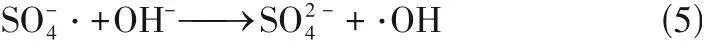
因此,CaO2的加入量越多,产生的·OH 量越多,·OH 的强氧化作用可以促使餐厨垃圾中有机组分的释放和分解,为单体与其接枝共聚提供更多反应位点,形成更为致密的三维网络。但当CaO2投加量过多时,引进的Ca2+会对均质的餐厨垃圾组分造成一定的絮凝团聚作用[24],从而对水凝胶网络形成阻碍,水凝胶的溶胀性能随之下降。
2.1.5 交联剂用量对水凝胶溶胀率的影响
量取50mL 的FWS,控制CaO2用量为0.70g,尿素用量为4.60g,单体AM 用量为2.80g,改变交联剂MBA 加入量,引发剂SPS 用量为0.38g,制得水凝胶,测定其溶胀性能,结果如图6所示。

图6 交联剂用量对水凝胶溶胀率的影响
由图6 分析,在MBA 加入量过低时,尿素、餐厨和单体的支链交联反应效果较差,此时水凝胶结构以线性结构为主,溶胀性能较差;随着MBA加入量的增加,水凝胶交联呈现的网状结构增加,溶胀性能改善,当MBA 的加入量为0.14g 时,Sr达到1429.78%。之后继续增加MBA 的加入量,MBA产生自聚倾向,此时水凝胶内部的网状结构变得紧密,微孔结构不断减少,溶胀性能下降。
2.2 水凝胶的溶胀动力学分析
考虑到CaO2对于餐厨垃圾碳组分释放的影响,此处实验固定尿素、单体、交联剂和引发剂的用量为2.1 节中的最佳值,分别控制CaO2的加入量为0.60g(S1)、0.65g(S2)、0.70g(S3)、0.75g(S4)制备水凝胶,对水凝胶进行了108h的溶胀率测定,并采用方程对凝胶的溶胀性能进行拟合,进而分析水凝胶的溶胀动力学行为,结果如图7所示。
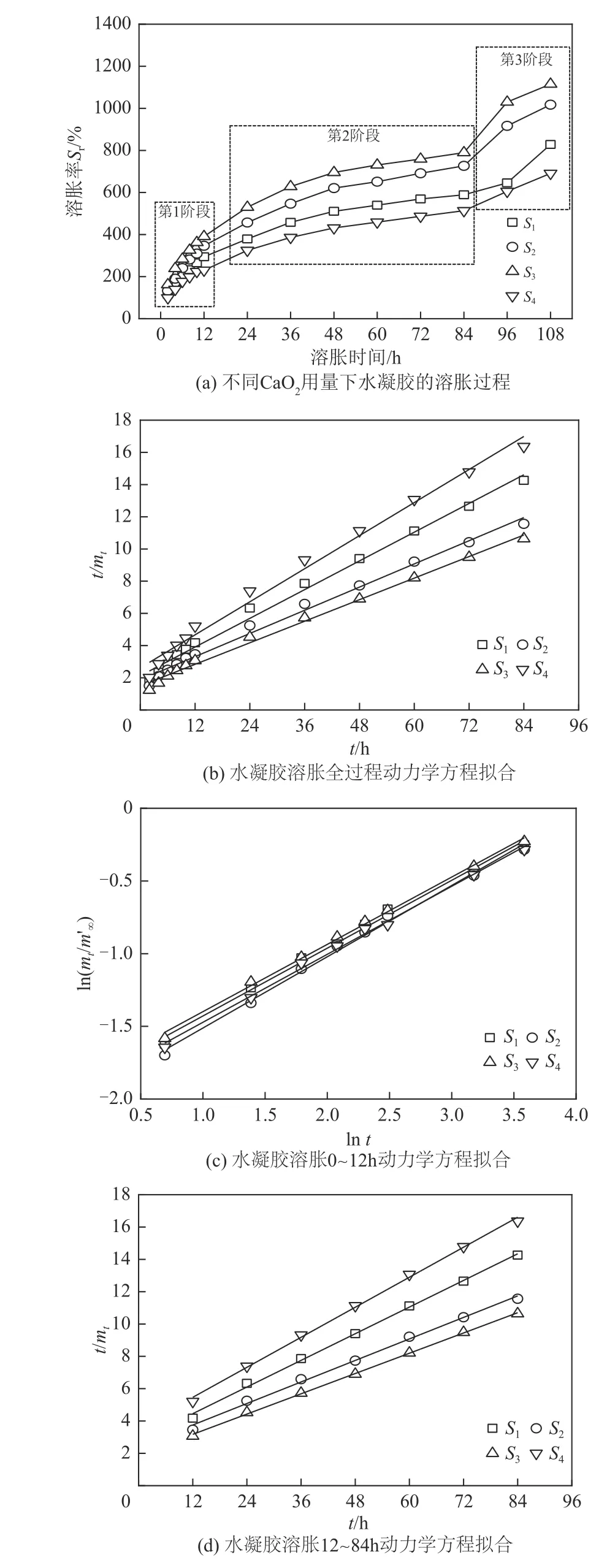
图7 水凝胶的溶胀动力学分析
由图7(a)分析,水凝胶的溶胀过程可以划分为3 个阶段,在溶胀的0~12h 内,水凝胶的Sr迅速升高,这是由于一方面当水凝胶浸入H2O中时,水凝胶内外存在渗透压差,H2O进入水凝胶内部的速率较快,导致水凝胶内部迅速填满H2O分子,Sr快速升高[25];另一方面,由于水凝胶内部存在的不规则褶皱、沟壑以及网络结构,使得H2O分子更容易进入水凝胶内部,极大缩短了水凝胶到达溶胀终点所需的时间,而随着溶胀时间的延长,12h之后水凝胶内外渗透压差逐渐相等,溶胀率升高的变化情况趋向平缓[26];但在溶胀84h 后,溶胀曲线出现了陡增,此时实验中观察到水凝胶已经出现明显的破碎现象,而这种破碎的诱因是水凝胶中网络结构的刚性被破坏,H2O分子在水凝胶中的吸附不再受到原有网络结构的束缚,溶胀行为不再遵循前两个阶段的规律。
为了更加合理地解释水凝胶的溶胀行为,尝试采用Schott 溶胀动力学模型[27]对水凝胶溶胀的第一和第二阶段进行分析,其计算过程如式(6)~式(11)。

使用上述方程对水凝胶溶胀数据进行拟合,t/mt-t关系如图7(b)所示。由图7(b)分析,使用该模型对水凝胶84h的溶胀进行拟合时,S1、S2、S3、S4的拟合R2分别为0.9919、0.9911、0.9941、0.9890,均大于0.9,具有较好的相关性;但模型计算得到的m∞会受到初期溶胀速率快速增大的影响,与实际值相比偏小,S1、S2、S3、S4理论值与实测值分别相差-18.77%、-18.10%、-19.62%、-15.43%。
由对图7(a)的分析可知水凝胶溶胀的3 个阶段存在差异,因此对水凝胶溶胀行为进行了分段模拟。在0~12h水凝胶在溶胀过程中,浓度梯度和高分子链的松弛有助于H2O 分子渗透到水凝胶内部,此阶段水凝胶的溶胀行为主要受H2O 的扩散影响。当水凝胶与H2O分子接触时,H2O分子扩散到水凝胶基质中,从而使其溶胀。这种扩散过程包括将H2O分子迁移到大分子链之间预先存在的或动态形成的空间中,水凝胶的溶胀涉及更大规模的分段运动,最终导致大分子链之间的距离增加[28]。为了分析水凝胶初期吸水溶胀过程,对原数据进行处理,采用Fickian 模型方程来描述实验数据[29],具体如式(12)所示。

等式变形,得到式(13)。
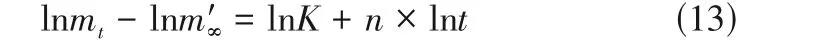
通过ln(mt/m'∞)对lnt的曲线进行线性拟合,计算得到的溶胀动力学参数和拟合结果如图7(c)所示,根据计算所得n值可以来分析水凝胶在蒸馏水中扩散行为契合Fickian 或non-Fickian 扩散模型[30-31]。由图7(c)可得S1、S2、S3、S4的n值分别为0.4666、0.4903、0.4630、0.4677,均小于0.5,水凝胶的吸水溶胀过程符合Case I 扩散[32],符合Schott 溶胀动力学的一级模型。同时,S1、S2、S3、S4拟合的R2分别为0.9933、0.9942、0.9966、0.9958,证明了拟合具有良好的相关性。
而对水凝胶溶胀12h 后直至84h 的行为进行模拟则发现,该阶段水凝胶的溶胀行为更加符合Schott 溶胀动力学的二级模型,拟合结果如图7(d)所示。该拟合模型中S1、S2、S3和S4的拟合R2分别为0.9975、0.9954、0.9992 和0.9977,均大于0.99,相较于溶胀第一阶段和第二阶段的全过程模拟具有更好的相关性,此时4 组样品对应的m∞分别为7.2801、9.0147、9.5685和6.4612,与实测值接近。
水凝胶溶胀84h直至溶胀终点的过程拟合并无明显规律,最后通过对比水凝胶溶胀第一阶段模型中的K值和第二阶段模型中的r0值发现,在CaO2投加量为0.70g 时,水凝胶的Sr均为最大值,这与单因素实验得到的结论相一致。
2.3 水凝胶的溶胀机理及热稳定性分析
为了探究水凝胶的溶胀机理,对餐厨垃圾和水凝胶的结构及微观形貌进行了表征,XRD 图谱和FTIR图谱如图8所示。
由图8(a)可知,餐厨垃圾原料在17.04°、19.76°各存在一处含有C、H、O元素的有机化合物特征峰,而水凝胶中这两处特征峰消失,变为明显的广谱峰,峰值在2θ=15°~25°,表明水凝胶是无定形结构;同时,水凝胶图谱中在2θ=22.89°、29.37°、31.71°处可以看到有3 个较弱的衍射峰,分别对应Na2SO4的(012)、(104)、(006)晶面,说明水凝胶表面的晶体结构物质是SPS反应生成的Na2SO4晶体。
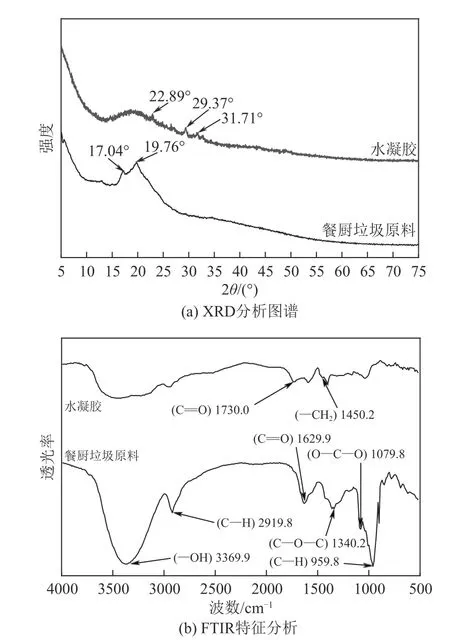
图8 餐厨垃圾、水凝胶的XRD分析图谱和FTIR特征分析
由图8(b)可知,由于样品对空气中水分的吸附,餐厨垃圾原料在3369.9cm-1处存在明显的—OH伸缩振动峰;在2919.8cm-1处存在的C—H伸缩振动峰,来源于餐厨垃圾中碳氢化合物;在1629.9cm-1处的伸缩振动吸收峰对应酰胺I 峰中的C==O,在1079.8cm-1和1340.2cm-1处两个C—O—C 伸缩振动峰来源于餐厨垃圾中的脂类,959.8cm-1处存在羧酸的—OH 伸缩振动吸收峰,这些均是餐厨垃圾中典型的官能团特征峰。
在水凝胶样品中,除了与餐厨垃圾原料具有相同的—OH、C==O、C—H 等特征官能团外,在3300~3500cm-1附近峰变宽是存在—NH2、—NH 吸收重叠而成的多重吸收峰[33],在1730.0cm-1处存在酯键C==O 振动特征吸收峰,说明水凝胶中存在酯羰基,可以推断出餐厨垃圾浆液转化为水凝胶的过程中含碳组分被成功接枝聚合为了大分子的酯类;同时在1450.2cm-1处出现了—CH2中C—H的弯曲振动,由此可以推测出水凝胶中的MBA 嫁接在餐厨垃圾中的碳组分骨架上,引入的MBA与AM与餐厨垃圾碳组分之间发生了接枝聚合反应,由官能团的变化可推测出—OH、C==O等含氧官能团能以表面络合反应的形式参与到水凝胶的合成过程。
餐厨垃圾和水凝胶的SEM图像如图9所示。

图9 餐厨垃圾原料及溶胀前后水凝胶的SEM图
由图9可以发现,图9(a)中餐厨水凝胶原料呈现出杂乱的分散片状结构,与之形成对比的是图9(b)中溶胀前的水凝胶呈现出类似于网状的交错褶皱结构,孔壁较厚,孔与孔之间的间隙并不明显;而在水凝胶溶胀6h后的图9(c)中可以观察到清晰的网络结构,水凝胶由于吸水产生网络结构的拉伸,原本较厚的孔壁结构被打开,孔壁变薄,且这种变化并不可逆;当水凝胶达到溶胀平衡后,图9(d)中可以看到水凝胶孔壁变薄得更为明显,内部结构已经完全展开,可以清晰地观察到网络结构,此时水凝胶宏观体积达到最大。
餐厨垃圾原料与水凝胶的TGA 分析结果如图10 所示。由图10(a)可以看出两者的失重温度区间为150~450℃,因为结构性质的差异,餐厨垃圾原料的失重速率高于水凝胶,在此区间内,餐厨垃圾原料的失重比例为52.7%,水凝胶的失重比例为52.4%。由图10(b)分析,餐厨垃圾原料分别在85.6℃、210.0℃和288.9℃处失重速率较快,其中210.0℃前发生的主要是自由水分和结合水分的物理蒸发损失过程,之后温度区间发生是木质素、半纤维素、纤维素等大分子物质的分解[34]。而水凝胶失重较快的温度点相较于餐厨垃圾原料均呈现后移的趋势,最大的失重在355.0℃,水凝胶热分解温度显著提高,热稳定性能增强,便于更好地应用于后续的工业、农业和环保等领域。
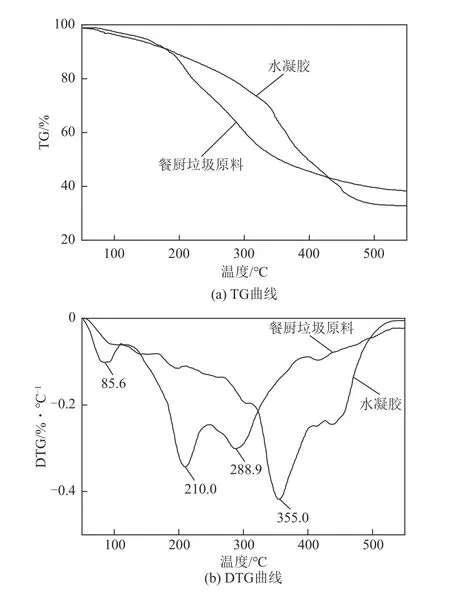
图10 餐厨垃圾、水凝胶的TGA分析
3 结论
(1)在餐厨垃圾制备水凝胶的过程中,氧化剂、改性剂、单体、交联剂和引发剂均会对水凝胶的溶胀率造成影响,在氧化剂用量为0.70g、改性剂用量为4.60g、单体用量为2.80g、交联剂用量为0.14g、引发剂用量为0.38g时,水凝胶的溶胀率可以达到1429.78%。
(2)水凝胶在去离子水中84h的溶胀行为总体符合Schott的二级溶胀动力学模型,其中第一阶段0~12h的溶胀行为更加符合Fickian 的Case I 扩散模型,第二阶段12~84h与Schott溶胀动力学的二级模型吻合良好,第3 阶段84h后的溶胀行为不再遵循前两个阶段的规律。
(3)XRD 和FTIR 分析说明与餐厨垃圾原料相比,制备的水凝胶为无定形结构,由官能团的变化可推测出—OH、C==O等含氧官能团能以表面络合反应的形式参与到水凝胶的合成过程中。
(4)SEM 表征结果证明餐厨垃圾原料与水凝胶呈现出的杂乱分散片状结构相比,水凝胶的溶胀性主要与其复杂的网状结构相关,随着溶胀时间的变化,水凝胶孔壁变薄且不可逆。TGA分析表明水凝胶在温度低于355.0℃条件下具有良好的热稳定性。
符号说明
K—— 水凝胶溶胀常数
ks—— 水凝胶的溶胀速率常数,g/(g·min)
mt—— 水凝胶在t时刻溶胀率,g/g
m∞—— 水凝胶理论终点溶胀率,%
m′∞—— 水凝胶终点时溶胀率,g/g
n—— 溶胀指数
r0—— 水凝胶初始阶段的溶胀速率,%
Sr—— 水凝胶的溶胀率,%
t—— 水凝胶在蒸馏水中的浸泡时间,h
W0—— 水凝胶溶胀前的质量,g
W∞—— 水凝胶达到溶胀终点的质量,g
下角标
0 —— 溶胀前
r —— 比率
S —— 溶胀平衡
t—— 时间
∞—— 终点
