多孔TiO2/CdS纳米材料制备与光催化性能研究*
2022-12-10张海俊张国栋
张海俊,张国栋,王 超
(1.银川能源学院 化学与生物工程学院,宁夏 银川 750100;2.青岛科技大学 机电工程学院,山东 青岛710065;3.陕西理工大学 材料科学与工程学院,陕西 汉中 723001)
0 引 言
纳米二氧化钛(TiO2)由于具有无毒、制备成本低、良好的光学特性以及物理化学稳定性等,而被广泛应用于能源(光解水制氢、TiO2还原等)、环保(降解有机污染物、还原重金属离子等)和太阳能电池等领域[1]。作为典型的金属氧化物半导体材料,TiO2基纳米材料在光催化、锂离子电池储能和气体传感器等领域应用较为广泛,但是由于其较快的光生载流子复合率、较窄的光响应范围和较低的太阳光利用率等[2,3],仍然在很大程度上限制了其在光催化领域的应用,较为可行的方法是对其进行结构设计和掺杂改性等来增强其光催化活性,包括调控TiO2的形貌和结构(多级孔、空心球和纳米片等)以及元素掺杂改性(Au、Ag、C、N和S等)等[4~6]。其中,将能在可见光范围内激发并产生电子和空穴的硫化镉(CdS)与TiO2复合形成多级孔框架结构的异质结催化剂,被认为是提高TiO2基纳米材料光催化性能的有效手段,而目前这方面的研究报道较少[7]。在此基础上,本文通过水热法将CdS颗粒嵌入至溶胶—凝胶法制备的多孔TiO2(porous TiO2,简称PT)中,对比分析了改性后的PT与改性前TiO2的物相组成、微观结构和光催化性能等,并优化了CdS的负载量,结果将有助于良好光催化性能的TiO2基纳米材料的开发与应用。
1 试验材料与方法
1.1 试验原料
试验原料包括北京化学试剂厂生产的乙醇、乙腈和对苯醌,国药集团化学试剂有限公司生产的Cd(NO3)2、钛酸正丁酯、罗丹明B、叔丁醇(tert butyl alcohol,TBA)、对苯醌(p-benzoquinone,BQ)和乙二胺四乙酸钠(Na2-EDTA),Aldddin公司生产的L—半胱氨酸和聚乙二醇醚P123,以及实验室自制去离子水。
1.2 试样制备
采用溶胶—凝胶法制备多孔TiO2:10.7 g乙腈+10 mL去离子水+0.1 g聚乙二醇醚混合均匀后加入0.83 g钛酸正丁酯,搅拌均匀后室温静置24 h,离心分离后的粉末依次进行58 ℃干燥1 h和425 ℃空气煅烧2 h,得到改性前试样,记为PT0。
采用水热法制备Cd(NO3)2改性的TiO2:0.06 g 多孔TiO2+0.03 mmolCd(NO3)2+0.09 mmol L—半胱氨酸+20 mL去离子水混合均匀后,在不锈钢高压釜中进行125 ℃/12 h的干燥处理,离心分离后的粉末分别采用乙醇和去离子水清洗,58 ℃/1 h干燥处理后得到Cd(NO3)2改性TiO2,简称PT1;此外,改变混合溶液中Cd(NO3)2的含量并确保L—半胱氨酸︰Cd(NO3)2=3︰1,Cd(NO3)2用量为0.06 mmol 和0.24 mmol的Cd(NO3)2改性TiO2分别简称为PT2和PT3。
1.3 测试与表征
采用帕纳科Empyrean锐影X射线衍射仪对PT的物相组成进行了分析,Cu靶Kα辐射;分别采用JSM—6800型扫描电镜和JEOL 2010型透射电镜观察微观形貌;采用ESCALAB—250XI型X—射线光电子能谱仪测试X射线光电子能谱;采用ASAP—2420型全自动比表面积及孔隙分析仪进行氮气吸附—脱附测试;采用UV—2550型紫外分光光度计进行紫外—可见漫反射吸收光谱测试;采用F9700系列荧光分光光度计进行光致发光光谱测试。光催化性能测试在9005型氙灯下进行,将50 mg PT0试样加入100 mL 罗丹明B溶液中,没有可见光的条件下搅拌0.5 h后进行可见光照射,间隔10 min取出5 mL溶液进行离心处理,并在Evolution 200型紫外—可见光光谱仪上进行降解效率测试;自由基捕获试验中的捕获剂包括对应超氧自由基、羟基自由基和空穴的BQ、TBA和Na2-EDTA,将1 mmol/L 捕获剂加入反应体系中,通过对比降解效率得到活性基团对光催化的影响。
2 试验结果与分析
图1为PT的XRD图谱。可见,改性前的PT0为典型的锐钛矿型TiO2(图1a);改性后的TiO2除具有的锐钛矿型TiO2特征衍射峰外,还在(002)、(101)、(110)和(112)晶面出现了六方相CdS的特征衍射峰,改性后的PT1、PT2和PT3试样的物相组成相同,且未出现其他杂质相的衍射峰,表明改性后的TiO2具有较高的纯度。此外,对比分析可见,随着改性TiO2中Cd(NO3)2浓度的提高,锐钛矿型TiO2衍射峰逐渐减弱、六方相CdS的衍射峰强度逐渐增强。根据Scherrer公式可计算得到CdS的平均晶粒尺寸D(nm)[8]
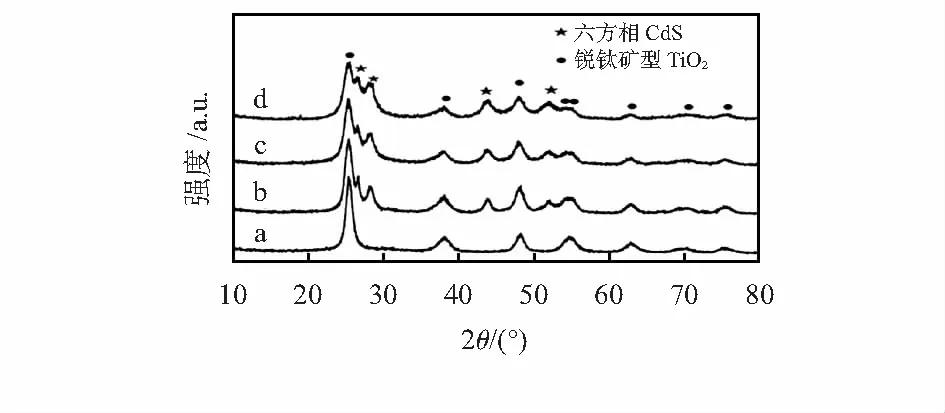
图1 PT的XRD图谱(a)PT0(b)PT1(c)PT2(d)PT3
(1)
式中K为Scherrer常数(0.89),B为衍射峰半宽高(rad),θ为衍射角(°),γ为波长(0.154 nm)。根据式(1)可计算得到PT1、PT2和PT3试样中CdS的平均晶粒尺寸分别为12,14,16 nm。
图2为PT的扫描电镜和透射电镜显微形貌,分别列出了改性前的PT0和改性后的PT2试样的显微形貌。图2(a),(b)中可见,PT0试样表面存在尺寸较大且孔径不均的微孔,表面较为光滑,尺寸较大的孔径可达800 nm;图2(c),(d)中可见,PT2试样表面的孔径明显变小且尺寸分布更加均匀,由于附着了较多的均匀分布的CdS颗粒而变得更为粗糙。图2(e),(f)中可见,PT0试样除表面存在由高结晶性的TiO2颗粒堆积而成的微孔外,内部未见明显介孔通道;图2(g),(h)中可见,PT2试样表面附着细小、高分散性的CdS颗粒,高分辨透射电镜中可见(101)晶面的锐钛矿型TiO2和(002)晶面的六方相CdS的晶格常数分别为0.35 nm和0.33 nm。综合而言,改性后的PT2试样表面存在孔径分布均匀的微孔结构,细小、高分散性的CdS颗粒附着在表面而使得表面较为粗糙,CdS相已成功嵌入PT结构中。

图2 PT的扫描电镜和透射电镜显微形貌
图3为PT的氮气吸附—脱附和孔径分布曲线,表1中同时列出了相应的PT试样的比表面积、孔体积和平均孔径。从图3(a)中可见,PT0、PT1、PT2和PT3试样的氮气吸附—脱附曲线为IV型吸附等温曲线,同时含有H2型迟滞环特征[9],表明改性前和改性后的TiO2都具有介孔结构;图3(b)的孔径分布曲线中可见PT0、PT1、PT2和PT3试样都具有较宽的介孔分布,且随着Cd(NO3)2浓度的提高,PT的介孔分布曲线有朝着左侧偏移的特征,这表明PT的孔径分布会随着Cd(NO3)2浓度提高而愈发不均,这主要与Cd(NO3)2浓度增加造成更多细小、高分散性的CdS颗粒附着在表面而堵塞介孔,从而使得孔径分布不均匀性增大有关[10]。表1中可见,改性前的PT0试样的比表面积为107.3 m2/g、孔体积为0.112 cm3/g、平均孔径为3.91 nm;改性后的PT1、PT2和PT3试样的比表面积、孔体积和平均孔径都有不同程度减小,且随着Cd(NO3)2浓度提高,改性PT的比表面积和孔体积逐渐减小,这主要与Cd(NO3)2浓度增加形成了更多的CdS颗粒堵塞了介孔孔道有关[11]。

图3 PT的氮气吸附—脱附和孔径分布曲线
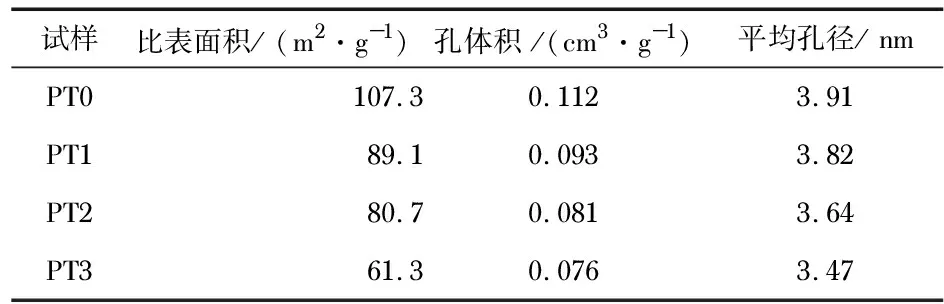
表1 PT的特征值
图4为PT的X射线光电子能谱曲线。从图4(a)的全谱图中可知,改性前的PT0试样主要含有C、Ti和O,而改性后的PT2试样还含有Cd和S特征峰;图4(b)中可见,PT0和PT2试样中都含有Ti 2p1/2和Ti 2p3/2特征峰,PT0试样的两个特征峰之间的结合能差值约5.8 eV,而PT2试样由于TiO2与负载CdS的交互作用而使得Ti 2p特征峰出现少量红移[12],Ti 2p1/2和Ti 2p3/2特征峰强度有所降低,此时PT0和PT2试样中的Ti都以Ti4+形式存在。图4(c)和图4(d)中可见,PT2试样中的Cd 3d和S 2p的XPS曲线中分别可见Cd 33/2/Cd 35/2和S 2p1/2/S 2p3/2特征峰,表明PT2试样中Cd和S分别以Cd2+和S2-形式存在。
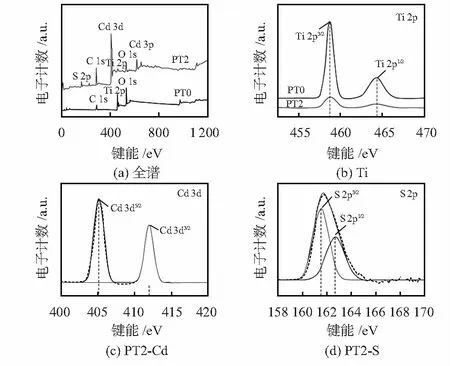
图4 PT的X射线光电子能谱曲线
图5为PT的紫外可见漫反射光谱。可见,改性前PT0试样在400 nm附近出现了光响应,而改性后的PT1、PT2和PT3试样的光响应都朝着可见光区域移动,究其原因,这主要与改性后PT试样表面负载了具有出色可见光响应的CdS颗粒,且二者的相互作用可以进一步拓宽PT试样的光响应范围[13]。此外,对比分析可见,随着Cd(NO3)2浓度提高,改性后PT试样的光响应吸收边缘不断宽化,表明Cd(NO3)2浓度提高可以提升PT试样可见光的响应性,这主要与试样表面形成了更多的CdS颗粒有关[14]。
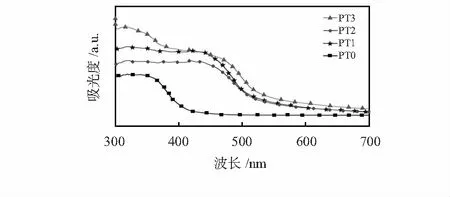
图5 PT的紫外可见漫反射光谱
图6为PT的光致发光光谱。可见,改性前的PT0试样的光致发光光谱具有最高的峰强度,而改性后的PT1、PT2和PT3试样的峰强度都有明显降低,这主要是因为在光照射条件下,改性前的PT0试样会产生最大的载流子复合率,而改性后的PT1、PT2和PT3试样由于负载了CdS颗粒而实现了电子和空穴对的分离[15],使得改性后的PT具有更高的光催化活性,且相对而言,PT2试样的峰强度最低,光催化活性最好。
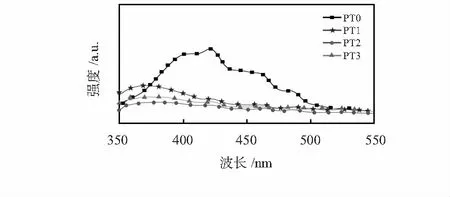
图6 PT的光致发光光谱
图7为PT的光催化活性测试结果,其中,C和C0分别表示t时刻罗丹明 B的浓度和初始状态下罗丹明 B的浓度。图7(a)的PT0、PT1、PT2和PT3试样对罗丹明 B的降解曲线中,可见光照射前由于PT具有吸附平衡而都存在少量罗丹明 B的吸附,可见光照射下改性后的PT1、PT2和PT3试样的光催化效率都相较改性前PT0试样和CdS更高,这主要与负载CdS颗粒有助于载流子的分离并提升光催化活性有关[16~18],且相同时间下改性后PT2试样具有最大的光降解活性(60 min时约88 %)。图7(b)的-ln(C/C0)—时间曲线中可见,改性前PT0试样和CdS的拟合线斜率相较改性后PT1、PT2和PT3试样更低,且PT2试样具有最大的拟合线斜率,分别为改性前PT0试样和CdS的31倍和5.4倍。图7(c)的PT2试样的光催化循环测试结果中可见,经过3轮光循环测试后,PT2试样对罗丹明B的降解效率约为72 %,表明改性后的PT2试样具有较好的光催化循环稳定性。图7(d)的PT2试样的C/C0—时间曲线中可见,在可见光照射下,添加BQ和TBA会明显降低PT2试样的光催化活性,而添加Na2—乙二胺四乙酸(EDTA)不会对PT2试样的光催化活性造成明显影响,这也就说明降解罗丹明 B过程中起主要作用的活性物质是超氧自由基和羟基自由基,而空穴对光催化的影响较小[19,20]。
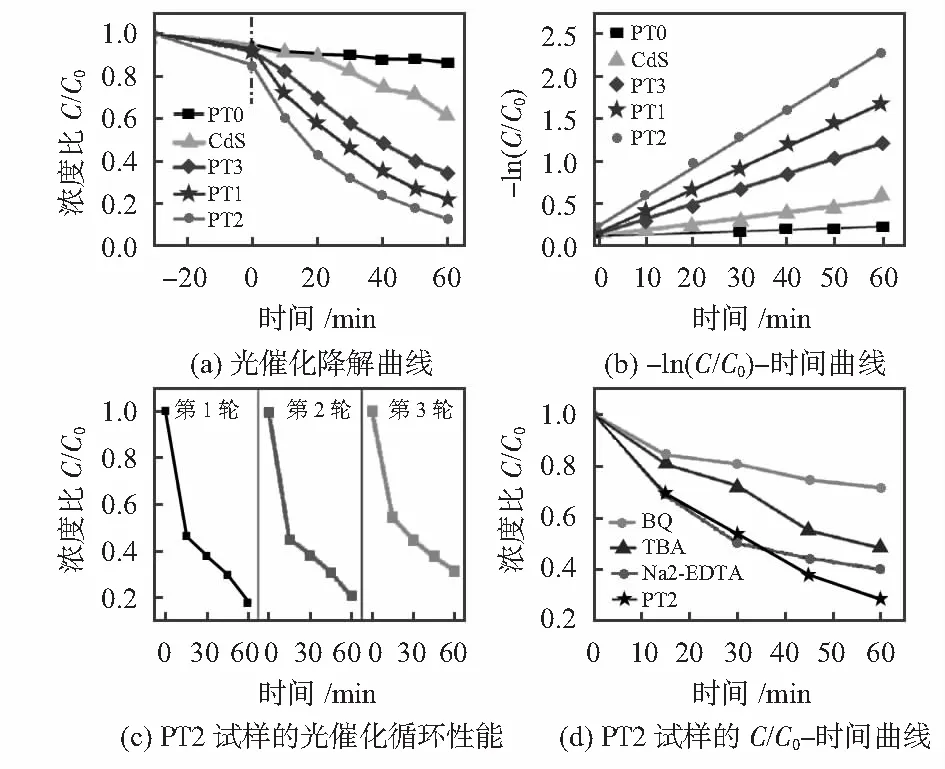
图7 PT的光催化活性
3 结 论
1)改性前的PT0试样为典型的锐钛矿型TiO2,改性后的PT1、PT2和PT3试样含有锐钛矿型TiO2和六方相CdS特征衍射峰;随着改性TiO2中Cd(NO3)2浓度的提高,锐钛矿型TiO2衍射峰逐渐减弱、六方相CdS的衍射峰强度逐渐增强。
2)改性后的PT2试样表面存在孔径分布均匀的微孔结构,细小、高分散性的CdS颗粒附着在表面而使得表面较为粗糙,CdS相已成功嵌入PT结构中。
3)改性前的PT0试样的比表面积为107.3 m2/g、孔体积为0.112 cm3/g、平均孔径为3.91 nm;改性后的PT1、PT2和PT3试样的比表面积、孔体积和平均孔径都有不同程度减小,且随着Cd(NO3)2浓度提高,改性PT的比表面积和孔体积逐渐减小。
4)光照射下改性后的PT1、PT2和PT3试样的光催化效率都相较改性前PT0试样和CdS更高,且PT2试样具有最大的光降解活性和较好的光催化循环稳定性。
