海洋水中罗丹明B 示踪剂的快速检测方法研究
2019-12-19王志龙
闫 峻,王志龙,徐 静,冯 硕
(核工业北京地质研究院, 北京 100029)
近年来, 随着工业生产的不断发展, 大量的工业、 生活垃圾以及排放进入海洋的污染物质, 或以离子状态存在, 或以颗粒和胶状状态存在。 以后两种状态存在的物质可能在较近的海区聚胶和下沉下来, 而以离子状态存在的污染物质可能随水体运动而扩散到很远的地方。 因此在海洋污染监测的过程中,对于污染物的流向是环境监测的重点和难点[1-3]。 罗丹明B, 又称玫瑰红B, 是一种碱性玫瑰红色的荧光染料, 具有价格低廉、 色泽红艳、 稳定性强等特点, 很容易溶于水和醇, 在海洋水中扩散后可以直接观察和追踪扩散径迹, 从而达到研究污染物运动规律的目的[4-5]。 因此用罗丹明B 作为示踪剂可以很好地代表离子状态污染物质的运动规律。
目前, 对罗丹明B 的检测方法主要有高效液相色 谱 法[6]、 液相色谱与质 谱联用 法[7]、超高效液相色谱与荧光联用法[8]和电化学法[9]等。 但是这些方法样品制备较为复杂, 而且仪器设备无法应用于野外监测。 而荧光分光光度法和分光光度法仪器设备经济、 便携, 样品前处理流程简单, 可以满足野外检测的各种要求, 是海洋污染监测过程中切实可行的方法。
本研究采用荧光分光光度法和分光光度法, 以罗丹明B 为研究对象, 建立了以罗丹明B 为海洋示踪剂的快速分析方法, 以期为海洋污染物监测提供快捷、 准确的分析方法。
1 实验仪器和试剂
1.1 实验仪器
F97XP 荧光分光光度计, 上海棱光技术有限公司; 721G 分光光度计, 上海第三分析仪器厂。
1.2 实验试剂
罗丹明B、 乙酸钠、 碳酸钠, 阿拉丁试剂(上海) 有限公司; 邻苯二甲酸氢钾、 混合磷酸盐、 硼砂标准缓冲溶液, 中国计量科学研究院; 海洋水由交通运输部天津水运工程科学研究院提供; 地热水由北京市地质工程勘察院提供; 地下水由中国地质科学院国家地质实验测试中心提供; 纯水为实验室自制去离子水, 符合GB/T 6682-2008 的要求。
2 荧光分光光度法
2.1 罗丹明B 最大吸收波长
应用荧光分光光度计进行测量时, 被测样品的最大吸光度值是测量的重要指标。 采用F97XP 荧光分光光度计, 在负高压为500 V的条件下, 分别对1.0 g/L 的罗丹明B 溶液在激发波长300~900 nm, 发射波长为300~900 nm 的范围内进行三维扫描, 获得罗丹明B 波长扫描等高图(图1)。
由图1 可见, 罗丹明B 的最大荧光值处的激发波长为553 nm、 发射波长为578 nm。因此, 选择激发波长为553 nm、 发射波长为578 nm 作为罗丹明B 的测定波长。
2.2 溶液pH 对罗丹明B 吸光度的影响
由于地下水、 海洋水和自来水等的pH 值存在一定的差异, 因此本试验分别用一定体积的邻苯二甲酸氢钾缓冲溶液、 磷酸盐缓冲溶液、 硼酸钠缓冲溶液、 1 mol·L-1乙酸钠溶液和1 mol·L-1碳酸钠溶液作为酸度调节剂,对0.4 mg·L-1的罗丹明B 溶液的pH 值进行调节, 并在荧光最大吸收波长处测定罗丹明B溶液的荧光吸光度值, 结果见表1。

图1 罗丹明B 荧光波长扫描等高图Fig. 1 The scanning contour map of rhodamine B fluorescence wavelength
由表1 可见, 罗丹明B 在酸性和碱性的条件下, 荧光吸光度值均比较稳定, 无论是加入不同体积的相同缓冲溶液, 还是加入相同体积的不同缓冲溶液, 荧光吸光度值相对标准偏差均在2%以下。 因此在测量过程中,无需添加额外的酸度调节剂。
2.3 不同基体对罗丹明B 含量测定的影响
取5 支25 mL 的比色管, 分别加入1.00 mL浓度为10 mg·L-1的罗丹明B 溶液, 并分别以去离子水、 自来水、 海水、 地热水和地下水定容至刻度, 在荧光最大吸收波长处测定罗丹明B 溶液的荧光吸光度值, 结果见表2。

表1 不同pH 值条件下罗丹明B 的荧光吸光度值Table 1 Fluorescence absorption value of rhodamine B at different pH value

表2 不同基体水样对罗丹明B 荧光吸光度的影响Table 2 Effect of different matrix water samples on fluorescence absorption of rhodamine B
由表2 可见, 不同基体水样对罗丹明B溶液的荧光吸光度值的的影响较小, 说明罗丹明B 可作为该基体水样的示踪剂从事科学研究工作。
2.4 罗丹明B 线性关系研究
在实际的测量中, 由于加入罗丹明B 示踪剂后, 不同的监测时间和不同的监测地点的罗丹明B 示踪剂的浓度差异较大, 最低浓度和最高浓度往往相差100 倍以上。 因此,本研究在4 μg·L-1~800 μg·L-1的浓度范围内, 分别做了低浓度和高浓度的标准曲线,具体方法如下。
2.4.1 低浓度标准曲线
分别准确移取标准溶液0.10、 0.20、0.30、 0.40、 0.50 mL 1.00 mg·L-1的罗丹明B于25 mL 比色管中, 加纯水定容至刻度, 摇匀。 用1 cm 比色皿, 在激发波长为553 nm、发射波长为578 nm, 负高压为500 V 的条件下分别测定荧光吸光度值, 以溶液中罗丹明B的质量(μg)为横坐标, 荧光吸光度值为纵坐标做线性回归方程。 结果见图2。
由 图2 可 见, 罗 丹 明B 在4 μg·L-1~20 μg·L-1的范围内线性关系良好, 线性回归方程为y=147.38x+6.22, 相关系数r=0.998 9,该线性回归方程适用于较低浓度的罗丹明B示踪剂的测量。
2.4.2 中浓度标准曲线
分 别 准 确 移 取1.00、 2.00、 3.00、 4.00、5.00 mL 1.00 mg·L-1的罗丹明B 标准溶液于25 mL 比色管中, 加纯水定容至刻度, 摇匀。用1 cm 比色皿, 在激发波长为553 nm、 发射波长为578 nm, 负高压为500 V 的条件下分别测定荧光吸光度值, 以溶液中罗丹明B 的质量(μg)为横坐标, 荧光吸光度值为纵坐标做线性回归方程。 结果见图3。

图2 低浓度罗丹明B 的线性回归方程Fig. 2 The regression curve of low concentration rhodamine B

图3 高浓度罗丹明B 的线性回归方程Fig. 3 The regression curve of high concentration rhodamine B
由图3 可见, 罗丹明B 在40 μg·L-1~200 μg·L-1的范围内线性关系良好, 线性回归方程为y=132.57x+18.19, 相关系数r=0.999 4,该线性回归方程适用于中等浓度的罗丹明B示踪剂的测量。
2.4.3 高浓度标准曲线
分 别 准 确 移 取1.00、 2.00、 3.00、 4.00、5.00、 10.00、 20.00 mL 1.00 mg·L-1的罗丹明B 标准溶液于25 mL 比色管中, 加纯水定容至刻度, 摇匀。 用1 cm 比色皿, 在激发波长为553 nm、 发射波长为578 nm, 负高压为500 V的条件下分别测定荧光吸光度值, 以溶液中罗丹明B 的质量(μg)为横坐标, 荧光吸光度值为纵坐标做线性回归方程。 结果见图4。

图4 中浓度罗丹明B 的线性回归方程Fig. 4 The regression curve of medium concentration rhodamine B
由图4 可见, 罗丹明B 在40 μg·L-1~800 μg·L-1的范围内线性关系良好, 线性回归方程为y=109.59x+93.12, 相关系数r=0.997 9,该线性回归方程适用于高浓度的罗丹明B 示踪剂的测量。 对于更高浓度样品, 可将样品稀释后进行测量。
2.5 罗丹明B 的正确度和检出限
配制含罗丹明B 浓度分别为0.004、0.006、 0.008、 0.010 和0.020 mg·L-1的海水样品, 用1 cm 比色皿, 在激发波长为553 nm、发射波长为578 nm, 负高压为500 V 的条件下分别测定荧光吸光度值, 并计算样品中罗丹明B 的含量, 结果见表3。

表3 罗丹明B 测量正确度结果Table 3 Correctness result of rhodamine B measurement
由表3 可见, 罗丹明B 的含量在0.004 mg·L-1~0.020 mg·L-1的范围内正确度良好。将0.004 μg·L-1的 罗 丹 明B 溶 液 继 续 稀 释,荧光吸光度值的平行性较差, 无法计算溶液中罗丹明B 的含量, 因此荧光分光光度法测定海水中罗丹明B 的含量的检出限为0.004 mg·L-1。
2.6 罗丹明B 的加标回收率
配制含罗丹明B 浓度分别为0.005 和0.050 mg·L-1的海水样品, 并加入一定量的罗丹明B, 用1 cm 比色皿, 在激发波长为553 nm、发射波长为578 nm, 负高压为500 V 的条件下分别测定荧光吸光度值, 并计算加标前后样品中罗丹明B 的含量, 结果见表4。
由表4 可知, 用该方法测量海水中罗丹明B 的回收率在98.7%~106%之间, 加标回收率良好。
3 分光光度法
3.1 罗丹明B 最大吸收波长
应用分光光度法进行测量时, 被测样品的最大吸光度值是测量的重要指标。 采用721G 型分光光度计, 以去离子水为参比, 采用3 cm 比色皿对1.0 g·L-1的罗丹明B 溶液在480~580 nm 的波长范围内进行扫描, 记录吸光度值, 结果见图5。

表4 罗丹明B 加标回收率测量结果Table 4 Result of recovery rate of rhodamine B
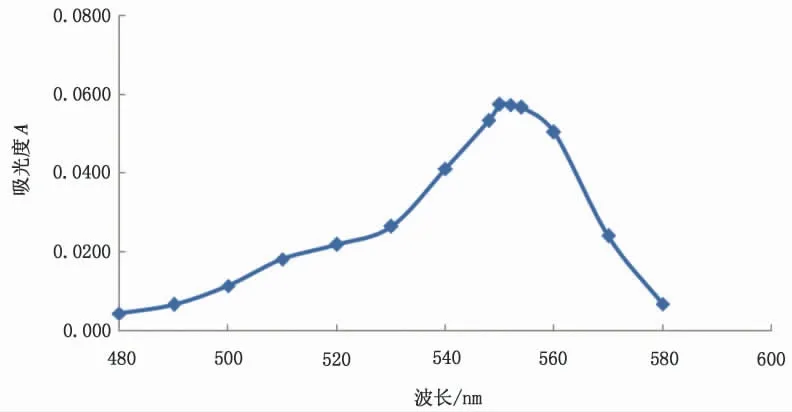
图5 罗丹明B 在可见光区的吸收曲线Fig. 5 Absorption curve of rhodamine B in visible wavelength
由图5 可见, 罗丹明B 的最大吸收波长为550 nm, 因此选择550 nm 作为罗丹明B 的测定波长。
3.2 溶液pH 对罗丹明B 吸光度的影响
由于地下水、 海洋水、 自来水等的pH 值存在一定的差异, 因此本试验分别用一定体积的邻苯二甲酸氢钾缓冲溶液(pH=4.00)、 磷酸盐缓冲溶液(pH=6.86)、 硼酸钠缓冲溶液(pH=9.18)、 1 mol·L-1乙酸钠溶液和1 mol·L-1碳酸钠溶液作为酸度调节剂, 对0.4 mg·L-1的罗丹明B 溶液的pH 值进行调节, 并在550 nm 波长处测定罗丹明B 溶液的吸光度值, 结果见表5。
由表5 可见, 罗丹明B 在酸性和碱性的条件下, 吸光度值均比较稳定, 无论是加入不同体积的相同缓冲溶液, 还是加入相同体积的不同缓冲溶液, 荧光吸光度值相对标准偏差均在2.4% 以下。 因此在测量过程中, 无需添加额外的酸度调节剂。
3.3 不同基体对罗丹明B 含量测定的影响
取5 支25 mL 的比色管, 分别加入1.00 mL浓度为10 mg·L-1的罗丹明B 溶液, 并分别以去离子水、 自来水、 海水、 地热水和地下水定容至刻度, 在550 nm 波长处测定罗丹明B溶液的吸光度值, 结果见表6。
由表6 可见, 不同基体水样对罗丹明B溶液的吸光度值的的影响较小, 说明罗丹明B可作为该基体水样的示踪剂从事科学研究工作。
3.4 罗丹明B 线性关系
在实际的测量中, 由于加入罗丹明B 示踪剂后, 不同的监测时间和不同的监测地点的罗丹明B 示踪剂的浓度差异较大, 最低浓度和最高浓度往往相差100 倍以上。 因此,本研究在4 μg·L-1~800 μg·L-1的浓度范围内, 分别做了低浓度和高浓度的标准曲线,具体方法如下:
3.4.1 低浓度标准曲线
分别准确移取0.10、 0.20、 0.30、 0.40 和0.50 mL 1.00 mg·L-1的罗丹明B 标准溶 液于25 mL 比色管中, 加纯水定容至刻度, 摇匀。用10 cm 比色皿, 以纯水为参比, 在550 nm波长下分别测定吸光度值, 以溶液中罗丹明B的质量(μg)为横坐标, 吸光度值为纵坐标做线性回归方程。 结果见图6。

表5 不同pH 值条件下罗丹明B 的吸光度值Table 5 Absorption value of rhodamine B at different pH value

表6 不同基体水样对罗丹明B 吸光度的影响Table 6 Effect of different matrix water samples on absorption of rhodamine B

图6 低浓度罗丹明B 的线性回归方程Fig. 6 The regression curve of low concentration rhodamine B
由图6 可见, 罗丹明B 在4 μg·L-1~20 μg·L-1的范围内线性关系良好, 线性回归方程为y=0.080 1x+0.005 1, 相关系数r=0.999 7,该线性回归方程适用于较低浓度的罗丹明B示踪剂的测量。
3.4.2 中浓度标准曲线
分别准确移取1.00、 2.00、 3.00、 4.00 和5.00 mL 1.00 mg·L-1的罗丹明B 标准溶液于25 mL 比色管中, 加纯水定容至刻度, 摇匀。用1 cm 比色皿, 以纯水为参比, 在550 nm波长下分别测定吸光度值, 以溶液中罗丹明B的质量(μg)为横坐标, 吸光度值为纵坐标做线性回归方程, 结果见图7。

图7 中浓度罗丹明B 的线性回归方程Fig. 7 The regression curve of medium concentration rhodamine B
由图7 可见, 罗丹明B 在40 μg·L-1~200 μg·L-1的范围内线性关系良好, 线性回归方程为y=0.024 0x+0.018 5, 相关系数r=0.999 7,该线性回归方程适用于中浓度的罗丹明B 示踪剂的测量。
3.4.3 高浓度标准曲线
分 别 准 确 移 取1.00、 2.00、 3.00、 4.00、5.00、 10.00 和20.00 mL 1.00 mg·L-1的罗丹明B 标准溶液于25 mL 比色管中, 加纯水定容至刻度, 摇匀。 用1 cm 比色皿, 以纯水为参比, 在550 nm 波长下分别测定吸光度值, 以溶液中罗丹明B 的质量(μg)为横坐标, 吸光度值为纵坐标做线性回归方程, 结果见图8。

图8 高浓度罗丹明B 的线性回归方程Fig. 8 The regression curve of high concentration rhodamine B
由图8 可见, 罗丹明B 在40 μg·L-1~800 μg·L-1的范围内线性关系良好, 线性回归方程为y=0.007 8x+0.023 6, 相关系数r=0.999 6,该线性回归方程适用于高浓度的罗丹明B 示踪剂的测量。 对于更高浓度的样品, 可将样品稀释后进行测量。
3.5 罗丹明B 正确度和检出限
配制含罗丹明B 浓度分别为0.004、0.006、 0.008、 0.010、 0.020 和0.040 mg·L-1的海水样品, 用10 cm 比色皿在550 nm 波长下测定各样品的吸光度值, 并计算各样品中罗丹明B 的含量, 结果见表7。

表7 罗丹明B 测量正确度结果Table 7 Correctness result of rhodamine B measurement
由表7 可见, 罗丹明B 的含量在0.010 mg·L-1以上时正确度良好, 低于0.010 mg·L-1时罗丹明B 计算结果偏差较大。 因此分光光度法测定海水中罗丹明B 的含量的检出限为0.010 mg·L-1。
3.6 罗丹明B 的加标回收率
配制含罗丹明B 浓度分别为0.005、0.050、 0.500 和5.00 mg·L-1的海水样品, 并加入一定量的罗丹明B, 其中0.005 和0.050 mg·L-1的样品用10 cm 比色皿, 0.500 mg·L-1的样品用3 cm 比色皿, 5.00 mg·L-1的样品用1 cm 比色皿, 在550 nm 波长下分别测定吸光度值, 并计算加标前后样品中罗丹明B 的含量, 结果见表8。
由表8 可见, 用该方法测量海水中罗丹明B 的回收率在89.9%~116%之间, 加标回收率可以满足要求。

表8 罗丹明B 加标回收率测量结果Table 8 Result of recovery rate of rhodamine B
4 结论与建议
本研究建立的荧光分光光度法和分光光度法二者均可用于海洋水中罗丹明B 示踪剂的定量分析。 通过对比可知, 两种方法均不受基体种类和pH 等因素的影响, 且样品前处理简单、 快速。 荧光分光光度法的检出限 (0.004 mg·L-1) 优 于 分 光 光 度 法(0.010 mg·L-1), 但是在野外监测过程中, 荧光分光光度法对环境的要求高于分光光度法,且荧光分光光度计长时间开机光源需要散热,需要定时停机 “休息”, 从而影响野外检测进度[10]。 而分光光度计对环境的要求较为简单,仪器较荧光分光光度计更加便携, 且可长时间连续工作。 因此, 在海洋监测活动中, 可根据实际的工作量和需求, 选取荧光分光光度法或分光光度法进行测试。
