乌鸡白凤丸联合抗病毒治疗对慢性病毒性肝炎和肝硬化临床疗效和安全性的Meta分析
2022-12-08江永萍强晓钰彭莹莹
周 鸿,江永萍,陈 哲,强晓钰,彭莹莹,王 辉*
乌鸡白凤丸联合抗病毒治疗对慢性病毒性肝炎和肝硬化临床疗效和安全性的Meta分析
周 鸿1, 2,江永萍3,陈 哲4,强晓钰4,彭莹莹5, 6,王 辉4*
1. 津药达仁堂集团股份有限公司第六中药厂,天津 300401 2. 津药达仁堂集团股份有限公司,天津 300193 3. 津药达仁堂集团股份有限公司乐仁堂制药厂,天津 300380 4. 天津中医药大学循证医学中心,天津 301617 5. 天津中医药大学第一附属医院,天津 300382 6. 国家中医针灸临床医学研究中心,天津 300382
系统评价乌鸡白凤丸联合抗病毒治疗对慢性病毒性肝炎(慢性肝炎)和肝硬化的临床疗效和安全性。计算机检索中国知网(CNKI)、万方数据库(Wanfang Data)、维普(VIP)、中国生物医学文献服务系统(SinoMed)、PubMed、Embase、Cochrane Library 7个中英文数据库,检索的文献类型为乌鸡白凤丸治疗慢性肝炎和肝硬化的随机对照试验,检索时间为数据库建立到2021年3月1日。由专业人员进行双检索、双提取和双评价,使用RevMan 5.3软件进行Meta分析。最终纳入10篇文献,涉及867例患者。Meta分析结果显示,与单用抗病毒药物比较,乌鸡白凤丸联合抗病毒药物在改善临床总有效率[RR=1.32,95%CI(1.15, 1.51),<0.000 1]、白蛋白[MD=2.88,95%CI(0.80,4.97),=0.007]、丙氨酸氨基转移酶[MD=−28.49,95%CI(−46.15,−10.83),=0.002]、天冬氨酸氨基转移酶 [MD=−32.04,95%CI(−49.40,−14.67),=0.000 3]、总胆红素 [MD=−19.10,95%CI(−27.37,−10.84),<0.000 01]、透明质酸 [MD=−49.67,95%CI(−76.59,−22.75),=0.000 3]、层黏连蛋白 [MD=−36.16,95%CI(−56.32,−16.00),=0.000 4]、血清Ⅲ型前胶原 [MD=−24.25,95%CI(−48.43,−0.06),=0.05] 和Ⅳ型胶原 [MD=−21.06,95%CI(−37.98,−4.14),=0.01] 方面差异显著,均具有统计学意义。安全性方面较好,但还需要进一步研究佐证。乌鸡白凤丸联合抗病毒治疗可以有效改善慢性肝炎和肝硬化的临床疗效,还需要开展大量高质量临床研究进一步验证。
乌鸡白凤丸;慢性病毒性肝炎;肝硬化;随机对照试验;抗病毒
肝炎是一种肝脏炎症的感染性疾病,是由肝炎病毒引起,可以通过粪便直接或间接接触、注射及性交等方式传播[1]。肝炎病毒感染的范围包括从无症状感染到暴发性肝炎这一过程[2]。肝炎患者感染后的临床症状多表现为皮肤黄疸、眼睛发黄、乏力、发烧、恶心、呕吐等症状[1,3]。肝炎的预防方式以接种疫苗为主要方式[1],但是较多的肝炎患者往往忽视接种疫苗,也是导致该病发病率增加的主要因素之一[4]。肝炎相关疾病为递进式病变的形式,包括慢性病毒性肝炎(慢性肝炎)和肝硬化等[5]。相关遗传学研究表明慢性肝炎感染过程中,可以造成肝硬化发展为肝癌的概率较大,其中有70%肝癌患者感染的病毒为乙型肝炎病毒和丙型肝炎病毒[6]。慢性肝炎和肝硬化患者的临床治疗方式多是采用抗病毒药物治疗,但是如果长期使用,也会造成耐药性和疗效不稳定的问题[7-8]。乌鸡白凤丸虽是妇科常用药物,但乌鸡白凤丸可以治疗肝气郁结相关疾病,在治疗肝损伤方面有着一定临床优势[9]。基于目前大量的中医理论基础,肝气郁结和瘀血阻滞与肝炎、肝硬化的相关生化指标有着较强的关联性[10]。目前乌鸡白凤丸联合抗病毒药物治疗肝炎及肝硬化缺乏系统性梳理和评价。因此,本研究对乌鸡白凤丸联合抗病毒药物治疗慢性肝炎和肝硬化的临床研究进行Meta分析,以此评价其临床疗效的有效性和安全性。
1 资料与方法
1.1 纳入标准
1.1.1 研究类型 纳入的研究均为乌鸡白凤丸治疗肝炎及肝硬化的随机对照试验(randomized controlled trial,RCT)。对所纳入研究的语言类型不进行限制,无论是否使用盲法和分配隐藏。
1.1.2 研究对象 临床诊断为慢性病毒性肝炎和肝硬化的患者。
1.1.3 干预措施 试验组的干预措施为乌鸡白凤丸联合抗病毒治疗,对照组为抗病毒治疗。抗病毒治疗包括西医常规抗病毒药物(阿德福韦酯、拉米夫定等)以及保肝药物治疗等措施。试验组和对照组的干预措施的基础治疗必须一致。
1.1.4 结局指标 结局指标主要包括临床总有效率、白蛋白(albumin,ALB)、丙氨酸氨基转移酶(alanine aminotransferase,ALT)、天冬氨酸氨基转移酶(aspartate aminotransferase,AST)、总胆红素(total bilirubin,TBIL)、透明质酸(hyaluronic acid,HA)、层黏连蛋白(laminin,LN)、Ⅲ型前胶原(procollagen-Ⅲ-peptide,PCⅢ)、Ⅳ型胶原(collage type IV,IV-C)和不良反应/不良事件情况(adverse events,AEs)。
1.2 排除标准
①动物实验、细胞实验等不符合纳入标准的研究类型;②缺乏结局指标;③重复发表文献;④数据存在严重缺失和显著问题文献以及未检索到全文的研究。
1.3 文献检索策略
本研究由双人进行文献检索,以确保文献的准确性和全面性。检索所涉及的中文数据库包括中国知网(CNKI)、万方数据库(Wanfang Data)、维普(VIP)和中国生物医学文献服务系统(SinoMed)数据库。检索所涉及的英文数据库为PubMed、Embase、Cochrane Library数据库。检索乌鸡白凤丸治疗肝炎及肝硬化的相关RCTs。检索的时间为数据库建立到2021年3月1日。本研究使用主题词与自由词进行检索,中文检索词为乌鸡白凤丸、肝炎、肝硬化、慢性肝炎、慢性肝硬化等。英文检索词为Wuji Baifeng、Wuji Baifeng Wan、hepatitis、liver cirrhosis、posthepatitic cirrhosis等。中文检索策略为SU=“乌鸡白凤丸”AND(“肝炎”+“慢性肝炎”+“病毒性肝炎”+“甲型肝炎”+“乙型肝炎”+“丙型肝炎”+“丁型肝炎”+“戊型肝炎”+“肝硬化”+“慢性肝硬化”)。除此之外,本研究还对所有纳入研究的参考文献进行筛查和检索,以此来补充和获得更多的研究。
1.4 文献筛选与数据提取
由2名专业人员分别独立地进行文献筛选,文献筛选完成后再进行研究的交叉核对。在文献筛选时,首先阅读全部文献的题目和摘要内容,再进一步详细阅读全文内容,最终判断是否符合本研究的纳入标准。2名专业人员在数据提取过程中需要使用相同的纳入标准与排除标准。如果在此过程中出现分歧,必须交由第3方专业人员进行裁定,并给出最终决定和意见。
1.5 偏倚风险评价
本研究遵循Cochrane系统评价员手册5.1.0的RCT偏倚风险评估工具进行偏倚风险评价[11],包括①随机方法是否正确;②分配隐藏是否提及;③是否使用盲法(对研究人员施盲、对患者施盲和对结果评价者施盲);④是否存在人员失访和退出;⑤文献是否存在选择性发表偏倚;⑥是否存在其他偏倚。
1.6 统计学方法
本研究所涉及的结局指标为二分类数据和连续性数据。二分类数据使用风险比(risk ratio,RR)作为效应指标,连续性数据使用均数差(mean difference,MD)或标准均数差(standardized mean difference,SMD)。针对研究的异质性,选择随机效应模型和固定效应模型。异质性较大(<0.1,2>50%),选择随机效应模型;异质性较小(≥0.1,2≤50%),选用固定效应模型。根据对照组用药的方式进行亚组分类,分为中医药治疗和西医抗病毒治疗,以此来探究异质性来源。结局指标所涉及的研究文献量≥10时,进行漏斗图的绘制来寻找潜在的发表偏倚。本研究均使用RevMan 5.3进行图形绘制和数据分析。
2 结果
2.1 文献检索结果
本研究对数据库进行系统和详细检索后,共检索到173篇文献。初次文献查重后,一共得到73篇文献;再对文献进行题目和摘要阅读后,排除了52篇,剩余21篇文献。对所得到的文献进行全文阅读和结局指标核对,最终得到10篇文献。文献检索流程见图1。
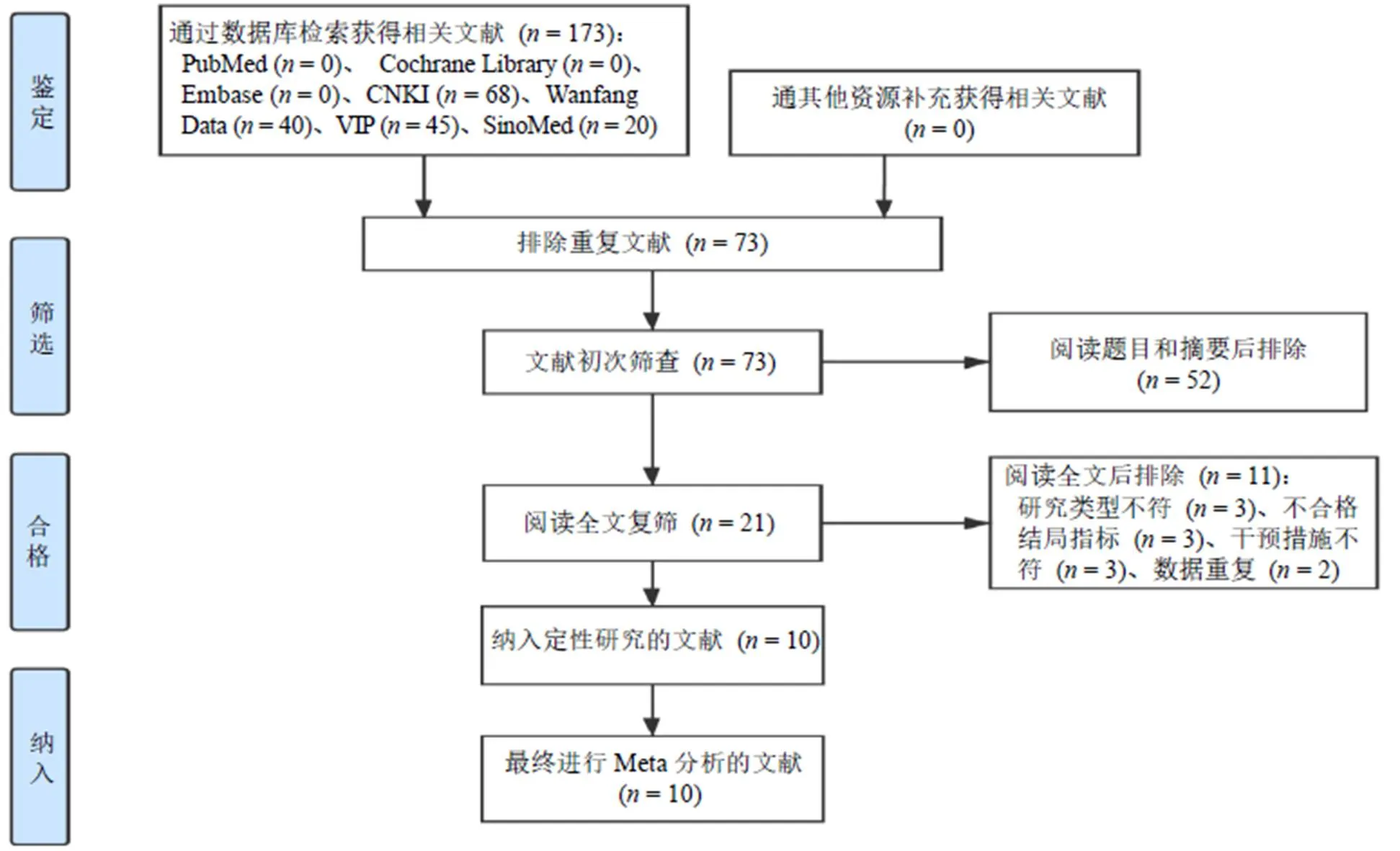
图1 文献筛查流程
2.2 文献的基本特征
最终纳入10项RCTs[12-21],涉及慢性肝炎及肝硬化患者867例。患者的年龄平均中位数为41岁,平均疗程为6.04个月。全部纳入的RCTs的治疗组均为乌鸡白凤丸联合西医抗病毒治疗,对照组是西医抗病毒治疗。6项研究[12-17]报道了治疗前后的临床总有效率,3项研究[18-20]报道了治疗前后的ALB,2项研究[19,21]报道了治疗前后的ALT、AST、TBIL、HA、LN、PCⅢ、IV-C,6项研究[13,15-16,19-21]报道了治疗前后的AEs。文献基本特征见表1。
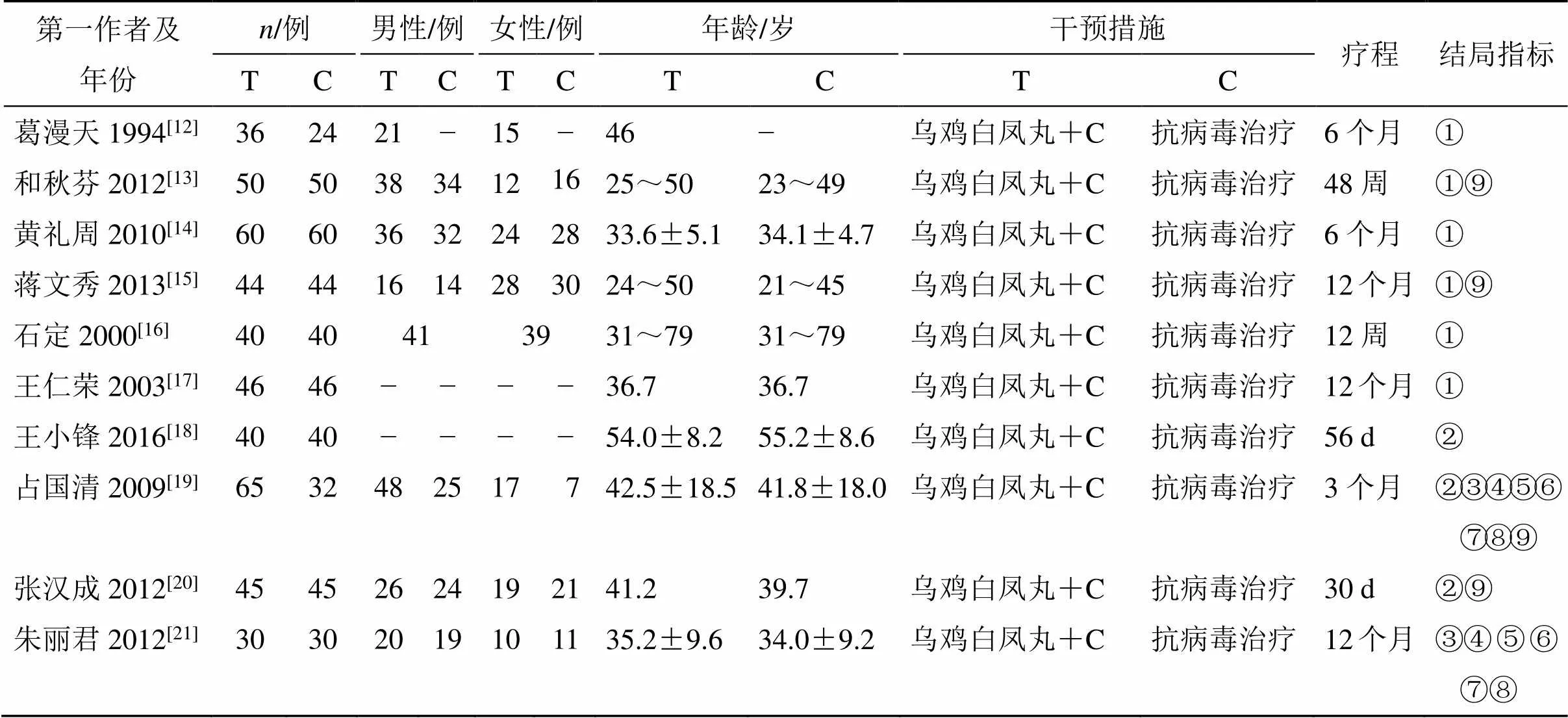
表1 文献基本特征
T-试验组 C-对照组 “−”-未提及 ①临床总有效率 ②白蛋白 ③丙氨酸氨基转移酶 ④天冬氨酸氨基转移酶 ⑤总胆红素 ⑥透明质酸⑦层黏连蛋白 ⑧Ⅲ型前胶原 ⑨Ⅳ型胶原
T-treatment group C-control group “−”-did not mention ①total clinical effective rate ②albumin ③alanine aminotransferase ④aspartate aminotransferase ⑤total bilirubin ⑥hyaluronic acid ⑦laminin ⑧procollagen-Ⅲ-peptide ⑨collage type IV
2.3 研究的质量评价
纳入的10篇RCTs均使用了随机方法,其中只有1项RCTs[18]明确提及使用了随机数字表法。大部分RCTs没有提及分配隐藏,仅有1项研究[14]提及使用了信封法。80%的RCTs可能存在选择性发表偏倚[12-18,20]。所有纳入的RCTs均未提及盲法和其他发表偏倚。所有纳入RCTs的偏倚风险评价质量见图2。
2.4 Meta分析结果
2.4.1 临床总有效率 6项RCTs[12-17]报道了临床总有效率,经过Meta分析和异质性检测后,发现异质性较大(=0.03,2=60%)。使用随机效应模型进行Meta分析,结果显示试验组与对照组比较差异存在统计学意义[RR=1.32,95%CI(1.15,1.51),<0.000 1]。根据疾病类型(肝炎和肝硬化)进行了亚组分析,疾病类型的亚组分析结果显示,临床诊断为肝炎(=0.007,2=75%)异质性较大,肝硬化(=0.30,2=6%)异质性较小。在肝炎[RR=1.36,95%CI(1.10,1.68),=0.004] 和肝硬化 [RR=1.24,95%CI(1.05,1.45),=0.009]中,乌鸡白凤丸联合抗病毒治疗均优于单纯使用抗病毒治疗,差异具有统计学意义。见图3。
2.4.2 ALB 3项RCTs[18-20]报道了肝硬化患者ALB的情况,经异质性检测后发现异质性较大(=0.05,2=67%),采用随机效应模型进行分析。Meta分析结果显示,试验组要优于对照组,差异具有统计学意义[MD=2.88,95%CI(0.80,4.97),=0.007]。见图4-A。
2.4.3 ALT 2项RCTs[19,21]报道了肝硬化患者ALT的情况,经异质性检测后发现异质性较小(=0.76,2=0),采用固定效应模型进行分析。Meta分析结果显示,试验优于对照组,差异具有统计学意义[MD=−28.49,95%CI(−46.15,−10.83),=0.002]。见图4-B。
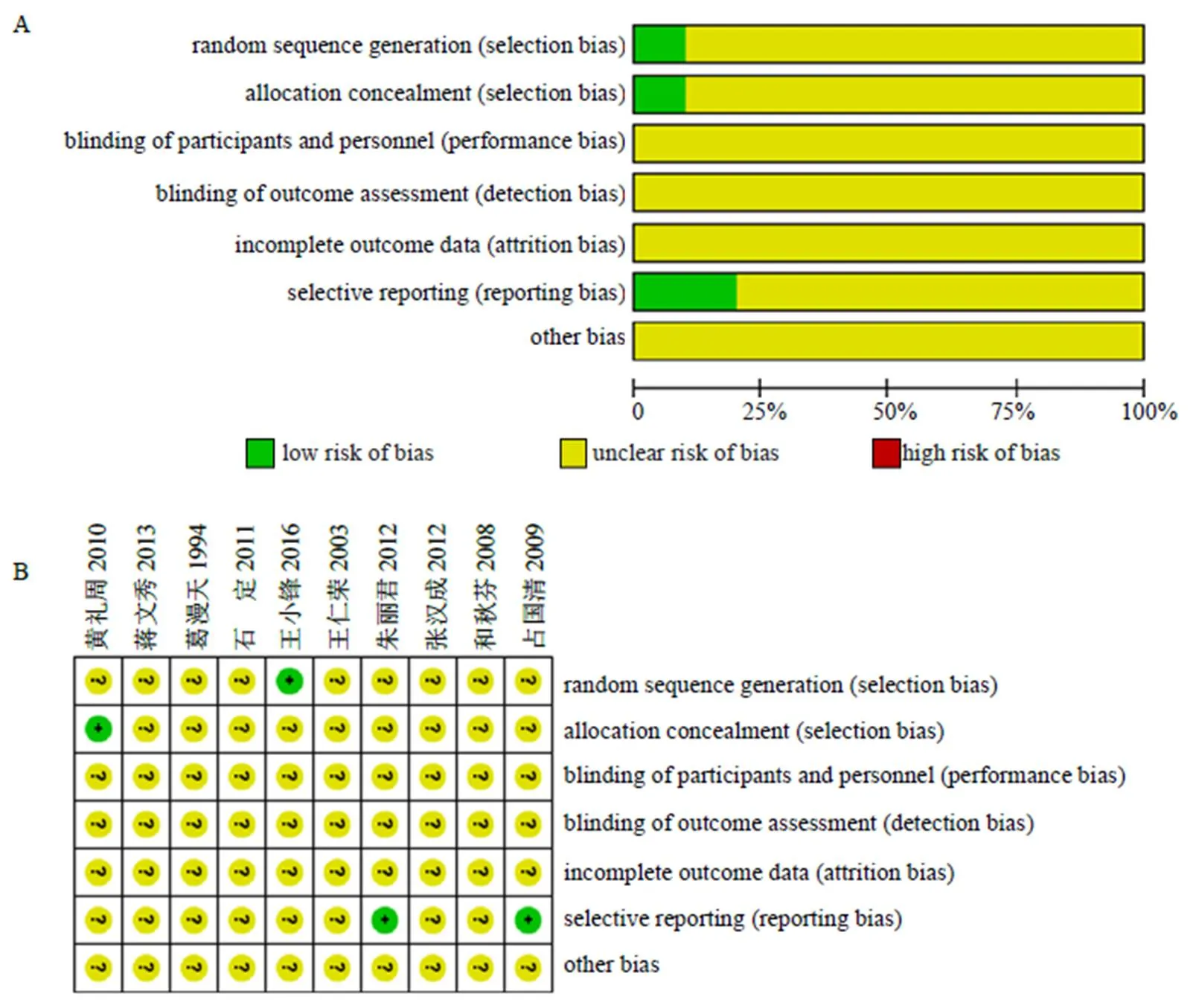
A-研究产生的偏倚风险项目占比 B-研究产生的偏倚风险的各个项目
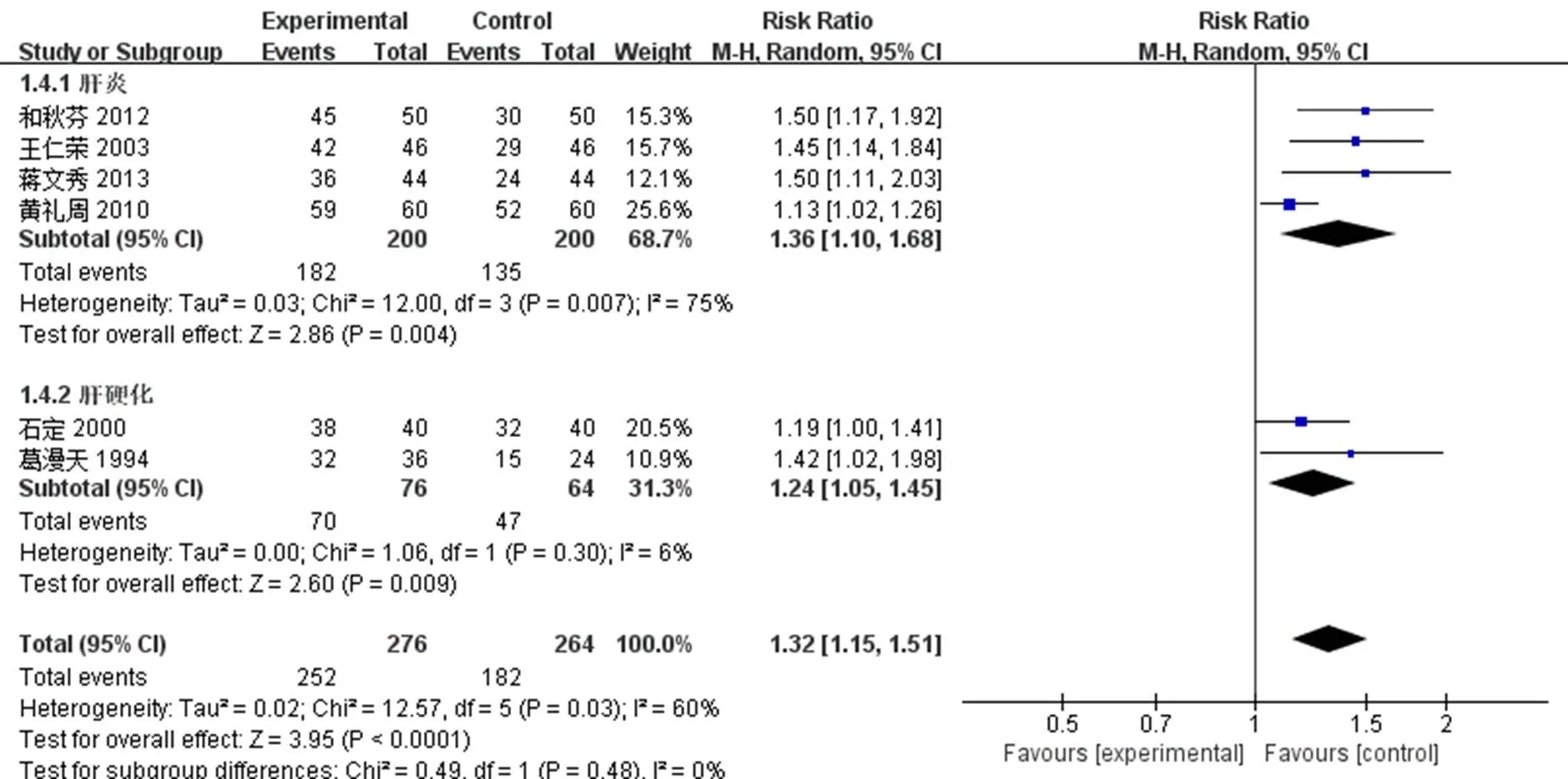
图3 临床总有效率森林图
2.4.4 AST 2项RCTs[19,21]报道了肝硬化患者AST的情况,经异质性检测后发现异质性较小(=0.96,2=0),采用固定效应模型进行分析。Meta分析结果显示,试验组优于对照组,差异具有统计学意义[MD=−32.04,95%CI(−49.40,−14.67),=0.000 3]。见图4-C。
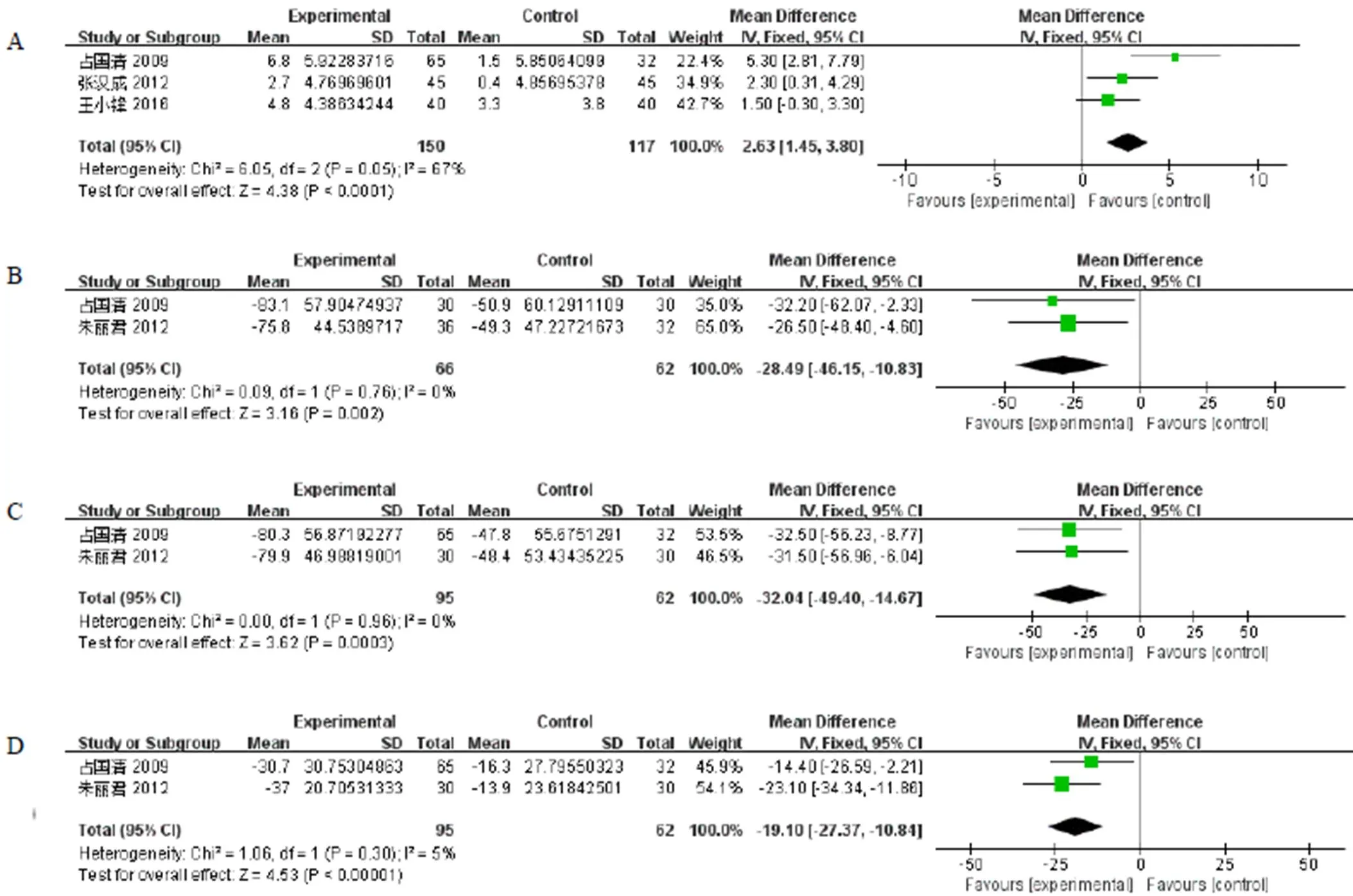
2.4.5 TBIL 2篇RCTs[19,21]报道了肝硬化患者TBIL的情况,经异质性检测后发现异质性较小(=0.30,2=5%),采用固定效应模型进行分析。Meta分析结果显示,试验组优于对照组,差异具有统计学意义[MD=−19.10,95%CI(−27.37,−10.84),<0.000 01]。见图4-D。
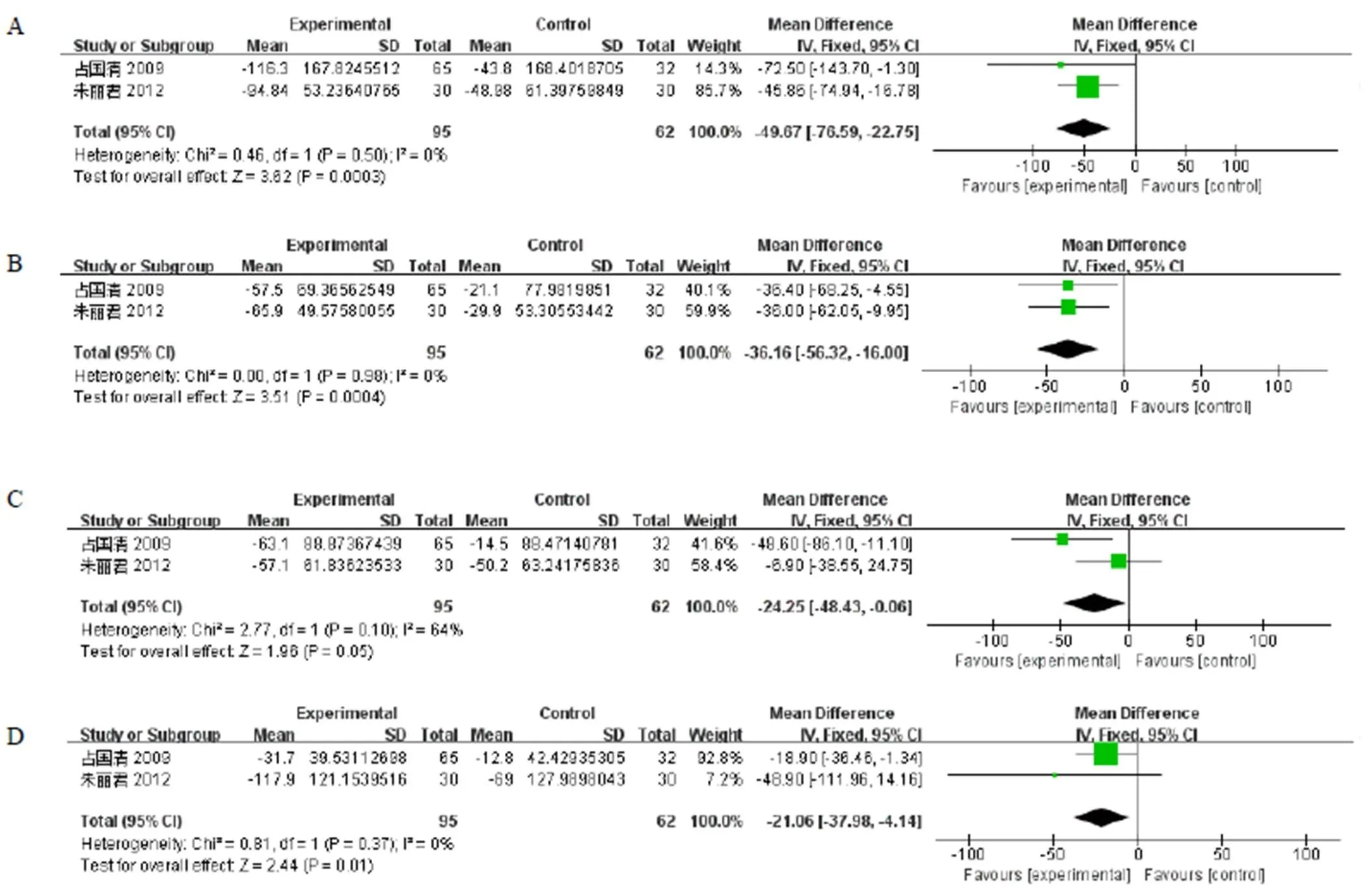
2.4.6 HA 2项RCTs报道了肝硬化患者HA[19,21]的情况,异质性检测后发现异质性较小(=0.50,2=0),采用固定效应模型进行分析。Meta分析结果显示,试验组优于对照组,差异具有统计学意义[MD=−49.67,95%CI(−76.59,−22.75),=0.000 3]。见图5-A。
2.4.7 LN 2项RCTs报道了肝硬化患者LN[19,21]的情况,异质性检测后发现异质性较小(=0.98,2=0),采用固定效应模型进行分析。Meta分析结果显示,试验组优于对照组,差异具有统计学意义[MD=−36.16,95%CI(−56.32,−16.00),=0.000 4]。见图5-B。
2.4.8 PCⅢ 2项RCTs[19,21]报道了肝硬化患者PCⅢ的情况,异质性检测后发现异质性较小(=0.10,2=64%),采用固定效应模型进行分析。Meta分析结果显示,试验组优于对照组,差异具有统计学意义[MD=−24.25,95%CI(−48.43,−0.06),=0.05]。见图5-C。
2.4.9 IV-C 2项RCTs[19,21]报道了肝硬化患者IV-C的情况,异质性检测后发现异质性较小(=0.37,2=0),采用固定效应模型进行分析。Meta分析结果显示,试验组优于对照组,差异具有统计学意义[MD=−21.06,95%CI(−37.98,−4.14),=0.01]。见图5-D。
2.5 不良反应/事件情况
共有6篇文献报道了不良反应情况,其中5项RCTs[13,15,19-21]报道试验组与对照组之间无不良反应。仅有1项RCT[16]报道了不良反应情况:试验组的不良反应为4例恶心,对照组不良反应为3例恶心,均在对症治疗后,症状有所缓解。
2.6 发表偏倚报告
本研究的各个结局指标所纳入的研究数均未到10篇,因此无法绘制漏斗图来解释可能存在的发表偏倚。
3 讨论
3.1 研究的意义
慢性肝病是由于肝炎病毒、酒精、药物、寄生虫等致病因素所导致的代谢异常和免疫系统紊乱相关疾病[22-23]。慢性肝炎、肝纤维化和肝硬化,三者往往是呈递进性疾病发展历程[24]。相关研究表明,肝硬化死亡率随年龄呈上升趋势,并且60%的肝硬化死亡率是由于感染乙型肝炎病毒和丙型肝炎病毒造成[25]。除此之外,肝炎和肝硬化作为危险因素,能够导致其他疾病的发生[26-27]。目前,临床上治疗慢性肝炎和肝硬化,主要采用抗病毒药物进行治疗。如果长期采用抗病毒治疗,会存在耐药性、远期疗效不稳定等问题[7-8]。相关研究表明,乌鸡白凤丸可以对肝细胞进行保护,有效防止肝脏损伤,调节氨基酸代谢异常,增强免疫功能,促进肝糖元和相关蛋白质合成代谢等[28-29],可能会在一定程度上改善抗病毒药物的不良反应情况。基于现有的临床RCTs,本研究认为有必要进行深入性研究探究乌鸡白凤丸治疗肝炎和肝硬化的整体性疗效和安全性。
3.2 研究的结果
研究最终纳入10篇RCTs,涉及867例患者,其中6项RCTs报道了临床总有效率;3项研究报道了ALB;ALT、AST、TBIL、HA、LN、PCⅢ和IV-C分别有2项研究进行了报道;6项研究报道了AEs的发生情况,其中5项研究报道无不良反应发生,1项研究报道了不良反应发生情况。
通过Meta分析结果显示,乌鸡白凤丸联合抗病毒药物在慢性肝炎和肝硬化的临床治疗效果较好,优于抗病毒治疗。在改善患者ALB、ALT、AST、TBIL、HA、LN、PCⅢ和IV-C方面,乌鸡白凤丸联合抗病毒治疗存在一定优势,但是部分异质性无法进行消除,还需要增加样本量和研究数量进一步减少异质性。在安全性方面,有多项研究报道无不良反应发生,表明乌鸡白凤丸临床安全性较好。综上,本研究认为乌鸡白凤丸在治疗慢性肝炎和肝硬化方面起到较好的临床治疗效果,但还是需要高质量的临床研究进一步对其进行验证。
3.3 对临床指导意见
本研究制定了纳入、排除标准和干预措施。根据Meta分析结果显示,仍然有部分异质性无法充分说明,但不影响结果的稳定性。由于纳入的研究本身质量较差,存在一定发表偏倚,希望今后在进行临床试验时,注意研究的顶层设计和科学严谨性。严格遵循Cochrane质量报告规范,从而有助于进一步建立中医药临床疗效体系。在临床药物使用时,乌鸡白凤丸作为妇科类常用药,临床医生在治疗相关性疾病时,要注意全面诊疗。临床医师还要不断积累临床经验,在开具处方时将中医临床经验和领域内的高质量研究进行综合运用,从而更好地服务患者。
3.4 本研究的局限性
本研究存在以下几个方面的局限性:(1)纳入文献的数量较少,并且大部分文献可能存在一定选择性发表偏倚。文献的质量较低,仅有少数研究提及了随机序列生成方法,均没有提及盲法,可能在一定程度上影响结果的可信度和真实性。纳入的文献全部为中文文献,也可能存在语言和地域性影响。(2)慢性肝炎的发病病程一般较长,而本研究所纳入文献的疗程较短,仅能够对短期疗程进行评价,均没有随访,无法全面和综合性评价疗效。(3)结局指标的数量较多,但是涉及研究不足,无法消除部分异质性的影响。(4)虽然有5篇研究报道没有不良反应发生,极有可能是受到样本量的影响,所以安全性问题不容忽视。
4 结论
乌鸡白凤丸联合抗病毒治疗在治疗慢性肝炎和肝硬化方面有着较好的临床治疗效果。在临床疗效有效率、ALB、ALT、AST、TBIL、HA、LN、PCⅢ和IV-C方面,乌鸡白凤丸联合抗病毒治疗要优于单纯使用抗病毒治疗。基于目前研究来看,乌鸡白凤丸的安全性较好,但还需要进一步研究证实。希望今后可以开展更多高质量研究来进一步验证和阐述乌鸡白凤丸的临床疗效和安全性。
利益冲突 所有作者均声明不存在利益冲突
[1] Linder K A, Malani P N. Hepatitis a [J]., 2017, 318(23): 2393.
[2] 王瑞, 李嘉. 《慢性乙型肝炎防治指南(2019年版)》更新要点解读 [J]. 实用器官移植电子杂志, 2021, 9(1): 1-5.
[3] Aggarwal R, Goel A. Hepatitis A: Epidemiology in resource-poor countries [J]., 2015, 28(5): 488-496.
[4] 中国肝炎预防控制基金会, 中华医学会传染病学会, 中华医学会肝病学分会. 阻断乙型肝炎病毒母婴传播临床管理流程(2021年) [J]. 临床肝胆病杂志, 2021, 37(3): 527-531.
[5] Morrison L M, Rosenthal M, Holeman R,The relationship of viral hepatitis to cirrhosis of the liver [J]., 1961, 35: 371-384.
[6] Kanda T, Goto T, Hirotsu Y,. Molecular mechanisms driving progression of liver cirrhosis towards hepatocellular carcinoma in chronic hepatitis B and C infections: A review [J]., 2019, 20(6): 1358.
[7] Pawlotsky J M. Hepatitis C virus resistance to direct-acting antiviral drugs in interferon-free regimens [J]., 2016, 151(1): 70-86.
[8] Reig M, Mariño Z, Perelló C,. Unexpected high rate of early tumor recurrence in patients with HCV-related HCC undergoing interferon-free therapy [J]., 2016, 65(4): 719-726.
[9] 徐慧媛. 治疗痛经中成药的合理使用 [J]. 中华全科医师杂志, 2010, 9(4): 291-292.
[10] 靳天怡, 刘汶. 肝硬化中医证型与生物学指标相关性近10年研究进展 [J]. 环球中医药, 2020, 13(1): 163-168.
[11] The Cochrane Collaboration. Cochrane handbook for systematic reviews of interventions version 5.1.0. [EB/OL]. (2011-03-01). http://www.handbook.cochrane.org.
[12] 葛漫天. 乌鸡白凤丸治疗肝硬化所致血清蛋白比例倒置的临床观察 [J]. 山西中医, 1994, 10(5): 18-19.
[13] 和秋芬. 拉米夫定联合乌鸡白凤丸对慢性乙型肝炎抗病毒疗效的临床观察 [J]. 中医临床研究, 2012, 4(13): 92-93.
[14] 黄礼周. 加用同仁乌鸡白凤丸治疗慢性乙型病毒性肝炎乏力60例 [J]. 广西中医药, 2010, 33(2): 25-26.
[15] 蒋文秀. 拉米夫定联合乌鸡白凤丸对慢性乙型肝炎治疗效果的临床研究 [J]. 医药前沿, 2013(5): 180-181.
[16] 石定, 艾宏伟, 王文菊. 乌鸡白凤丸与马洛替酯联合治疗肝炎后肝硬化低白蛋白血症40例 [J]. 中国中西医结合脾胃杂志, 2000, 8(4): 247.
[17] 王仁荣, 姚杰良, 华伟, 陈静, 梁辉. 中西药合用治疗慢性乙型肝炎疗效观察 [J]. 实用中医药杂志, 2003, 19(11): 586-587.
[18] 王小锋, 伏沿蓉, 樊晓丹. 乌鸡白凤丸治疗肝硬化脾功能亢进症的临床研究 [J]. 现代中医药, 2016, 36(6): 18-20, 25.
[19] 占国清, 郑三菊, 朱琳, 等. 促肝细胞生长素联合乌鸡白凤丸治疗肝硬化65例疗效观察 [J]. 中国药房, 2009, 20(36): 2861-2863.
[20] 张汉成, 王明. 浅谈乌鸡白凤丸治疗慢性乙型肝肝硬化临床观察 [J]. 大家健康: 学术版, 2012, 6(8): 17-18.
[21] 朱丽君. 中西药联用对乙型肝炎肝硬变代偿期的临床观察 [J]. 河南中医, 2012, 32(9): 1147-1148.
[22] 中华医学会肝病学分会, 中华医学会感染病学分会. 丙型肝炎防治指南(2019年版) [J]. 实用肝脏病杂志, 2020, 23(1): 后插33-后插33.
[23] Trautwein C, Friedman S L, Schuppan D,. Hepatic fibrosis: Concept to treatment [J]., 2015, 62(Suppl 1): S15-S24.
[24] 徐列明, 刘平, 沈锡中, 等. 肝纤维化中西医结合诊疗指南(2019年版) [J]. 中国中西医结合杂志, 2019, 39(11): 1286-1295.
[25] Rezaei N, Asadi-Lari M, Sheidaei A,. Liver cirrhosis mortality at national and provincial levels in Iran between 1990 and 2015: A Meta regression analysis [J]., 2019, 14(1): e0198449.
[26] Wang J H, Hung S J. Lichen planus associated with hepatitis B, hepatitis C, and liver cirrhosis in a nationwide cohort study [J]., 2021, 84(4): 1085-1086.
[27] Li X, Wang Z F, Wang L,. Liver cirrhosis: A risk factor for gallstone disease in chronic hepatitis C patients in China [J]., 2017, 96(26): e7427.
[28] 刘西忠, 赵凤华, 金庆香. 肝硬化低蛋白血症的研究进展 [J]. 中国中西医结合消化杂志, 2011, 19(1): 57-60.
[29] 喻松仁, 程绍民, 饶建波, 等. 中药抗肝损伤作用临床研究进展 [J]. 中医药临床杂志, 2008, 20(6): 634-637.
Clinical efficacy and safety of Wuji Baifeng Pills combined with antiviral treatment for chronic virus hepatitis and liver cirrhosis: A Meta-analysis
ZHOU Hong1, 2, JIANG Yong-ping3, CHEN Zhe4, QIANG Xiao-yu4, PENG Ying-ying5, 6, WANG Hui4
1. The Sixth Traditional Chinese Medicine Factory, Tianjin Pharmaceutical Da Ren Tang Group Corporation Ltd., Tianjin 300401, China 2. Tianjin Pharmaceutical Da Ren Tang Group Corporation Ltd., Tianjin 300193, China 3. Lerentang Pharmaceutical Factory, Tianjin Pharmaceutical Da Ren Tang Group Corporation Ltd., Tianjin 300380, China 4. Evidence-based Medicine Center, Tianjin University of Traditional Chinese Medicine,Tianjin 301617, China 5. The First Affiliated Hospital of Tianjin University of Traditional Chinese Medicine, Tianjin 300382, China 6. National Clinical Research Center for Chinese Medicine Acupuncture and Moxibustion, Tianjin 300382, China
To systematically evaluate the clinical efficacy and safety of Wuji Baifeng Pills (乌鸡白凤丸) combined with antiviral treatment for chronic hepatitis and liver cirrhosis.Seven Chinese and English databases, including China National Knowledge Infrastructure (CNKI), Wanfang Data, VIP, SinoMed, PubMed, Embase and Cochrane Library, were searched by computer. The type of literature searched was the randomized controlled trial of Wuji Baifeng Pills in the treatment of chronic hepatitis and liver cirrhosis. The retrieval time was from the establishment of the database to March 1, 2021. Double retrieval, double extraction and double evaluation were carried out by professionals, and RevMan 5.3 software was used for Meta-analysis.A total of 10 studies were included with 867 patients. The results of Meta-analysis showed that compared with antiviral drugs alone, Wuji Baifeng Pills combined with antiviral drugs could significantly improve the clinical response rate [RR = 1.32, 95%CI (1.15, 1.51),< 0.000 1], albumin [MD = 2.88, 95%CI (0.80, 4.97),= 0.007], alanine aminotransferase [MD = −28.49, 95%CI (−46.15, −10.83),= 0.002], aspartate aminotransferase [MD = −32.04, 95%CI (−49.40, −14.67),= 0.000 3], total bilirubin [MD = −19.10, 95%CI (−27.37, −10.84),< 0.000 01], hyaluronic acid [MD = −49.67, 95%CI (−76.59, −22.75),= 0.000 3], laminin [MD = −36.16, 95%CI (−56.32, −16.00),= 0.000 4], procollagen-Ⅲ-peptide [MD = −24.25, 95%CI (−48.43, −0.06),= 0.05], and collage type IV [MD = −21.06, 95%CI (−37.98, −4.14),= 0.01], with statistical differences. Better safety, but further research was needed to confirm.Wuji Baifeng Pills combined with antiviral therapy could effectively improve the clinical efficacy of chronic hepatitis and liver cirrhosis, which needs to be further verified by a large number of high-quality studies.
Wuji Baifeng Pills; chronic virus hepatitis; liver cirrhosis; randomized controlled trial; antiviral
R285.64
A
0253 - 2670(2022)23 - 7491 - 08
10.7501/j.issn.0253-2670.2022.23.020
2022-03-13
天津市青年拔尖人才计划项目(125Z15XSGC31);津教委“十三五”创新团队培养计划-中药临床评价方法(TD13-5047)
周 鸿,男,高级工程师,研究方向为中药研发。E-mail: tjzhouhong@163.com
通信作者:王 辉,女,副研究员,研究方向为中医药临床评价和循证医学研究。E-mail: wangh@tice.com.cn
[责任编辑 潘明佳]
