基于多成分质量控制的柴芍疏肝调神胶囊制备工艺研究
2022-12-08杨新荣李国峰宋沁洁李咸慰吴红伟李东辉辛二旦孙宇靖张育贵边甜甜李越峰
杨新荣,窦 霞,李国峰,宋沁洁,李咸慰,吴红伟,李东辉,辛二旦,孙宇靖,张育贵,边甜甜,李越峰*
基于多成分质量控制的柴芍疏肝调神胶囊制备工艺研究
杨新荣1, 2, 3,窦 霞3,李国峰1, 2,宋沁洁1, 2,李咸慰1, 2,吴红伟1, 2,李东辉1, 2,辛二旦3,孙宇靖1, 2,张育贵1, 2,边甜甜1, 2,李越峰1, 2*
1. 甘肃中医药大学,甘肃 兰州 730000 2. 甘肃省中药制药工艺工程研究中心,甘肃 兰州 730000 3. 甘肃中医药大学附属医院,甘肃 兰州 730000
以经典名方四逆散为基础加减得柴芍疏肝调神方,将其制备为柴芍疏肝调神胶囊(Chaishao Shugan Tiaoshen Capsules,CSTC),对其进行制备工艺优化和多成分质量控制研究。采用水提醇沉、湿法制粒、填充制备成CSTC。选取6种指标成分辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵的含量,以其综合评分为指标,严格考察料液比、提取次数、提取时间、药液相对密度、醇沉浓度、醇沉时间对水提醇沉精制工艺的影响。另以休止角、堆密度、成型率、吸湿率的综合得分为条件,筛选辅料种类、辅料比、药辅比、95%乙醇用量对成型工艺的影响。得到CSTC剂的最佳制备工艺为料液比1∶12,提取次数2次,提取时间69 min,药液相对密度1.15(50 ℃),醇沉乙醇体积分数为60%,醇沉时间36 h,辅料为糊精+微晶纤维素(3∶2),药辅比(1∶1),95%乙醇用量占药辅量的23%。优选的制备工艺,科学合理,可行性高,可以为CSTC及相关中药制剂的开发提供参考,为其质量控制评价提供依据。
四逆散;柴芍疏肝调神胶囊;标准胶囊;Box-Behnken响应面法;正交试验;制备工艺;质量控制;辛弗林;栀子苷;芍药苷;甘草苷;柚皮苷;甘草酸铵;休止角;堆密度;成型率;吸湿率
四逆散为“医圣”张仲景的经典名方,始记载于《伤寒论》少阴篇,由柴胡、枳实、芍药、炙甘草4味组成,具有透邪解郁、疏肝理脾之功效,适用于肝失疏泄引发的肝脾不和之症[1]。其组方精简、配伍严谨,是疏肝解郁首方[2]。现代研究发现,其在失眠[3]、焦虑[4]和抑郁[5]等精神障碍类疾病的治疗中有显著优势,且还具有一定的“安神”功效[6]。而本课题组前期大量研究和连续6年临床应用发现,由四逆散加味而成的柴芍疏肝调神方在防治失眠、焦虑和抑郁方面的效果要优于四逆散。全方由柴胡、白芍、枳实、栀子、炙甘草、制远志、酸枣仁、枸杞子、石决明9味药组成。方中柴胡疏肝解郁,白芍养血柔肝,二药相伍,补肝体而助肝用,共为君药;枸杞子,补肝阴而益肝体,增强白芍养血之作用,酸枣仁滋阴安神,既可助白芍以养肝血补肝体,又可宁心安神,远志宁心安神,一则与酸枣仁相伍以养心安神,一则防诸药滋腻之性共为臣药;枳实助柴胡理气解郁,一升一降,斡旋气机,栀子清热凉肝,一镇一清,使阳潜气平,肝得以正常疏泄,石决明重镇平肝,共为佐药;甘草调和诸药,补养中州,脾气健忘则肝木不得横逆,为使药;诸药相伍,共奏疏肝理气,宁心调神,清热除烦之功。全方具有疏肝理气,宁心调神,清热除烦的功效,用于胸胁胀满疼痛,心烦易怒,失眠多梦、头痛、失眠、焦虑、抑郁等症的治疗。
经典名方是我国中医药领域的宝藏,自国家《古代经典名方目录》颁布以来,有关其物质基准和制剂开发的研究备受青睐[7]。因此,结合6种指标成分辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵含量的综合得分变化,考察料液比、提取次数、提取时间、药液相对密度、醇沉浓度、醇沉时间、休止角、堆密度、成型率、吸湿率对柴芍疏肝调神胶囊(Chaishao Shugan Tiaoshen Capsules,CSTC)的影响,进一步筛选出CSTC最佳制备工艺,以期为今后CSTC剂及其相关制剂的研究提供参考。
1 仪器与材料
1.1 仪器
Agilent 1260型高效液相色谱仪,美国安捷伦公司公司;BT125D型十万分之一天平,赛多利斯科学仪器有限公司;PL-S60型超声波清洗器,东莞康士洁超声波科技有限公司;L2-5K型台式低俗离心机,湖南可成仪器设备有限公司;DHG-9123A型电热鼓风干燥箱,上海一恒科学仪有限公司;FLP- 500A高速多功能摇摆粉碎机,上海菲力博实业公司;标准检验筛,10、18、20、80、100目,浙江上虞市金鼎标准筛具厂;0#100孔胶囊板胶囊灌装板,浙江诚挚精密机械有限公司。
1.2 材料
1.2.1 对照品 辛弗林(批号PS000966)、栀子苷(批号PS001144)、芍药苷(批号PS000826)、甘草苷(批号PS012028)、柚皮苷(批号PS001114)、甘草酸铵(批号PS011584)均购自成都普思生物科技股份有限公司,所有对照品质量分数均≥98%。
1.2.2 试剂 甲醇(色谱纯,批号20210515,体积分数≥99.9%)、乙腈(色谱纯,批号20210515,体积分数≥99.9%)、异丙醇(色谱纯,批号20200815,体积分数≥99.8%)、无水乙醇(分析纯,批号20210301,体积分数≥99.7%)均购自天津市大茂化学试剂厂;磷酸水(分析纯,批号20150707,体积分数≥85%),天津市科密欧化学试剂有限公司;水为娃哈哈饮用纯净水。糊精(批号20190301)和可溶性淀粉(分析纯,批号20200901)均为天津市大茂化学试剂厂;微晶纤维素(批号20210916)厂家为湖南新绿方药业有限公司;磷酸氢钙(批号20180601,质量分数≥98%)厂家为天津市光复精细化工研究所;0号胶囊,浙江省浦江县恩尔康胶囊有限公司。
1.2.3 药材 实验用CSTC的9味饮片如下:柴胡为伞形科柴胡属植物柴胡DC.的干燥根、白芍为毛茛科芍药属植物芍药Pall.的干燥根、枸杞子为茄科枸杞属植物宁夏枸杞L.的干燥成熟果实、酸枣仁为鼠李科枣属植物酸枣Mill. var.(Bunge) Hu ex H. F. Chou的干燥成熟种子、远志为远志科远志属植物远志Willd.的干燥根、枳实为芸香科柑橘属植物酸橙L.及其栽培变种的干燥未成熟果实、栀子为茜草科栀子属植物栀子Ellis的干燥成熟果实、石决明为鲍科鲍属动物杂色鲍Reeve的贝壳、炙甘草为豆科甘草属植物甘草Fisch.的干燥根和根茎,均为市售饮片,购自兰州惠仁堂药房,具体信息见表1,经甘肃中医药大学药学院王明伟副教授鉴定,均符合《中国药典》2020年版要求。
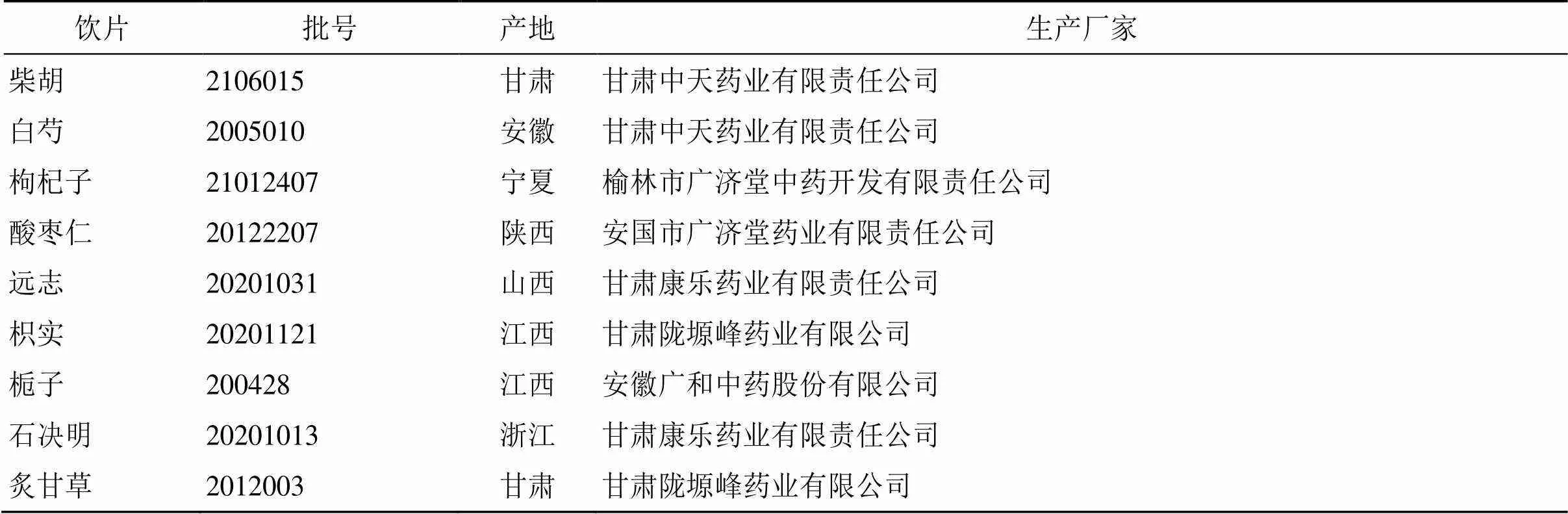
表1 CSTC所用饮片来源信息
2 方法与结果
2.1 标准胶囊剂的制备
分别按处方取白芍、枸杞子、酸枣仁、远志、枳实、栀子、石决明、炙甘草适量开展预实验。以料液比(1∶10)、提取次数(1次)、提取时间(60 min)、药液相对密度(1.15)、醇沉乙醇体积分数(50%)、醇沉时间(12 h),获得干浸膏。将所得干浸膏与适量柴胡一起混合粉碎,过100目筛(6号筛),根据辅料种类为糊精+微晶纤维素(1∶1)、药物与辅料比(1∶1)、95%乙醇用量占药辅量20%的预实验条件制粒,低温干燥(50 ℃),18目整粒,填充0号胶囊得到CSTC标准胶囊剂(0.25 g/粒)。
2.2 多指标含量测定方法学考察
2.2.1 对照品溶液的制备 取辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵对照品适量,精密称定,置于10 mL量瓶中,加入甲醇定容,制成质量浓度分别为30.75、69.00、97.75、19.50、163.25、49.00 μg/mL的混合对照品溶液。
2.2.2 供试品溶液制备 根据胶囊载药量及预实验结果,取“2.1”项下制备的CSTC内容物2 g,将其置于50 mL量瓶内,加甲醇定容,超声溶解30 min(功率200 W,频率40 kHz),混匀,4000 r/min离心15 min(离心半径140 mm),取上清液,即为CSTC供试品溶液。
2.2.3 色谱条件 色谱柱为Agilent Technologies 1260 Infinity C18柱(250 mm×4.6 mm,5 μm),流动相为甲醇-0.05%磷酸水溶液,最佳梯度洗脱:0~5 min,2%~8%甲醇;5~12 min,8%~22%甲醇;12~40 min,22%~50%甲醇;40~50 min,50%~65%甲醇;50~62 min,65%~85%甲醇;62~72 min,85%~95%甲醇;72~86 min,95%~100%甲醇;体积流量0.8 mL/min;检测波长228 nm;柱温30 ℃;进样量10 μL。在此条件下供试品溶液中的辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵与其他成分分离良好,色谱图见图1。
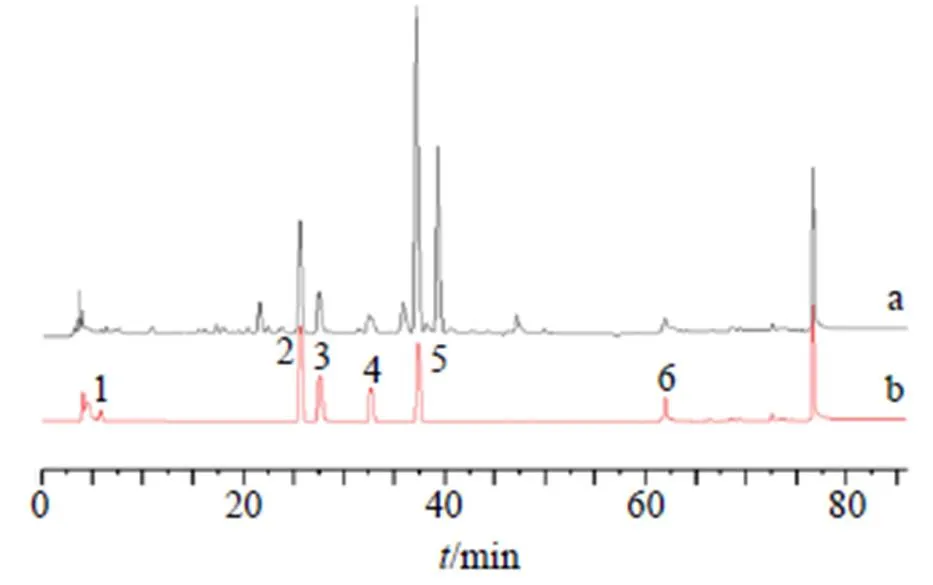
1-辛弗林 2-栀子苷 3-芍药苷 4-甘草苷 5-柚皮苷 6-甘草酸铵
2.2.4 线性关系考察 精密吸取混合对照品溶液,制成6个不同质量浓度的系列对照品溶液,按照“2.2.3”项下色谱条件进行测定,并记录色谱峰面积。以峰面积为纵坐标(),对照品质量浓度为横坐标(),绘制标准曲线,并进行线性回归,得6个指标成分的线性回归方程分别为辛弗林=3.978 4-1.251 7,=0.999 8,线性范围3.84~123.0 μg/mL;栀子苷=12.86+60.759,=0.999 8,线性范围8.63~276.0 μg/mL;芍药苷=16.251+40.269,=0.999 9,线性范围12.23~211.7 μg/mL;甘草苷=34.703+46.504,=0.999 8,线性范围2.44~78.0 μg/mL;柚皮苷=23.451+265.18,= 0.999 9,线性范围20.41~653.00 μg/mL;甘草酸铵=7.209 2+87.834,=0.999 8,线性范围6.13~196.0 μg/mL。
2.2.5 精密度试验 取同一批CSTC样品,按“2.2.2”项下方法制备供试品溶液,在“2.2.3”项色谱条件下连续进样6次,记录峰面积,测得辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵峰面积的RSD分别为2.92%、1.96%、2.63%、1.30%、0.96%、1.60%,表明仪器精密度良好。
2.2.6 稳定性试验 取同一批CSTC供试品溶液,按“2.2.3”项下色谱条件,分别于制备后0、2、4、6、8、12、24 h进样测定,记录峰面积,测得辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵峰面积的RSD分别为2.75%、0.89%、2.03%、1.56%、0.67%、2.37%,表明供试品溶液在24 h内稳定性良好。
2.2.7 重复性试验 取同一批CSTC样品,按照“2.2.2”项下方法平行制备供试品溶液6份,在“2.2.3”项色谱条件下进样分析,记录峰面积并计算各成分质量分数,测得辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵质量分数的RSD分别为2.13%、1.44%、2.08%、1.99%、1.55%、1.80%,表明该方法重复性良好。
2.2.8 加样回收率试验 取同一批CSTC样品(S1)内容物1 g,平行6份,分别加入“2.2.1”项下的混合对照品溶液5 mL,按“2.2.2”项下方法制备供试品溶液,在“2.2.3”项色谱条件下进样分析,记录峰面积并计算各成分的质量分数及其加样回收率,测得辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵的平均加样回收率分别为99.50%、100.29%、100.56%、99.78%、99.55%、99.69%,RSD分别为1.71%、1.37%、1.67%、2.85%、1.15%、2.47%,表明所建立含量测定方法准确度良好。
2.2.9 样品测定 取同一批CSTC样品,按照“2.2.2”项下方法平行制备供试品溶液,在“2.2.3”项下色谱条件进样测定,计算辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵的质量分数依次为0.51、9.24、5.24、0.92、8.97、4.13 mg/g。
2.3 水提工艺研究
2.3.1 综合评分计算 熵权法是根据各项指标值的变异程度来确定指标权数的客观赋权法,其熵值越小,提供的信息量就越大,其在综合评价中所起的作用也越大,即所占权重就越大。其具体算法如下所示。
①用公式(1)对数据进行标准化处理。
X′=(X-min)/(max-min) (1)
X′为各个指标的标准化数据,X为第个指标下第组的含量,min为每个指标下测得的含量最小值,max为每个指标下测得的含量最大值
②再用公式(2)、(3)、(4)计算各指标的信息熵(E)。
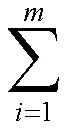
=1/ln(3)
E=−PlnP(4)
P为第个指标下第组的概率,且0≤P≤1,为样本数对数的倒数,为实验中的样本数
③最后用公式(5)计算权重系数(W)。
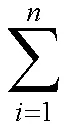
本实验结合熵权法最终测得辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵的权重系数分别为0.227、0.108、0.170、0.128、0.184、0.182。
综合评分()=辛弗林质量分数×0.227+栀子苷质量分数×0.108+芍药苷质量分数×0.170+甘草苷质量分数×0.128+柚皮苷质量分数×0.184+甘草酸铵质量分数×0.182
2.3.2 料液比考察 按处方配比取所需饮片适量,以提取次数(1次)、提取时间(60 min)为固定量,考察不同料液比对辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵质量分数的影响,结果见表2。结合综合评分法优选得最佳料液比为1∶10。
2.3.3 提取次数考察 按处方配比取所需饮片适量,以提取时间(60 min)、料液比(1∶10)为固定量,考察不同提取次数对辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵质量分数的影响结果见表3。结合综合评分法优选得最佳提取次数为2次。
2.3.4 提取时间考察 按处方配比取所需饮片适量,以料液比(1∶10)、提取次数(2次)为固定量,考察不同提取时间下,辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵的质量分数变化,结果见表4。结合综合评分法优选得最佳提取时间为60 min。
2.3.5 Box-Behnken设计-响应面法优化最佳水提工艺 在以上考察试验的基础上,分别选取料液比(1)、提取次数(2)、提取时间(3)作为自变量,采用Design Expert 8.0.6软件中的Box-Behnken响应面试验设计方法,以辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵质量分数为因变量,依据其综合评分优选最佳水提取工艺参数[10],因素水平及试验设计与结果见表5。
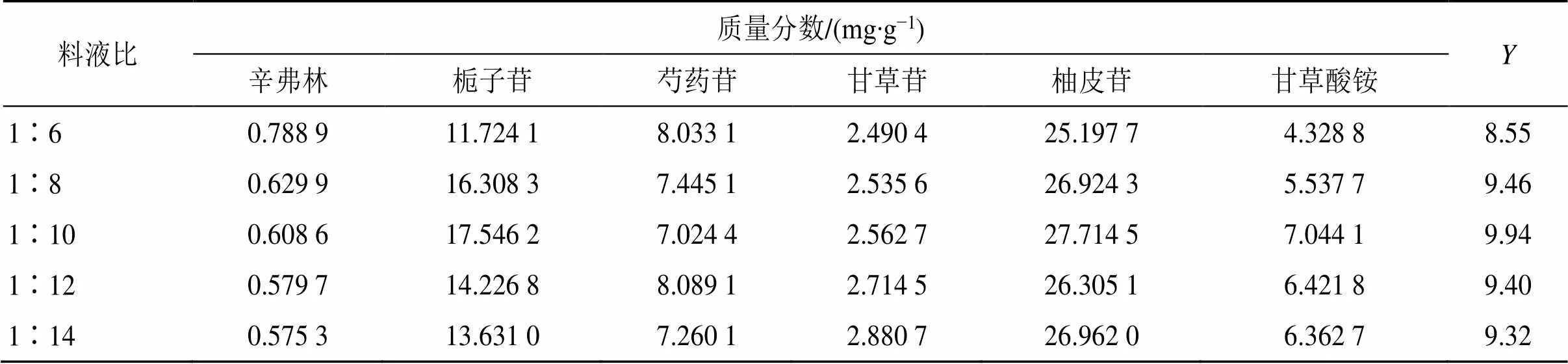
表2 不同料液比对6种指标成分及Y的影响
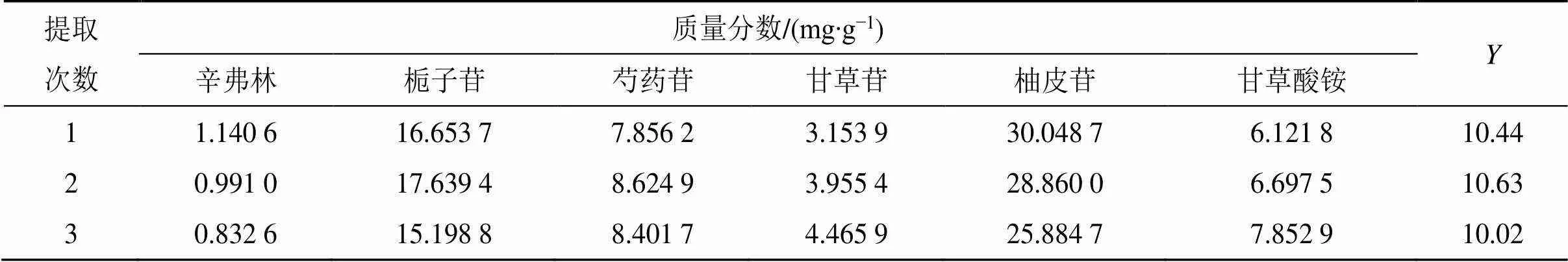
表3 不同提取次数对6种指标成分及Y的影响
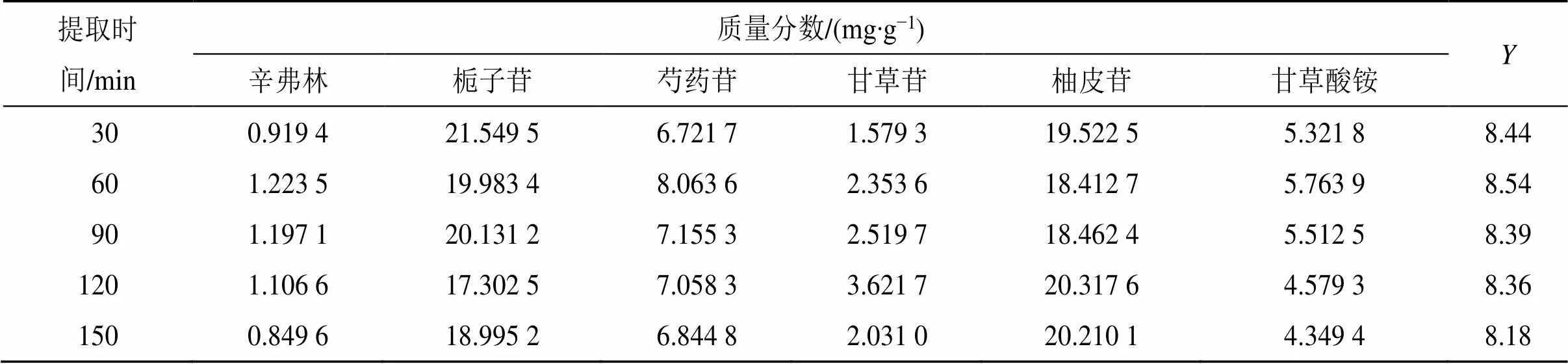
表4 不同提取时间对6种指标成分及Y的影响
对表中实验数据进行多元线性和非线性回归分析,得到综合评分()对料液比(1)、提取次数(2)和提取时间(3)的2次回归模型方程:=10.04+0.281 31+0.555 02+0.586 33+0.5512-0.077 513+0.4123-1.0712-0.691 322-0.893 732。模型=54.21,<0.000 1,失拟项>0.05不显著,表明该模型具有较高的可靠性,相关系数()=0.992 9,校正系数(adj)=0.983 7,变异系数(CV)=2.25%,模型信噪比=19.167 1>4,表明该模型拟合度良好,试验误差小,可用此模型对综合评分进行分析和预测[11]。
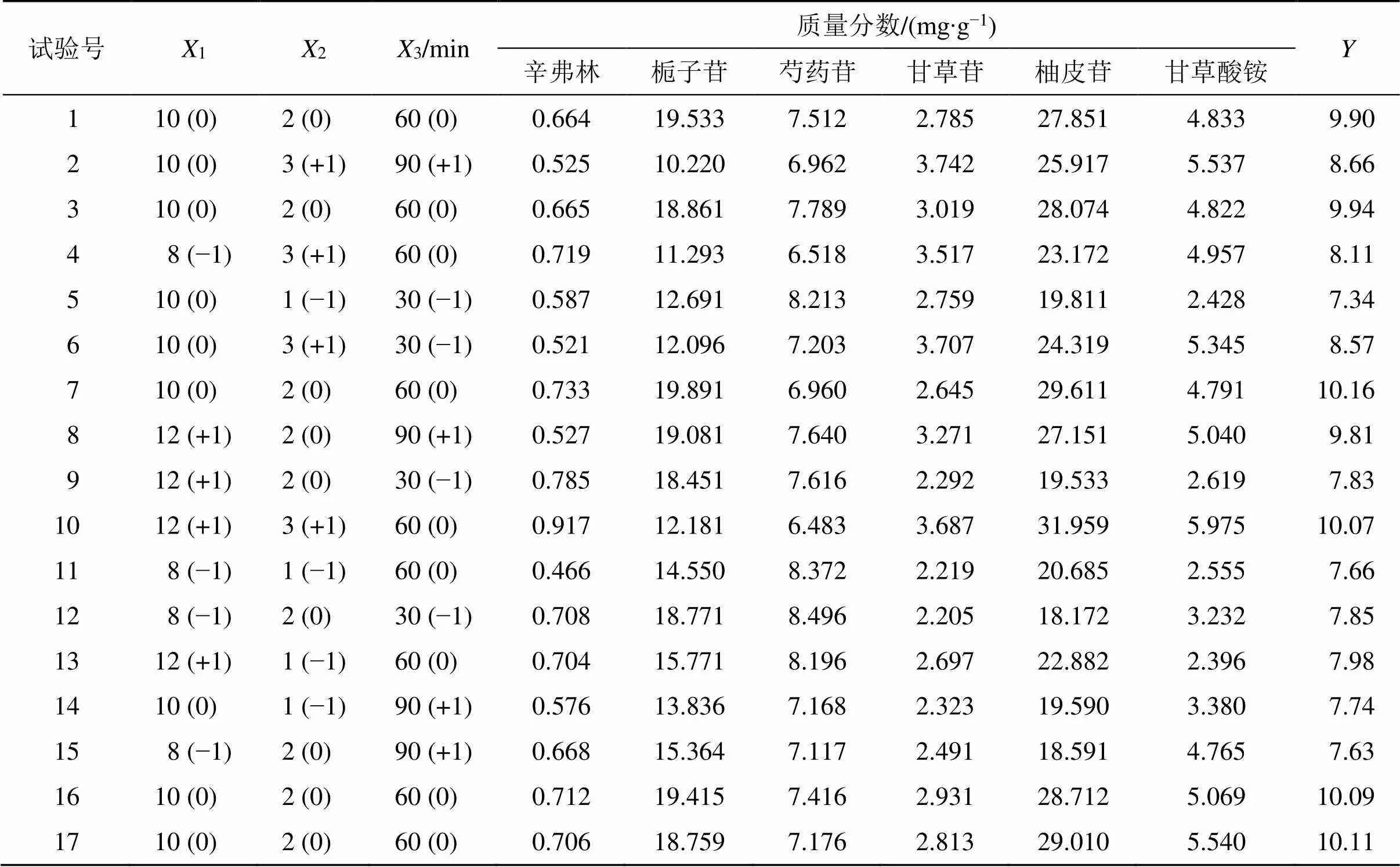
表5 Box-Behnken设计-响应面法试验设计与结果
方差分析结果见表6,自变量1次项2、3,2次项12、32极显著(<0.001),1次项1、2次项22、交互项12、23显著(<0.01);表明1和2、2和3之间有交互作用、模型具有统计学意义,各因素对值的影响顺序为提取时间(3)>提取次数(2)>料液比(1)。
此外,结合回归方程所绘制所得各因素交互作用的响应面及等高线图发现,等高线图呈椭圆型表示2因素交互作用较强,圆形则表示交互作用较弱;响应面图越陡峭则2因素交互作用越强,反之,则越弱,具体见图2。由Design Expert 8.0.6软件预测最佳水提取工艺为料液比11.30、提取次数2.47次、提取时间68.44 min,综合评分为10.39分。
2.3.6 模型验证试验 结合实际生产情况,可将最佳水提取优选工艺参数调整为料液比(1∶12)、提取次数2次、提取时间69 min,并按照此工艺进行3批次验证实验,结果见表7,得其综合评分平均值为10.20,RSD为0.54%,与预测值(10.39)较接近,表明该优化水提取工艺稳定、重复性好、可操作性强。
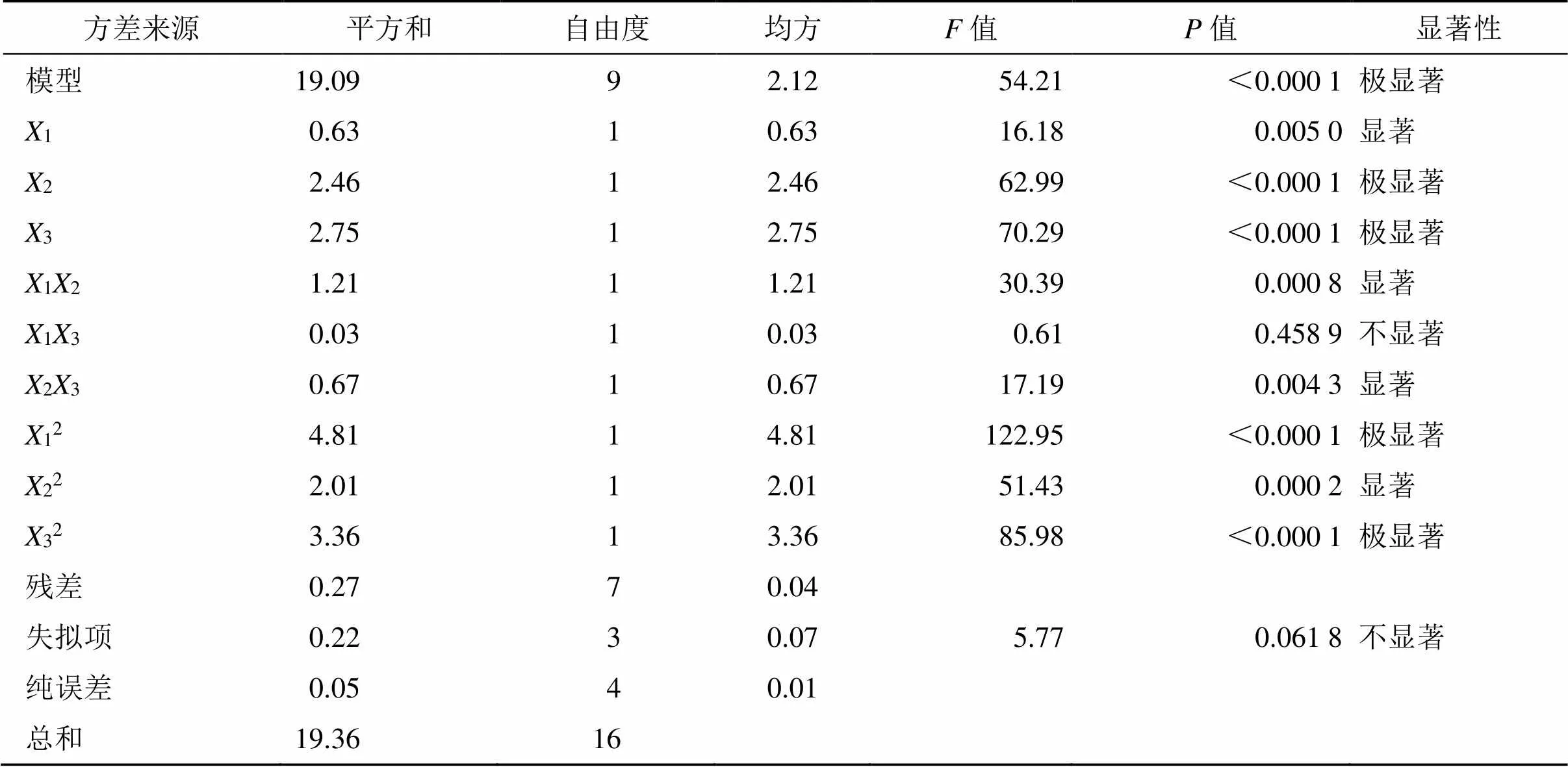
表6 方差分析结果
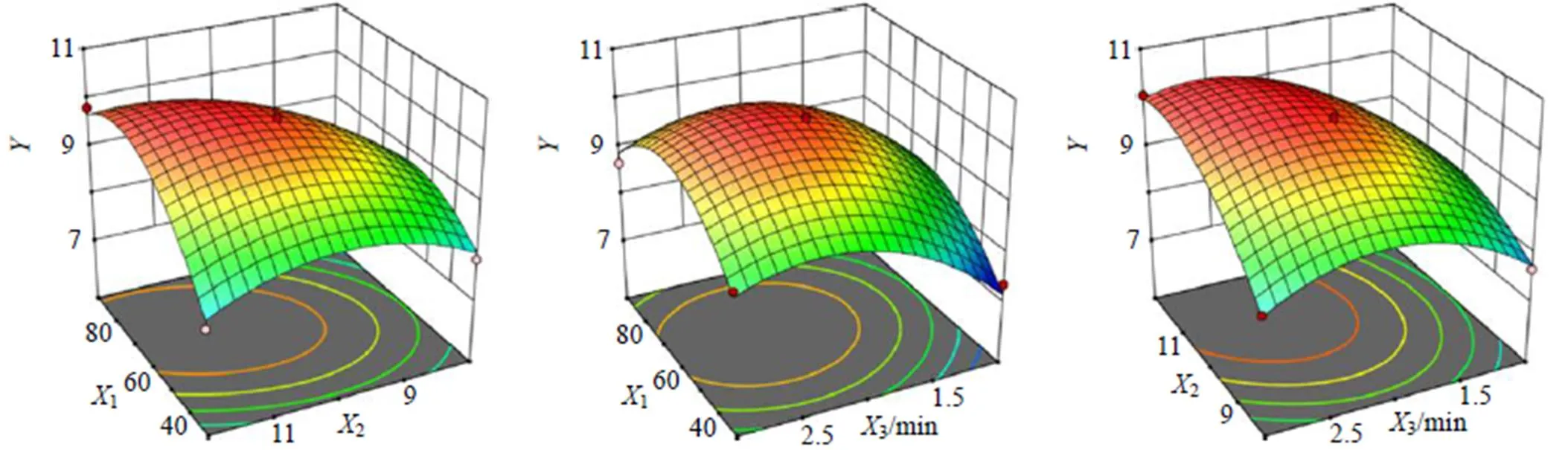
图2 各因素交互作用对CSTC水提取工艺综合评分的响应面和等高线
2.4 醇沉淀精制工艺研究
因中药水提液杂质较多,为减少患者服用量,提高制剂稳定性,则进行醇沉精制工艺优化。根据以上所得的最佳水提取工艺参数,连续提取3次,合并药液,4000 r/min离心15 min,取上清液。分别以药液相对密度、醇沉乙醇体积分数和醇沉时间作为考察因素、同时以各指标成分综合评分(,权重系数0.85)及干膏得率(权重系数0.15)作评价指标对醇沉精制工艺作综合评分(),=/max× 85+干膏得率min/干膏得率×15[12]。的具体算法同“2.3.1”项。
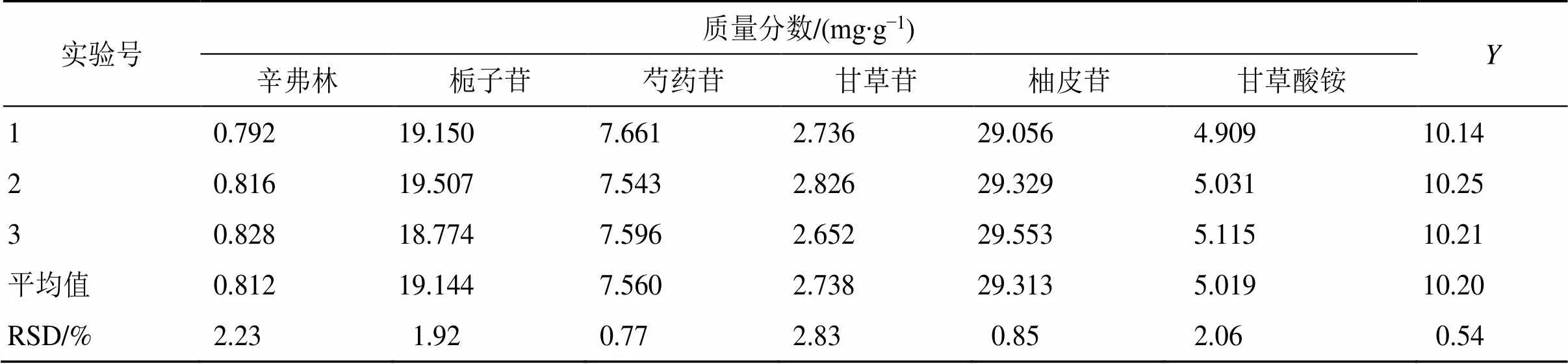
表7 验证试验结果(n = 3)
2.4.1 药液相对密度考察 取“2.3.6”项下所得药液100 mL,以醇沉乙醇体积分数(50%)、醇沉时间(12 h)为固定量,考察不同药液相对密度条件下辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵的质量分数,结果见表8。结合综合评分法优选得最佳药液相对密度为1.15。
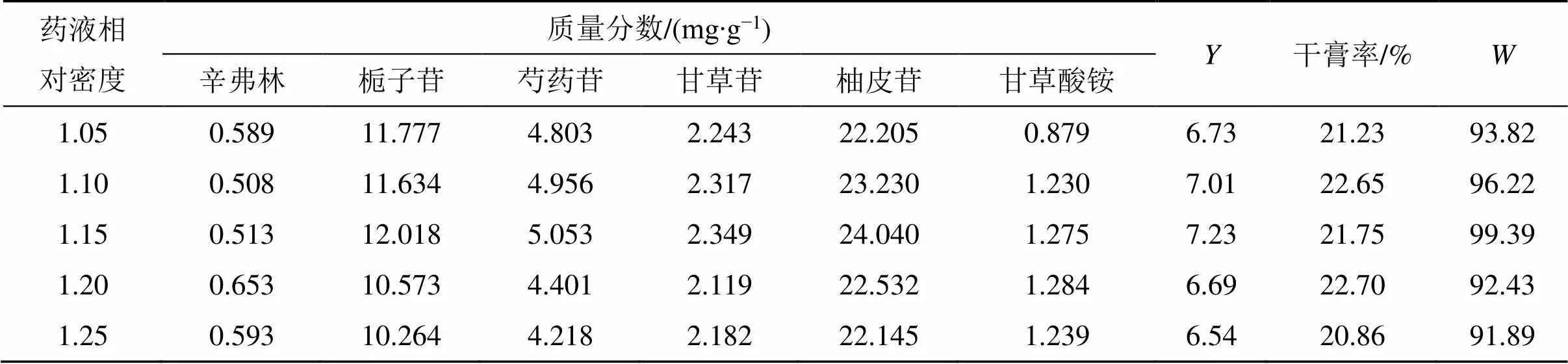
表8 不同药液相对密度对各考察指标的影响
2.4.2 乙醇体积分数考察 取“2.3.6”项下所得药液100 mL,以醇沉时间(12 h)、药液相对密度(1.15)为固定量,考察不同乙醇体积分数条件下辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵的质量分数,结果见表9。结合综合评分法优选得最佳乙醇体积分数为60%。
2.4.3 醇沉时间考察 取“2.3.6”项下所得药液100 mL,以药液相对密度(1.15)、乙醇体积分(60%)为固定量,考察不同醇沉时间条件下辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵的质量分数,结果见表10。并结合综合评分法优选得最佳醇沉时间是24 h。
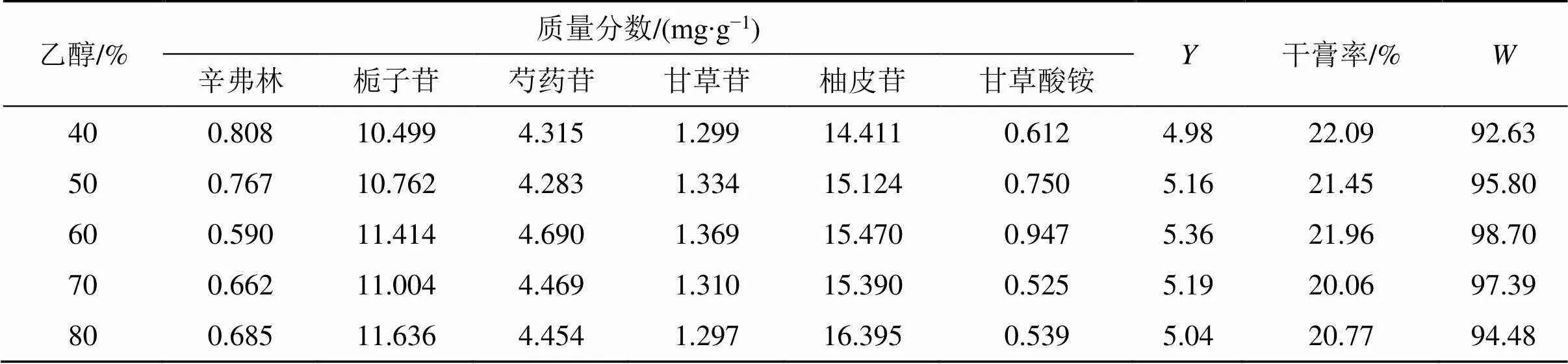
表9 不同乙醇体积分数对各考察指标的影响
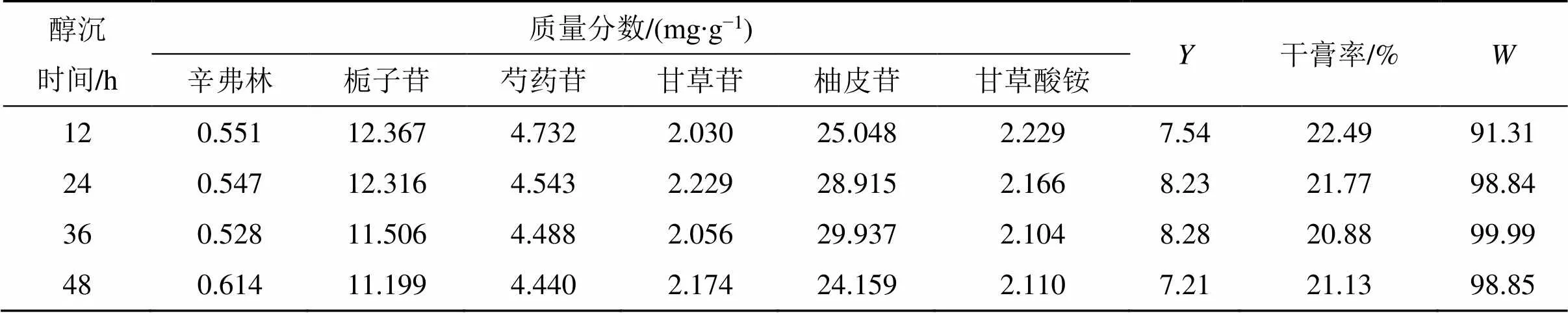
表10 不同醇沉时间对各考察指标的影响
2.4.4 醇沉精制正交试验设计 在以上醇沉单因素考察试验的基础上,分别选取药液相对密度(A)、醇沉乙醇体积分数(B)、醇沉静置时间(C)作为自变量,采用SPSS 25正交试验设计方法,以辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵质量分数为评价指标,依据其综合得分(),采用L9(34)表进行正交试验,优选出最佳的醇沉精制工艺[13]。因素水平及试验设计与结果见表11。
由正交试验直观分析表明,3个主要因素对CSTC醇沉精制工艺的影响程度依次是C(醇沉静置时间)>A(药液相对密度)>B(乙醇体积分数),各因素不同水平程度依次是A3>A2>A1、B2>B3>B1、C3>C2>C1,再通过方差分析(表12)进一步分析,C(醇沉静置时间)对醇沉精制环节的影响有统计学意义(<0.05)。而A(药液相对密度)和B(乙醇体积分数)对醇沉精制环节的影响没有统计学意义(>0.05)。综合评分表明最佳水提工艺为A2B2C3,即药液相对密度1.15,乙醇体积分数60%,醇沉静置时间36 h。
2.4.5 验证试验 结合实际操作,根据拟合的最优条件,可将最佳醇沉工艺参数调整为药液相对密度1.15、乙醇体积分数60%、醇沉静置时间36 h。并据此条件进行3次验证实验,结果见表13。得其综合评分平均值为98.69,RSD为1.11%,与预测值(98.88)较接近,表明该醇沉精制工艺质量稳定、重现性好、可操作性强。
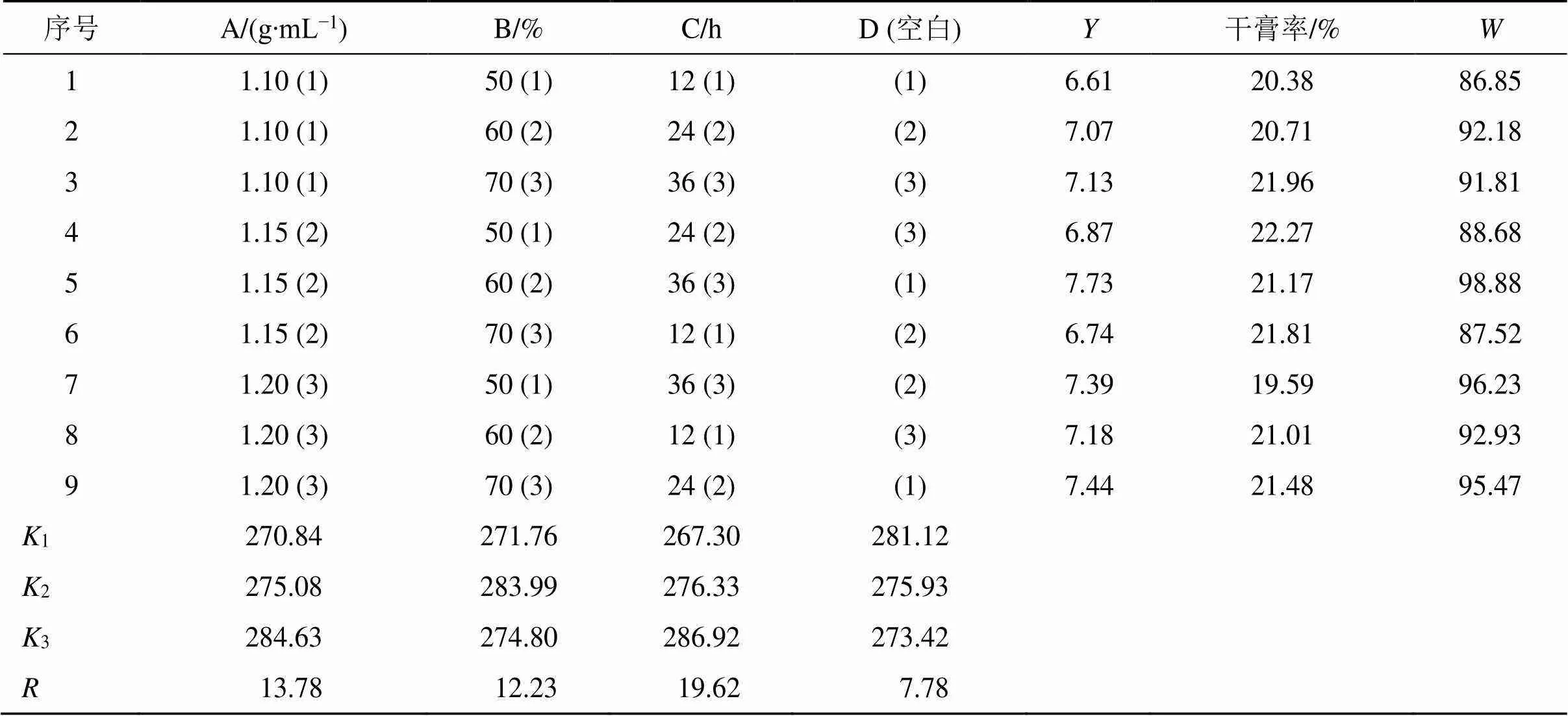
表11 醇沉精制工艺L9(34)正交试验设计与结果
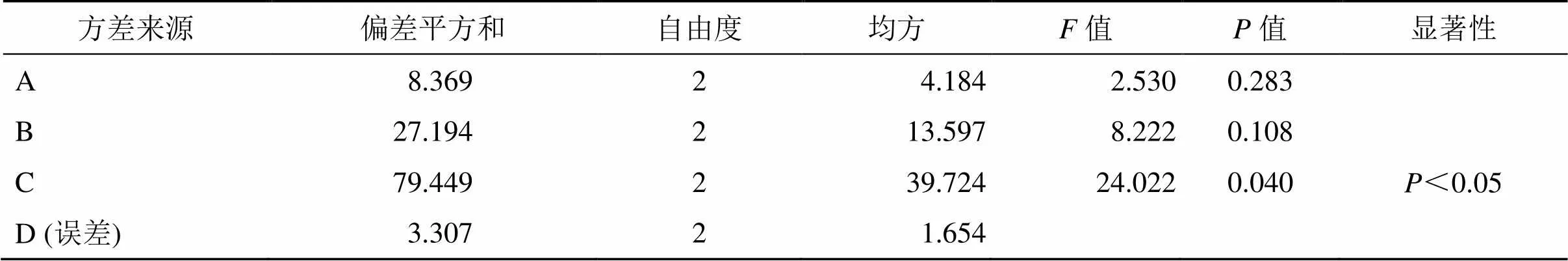
表12 醇沉精制工艺方差分析结果
0.05(2, 2) = 19.000.01(2, 2) = 99.00
2.5 CSTC中颗粒剂成型工艺考察
2.5.1 CSTC中颗粒剂的制备 取柴胡饮片适量,低温干燥(50 ℃),与“2.4.5”项下所得干浸膏一起粉碎,过100目筛(6号筛)。取适量细粉进行粉体学考察,采用固定漏斗法[14],平行测定3次,得其平均休止角为42.30°。表明其流动性较差,不适合直接装胶囊,故应加入辅料制成相应颗粒以增加其流动性。
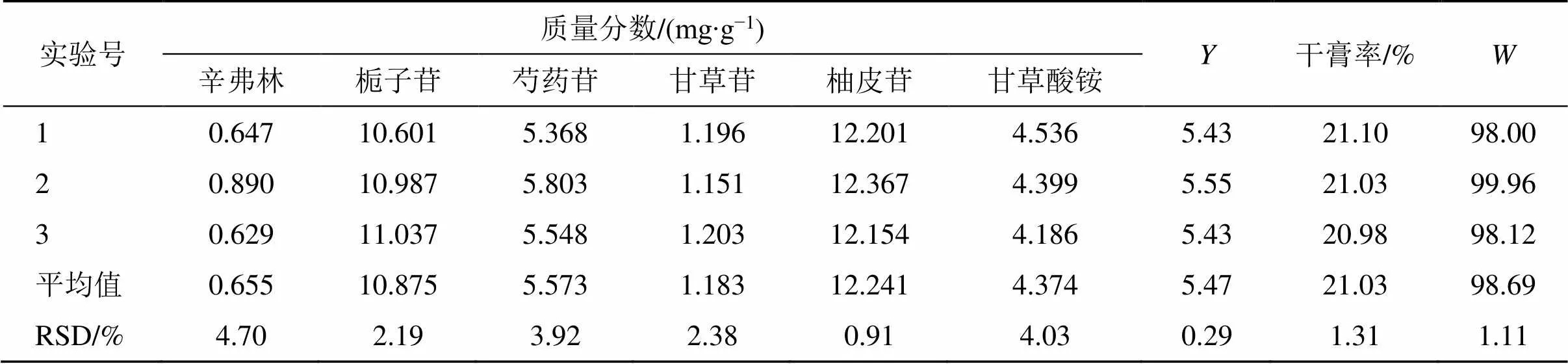
表13 L9(34)正交实验优化法的验证(n = 3)
2.5.2 润湿剂的考察 取“2.5.1”项下细粉适量,以不同体积分数的乙醇做润湿剂,考察其制软材的情况,结果见表14,由结果知选择95%乙醇作润湿剂、制软材较好。
2.5.3 辅料种类的考察 辅料决定了胶囊内容物颗粒的吸湿性、流动性和成型性。据文献报道中药制剂中常用的辅料有:可溶性淀粉、微晶纤维素、糊精、微粉硅胶、磷酸钙、磷酸氢钙、磷酸二氢钙等[15],而胶囊剂常用辅料以微晶纤维素、糊精、磷酸氢钙和可溶性淀粉居多[16]。
因此,结合前期预实验结果,取“2.5.1”项下细粉适量,先以药辅比1∶1、95%乙醇用量占药辅量的20%作基本条件,进行辅料种类的筛选。并以休止角[14]、堆密度[17]、成型率[18]、吸湿率[19]为考察指标,进行胶囊内容物颗粒的综合评价,得到最佳辅料种类为糊精+微晶纤维素(1∶1)。综合评分()=最小休止角×20/休止角+20/最大堆密度×堆密度+25/最大成型率×成型率+最小吸湿率×35/吸湿率[18]。结果见表15。

表14 润湿剂(乙醇)体积分数的考察
2.5.4 95%乙醇用量优化 取“2.5.1”项下细粉适量,依据“2.5.3”项下所得最佳辅料种类条件,按药辅比为1∶1,考察不同95%乙醇用量条件下休止角、堆密度、成型率、吸湿率的变化,结果见表16。结合综合评分法优选得最佳95%乙醇用量占药辅料总量的23%。
2.5.5 辅料配比优化 取“2.5.1”项下细粉适量,依据“2.5.3”项和“2.5.4”项下所得最佳条件,按药辅比为1∶1,考察不同辅料配比条件下休止角、堆密度、成型率、吸湿率的变化,结果见表17。结合综合评分法优选得最佳辅料配比为“糊精-微晶纤维素(3∶2)”。
2.5.6 药物与辅料配比优化 取“2.5.1”项下细粉适量,依据“2.5.3”“2.5.4”项和“2.5.5”项下所得最佳条件,以休止角、堆密度、成型率、吸湿率的变化为指标,考察药物与辅料配比对颗粒剂成型的影响,结果见表18。结合综合评分法优选得最佳药辅配比为1∶1。
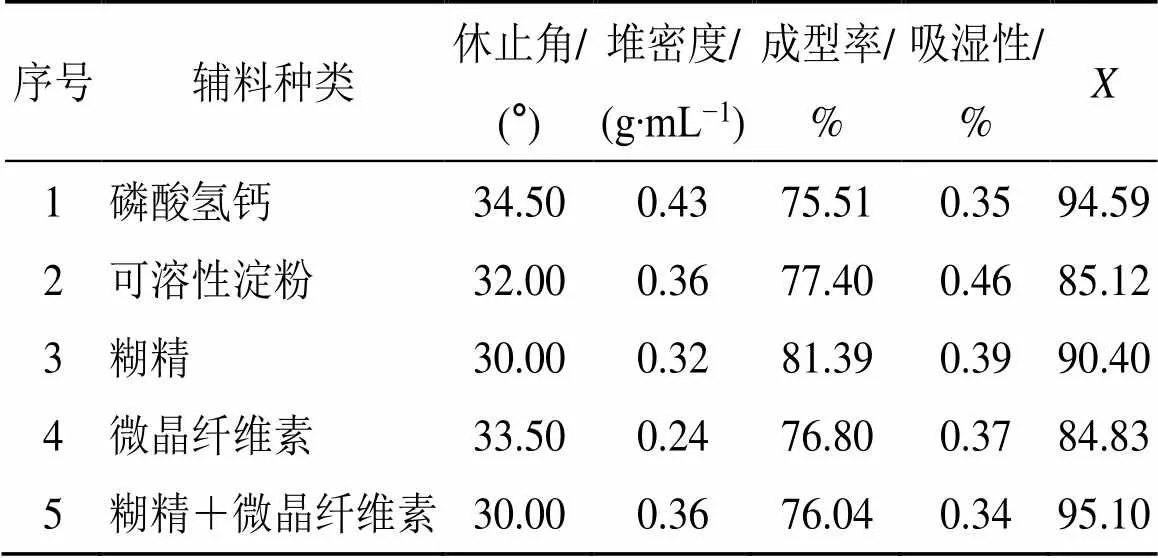
表15 辅料种类筛选结果显示
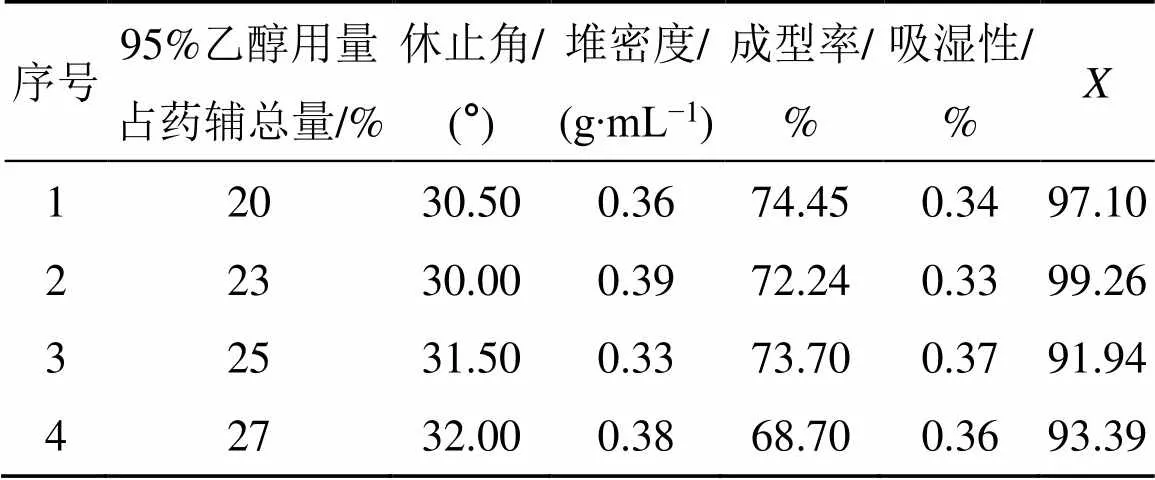
表16 95%乙醇用量优化结果显示

表17 辅料配比优化结果显示
2.5.7 成型工艺验证 结合实际操作,为进一步验证所选成型最佳工艺,根据拟合的最优条件,得到最佳成形工艺参数为95%乙醇用量占药辅总量的23%、糊精与微晶纤维素比例为3∶2、药物与辅料比例为1∶1。据此条件进行3次验证实验,结果见表19,得其综合评分分别为98.53、98.40和99.83,平均值为98.20,RSD为0.79%,表明该成型工艺稳定、可靠,符合大生产要求。
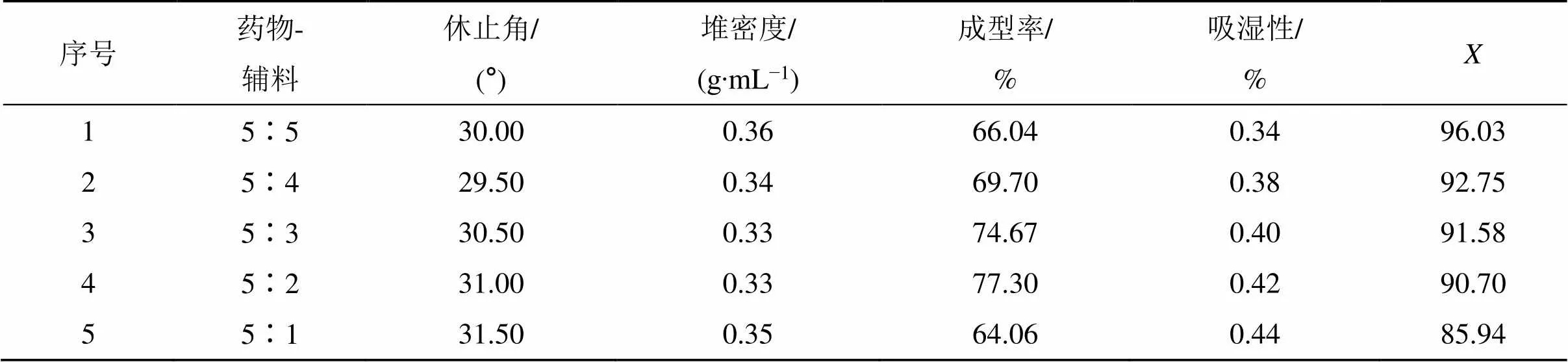
表18 药辅配比优化结果显示
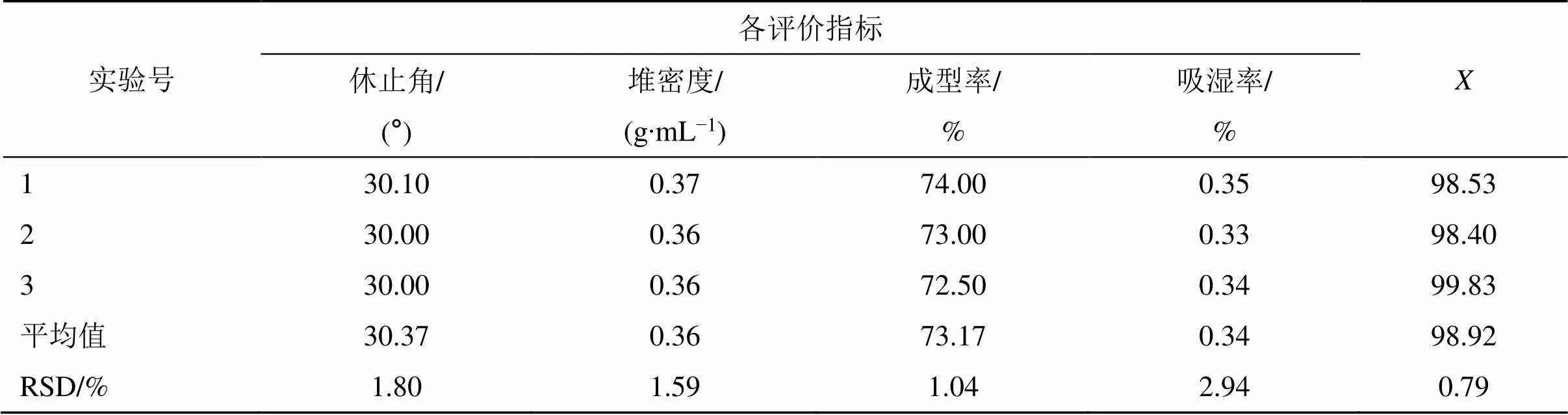
表19 成型工艺验证优化法的实验验证(n = 3)
3 讨论
本方由四逆散基础方加味而来,由9味中药组成、方中化学成分复杂、且各个成分的最大吸收波长不一,为了尽可能使各成分的色谱峰基本分离,前期预实验分别考察了在水-甲醇、水-乙腈、0.05%磷酸水溶液-乙腈以及0.05%磷酸水溶液-甲醇4种流动相体系下各成分的色谱峰分离情况,最终优化得0.05%磷酸水溶液-甲醇为最佳流动相。并结合预实验所得色谱峰的基线、峰形、峰数、指标成分分离度及响应值等因素,最终选择228 nm为该方各成分的最佳吸收波长。
由于复方制剂的药效取决于方中多种成分的配伍增效作用。因此,在水提取工艺的优化中,采用熵权法客观赋予6中指标成分权重系数,分别为辛弗林(0.227)、栀子苷(0.108)、芍药苷(0.170)、甘草苷(0.128)、柚皮苷(0.184)和甘草酸铵(0.182)。在醇沉精制工艺筛选中,为尽可能保留药效成分,除去无效成分,则希望干膏率越小越好,所以结合相关文献[12],本环节干膏率评分的权重系数占0.15,6种指标成分综合评分的权重系数占0.85。在成型工艺中,为了控制胶囊内容物吸湿性、流动性和成型性,保证胶囊确质量,希望所得颗粒得休止角、吸湿性越小越好,而堆密度和成型率则是越大越好。因此结合实际实验情况,分别设休止角、堆密度二者的权重系数各占0.20、成型率权重系数占0.25、吸湿率权重系数占0.35。
在整个制备工艺环节中,就单因素提取次数考察环节中,虽结合综合评分法优选得最佳提取次数是2次,但在企业的实际生产中,结合成本等因素,选择1次是可以的。另外就实验优化选择95%乙醇作润湿剂、制软材的结果,在实际生产应用中,结合药品质量与用药安全问题,可以做出调整,具体数据应该以实际操作中的质量检验为准则。此外,为了有效监测CSTC在整个制备环节中各成分的稳定性、重复性,明确含量变化,确保胶囊质量,以6种指标成分辛弗林、栀子苷、芍药苷、甘草苷、柚皮苷和甘草酸铵的出峰情况作为质量控制条件。发现提取环节6种指标成分质量分数综合评分的RSD为0.43%。醇沉精制除杂环节6种指标成分质量分数综合评分的RSD为0.27%。成型环节4种考察指标(休止角、堆密度、成型率、吸湿率)指标成分质量分数综合评分的RSD为0.79%。表明实验涉及制备工艺考察科学合理、工艺参数稳定、重复性好、可操作性强,胶囊质量有一定保证。综上,本实验基于多指标定量的制备工艺及质量控制研究,能够比较全面地对该胶囊剂进行质量控制与评价,可以为CSTC质量控制评价提供参考依据。
利益冲突 所有作者均声明不存在利益冲突
[1] 孙志明, 李小娜. 四逆散复方的研究进展 [J]. 现代中西医结合杂志, 2011, 20(25): 3244-3246.
[2] 张福华. 四逆散及其类方的研究 [D].济南: 山东中医药大学, 2005.
[3] 李越峰, 徐富菊, 张泽国, 等. 四逆散对大鼠睡眠时相影响的实验研究 [J]. 中国临床药理学杂志, 2014, 30(10): 936-938.
[4] 侯磊, 李晓宇, 黄娜娜, 等. 四逆散干预焦虑症作用机制的网络药理学分析 [J]. 中草药, 2019, 50(21): 5154-5161.
[5] 宗阳, 陈婷, 董宏利, 等. 基于网络药理学四逆散治疗抑郁症的作用机制探讨 [J]. 中草药, 2019, 50(20): 4995-5002.
[6] 张育贵, 张淑娟, 牛江涛, 等. 四逆散镇静催眠作用研究进展及其新药开发的策略分析 [J]. 中草药, 2020, 51(13): 3575-3584.
[7] 国家药品监督管理局. 古代经典名方中药复方制剂简化注册审批管理规定 [S]. 2018.
[8] 陈健, 张越, 崔小兵, 等. 基于多成分质量控制的温经汤制备工艺研究 [J]. 中草药, 2021, 52(2): 404-412.
[9] 任伟光, 吴玉林, 林兰, 等. 糖心平方水提醇沉的工艺研究 [J]. 时珍国医国药, 2019, 30(8): 1876-1878.
[10] 吴红伟, 李东辉, 边甜甜, 等. 基于响应面法结合熵权法多指标优选黄芪药材产地加工炮制一体化工艺 [J]. 中草药, 2021, 52(19): 5854-5861.
[11] 柳兰, 李雅, 郭志华, 等. Box-Behnken响应面法结合G1-熵权法的理气活血复方浸膏喷雾干燥工艺研究 [J]. 中草药, 2019, 50(11): 2560-2566.
[12] 杜正彩, 齐彪, 张明哲, 等. 正交设计结合药效学实验优选桂栀助眠胶囊提取工艺研究 [J]. 中草药, 2019, 50(3): 618-625.
[13] 尚芳红, 阳勇, 宋旭红, 等. 正交设计结合药效学实验优选四君子汤颗粒水提及精制工艺 [J]. 中草药, 2020, 51(16): 4191-4200.
[14] 秦贞苗, 李海龙, 谭银丰, 等. 高良姜胶囊成型工艺研究 [J]. 中国现代中药, 2015, 17(8): 847-850.
[15] 王宏顺, 熊学敏. 中药颗粒剂辅料筛选的研究 [J]. 江西中医药, 2010, 41(7): 65-67.
[16] 李旸. 复方连萸胶囊的制备工艺及质量标准研究 [D].武汉: 华中科技大学, 2011.
[17] 潘艳琳, 肖钦, 程心玲, 等. 肾康灵胶囊成型辅料的选择与工艺研究 [J]. 海峡药学, 2017, 29(10): 5-7.
[18] 马馨桐, 肖凤琴, 邱明阳, 等. 多指标综合评分法优选复方降脂缓释片的水提醇沉工艺及活性研究 [J]. 中国医院药学杂志, 2019, 39(17): 1759-1765.
[19] 曹青云. 舒润胶囊的制备工艺及质量标准研究 [D].北京: 北京中医药大学, 2018.
Preparation technology and quality control of Chaishao Shugan Tiaoshen Capsules based on multi-index quantification
YANG Xin-rong1, 2, 3, DOU Xia3, LI Guo-feng1, 2, SONG Qin-jie1, 2, LI Xian-wei1, 2, WU Hong-wei1, 2, LI Dong-hui1, 2, XIN Er-dan3, SUN Yu-jing1, 2, ZHANG Yu-gui1, 2, BIAN Tian-tian1, 2, LI Yue-feng1, 2
1. Gansu University of Chinese Medicine, Lanzhou 730000, China 2. Gansu Province Chinese Medicine Pharmaceutical Process Engineering Research Center, Lanzhou 730000, China 3. Affiliated Hospital of Gansu University of Chinese Medicine, Lanzhou 730000, China
To prepare Chaishao Shugan Tiaoshen Capsules (柴芍疏肝调神胶囊, CSTC) from Chaishao Shugan Tiaoshen prescription based on the classic famous prescription Sini Powder (四逆散), and carry out the quality control analysis by optimizing the preparation process and evaluating the multi-component.The CSTC were prepared by water extraction and alcohol precipitation, wet granulation and filling. According to the fingerprints of six index components synephrine, geniposide, paeoniflorin, liquiritin, naringin and ammonium glycyrrhizinate, and the comprehensive scores were analyzed to investigate the effects of the ratio of solid to liquid, extraction times, and extraction time, the relative density of liquid medicine, alcohol precipitation concentration and alcohol precipitation time on the refining process of water extraction and alcohol precipitation. In addition, based on the comprehensive score of angle of repose, bulk density, molding rate, moisture absorption rate to screen the effect of excipient types, excipient ratio, drug adjuvant ratio, and 95% ethanol dosage on the molding process.The optimal preparation process of CSTC was the ratio of solid to liquid of 1:12, extraction times of two times, extraction time of 69 min, relative density of medicinal liquid of 1.15 g/mL (50 ℃), alcohol precipitation concentration of 60%, alcohol precipitation time of 36 h, the excipient of dextrin + microcrystalline cellulose (3:2), the ratio of drug adjuvant of 1:1, and the amount of 95% ethanol accounting for 23% of the amount of drug adjuvant.The optimal preparation process is scientific, reasonable and highly feasible in this experiment, and can provide a reference for the development of CSTC and related traditional Chinese medicine preparations, which can provide the theoretical guidance for the quality evaluation of CSTC.
Sini Powder; Chaishao Shugan Tiaoshen Capsules; standard capsule; Box-Behnken response surface method; orthogonal test; preparation process; quality control; synephrine; geniposide; paeoniflorin, liquiritin; naringenin; ammonium glycyrrhizinate; angle of repose; bulk density; molding rate; hygroscopic rate
R283.6
A
0253 - 2670(2022)23 - 7393 - 10
10.7501/j.issn.0253-2670.2022.23.009
2022-06-08
国家自然科学基金资助项目(81960713);国家自然科学基金资助项目(82160750);甘肃省教育厅产业支撑计划项目(2021CYZC-21);甘肃省中药制药工艺工程研究中心开放课题(ZYGY202003);甘肃省科技计划(创新基地与人才计划)基础研究创新群体项目(21JR7RA569)
杨新荣(1990—),男,硕士研究生,主要从事中药及复方加工炮制机制及活性成分研究。Tel: 18419612305 E-mail: 1678365753@qq.com
通信作者:李越峰,教授,博士生导师,博士后,主要从事中药及复方加工炮制机制及活性成分研究。E-mail: lyfyxk@126.com
[责任编辑 郑礼胜]
