慢性阻塞性肺疾病急性加重住院患者调整长效支气管扩张剂为短效支气管扩张剂治疗对发生心律失常风险的临床分析
2022-12-06娜合木古丽阿依达尔汗韩武新恩卡尔波拉提曾晓凤
娜合木古丽·阿依达尔汗,张 强,韩武新,金 洪,恩卡尔·波拉提,曾晓凤
0 引言
慢性阻塞性肺疾病(Chronic obstructive pulmonary disease,COPD)是一种以持续气流受限为特征的呼吸系统疾病,是全球第3大死因。在 COPD 导致的死亡中,90%发生在低收入和中等收入国家[1]。在全球范围内,由于持续暴露于风险因素和人口老龄化,预计未来COPD的负担将增加[2]。慢性阻塞性肺疾病急性加重(Acute exacerbetion of chronic obstructive pulmonary disease,AECOPD)是继发于呼吸道病毒或细菌感染的COPD危重事件,表现为呼吸道症状增加,严重时可导致呼吸衰竭、住院甚至死亡。AECOPD常有各种合并症,对疾病过程产生重大影响,如使呼吸系统症状恶化以及生活质量下降,严重影响急性发作程度及增加死亡率等[3]。在 AECOPD住院人群中,大约1/3的患者存在严重的心血管疾病(Coronary artery disease,CAD),包括缺血性心脏病、心力衰竭和心律失常等[4]。且在AECOPD期间,患者发生急性心血管事件的风险更高[5]。
COPD主要治疗药物是支气管扩张剂,即长效β2受体激动剂(Long-acting β2-agonist,LABA)和长效抗胆碱能药物(Long-acting muscarinic antagonist,LAMA)。既往试验提示,在病情平稳的合并心血管疾病的COPD患者中吸入适当剂量的LABA可能是安全的[3]。然而,对于严重的AECOPD,国际指南目前建议使用短效β2受体激动剂(Short-acting β2-agonist,SABA)联合短效抗胆碱能药物(Short-acting muscarinic antagonist,SAMA)[2]。但有研究显示,SABA,尤其是异丙托溴铵与心脏病风险增加有关[6],但在AECOPD期间这种风险是否会增加,目前尚不明确。因此,我们回顾性分析了住院接受SABA和/或SAMA治疗的AECOPD患者与继续接受LABA和/或LAMA吸入治疗的患者的临床特征,评估其新发心律失常的发生率,探究与心律失常事件发生相关的危险因素。
1 资料与方法
1.1 研究对象 回顾性选择新疆塔城地区人民医院呼吸科2020年1月-2021 年12月收治的207例确诊AECOPD的患者为研究对象。纳入标准:①年龄≥40岁;②根据慢性阻塞性肺疾病全球倡议(Global Initiative for Chronic Obstructive Lung Disease,GOLD)指南确诊为COPD,本次因AECOPD入院[2];③病历数据完整。排除标准:①既往已有永久性心房颤动;②既往长期应用SABA/SAMA治疗;③目前或既往确诊哮喘史或肺纤维化;④其他影响实验结果的疾病,如肺栓塞、细菌性/病毒性肺炎或急性心力衰竭。对于在观察期内多次住院的患者,只考虑最近一次住院。
1.2 研究方法 按照住院期间接受的吸入治疗药物进行分组[不考虑是否应用吸入激素(Inhaled corticosteroids,ICS)],住院后将LABA/LAMA调整为SABA和/或SAMA治疗的患者为SABA/SAMA组,继续应用LABA和/或LAMA治疗的患者为LABA/LAMA组。收集患者的性别、年龄、是否正在吸烟、肺功能(舒张后FEV1占预计值百分比和舒张后FEV1/FVC占预计值百分比)、心脏相关合并症、居家治疗中控制心律药物以及支气管扩张剂使用情况等临床资料,以及在院期间氧合指数(PaO2/FiO2)、心电图、住院日、死亡情况等指标。心律失常的诊断则根据心电图以及心内科会诊确定。
2 结果
2.1 SABA/SAMA组和LABA/LAMA组临床特征比较 患者平均年龄为(69.31±8.89)岁,男性患者占68.6%。157例患者住院后调整为SABA/SAMA治疗,50例继续LABA/LAMA吸入治疗。两组患者年龄、性别、吸烟、肺功能等差异无统计学意义;有缺血性心脏病史38例(18.36%),阵发性房颤病史30例(14.49%),充血性心力衰竭病史15例(7.25%),应用起搏器患者3例(1.45%),两组间差异无统计学意义(P>0.05)。居家治疗中控制心律失常药物以及支气管扩张剂的使用在两组中差异无统计学意义(P>0.05)。在院期间,两组间发生的心律失常以及住院日和死亡率差异无统计学意义(P>0.05)。但SABA/SAMA组较LABA/LAMA组有更低的氧合指数、更高的心率以及较高的吸氧浓度,差异有统计学意义(P<0.05)。具体见表1。
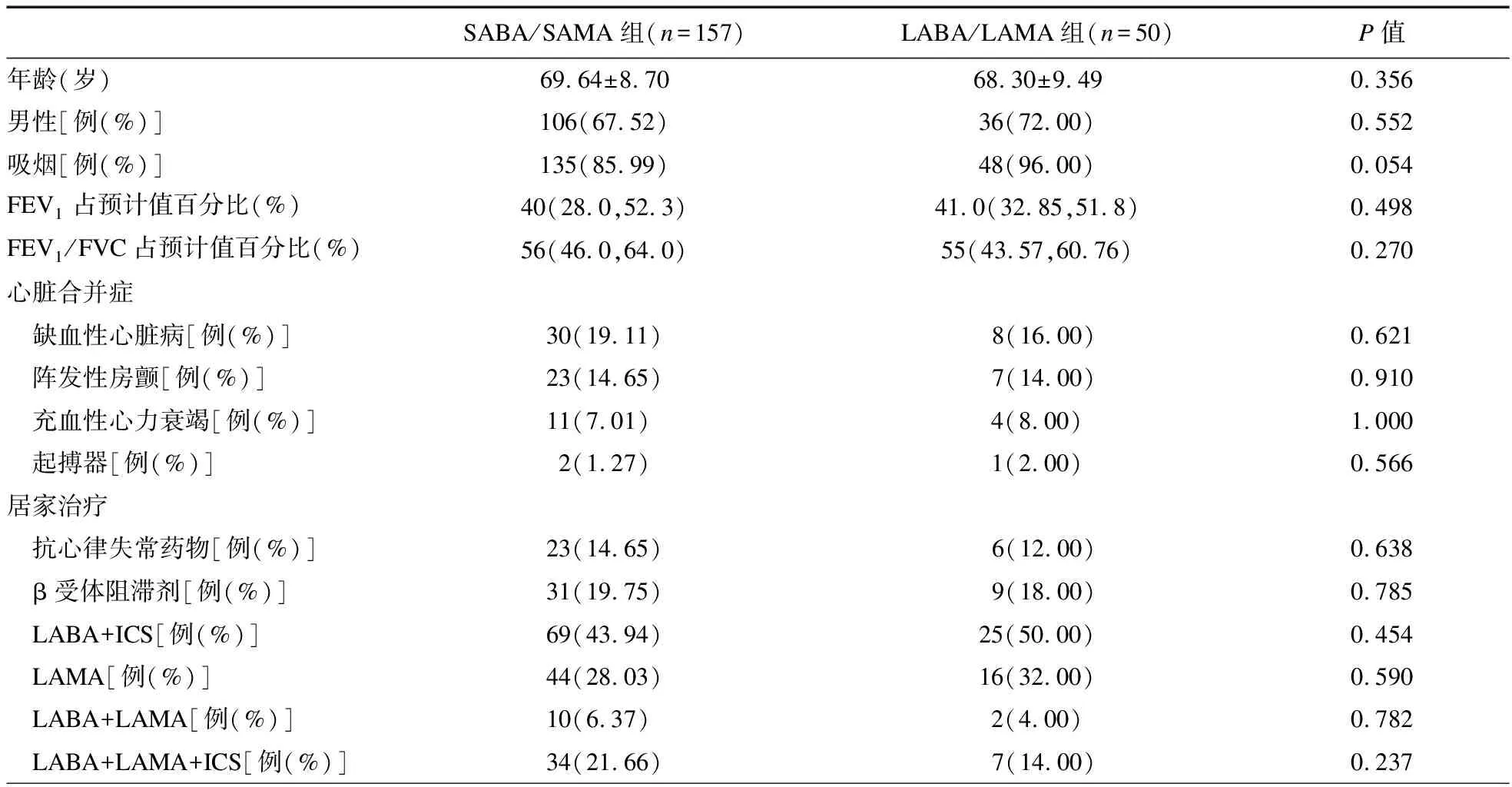
表1 SABA/SAMA组和LABA/LAMA组患者的临床特征比较
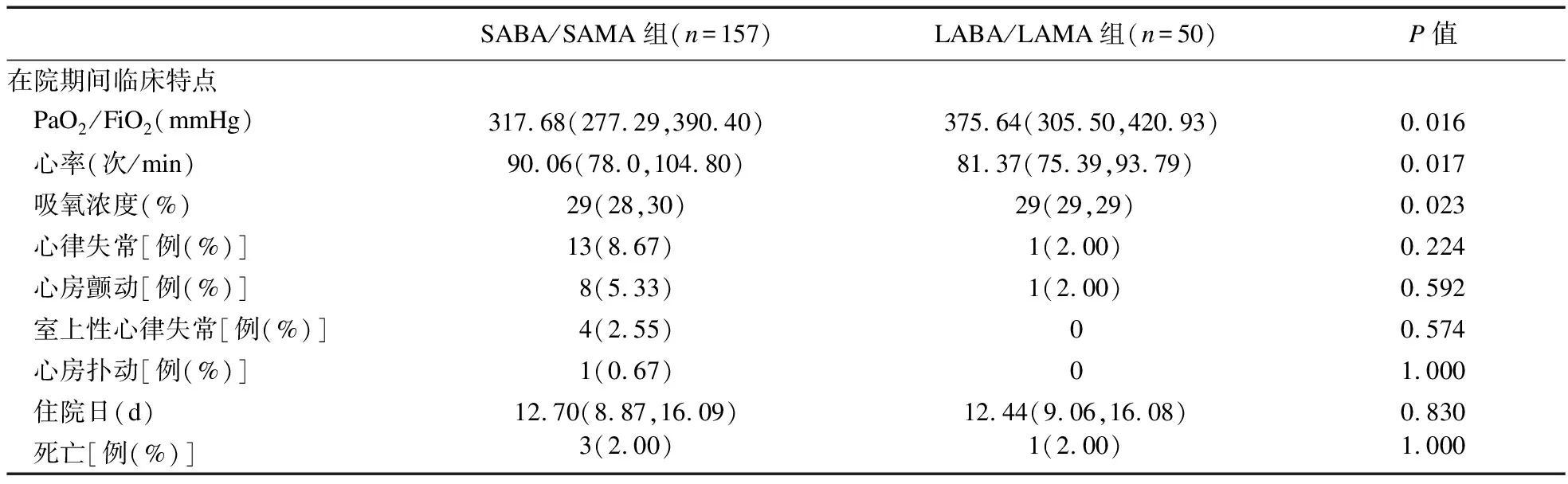
续表1
2.2 在院期间出现新发心律失常与无心律失常的临床特征比较 207例患者中有14例新发心律失常(6.76%)。有心律失常组有更多的患者具有阵发性房颤病史(P=0.006),入院时心率较高(P=0.038),吸氧浓度较高(P=0.020);有心律失常和无心律失常患者的年龄、性别、吸烟、肺功能、居家治疗中抗心律失常治疗以及支气管扩张剂、死亡率和住院时间的差异无统计学意义(P>0.05)。具体见表2。
2.3 对于在院新发心律失常的二元Logistic回归分析 对表2中有意义的变量进行二元Logistic回归分析,结果表明既往阵发性房颤史是住院期间出现新发心律失常的独立危险因素(OR=0.180,95%CI:0.054~0.601,P=0.005)。具体见表3。
3 讨论
COPD为一种全身性疾病,心血管合并症是 COPD 患者死亡的重要原因[7],对个体患者的预后有重要影响。COPD和心血管疾病间的联系机制是复杂、多因素的,且尚未被完全阐明,同时患有上述疾病的患者通常被排除在随机对照临床试验之外[3],导致COPD心血管风险增加的潜在病理生理机制仍不明确[8]。如QTc间期延长的AECOPD患者,提示潜在合并心血管疾病风险,与病情严重程度、死亡率以及再入院率增加相关[9]。长QTc常可引起致命性的心律失常[10],AECOPD期间新的心律失常数据非常有限,并且主要集中在呼吸衰竭以及需要呼吸机辅助通气的患者中[11]。尽管研究者普遍关注SABA可能存在的心血管不良反应,但较少研究 AECOPD 期间SABA使用与心律失常发生率的关系。

表2 有心律失常与无心律失常患者的临床特征比较
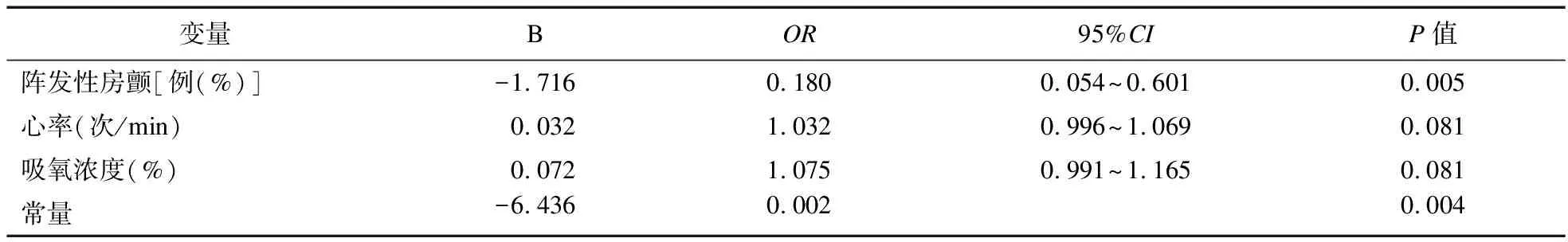
表3 新发心律失常的二元Logistic回归
本研究显示,AECOPD治疗过程中新发的心律失常约占6.76%,表明将COPD 患者从慢性LABA调整为SABA和/或SAMA治疗,不会增加急性加重期间心律失常的风险。阵发性房颤的既往史是住院期间新发心律失常的独立危险因素,与心率以及吸氧浓度等无关。
β2受体激动剂和毒蕈碱拮抗剂的安全性一直存在争议,特别是因为心血管事件风险较高的易感患者经常被排除在III期试验之外[8,12]。β2受体激动剂的使用与心肌梗死、充血性心力衰竭、心脏骤停和心源性猝死的风险增加有关[13],患有哮喘或COPD会放大这些药物对心脏的影响,使患心血管并发症的风险可能性增加。AECOPD患者年龄通常较大,心脏耐受能力下降,也更易发生心律失常。
常用的SABA为特布他林,虽然特布他林和沙丁胺醇都属于选择性肾上腺素β2受体激动药,但剂量较大时亦可激动β1受体,兴奋心脏作用增强,易诱发心律失常,尤其是快速型心律失常最常见。常用的SAMA为异丙托溴铵,为胆碱受体拮抗剂,可通过阻断窦房结M受体,使迷走神经对心脏的抑制作用减弱或阻断,导致心率增加。赵倩如等[14]对SABA+SAMA联合用药前后心率的变化进行前瞻性分析,研究结果提示,其兴奋心脏作用增强,诱发心律失常的可能性增大,结果显示,12.50%发生心律失常,且多为快速性心律失常。Czaja等[12]采用2个儿科卫生系统(2011-2013 年)电子健康记录数据,对335 041名18岁以下儿童进行回顾性队列研究,其中一个研究显示,接受SABA治疗的儿童心律失常调整风险增加(OR=1.89,95%CI:1.31~2.73),第2个系统中,SABA 应用与心律失常之间的关联较弱(OR=1.26,95%CI:0.30~5.33)。Kearns等[15]进行的一项随机交叉试验提示SABA比ICS/LABA引起更多的心血管不良事件。对于已经接受 ICS/LABA 联合治疗的 COPD 患者,将 LAMA 添加到联合治疗中时,可以在不增加心血管严重不良事件的情况下改善治疗效果[16]。大型随机试验已经证明了LAMA单药治疗以及LAMA/LABA联合治疗的心血管安全性,吸入抗胆碱能药物不会增加心血管危害[17]。Andreas等[18]对中度至极重度 COPD 患者动态心电图分析显示,噻托溴铵/奥达特罗联合疗法对心律失常没有影响。Nagy[19]证明了中度至重度 COPD 患者在单剂量GSK961081 (一种吸入性双功能分子,具有毒蕈碱拮抗β2受体激动剂特性)中加入超治疗剂量SABA或SAMA的心血管安全性。van Geffen等[20]研究提示,在稳定期 COPD 中,单次吸入LABA/LAMA干粉剂与雾化SABA/SAMA比较无显著改善,且不良事件无显著差异。这与本研究结果相似,调整为SABA/SAMA治疗不增加心律失常的发生。
既往研究提示,房颤患者在缺氧、炎症、β2受体激动剂的使用增加和自主神经变化等作用下,约25% 将合并COPD,反之,COPD 的急性加重也会暂时增加房颤风险,使全因死亡率风险增加 55%[5],严重气流受限和COPD频繁急性加重可使房颤和心房扑动的发生率增加2倍[21]。本研究也表明,只有先前的阵发性房颤病史构成了住院期间新发心律失常发展的危险因素,而与既往的抗心律失常药物和β受体阻滞剂使用无关。故需进一步关注房颤与COPD间的联系。
患者病情经历COPD急性加重至需住院治疗程度时,往往不能适当吸入支气管扩张剂,在这种情况下,通常首选雾化器吸入SABA以及激素等治疗。对应本研究中,在调整为SABA/SAMA治疗的患者中,呼吸衰竭患者的发病率更高,并需要更高的吸氧浓度,而在病情严重的患者中发生心律失常也是合理的。然而,与继续LABA治疗的患者相比,调整为SABA/SAMA的患者在临床结果或心律失常发生率方面差异无统计学意义。在COPD急性加重期间,尤其是在病情较重的患者中,患者的气流受限程度增加,导致呼吸困难,促使呼气末正压升高,发生低氧血症和高碳酸血症,增加了肺血管压力和舒张功能障碍[22]。
支气管扩张剂是防治COPD的关键,可改善气流阻塞,减少气道阻力和空气滞留,从而减少肺机械应力和胸腔内压,还通过降低肺动脉压以及维持心脏射血分数,改善心衰严重程度。SABA的益处可能超过其可能具有的促心律失常作用,具有显著的正风险比[23-24]。
本研究存在一定的局限性。首先,心律失常事件的数量较少,可能限制了研究的组间比较。其次,未来应进行前瞻性随机试验以证实这一观察。最后,应进行进一步试验,分别研究SABA或SAMA甚至ICS等具体分组对心律失常发生的影响。
总之,本研究显示,在严重急性加重期,COPD患者治疗方案由LABA/LAMA调整为SABA/SAMA不增加新发心律失常的风险,且阵发性房颤的既往史是住院期间新发心律失常的独立危险因素。
