天然蕨素结构及核磁共振谱特征的研究进展
2022-12-03彭财英雷志强卢健刘建群舒积成
彭财英 雷志强卢健 刘建群 舒积成
(江西中医药大学, 江西 南昌330004)
蕨素类化合物是具有1H⁃茚⁃1⁃酮母核结构的倍半萜,广泛存在于蕨类植物中,是此类植物特征性成分,具有较好的专属性。近年来研究发现,此类化合物具有抗肿瘤[1]、抗炎[2]、抗糖尿病[3]、抗结核[4]、降血脂[5]、抗病毒[6]等多种生物活性。天然蕨素类成分由于其结构的多样性及较好的生物活性,越来越受到研究者们的关注。据统计,迄今从自然界中分离得到约160 个蕨素类化合物[7],并有结构新颖的此类化合物仍在不断地被分离得到。虽然Fukuoka 等[8]在1983 年已经报道蕨素类化合物的核磁共振13C⁃NMR 特征,但近三十年来,随着核磁共振测定技术的发展,有100 多个新的蕨素类化合物被发现,有必要重新总结和补充其核磁共振谱特征,这对此类化合物结构推导有参考意义。基于此,本文根据课题组已分离得到的43个蕨素类化合物核磁共振(NMR)数据,并结合文献报道的其他代表性蕨素类成分的数据,分析与归纳各类天然蕨素成分的结构及其NMR 特征,以期为其进一步研究提供参考。
1 化合物结构
1.1 母核结构 蕨素类化合物的特征主要包括苯环(A环)、骈戊酮(B 环),其中A 环常见2 个甲基(C⁃5、C⁃7位)和乙基(C⁃6 位),B 环有羰基(C⁃1 位)和甲基(C⁃2 位)。根据B 环C⁃2 位的甲基取代的数目,蕨素类成分可分为15 碳蕨素类(C⁃2 位有2 个甲基)、14 碳蕨素类(C⁃2位有1 个甲基)、13 碳蕨素类(C⁃2 位无甲基)[7],见图1A。另外,天然蕨素成分还包括2 种型体的二聚体,分别为2 个蕨素单体通过C⁃2 位与C⁃3 位骈合四元环(Ⅰ型)和2 个蕨素单体通过C⁃2 位与C⁃12 位相连(Ⅱ型),见图1B~1C。据目前文献报道显示,15 碳与14 碳母核的蕨素为天然蕨素类成分的主体部分,占96%以上,而目前只报道了1 个13碳蕨素成分mukagolactone[9]和5 个蕨素二聚体[9⁃10]。
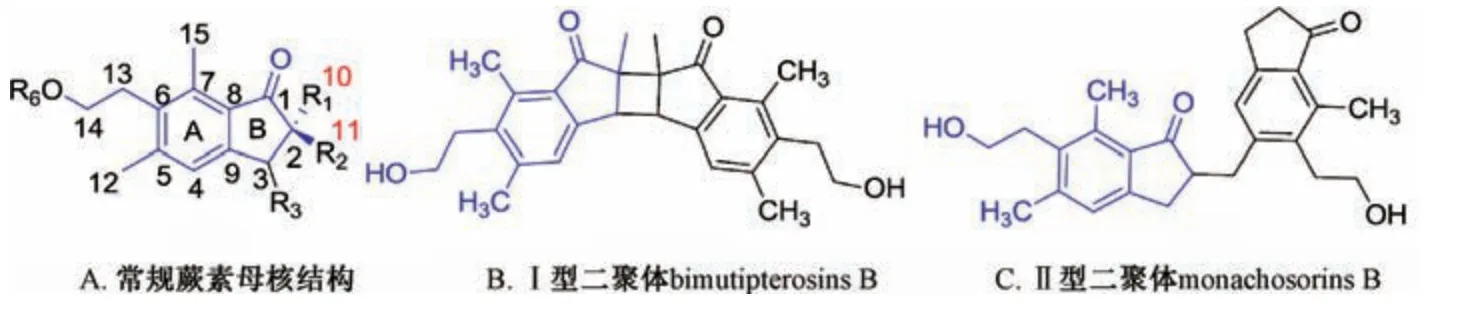
图1 天然蕨素类成分母核结构
1.2 常见取代基及其取代位置 蕨素类化合物取代基多样,但取代位置相对比较固定。常见取代基主要为羟基、葡萄糖、乙酰基,并有桂皮酰基、氯、硫酸根等取代基[11⁃13],但数量较少。羟基取代一般常见于C⁃3、C⁃11、C⁃13位,而在A 环甲基(C⁃12、C⁃15 位)取代的羟基也有个别报道[14]。C⁃3、C⁃14 位易形成葡萄糖糖苷[15]。另外,也有C⁃2、C⁃3 位双键[16],C⁃6、C⁃13、C⁃14 位三元环[17],C⁃5、C⁃6、C⁃12、C⁃13、C⁃14 位六元环,C⁃6、C⁃7、C⁃13、C⁃14、C⁃15 位六元环[18]等取代。
1.3 立体构型 天然蕨素类化合物的手性碳相对较少且集中,多数是由于羟基取代而产生手性。常见于B 环的C⁃2、C⁃3 位和A 环支链的C⁃13 位。C⁃2、C⁃3 位的R/S构型均有报道[19]。C⁃13 位由于羟基在烷基链上,迄今为止未有对C⁃13 位的羟基构型确定的报道。目前确定C⁃2、C⁃3 位立体构型常采用圆二色谱和二维NOE 谱相结合的方法[20]。若圆二色谱在325 nm 波长处显示正Cotton 效应,C⁃3 位为S构型,并与C⁃2 位的构型无关[20],再结合二维NOE 谱的信息,推导出C⁃2 位的构型。然而,天然蕨素类化合物中C⁃3 位羟基多为α 构型,β 构型较少[7]。
2 核磁共振谱特征
2.11H⁃NMR
2.1.1 A 环质子 A 环质子主要由芳香质子(H⁃4 位)、苯环上的甲基或羟甲基质子(H⁃12、H⁃15 位)、C⁃6 位连接的乙基链上质子(H⁃13、H⁃14 位)组成。
2.1.1.1 芳香质子(H⁃4 位)绝大多数天然蕨素类成分的1H⁃NMR 中为单峰,化学位移在7.50 左右[21⁃22],这是蕨素成分特征性较强的质子信息,见图2。
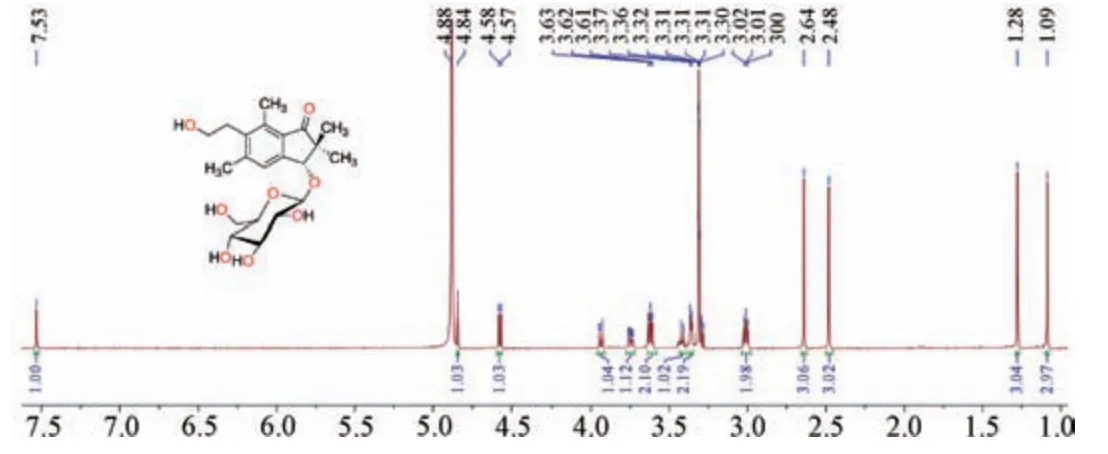
图2 蕨素D 3⁃O⁃β⁃D⁃葡萄糖苷的1H⁃NMR 谱图(CD3OD,600 MHz)
2.1.1.2 苯环上的甲基质子(12⁃CH3、15⁃CH3)12⁃CH3、15⁃CH3为蕨素1H⁃NMR 特征性质子信号,甲基均为单峰,因连接在苯环上,处于相对较低场,化学位移约为2.50~2.70。由于15⁃CH3受C⁃1 位羰基负屏蔽作用影响,其化学位移较12⁃CH3更低,化学位移为2.70 左右,而12⁃CH3化学移位处于2.50 左右,两者较易识别[12,23],见图2。
2.1.1.3 苯环上的次甲基质子(12⁃CH2OH 或15⁃CH2OH)苯环上的次甲基质子在蕨素成分的1H⁃NMR 中较少见[15,21,24],并且尚未见报道称A 环上2 个甲基可以同时被羟基取代。12⁃CH2OH 的2 个质子特征性明显,以单峰出现,化学位移为4.80。而15⁃CH2OH 的2 个质子由于受邻位羰基的磁各向异性影响,以同碳偶合的双峰(J=12.1 Hz)出现,分别位于5.10、5.00 左右,与C⁃12 位羟基取代区分明显。
2.1.1.4 C⁃6 位连接的乙基链上质子(H⁃13、H⁃14 位)C⁃6 位连接的乙基链上质子直接与A 环相连的H⁃13 位上2个质子显示三重峰(J=7.5 Hz),化学位移为3.10 左右,见图3;若C⁃13 位有羟基取代,则向低场移动约2.50,并且H⁃13 位裂分为双二重峰(J=4.9,8.3 Hz),见图4。目前报道的天然蕨素类化合物C⁃14 位除极个别为氯原子及硫酸根外均为羟基取代,H⁃14 位化学位移在3.70 左右,与C⁃13 位上2 个质子邻位偶合,形成三重峰,偶合常数为7.5 Hz。若H⁃14 位羟基被糖苷化或乙酰化,其化学位移向低场移动不明显,约0.05[25]。若C⁃13 位羟基取代,2 个质子裂分为双二重峰[J=8.3,11.4 Hz(H⁃14a)和J=4.9,11.4 Hz(H⁃14b)],化学位移分别为3.90、3.65,见图4。C⁃14 位硫酸根离子取代衍生物(如2S,3S⁃硫酸代蕨素C)和羟基取代物(如2S,3S⁃蕨素C),其H⁃13、H⁃14 位的化学位移非常接近,在1H⁃NMR 中无明显差异[13]。
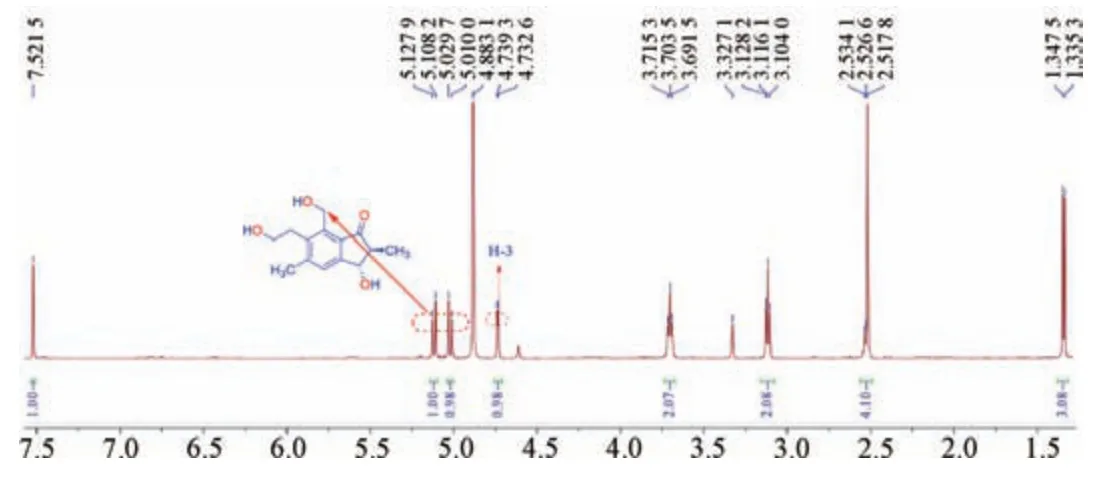
图3 (2S,3S)⁃蕨素S 的1H⁃NMR 谱图(CD3OD,600 MHz)
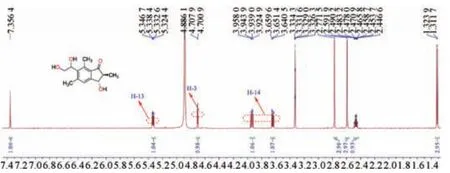
图4 (2S,3S)⁃蕨素Q 的1H⁃NMR 谱图(CD3OD,600 MHz)
2.1.2 B 环质子 B 环质子主要由H⁃2、H⁃3、C⁃2 位上的甲基(10⁃CH3、11⁃CH3)或羟甲基(10⁃CH2OH 或11⁃CH2OH)组成。
2.1.2.1 H⁃2位若蕨素类化合物为15 碳母核结构,则H⁃2 位无信号。若为14 碳母核结构,H⁃2 位的化学位移为2.45左右,与H⁃3、H⁃11 位偶合形成dq 峰[5]。H⁃2 与H⁃3 位的偶合常数会随着甲基(11⁃CH3)的构型不同而变化,若甲基为α 构型,J=6.5 Hz,若甲基为β 构型,J=4.0 Hz[5]。因此,可依据H⁃3 的偶合常数判断C⁃2 位的立体构型。
2.1.2.2 H⁃3位天然蕨素成分C⁃3 位常有OH 取代,且大部分为β 构型,化学位移为4.75 左右。若C⁃3 位羟基被糖苷化,H⁃3 位的化学位移向低场移动约0.1[26]。若C⁃11位羟基取代,H⁃3 位于其负屏蔽区,化学位移向低场移动约4.95[24]。若C⁃3 位无羟基取代,H⁃3 位的2 个质子产生同碳偶合外,并与H⁃2 位偶合,信号显示dd 峰[27]。
2.1.2.3 C⁃2 位上的甲基(10⁃CH3和11⁃CH3)蕨素类化合物为15 碳母核结构,2 个均为单峰甲基质子信号,化学位移分别为1.08、1.28 左右[28]。若为14 碳母核结构,其中1 个甲基信号消失,另1 个甲基依据不同的构型,其裂分和化学位移不相同。若甲基为β 构型,偶合常数为7.0 Hz 的双峰,化学位移为1.30 左右[19];若甲基为α 构型,偶合常数为7.5 Hz 双峰,化学位移为1.20 左右[19];若C⁃2位与C⁃3 位形成双键,11⁃CH3向低场移动,并与H⁃3 位远程偶合,偶合常数为1.6 Hz,化学位移约1.80,见图5。
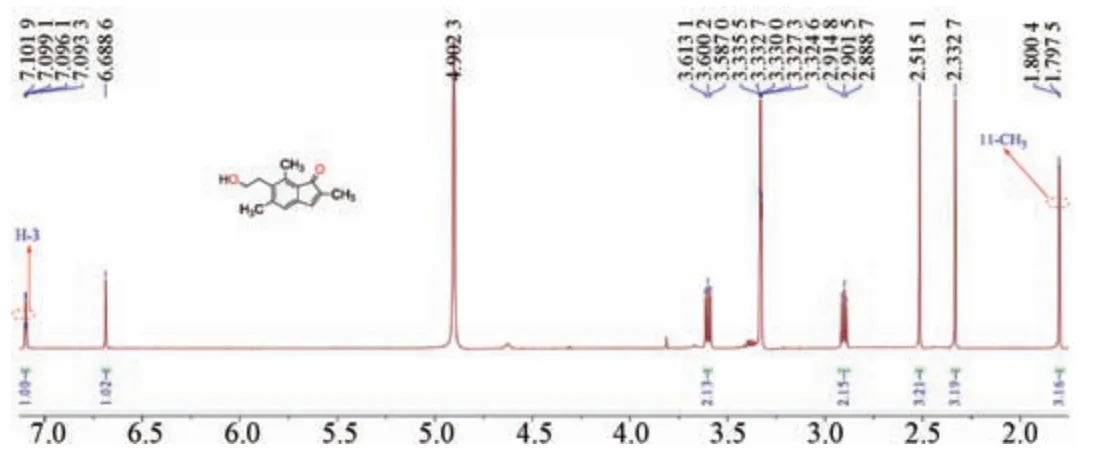
图5 脱氢蕨素B 的1H⁃NMR 谱图(CD3OD,600 MHz)
2.1.2.4 C⁃2 位上的羟甲基(10⁃CH2OH 或11⁃CH2OH)C⁃2 位仅见有1 个羟基取代。形成的连氧亚甲基2 个质子以偶合常数为12.0 Hz 的双峰出现,化学位移分别处于3.68、3.73 附近。若此位羟基进一步糖苷化,2 个质子偶合常变小(J=9.5 Hz),两者化学位移相差进一步拉大,分别处于3.48、4.10 附近,见图6。
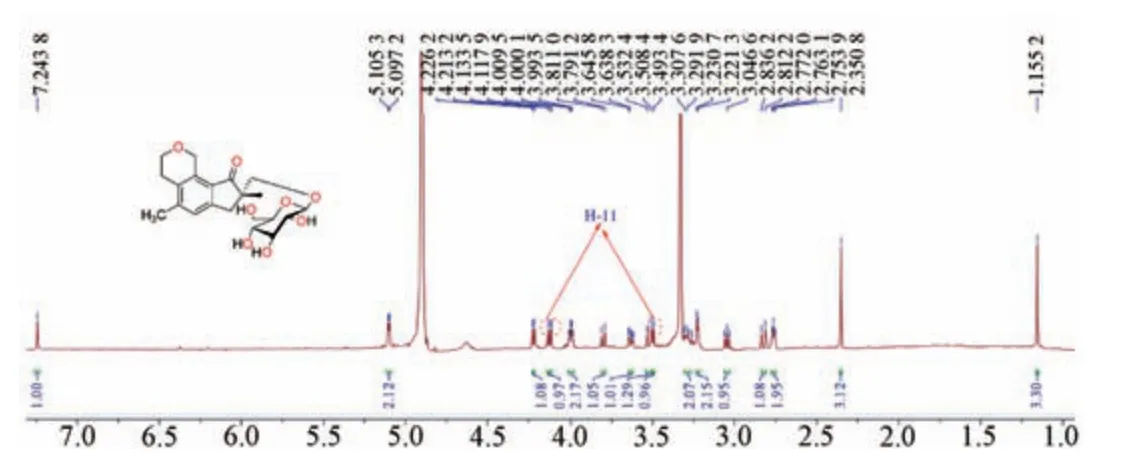
图6 creticoside A 的1H⁃NMR 谱图(CD3OD,600 MHz)
2.213C⁃NMR
2.2.1 A 环碳信号 A 环碳主要由6 个苯环碳(C⁃4~C⁃9位)、苯环上的甲基或羟甲基碳(C⁃12、C⁃15 位)及C⁃6 位连接的乙基碳(C⁃13、C⁃14 位)组成。
2.2.1.1 苯环碳(C⁃4~C⁃9 位)苯环碳的化学位移在126.0~156.0 之间,但一般具有相对的范围,从小到大依次为C⁃4<C⁃8<C⁃6≈C⁃7<C⁃5<C⁃9。C⁃4 位由于未取代(叔碳),其化学位移值最少,并受C⁃2、C⁃5、C⁃6 位苯环碳的取代情况影响较少,化学位移为1.0 左右。C⁃5 苯环碳的化学位移处于144.0~146.0。C⁃6、C⁃7 位的化学位移接近,处在134.0~139.0 之间,两者大小受不同取代基影响。C⁃8位化学位移处于131.0~133.0,而C⁃9 位由于受羰基的负屏蔽作用,其化学位移值最大,约为151.0~156.0,见图7。
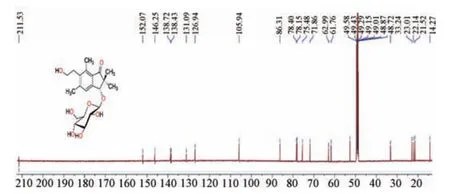
图7 蕨素D 3⁃O⁃β⁃D⁃葡萄糖苷的13C⁃NMR 谱图(CD3OD,150 MHz)
2.2.1.2 苯环上的甲基碳(C⁃12、C⁃15 位)12⁃CH3处于15⁃CH3较低场,受周围取代基的影响较小,故化学位移值相对固定,12⁃CH3的化学位移值在21.0~22.0,而15⁃CH3的化学位移值在13.0~14.0。
2.2.1.3 苯环上的羟甲基碳(C⁃12、C⁃15 位)若C⁃12位羟基取代,向低场移动,化学位移为63.5。若C⁃15 位羟基取代,化学位移约为58.0。两者羟基取代后化学位移有明显区别,在13C⁃NMR 上较易鉴别。若C⁃14 与C⁃15 位形成环醚(六元环为C⁃6、C⁃13、C⁃14、O、C⁃15、C⁃7),则C⁃15 位的化学位移值约为68.0[19]。
2.2.1.4 C⁃6 位连接的乙基碳(C⁃13、C⁃14 位)C⁃13 位的化学位移约为33.0,若C⁃14 位羟基糖苷化后,向高场移动,化学位移约为30.0[29];若C⁃13 位有羟基取代,向低场移动,化学位移约为72.5[30]。目前报道的天然蕨素类化合物的C⁃14 位均有羟基取代,化学位移为62.0;若C⁃13位羟基取代,C⁃14 位的化学位移向低场移动约3.0,处于65.0;若C⁃14 位羟基进一步糖苷化,其化学位移向低场移动更明显,在70.0 附近[31]。
2.2.2 B 环碳信号 B 环碳主要由C⁃2 位、C⁃3 位及C⁃2 位上的甲基(10⁃CH3、11⁃CH3)或羟甲基(10⁃CH2OH 或11⁃CH2OH)组成。
2.2.2.1 C⁃2位在15 碳蕨素结构中,由于C⁃2 位为季碳,化学位移在52.0 附近,并受C⁃11 位羟基取代影响较大,取代后向低场移动5.0 左右[32]。在14 碳蕨素结构中,化学位移与C⁃2 位甲基的构型有关,若甲基为α 构型,化学位移在50.0 附近[31];若甲基为β 构型,则化学位移约为55.0[29]。通过化学位移大小,有助于C⁃2 位的立体构型的确定。另外,若C⁃2 位与C⁃3 位形成双键,化学位移约为123.0[16]。
2.2.2.2 C⁃3 位 C⁃3 位常见有羟基取代。15 碳蕨素中,化学位移约为77.7。而在14 碳蕨素中,其化学位移受C⁃2位甲基立体构型影响最为明显,若甲基为β 构型,处于76.0 左右[29];若甲基为α 构型,则在70.0 附近[31]。依据化学位移值可判断C⁃2 位的立体构型。若C⁃3 位羟基有糖苷化,化学位移相应地向低场移动约8.0;若此处无羟基取代,化学位移约为35.0~38.0[16]。若C⁃2 位与C⁃3 位形成双键,化学位移由于羰基的负屏蔽作用处于较C⁃2 位低场,约为143.0[16]。
2.2.2.3 C⁃2 位上的甲基碳(10⁃CH3和11⁃CH3)在15 碳蕨素结构中,2 个甲基的化学位移约为21.0、23.5,与A 环上C⁃5 位的甲基化学位移较相近。而在14 碳蕨素结构中,其中1 个甲基碳信号消失,并且化学位移与其构型有关,若甲基为β 构型,化学位移约为13.0,并与A 环C⁃7 位甲基化学位移相近[29];若甲基为α 构型,化学位移约为11.0[33]。若C⁃2 位与C⁃3 位形成双键,甲基的化学位移约10.0[16]。
2.2.2.4 C⁃2 位上的羟甲基碳(10⁃CH2OH 或11⁃CH2OH)C⁃2 位仅见有1 个羟基取代,其化学位移约67.0。若进一步糖苷化,向低场位移约7.0[24]。
2.3 蕨素二聚体的核磁共振谱特征 Ⅰ型蕨素二聚体为2个相同的单个蕨素通过C⁃2、C⁃3 位骈合四元环而成,有C2⁃C2′、C3⁃C3′(头⁃尾)和C2⁃C3′、C3⁃C2′(头⁃头)这2 种相骈方式,并表现出不对称与对称2 种类型结构[10]。不对称二聚体的核磁共振谱显示2 套单个蕨素数据,其平面结构可通过异核多键相关谱推导确认,但对称结构的二聚体平面结构[(对称中心,头⁃尾相连)或(对称面,头⁃头相连)],仅通过核磁 共振多键相关谱(HMBC 谱)及Chemdraw 软件显示的化学结构模型难于确定。因为其13C⁃NMR、1H⁃NMR 数据表现为 1 套单个蕨素数据,如bimutipterosins B,见图8~9,并与单个蕨素的核磁共振谱非常相似,最大的不同是C⁃2 位与C⁃3 位分别为非连氧季碳和叔碳,且H⁃3 位和11⁃CH3均为单峰。对于首次鉴别对称结构属于头⁃尾相连还是头⁃头相连,需要借助于化合物的单晶衍射数据方可确定,故课题组在2011 年发表的对称性二聚体bimutipterosins B 的结构[10]值得商榷,若由此带来不便表示抱歉。后续课题组将分别选择头⁃头相骈和头⁃尾相骈的称性二聚体做单晶衍射(目前已培养出单晶),通过分析及总结其核磁共振谱的差异性,归纳出核磁共振谱的数据鉴定对称的类型。Ⅱ型蕨素二聚体为2 个蕨素单体通过C⁃2位与C⁃12′位相连,核磁共振谱显示2 套单个蕨素信号,其平面结构可根据HMBC 谱确认。
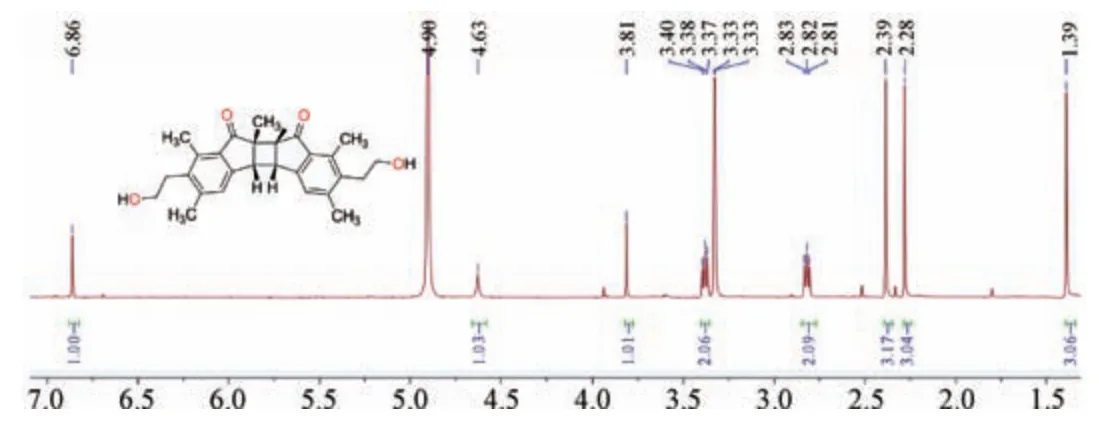
图8 bimutipterosins B 的1H⁃NMR 谱图(CD3OD,600 MHz)
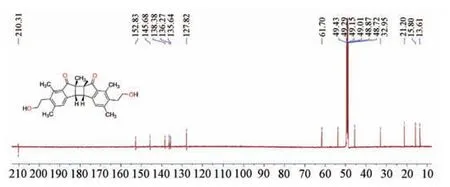
图9 bimutipterosins B 的13C⁃NMR 谱图(CD3OD,150 MHz)
3 小结
综上所述,蕨素类化合物的是波谱特征比较强,目前已积累了丰富的参考数据,对于绝大多数的蕨素类化合物而言,通过和已知的化合物数据对比,并借助1H⁃NMR 与13C⁃NMR基本可以完成结构的确定,但对于结构新颖如新骨架的蕨素成分的确定,还需要结合各种二维谱及高分辨质谱的数据。另外,本文中对于蕨类成分的立体构型未全面而具体归纳,确认立体构型可以参考其他相关文献。
