基于核心素养的有机结构与性质高考题命题特点及解题策略
2022-11-30湖北熊云贵
湖北 熊云贵
一、命题特点
核心素养背景下,有机结构与性质考题备受命题者青睐。这类考题,一般给出科学家合成的具有重要作用的某有机物的结构简式,考查该有机物的分子式、基团或者官能团的数目、手性碳原子数目、分子中的某原子共面或者共线情况、能够发生反应的类型、与某物质反应的数量关系等。题干部分创设真实情境,指出科学家合成的该有机物具有重要作用,体现了学科价值,起到学科育人功能,有利于培养学生的“科学态度与社会责任”;选项中涉及的问题,考查学生观察结构、根据结构推测物质性质的能力,有利于培养学生的“证据推理与模型认知”。
【考题示例1】(2022年全国甲卷,8题)辅酶Q10具有预防动脉硬化的功效,其结构简式如图1。下列有关辅酶Q10的说法正确的是
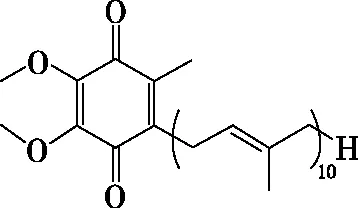
图1
( )
A.分子式为C60H90O4
B.分子中含有14个甲基
C.分子中的四个氧原子不在同一平面
D.可发生加成反应,不能发生取代反应
【答案】B
【分析】本题给出辅酶Q10的结构简式,考查分子式、分子中甲基数目、分子中的氧原子共面情况、是否发生加成反应和取代反应。
【考题示例2】(2022年海南卷,12题)化合物“E7974”具有抗肿痛活性,结构简式如图2,下列有关该化合物说法正确的是
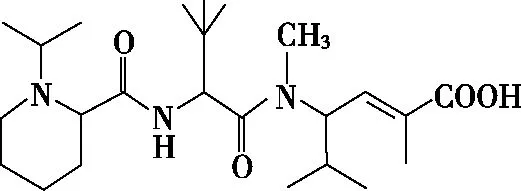
图2
( )
A.能使Br2的CCl4溶液褪色
B.分子中含有4种官能团
C.分子中含有4个手性碳原子
D.1 mol该化合物最多与2 mol NaOH反应
【答案】AB
【分析】本题给出“E7974”的结构简式,考查能否使Br2的CCl4溶液褪色、官能团的数目、手性碳原子数目、1 mol该化合物最多与NaOH反应的物质的量。
二、解题策略
(一)深刻领会有机物的结构特点
1.有机物分子式
确定有机物分子式,首先要把碳原子数目数对,氧原子、氮原子、卤素原子一般较少,比较容易确定。关键是氢原子,由于氢原子一般会在结构简式中省略,所以,我们要根据碳的成键原则,补充相关氢原子,确定总的氢原子数目。也可以根据相关通式,确定氢原子数目。如烷烃通式CnH2n+2,如果其中含有单键氧原子,不改变氢原子数目;如果其中含有卤素原子,则氢原子数目与卤素原子数目之和等于2n+2;如果其中含有单键氮原子,则氢原子数目比相应烷烃的氢原子数目多一个。如果出现一个双键或者一个环,氢原子数目比相应烷烃减少2个;如果出现一个三键,氢原子数目比相应烷烃减少4个;如果出现一个苯环,氢原子数目比相应烷烃减少8个。
考题示例1的A项,碳原子数目应该为59,所以A错。氢原子数目是90,可以按照碳的成键原则补充相关氢原子后直接数,也可以按照通式计算:59×2+2-15×2=90。氧原子4个,一目了然。
2.手性碳原子
手性分子是指含有手性碳原子的分子,由于4个原子或原子团在空间的排列不同,形成了如同左手与右手一样互为镜像,却在三维空间里不能重叠的分子。具有手性的分子,一般在一个C原子上按四面体方式连接上4个互不相同的原子或基团,如图3所示中左右两只手托出的两个呈镜像关系的乳酸分子。
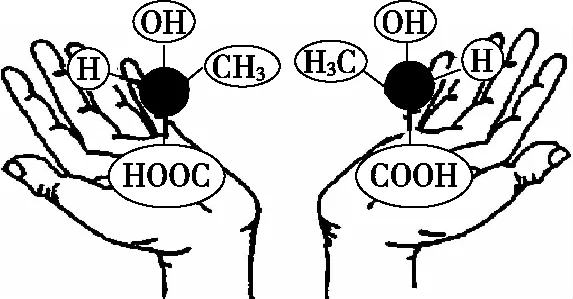
图3
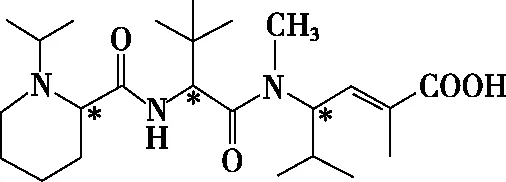
3.有机物原子的共面、共线
原子的杂化方式决定了分子的空间构型,是解决共面、共线问题的根本核心,同时可以借助分子模型加以理解。
①甲烷及烷烃
甲烷分子中碳原子采用sp3杂化,为正四面体构型的分子,键角为109°28′。在甲烷分子中,一个碳原子和任意两个氢原子可确定一个平面,其余两个氢原子分别位于平面的两侧,即甲烷分子中有且只有三原子共面(称为三角形规则)。当甲烷分子中某氢原子被其他原子或原子团取代时,取代该氢原子的原子可看作是在原来氢原子的位置。有机物分子中只要含有饱和碳原子,该碳原子采用sp3杂化,则所有原子不可能在同一平面。甲烷分子构型及球棍模型如图4和图5所示。
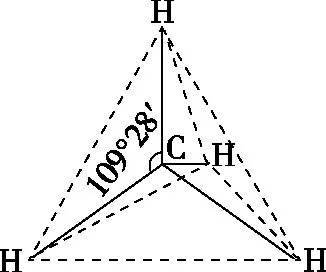
图4

图5
②乙烯及烯烃

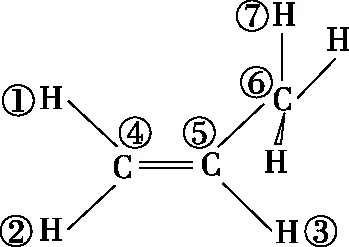
图6

③苯及芳香烃
苯分子中碳原子均以sp2杂化方式成键,如图7,苯分子中共有12个原子共面。当苯分子中的一个氢原子被其他原子或原子团取代时,取代该氢原子的原子一定在苯分子所在平面内。甲苯中甲基碳原子采用sp3杂化,所有原子不可能在同一平面。哪些原子可以在一个平面上呢?如图8,7个碳原子(苯环上的6个碳原子和甲基上的一个碳原子)、5个氢原子(苯环上的5个氢原子)这12个原子一定共面。此外甲基上1个氢原子(①H,②C,③C构成三角形)也可以旋转到这个平面上,其余两个氢原子分布在平面两侧。故甲苯分子中最多可能是13个原子共面。
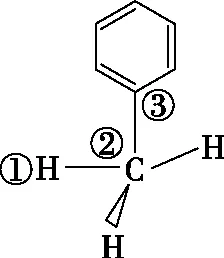
图8
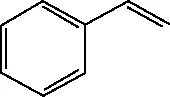
④乙炔及炔烃
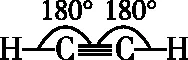
⑤多个平面(直线)连接
(二)全面掌握有机物结构与性质的关系
有机化学中结构决定性质体现得非常充分。教学中应该引导学生从定性、定量、定位、辩证等多角度全面掌握有机物结构与性质的关系。
1.从定性看
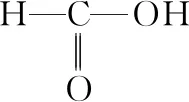
从物理性质看:烃一般是非极性或弱极性的分子。分子间的作用力比较小,因此烃的熔点、沸点比较低,碳原子数小于等于4的烃常温下为气态,烃一般难溶于强极性的溶剂水中;烃的衍生物随着官能团极性的增强,分子间作用力增大,其熔点、沸点都比相对分子质量相当的烃类要高,如乙醇的沸点为78℃,比相对分子质量相当的丙烷高出120.07℃;具有强极性的烃的衍生物,容易溶解在强极性的溶剂水中,如低碳原子的醇、醛、酸能与水互溶。
考题示例1的D项,分子中有碳碳双键,能发生加成反应,分子中含有甲基,能发生取代反应,D错误。考题示例2的A项,根据结构,“E7974”含有碳碳双键,可使Br2的CCl4溶液褪色,A正确。
2.从定量看
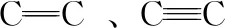
3.从定位看
对于给定有机物,我们有时候还要从定位角度进行思考,知道该有机物发生反应的部位以及原子或者原子团加到反应物的相关部位。
【考题示例3】(2022年浙江6月卷,15题)染料木黄酮的结构如图9,下列说法正确的是
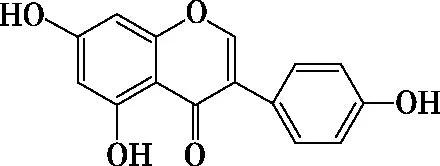
图9
( )
A.分子中存在3种官能团
B.可与HBr反应
C.1 mol该物质与足量溴水反应,最多可消耗4 mol Br2
D.1 mol该物质与足量NaOH溶液反应,最多可消耗2 mol NaOH
【答案】B
【分析】根据该物质结构简式可知分子中含有酚羟基、羰基、醚键和碳碳双键,共四种官能团,A错误;该物质含有碳碳双键,能与HBr发生加成反应,B正确;该分子中含有3个酚羟基,所以最多消耗3 mol NaOH,D错误。而解答C项时,要从定位角度考虑,该分子中酚羟基含有四种邻位或对位H,另外碳碳双键能和单质溴发生加成反应,所以最多消耗单质溴5 mol,C错误。
在有机学习中,我们还可以找到不少的这种定位思考。如醇类能催化氧化为醛、发生消去生成碳碳双键,但(CH3)3C—OH不能氧化成醛,CH3—OH、(CH3)3C—CH2—OH不能发生消去生成碳碳双键。这是因为醇的催化氧化是去掉—OH的氢以及和—OH相连碳上的一个氢。连有—OH的碳上有2个或2个以上氢原子时被氧化为醛,有1个氢原子时可被氧化为酮,(CH3)3C—OH中连有—OH的碳上不含 氢原子,不能发生催化氧化。醇发生消去反应时,与 —OH 相连的碳原子的邻位碳原子上必须有氢原子。(CH3)3C—CH2—OH中与羟基相连碳原子的邻位碳原子上没有氢原子,故不能发生消去反应。
4.从辩证看
结构决定性质,相同结构的有机物具有相似的性质,但由于有机物化学性质的“多面性”,具有相同结构的有机物在不同条件下可能发生不同的反应。所以分析有机反应,在首先考虑内因即物质结构的同时,还必须充分考虑外因,即反应条件对有机反应的影响。这种同时考虑内因和外因的思维就是辩证的思维。如乙醇与浓H2SO4共热至170℃,发生消去反应,主要生成乙烯;但若是140℃,则主要发生取代而得到乙醚。又如苯与Cl2在铁为催化剂时发生取代得到氯苯,但在紫外线照射时,则发生加成生成“六六六”(六氯环己烷)。卤代烃在NaOH醇溶液并加热时发生消去反应生成烯烃,但在NaOH水溶液并加热时发生水解反应生成醇。
甲醇、乙醇等易溶于水,苯酚不溶于冷水、可溶于热水,碳原子数较多的一元醇则不溶于水。从结构上来看,它们都含有羟基,羟基是亲水基团,有使它们溶于水的可能;但烃基是疏水基团,随着碳原子数的增多,疏水基团影响增大,使得碳原子数较多的一元醇不溶于水。这也包含着量变最终引起质变的辩证思维。
