创设情景,在实际应用中构建思维模型
——以平衡常数的考查和复习为例
2022-11-30新疆
新疆 吕 艳
平衡常数,是选择性必修课程中表征化学反应限度的物理量,是判断平衡状态、反应方向的重要依据。打通壁垒,构建平衡常数的思维模型,可以提高学生对化学反应规律认识的广度和思考的深度。本文梳理了2022年全国高考甲卷、乙卷中平衡常数的考查立意,结合几个真实的教学情景,尝试构建平衡常数的思维模型并利用该思维模型来解决实际问题。
一、关注基础,侧重相互转化和实际应用
2022年高考全国甲卷、乙卷中共有六处考查了平衡常数相关知识,分别是水解平衡常数大小判断、溶度积的计算、平衡常数在盖斯定律中的应用、平衡常数变式应用、平衡常数在弱电解质电离和沉淀转化中的应用。六处考查,笔者简单划分为单一应用、相互转化、综合应用三个能力层级,具体如表1.1、1.2、1.3所示:
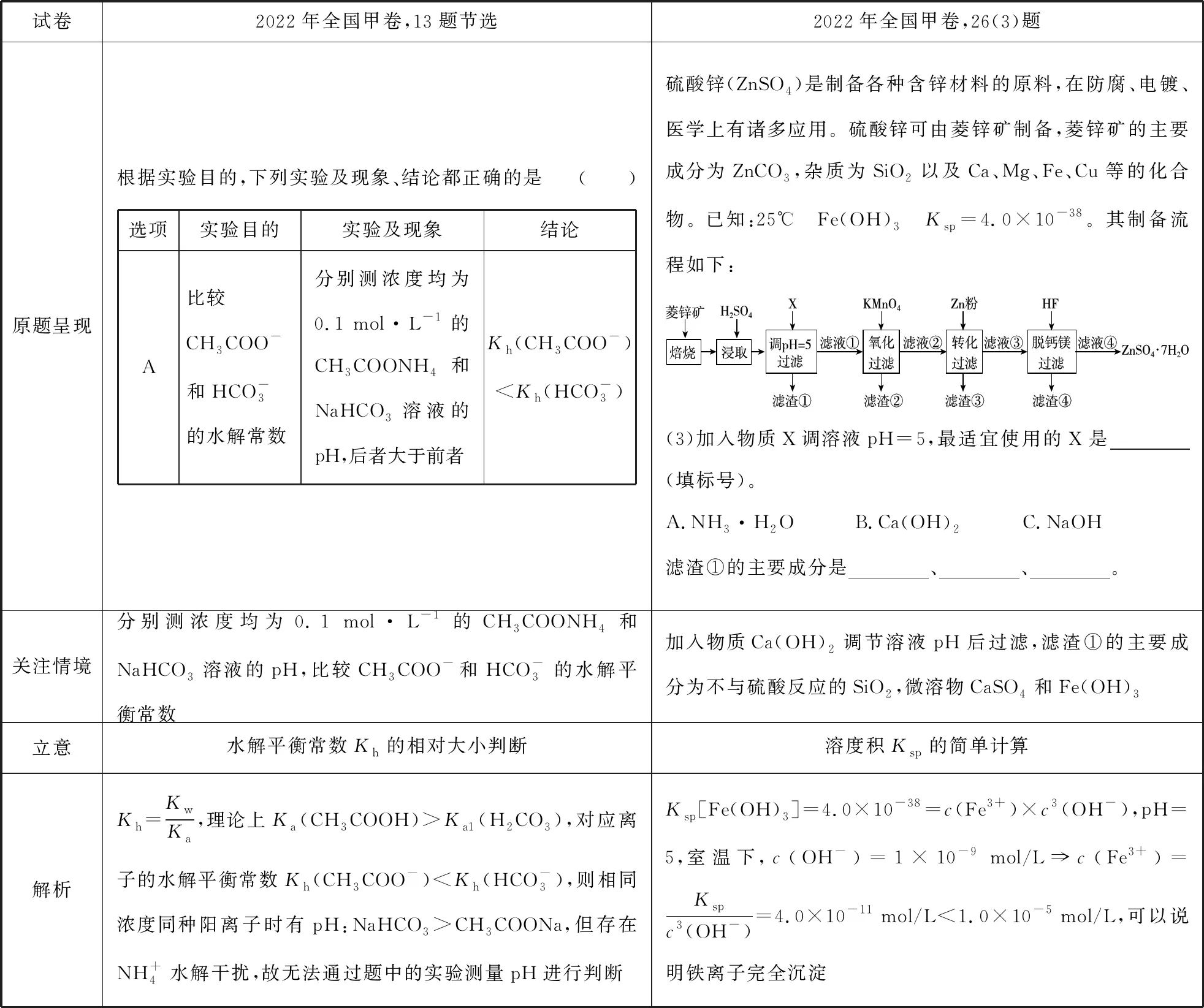
表1.1 平衡常数的单一应用
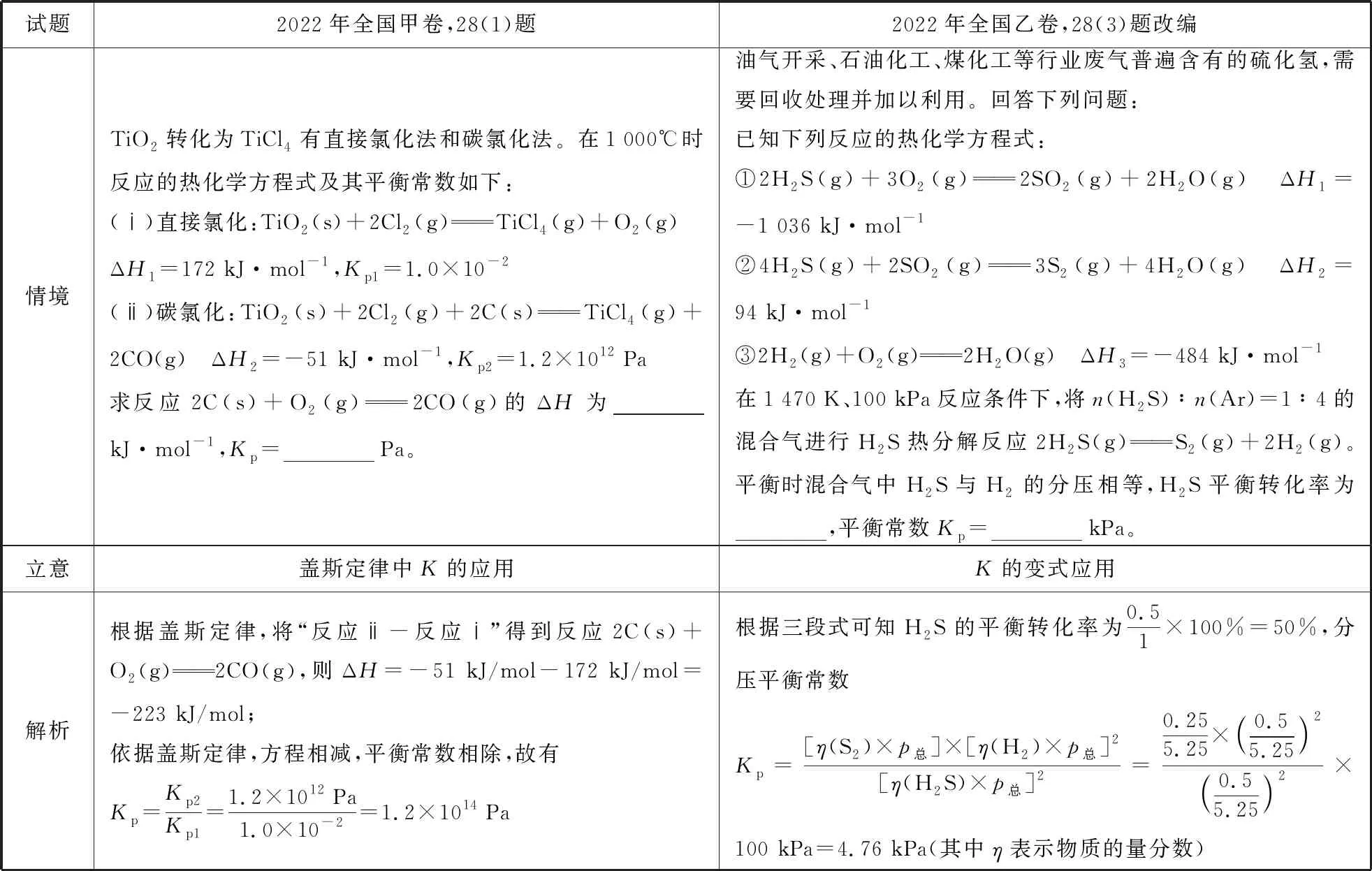
表1.2 平衡常数的变式应用

表1.3 平衡常数的综合应用
整体看,2022年高考全国甲卷、乙卷对平衡常数的考查注重基础,侧重平衡常数之间的相互转换,尤其关注在实际情景中应用平衡常数的知识解决问题。一轮复习需要帮助学生体会平衡常数在判断平衡状态、反应方向、分析预测平衡移动方向中的价值,即在巩固已有知识的基础上,结合学生困惑的问题创设真实的情景,在应用平衡常数解决问题中实现平衡常数思维模型的构建。
二、打通壁垒,多角度关注平衡常数在真实情景中的应用
(一)关注学生容易混淆的知识点,创设情景,一通百通
情景创设一:向少许碳酸钠溶液持续通入二氧化硫,反应发生的历程,用离子方程式该如何准确表达?
已知:两种酸的电离平衡常数:
H2CO3Ka14.5×10-7、Ka24.7×10-11
H2SO3Ka11.4×10-2、Ka26.0×10-8
请用电离平衡常数的相关知识进行反应历程的预判并完成对应离子方程式的书写。
【情景创设的目的】复分解反应中,涉及量的化学方程式书写,学生往往会比较纠结。这里给学生创设一个思考的情景,请学生利用电离平衡常数的视角来分析“酸与盐生成另外一种酸和盐”这一类型复分解反应发生的条件,并构建该类型复分解反应转化的思维模型。
【思维模型构建】
第一步:先判断反应的第一步是否发生,即
第二步:再判断反应的第二步是否发生,即
第一步K=3.0×108>1.0×105反应很彻底;
第二步K=3.1×104,接近1.0×105,也可认为反应较为彻底。
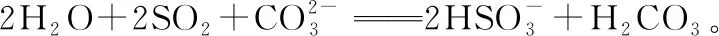
【拓展应用】将上述推演过程转化成为一种简单的判断方法:将电离平衡常数由大到小逐一排序,酸与一级电离的酸根上下对齐,用“N字型规则”进行判断。
举例:向碳酸钠溶液中加入足量的次氯酸溶液反应发生的历程。
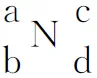
注:电离平衡常数的数据来自2019人教版化学选择性必修1教材附录
情景创设二:甲同学在完成新制氯水的成分的学习后,预测:向新制氯水中加入固体CaCO3可以增加次氯酸的浓度。请用溶度积和电离平衡常数的相关知识判断甲同学的预测是否正确?
已知1:两种电离平衡常数:
H2CO3Ka14.5×10-7、Ka24.7×10-11
HClOKa4.0×10-8
已知2:碳酸钙的溶度积常数:Ksp3.4×10-9
【情景创设的目的】碳酸钠会和次氯酸发生反应。但是,碳酸钙会不会与次氯酸反应?学生对此常常混淆。这里再创设一个情景,请学生利用电离平衡常数和溶度积常数来解决自身的困惑,以此来增加学以致用的成就感,增强一轮复习的自信心。
【思维模型构建】关键点:验证该反应发生的可能性。

推算该反应的平衡常数:
该反应的平衡常数K=2.6×10-7<1×10-5,该反应几乎不发生。
【拓展应用】请学生从反应竞争的角度思考:在次氯酸的环境中,碳酸根与氢离子结合与碳酸根与钙离子结合,哪一种趋势占主导?推理验证。
碳酸根与氢离子结合:
该过程的平衡常数:
该过程的平衡常数:
有K2>K1,故在次氯酸氛围中,碳酸根与钙离子结合的趋势占主导。
【结论】“向新制氯水中加入固体CaCO3,以增加次氯酸的浓度”是可行的。
(二)关注学生困惑的知识,创设情景,答疑解惑
情景创设三:实验室常用FeS与稀盐酸反应制备硫化氢气体。为什么CuS与稀盐酸不反应而FeS可以与稀盐酸反应?请利用溶度积和电离平衡常数的知识,梳理金属硫化物与非氧化性酸反应的条件。
已知1:电离平衡常数:H2SKa11.1×10-7、Ka21.3×10-13
已知2:两种硫化物的溶度积常数:FeSKsp6.3×10-18,CuSKsp6.3×10-36
【情景创设的目的】在人教版必修教材中,元素化合物的知识重在构建物质的不同类型的转化和不同价态物质之间的转化。教师可以在选择性必修模块学习完成后对个别必修课本中出现的问题进行复盘性验证和解答,将元素化合物知识与化学反应原理糅合以提高元素化合物知识的系统性和完整性。本情景选择硫化物与非氧化性酸反应作为一个突破点,梳理金属硫化物与非氧化性酸反应的条件。

利用平衡常数的变形:
带入硫化氢的电离平衡常数,可以推导出金属硫化物与非氧化性酸反应较为彻底的条件:金属硫化物的溶度积常数Ksp≥1.4×10-15。
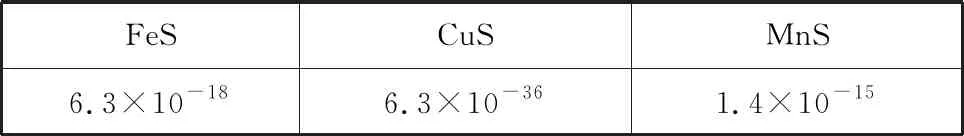
表2.2 三种常见硫化物的溶度积
【结论】FeS与稀盐酸反应时K=4.4×102,则FeS与MnS均可与稀盐酸反应制备硫化氢气体,同浓度的盐酸中,MnS反应更为彻底。
(三)关注教材,创设情景,反思与拓展兼顾
情景创设四:2019人教版化学选择性必修1第34页“探究浓度对化学平衡的影响”,以实验2-1为基础进行实验:向5 mL 0.005 mol/L 的FeCl3溶液中加入5 mL 0.015 mol/L 的KSCN溶液后,溶液呈红色。若向该体系中再加入少许氢氧化钠溶液。请你用化学平衡移动的知识预测反应的现象。
已知1:配位化合物的溶液中既存在配合反应,又存在离解反应,配合反应和离解反应最后达到平衡,这种平衡可称为配合平衡。

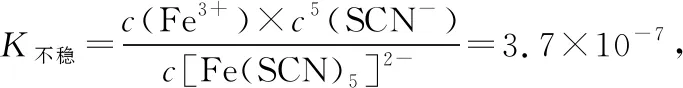
已知2:25℃ Fe(OH)3Ksp2.8×10-39
【情景创设的目的】挖掘人教版课本中的实验创设情景,将难溶电解质与配位化合物相互转化作为一个拓展思考点,学生通过提取信息获取新知识,结合已有知识在陌生情景中解决新问题,体现了“教、学、评一体化”的要求。
【思维模型构建】思维模型构建的历程:①原平衡体系会不会被打破?②如果打破,这种反应的趋势如何?

该反应的平衡常数为:
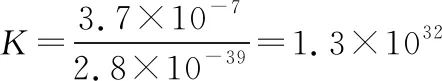
【深入思考】对比一下,同样是难溶电解质转化为配位化合物,两个实验中选取的氨水浓度不同。2019人教版化学选择性必修2第96页实验3-3“向4 mL 0.1 mol/L的硫酸铜溶液中加入几滴1 mol/L的氨水,首先形成难溶物,继续添加氨水并振荡试管,观察现象”。2019人教版化学选择性必修3第126页实验活动3中“用2%的硝酸银溶液、2%的氨水配制银氨溶液”。
已知1:K不稳[Cu(NH3)4]2+4.56×10-14、K不稳[Ag(NH3)2]+6.2×10-8
注:数据来自化学工业出版社《无机化学》附录
已知2:25℃KspCu(OH)22.2×10-20、AgOH 2.0×10-3
注:AgOH的溶度积常数数据来自化学工业出版社《无机化学》附录
问题抛出,引发学生的质疑和探寻究竟的求知心理。分析氢氧化铜转化为四氨合铜的反应

该反应的平衡常数
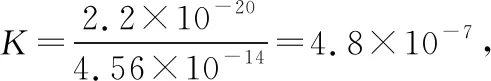

该反应的平衡常数
该反应的进行较为彻底,所以选择浓度较小的氨水就可以满足反应的条件。
用好教材,用好教材中的实例,对课本的实例进行情景再创设,比如酸碱指示剂的变色原理、氟化物防治龋齿的化学原理、铜蓝的形成,能帮助教师透过文字的表层含义,深入思考教材中每个实例承载的学科核心素养达成目标和育人功能。
高考试题在题干创设的情景下,需要满足基础性、综合性、应用性、创新性的要求,要求学生主动、灵活地应用已有知识来分析和解决问题。一轮复习,不仅仅要梳理基础知识、构建主干知识网络,还需要教师用好课本、用好高考真题,用学生的困惑点,积极创设情景,引领学生深入思考问题,用已有知识来解决问题,并在知识的实际应用中构建同一类型问题解决的思维模型,以实现知识融通应用、知识体系构建。每一次情景创设,都是对教材内容的二次研发,都是给学生创设一个思考的平台,让学生在这个平台上完成知识的重组和应用,在解决问题中完成学科能力的提升、学科核心素养的养成。所以,情景创设不是目的,知识应用是前提、学科能力养成是导向、学科核心素养提升是关键。
