锂离子电池超高镍正极材料的改性研究进展
2022-11-28李鸿峥许玉芬王延飞
李鸿峥,许玉芬,王延飞
(南华大学化学化工学院,湖南衡阳 421001)
锂电池作为新能源汽车重要支撑组分,良好的循环稳定性和宽泛的工作温度是衡量其性能的主要标准[1],而电池的正极材料决定着可充电电池的性能。富镍层状正极材料,如LiNiCoMn(NCM)与LiNiCoA(NCA),因容量高而备受关注[2]。一定程度上正极材料中的镍含量决定了电池容量,近些年,出现了超高镍含量(≥90%)的正极,相应减少了钴的含量,这种电池正极材料的研发成功对实现更高能量密度与低成本的锂离子电池具有重要意义。
超高镍正极材料在工作过程中,易形成微裂纹、Li/Ni混排、表面副反应等问题,而且形成程度较8系正极材料更为严重。目前的研究主要是通过掺杂修饰、包覆改性、单晶化、无钴化等方式来对超高镍正极材料进行改善,研究者在改善过程中,为提高电池稳定性,将钴离子或者锰离子换成其他能提高材料稳定性的离子,如Mg2+、Al3+、Zn2+等[3-5],这些离子有益于调整相间变化和结构演化,从而实现超高镍层状氧化物的稳定。
为此,本文简要分析超高镍正极材料容量衰退机理,并结合最新的国内外文献,阐述其多种改性策略,以期为超高镍正极材料的产业化生产提供参考。
1 超高镍材料的特征及性能
目前超高镍材料结构通式为LiNixCoyMnzO2或LiNixCoyAlzO2(x≥0.9),即α-NaFeO2型有序岩盐结构,结构形式为菱形面体R-3m[6]。Li占据八面体3b位点,Ni、Co和Mn占据八面体3a位点。整个晶体的形成是由[MO6]八面体层和[LiO6]八面体层交替叠加而成[7],在充放电过程中,锂离子在其中嵌入与穿出。
图1为不同镍含量的正极材料100次循环后的容量保持率与首次放电容量对比曲线[8]。从图中可以看出,随着镍含量的增加,其首次放电容量与容量保持率成反比。这是因为Ni2+的离子半径(0.069 nm)与Li+的离子半径(0.076 nm)近似,Ni2+很容易迁移至Li+位,导致阳离子混合。Li+和Ni2+这两个位点之间的阳离子无序排列会严重影响超高镍正极材料的结构稳定性。
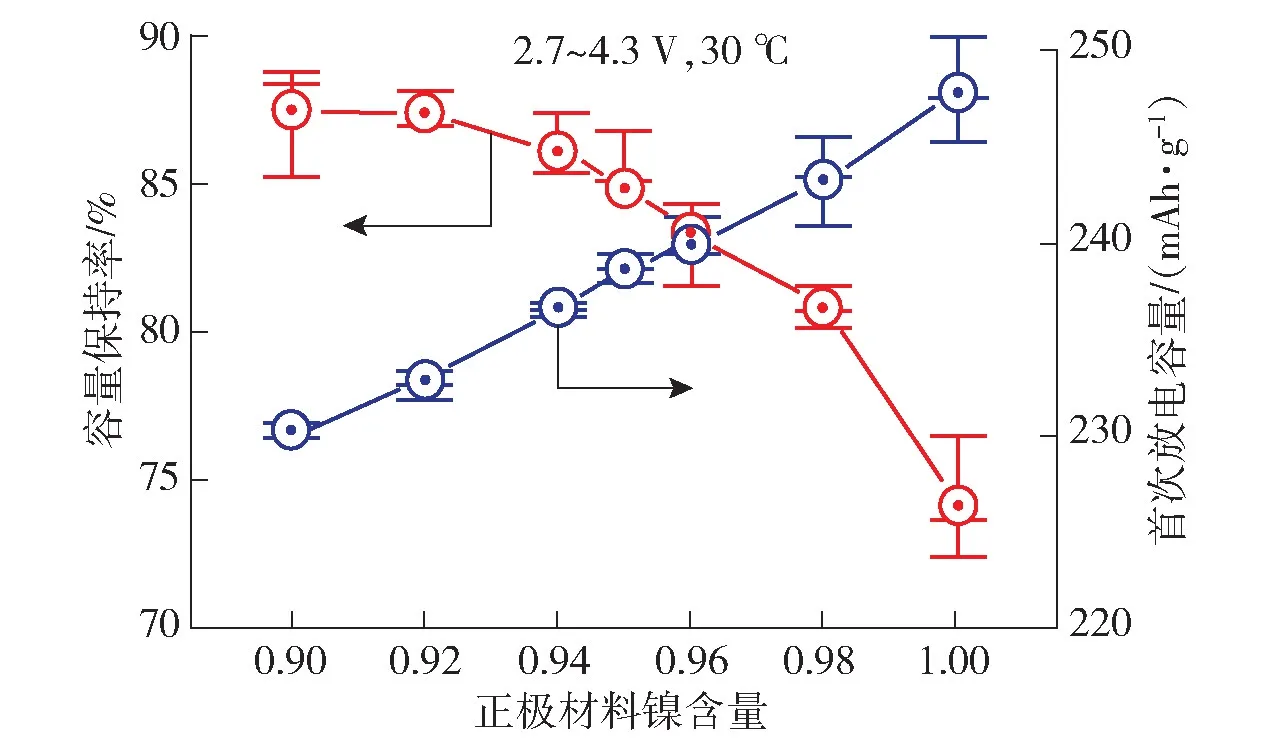
图1 不同镍含量的正极材料100次循环后的容量保持率和首次放电容量对比曲线Fig.1 Comparison curves of capacity retention rate and first discharge capacity of cathode materials with different nickel content after100 cycles
2 容量衰退机理
2.1 Li+/Ni+混排
超高镍正极材料在制备过程中,前驱体与锂混合进行烧结氧化时,Ni2+完全氧化为Ni3+极其困难,在超高镍正极材料中仍存在少量的Ni2+。在结构属性中,由于Ni2+与Li+离子半径差别不大,Ni2+很容易占据Li+的3b位点,导致Li/Ni混排,如图2(a)所示[6]。Li/Ni的混排不仅发生在材料的合成过程中,而且还发生在充放电过程中,很大程度上影响了超高镍材料的循环性能,特别是安全性能急速下降。在首次充电时,锂层中的Li+和过渡金属层中的Li+可以脱出,但在首次放电中,由于Li/Ni混排,Li+不能返回正晶格,导致库伦效率较低(通常低于90%),导致不可逆容量增加。
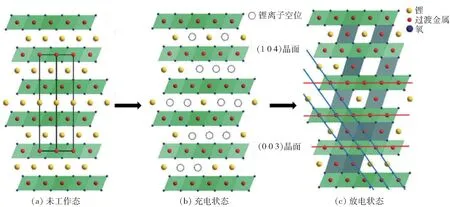
图2 Li+/Ni+混排过程图[6]Fig.2 Li+/Ni+mixed discharge process diagram
Zhao[9]等以Ni0.8Co0.2O2为研究主体,发现通过在烧结过程中改变温度、气氛、时间等因素,可以减少颗粒表面的锂损失和岩盐相的形成。优化后的高镍层状正极材料在工作电压(2.7~4.6 V)范围下比容量达到220 mAh·g-1以上,循环稳定性明显提高。
2.2 表面副反应
在合成超高镍正极材料时,往往需要在烧结过程中加入过量的锂源(LiOH、LiNO3或LiF)以应对锂源在高温下的损耗。但剩余的锂源往往以活性锂氧化物(Li2O、Li2O2)的形式黏附在材料表面,在环境空气中极易与空气中的H2O、CO2发生反应,生成氢氧化锂和碳酸锂层,即所谓“残余锂”[10]。这些残余锂会产生一些不良的影响:①残余锂导致正极材料表面高碱性(pH>11),引发聚偏氟乙烯(PVDF)黏合剂的脱氟化,这种行为会导致颗粒团聚,黏度急速增加,最终在正极涂布过程中形成凝胶,使正极力学性能恶化;②残余锂的生成过程加速了电解质(LiPF6)的分解,使颗粒表面附着一层氟化锂绝缘层,从而阻止Li+离子的扩散;③LiOH和Li2CO3在高压情况下易分解,导致比容量下降。
锂电池副反应的发生是从颗粒表面开始,有报道显示随着镍含量的提高,材料表面残余锂含量增多,受影响程度更大[10]。尽管“残余锂”会给超高镍正极材料的商业化带来危害,但Eyob[11]等发现当在NCM90中添加过量(4%锂)时,正极材料具有了良好的结晶度、较低的锂镍混排程度和更宽的Li+通道,能有效提高NCM90的速率性能和结构稳定性,如图3所示,图中L4-NCM表示4%锂过量的NCM90,其他同类表述类推。故优化超高镍正极材料中锂(过量)比例,可以减轻残余锂带来的限制,维护正极材料的稳定性能。
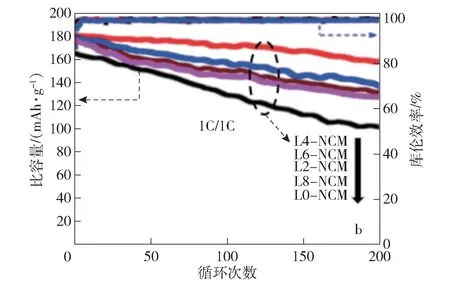
图3 不同锂过量NCM90在1C下循环200圈的性能曲线[11]Fig.3 Performance curve of NCM90 with different lithium excess at 1C for 200 cycles
2.3 不可逆相变
锂电池中镍含量增加会提高Li+与Ni2+相互迁移的概率,从而降低电池的稳定性,主要原因是在充放电过程中,随着锂离子的嵌入与脱出,发生了不可逆相变。当电压小于4.2 V时,由六方相H1→单斜相M→六边相H2转变;当电压大于4.2 V时,由六方相H1→单斜相M→六方相H2→H3转变。H2→H3为不可逆相变,该相变最初发生在粒子表面,随后传播到整体,随着厚度的增加,导致岩盐区形成,伴随结构降解,严重影响正极材料的循环稳定性。并超高镍正极材料的容量衰减主要取决于H2→H3的转变。
Wu等[12]采用共沉淀法合成了超高镍LiNi0.9Co0.1O2正极材料,发现掺杂Ti4+后正极材料减少了Li/Ni混排,并增强了H2→H3相变的可逆性,如图4所示。Ti4+最佳掺杂量为5 mol%,此时掺杂样品表现出良好的循环性能,在0.2C条件下,100次循环容量保留率从69.7%显著提高到97.9%。该试验结果表明,提高H2→H3相变可逆性的同时可实现超高镍正极材料的高容量与循环稳定性。
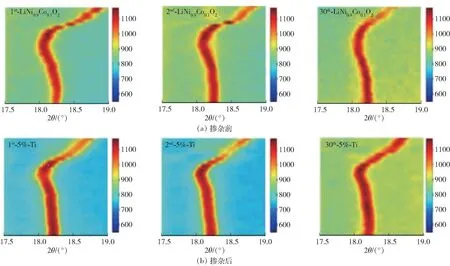
图4 5mol%Ti4+掺杂前、后在第1、2和30电荷周期原位XRD等高线图Fig.4 In-situ XRD contour map before and after doping 5 mol% Ti4+at the 1st,2nd and 30th charge cycles
2.4 微裂纹形成
超高镍正极材料在前驱体阶段主要是以共沉淀方法合成,而共沉淀法的实质是初级颗粒的聚集生成次级颗粒的过程,因为是随机性的原因,次级颗粒在合成过程中会受到不同程度的应力与变形。另外,正极在工作状态时导致微裂纹形成的原因有两方面:高压情况下,H2→H3不可逆相变形成,导致了体积变化较大;放电深度的范围决定了Li+迁移的程度,进一步影响整个充放电过程中的体积变化速率。这两方面均在各向异性的体积变化中起着作用,最终导致颗粒内部形成微裂纹。微裂纹的产生会引发阻抗的增加和活性物质的减少;同时,电解质也会渗透到裂纹中,降低电池的电化学性能。
Nam等[13]通过制备不同镍含量NCA,研究了高镍NCA正极的容量衰减现象。研究发现随着镍含量的递增,颗粒内微裂纹现象愈发严重,如图5所示。NCA80在100个循环后的初始比容量为202 mAh·g-1,容量保留率为91.3%;NCA95的初始比容量达到237 mAh·g-1,但其容量保留率仅为81.6%。微裂纹破坏了颗粒的内部完整性,导致电解质穿透颗粒核心,从而加速了内部初级颗粒的表面降解。
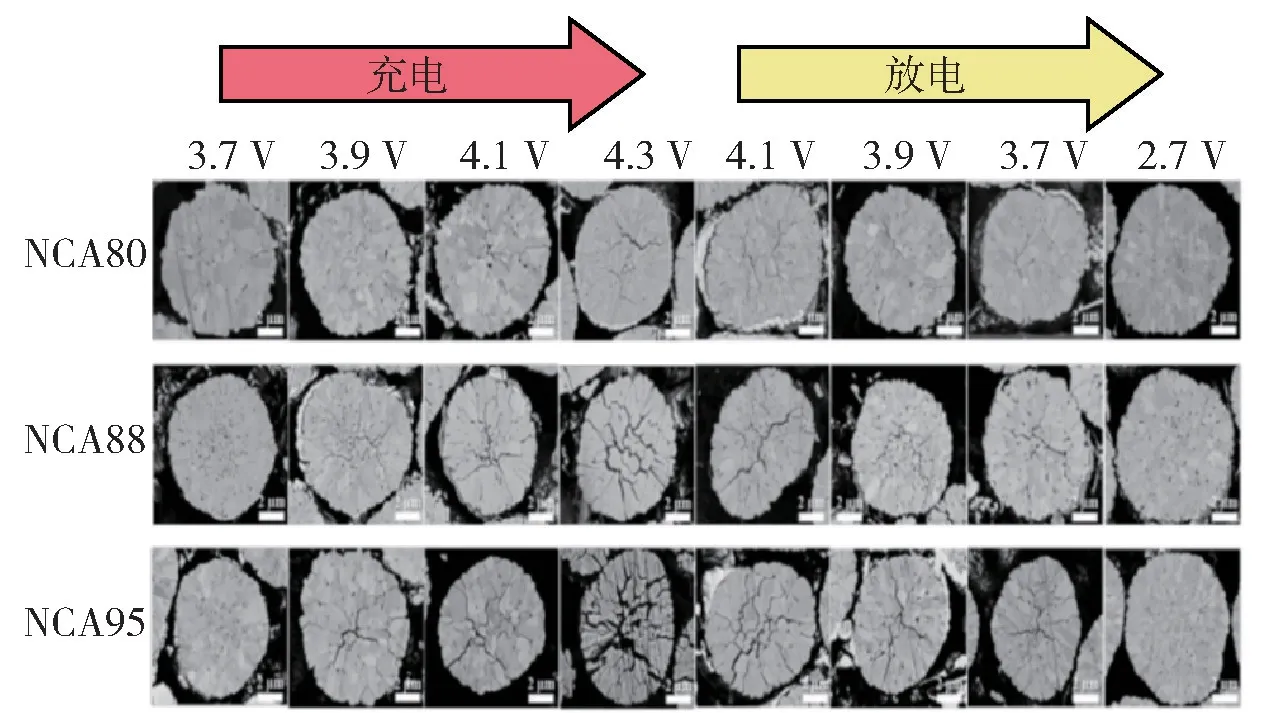
图5 比较不同SOC下NCA80、NCA88、NCA95正极材料Fig.5 Comparison of cathode materials of NCA80,NCA88 and NCA95 under different SOC
3 改性研究进展
3.1 掺杂改性
超高镍正极材料在循环过程容易发生微裂纹,特别是在高温或者高压下,这些裂纹会严重影响电池的稳定性能。为了减少其影响,大量研究人员通过掺杂各种元素来提高循环稳定性并提高电池容量。有研究表明,通过合理掺杂元素,取代Mn+或者Co+进行结构修饰,有助于降低Li+/Ni+混排程度,并会发挥每种元素特有的作用[14]。表1总结了各种元素掺杂提高超高镍正极材料电化学性能的数据汇总。
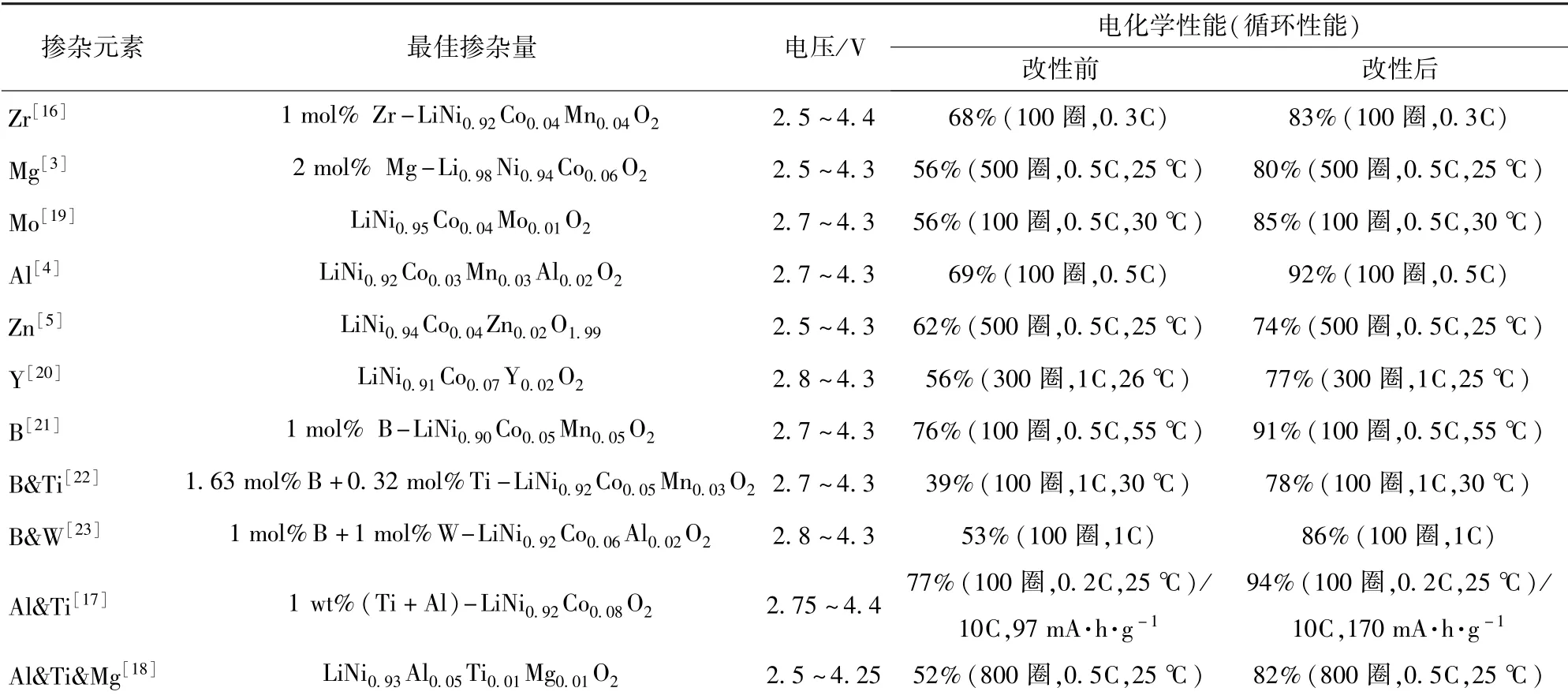
表1 超高镍正极材料元素掺杂改性电化学性能概述Table 1 Overview of electrochemical properties of ultra-high nickel cathode materials modified by element doping
3.1.1 单元素掺杂
对于单元素掺杂改性,Al元素对电池的性能影响较为显著。在超高镍正极材料中,Al元素往往以主元素的形式进行掺杂,其可以有效抑制晶格畸变与活性物质的溶解,极大提高循环稳定性[15]。Kim等[2]通过对NCM90进行铝元素掺杂,组成NCA89与NCMA89,发现当引入1%的Al时,可减少H2→H3相变过程中的体积收缩与膨胀,有效抑制微裂纹的形成;在1C、45℃条件下循环500圈,NCMA89容量保持率为82.6%,NCM90仅为53.8%。相较于铝掺杂,锆掺杂也是最为常用元素之一。Jung等[16]以共沉淀的方法合成了Zr掺杂富镍材料LiNi0.92Co0.04Mn0.04O2,在100个循环后容量保持率增加了15%,Zr掺杂对于晶格氧的稳定性起到了较大作用,可减少自身循环而造成的降解。
3.1.2 多元素掺杂
对比单元素掺杂,多元素掺杂的协同作用对于提升电池稳定性能更为显著。Ti4+和Al3+是稳定材料层状结构较为有效的掺杂剂。Wu等[17]对前驱体材料进行掺杂,先进行Ti4+掺杂,使其进入颗粒内部,然后在颗粒表面进行掺杂Al3+。与单纯的Ti4+掺杂相比,添加微量Al3+可有效分散Ti4+的分布,积极调节Ni2+的有序分布,从而减轻表面结构的随机组成,形成较薄的表面岩盐相重构层。这种表面结构结合了较强的Ti—O和Al—O键,能够实现可逆的H2→H3相变,进一步抑制微裂纹的形成。Cui等[18]以NC94与NCM90为参照,研究Al、Ti、Mg共掺杂对NATM93性能影响,如图6所示,研究发现,钛富集在表面,铝、镁作为NATM中的稳定离子元素,不仅能改善电解质和结构不完整性的不良副作用,而且还能减轻石墨阳极上的过渡金属溶解和活性锂的损失,在全电池800个深循环后,仍具有82%的容量保留率,优于94NC与90NCM。
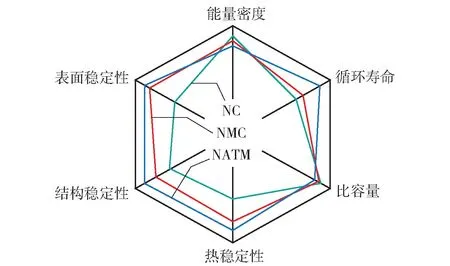
图6 多重元素掺杂对超高镍正极材料的性能影响Fig.6 Effect of multi-element doping on the performance of ultra-high nickel cathode material
3.2 表面包覆
岩盐相和残留锂的形成原因是Ni2+引起的颗粒表面的相对不稳定。通过表面涂层降低材料表面的Ni2+含量是解决问题的关键,并且要求涂层材料具有良好的Li+传输性能,否则会影响自身的容量大小。正极材料表面涂层有两方面作用:一方面,涂层能够提高材料电子导电性[24];另一方面,涂层材料能够减少正极材料与电解液之间的直接接触面积,阻止电解液的分解与副反应的生成,进一步防止正极材料被腐蚀导致晶体结构坍塌。以上两方面作用都会显著提高电池的电化学性能。
Kim等[25]以NCM91为基体,通过干法包覆方式在颗粒表面分别构建铝、铁、钴、钛涂层,研究4种离子涂层对于NCM91的电化学性能提升效果。研究发现,在各种金属离子中,虽然钛离子和铁离子涂层确实降低了NCM91中残留的锂含量,但涂层加剧了Ni3+的还原,导致Li+/Ni+混排更为严重,电化学性能下降更为严重,尤其是钛离子涂层的NCM91在经过100次0.5C循环后,容量保持率仅为78%,而纯相容量保持率为84%,如图7所示。对比之下,铝离子和钴离子涂层能够减少表面残留锂,并且减少Ni3+→Ni2+的还原转变。通过相关表征手段分析,发现钴离子涂层对提升正极材料的稳定性能更有效,因为钴离子涂层可以促进颗粒Ni3+稳定性,导致岩盐相和残留锂减少。目前,钴离子涂层被确定为基于相互扩散的表面重建策略的最佳涂层。Qian等[26]采用预涂层和同步锂化法,在富镍阴极材料LiNi0.9Co0.05Mn0.05O2上均匀包覆锂离子导体Li2SiO3层,在2C倍率下100次循环后容量保持率为88%,而未包覆纯相保持率仅为79%。通过多种物理表征技术发现,Li2SiO3包覆层改善了电极的锂离子扩散动力学,并防止其在电解质表面发生副反应;此外,具有强Si—O共价键的均匀Li2SiO3涂层作为缓冲层,降低了机械微应变,稳定了表面化学性能和结构。
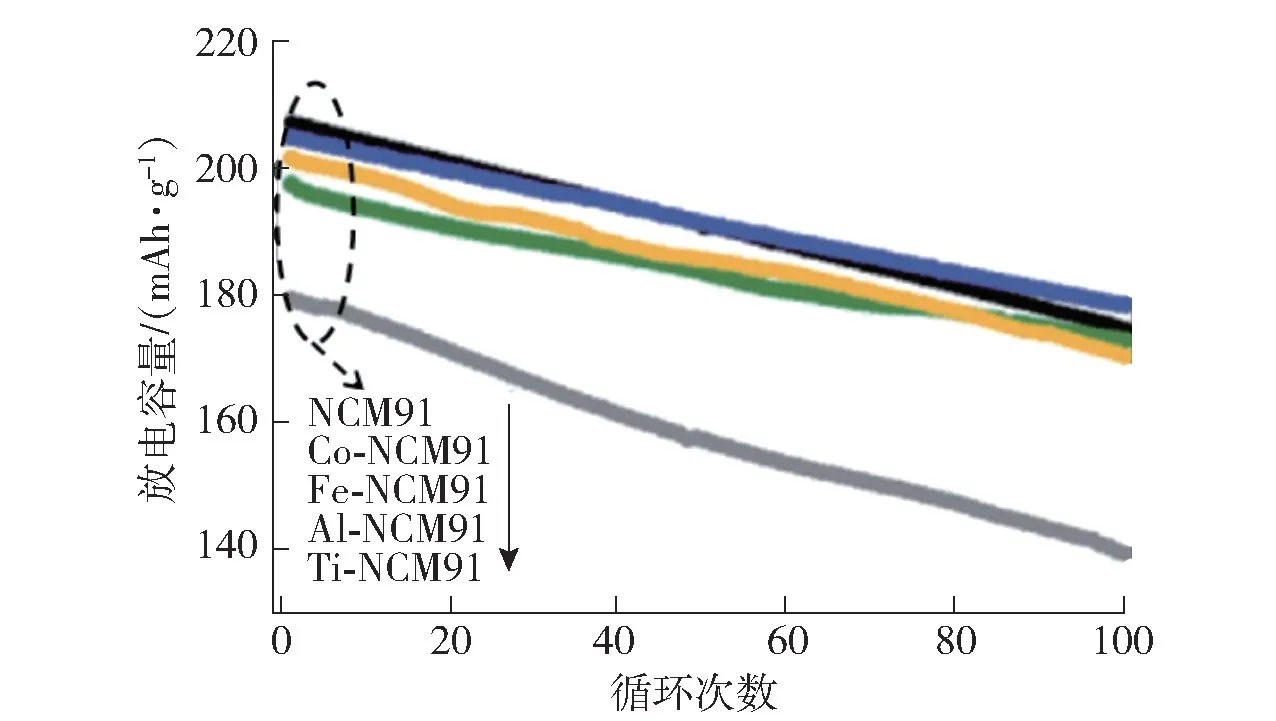
图7 0.5C下不同元素包覆NCM91循环100圈的性能曲线[25]Fig.7 Performance curve of NCM91 coated with different elements for 100 cycles at 0.5C
3.3 形态设计
目前对于超高镍正极材料的形态设计,主要偏向核壳结构。相对于包覆改性来说,核壳结构可以看成为高级版的包覆手法,本质上还是在颗粒表面包覆一层保护膜。
包覆改性主要以金属氧化物为包覆材料,往往电导率较低,导致容量降低,此外,由于表面涂层非常薄,因此很难完全保护内部材料免受与电解质发生副反应,使得超高镍正极材料的容量衰退和热稳定性较差问题更为严重,而核壳结构能有效解决这些问题。
Maeng等[27]采用以LiNi0.9Mn0.05Co0.05O2为核心,在表面附着一层LiNi0.33Mn0.33Co0.33O2的壳,采用共沉淀法成功合成了高镍核壳结构的NMC811材料,整体组成为LiNi0.8Mn0.1Co0.1O2,类似于商业均匀的NMC811。SEM与EDS横截面图和线扫描表明,核壳结构粒子从粒子中心到表面的局部成分变化与设计的粒子结构一致;当煅烧温度从700℃升高到800℃,核壳结构NMC811材料的主颗粒层变厚。经过200次循环后,商业化的NMC811的二次粒子被完全粉碎,而核壳结构的NMC811粒子大多保持其最初的球形形态;核壳结构NMC811容量保持率为81.1%,而商业化NMC811仅为39.6%。试验结果表明,核壳结构的超高镍正极材料具有明显改进的热稳定性、机械强度和高容量保持率,有望进行批量生产。Kim等[28]提出了一种核心部分为超高镍LiNi0.934Co0.043Al0.015O2(NCA),外层壳部分为LiNi0.886Co0.049Mn0.05Al0.015O2(NCMA)的正极材料,组装电池后发现,在3.0~4.2 V下循环1 000圈后,NCA-NCMA90正极显示90.5%的优越容量保持率,而NCA90正极只保持60.2%的初始容量(图8)。研究认为外壳部分的存在加速了锂的插入和纳米核心主粒子偏转,抑制了充放电过程中正极固有各向异性体积变化产生的微裂纹传播。
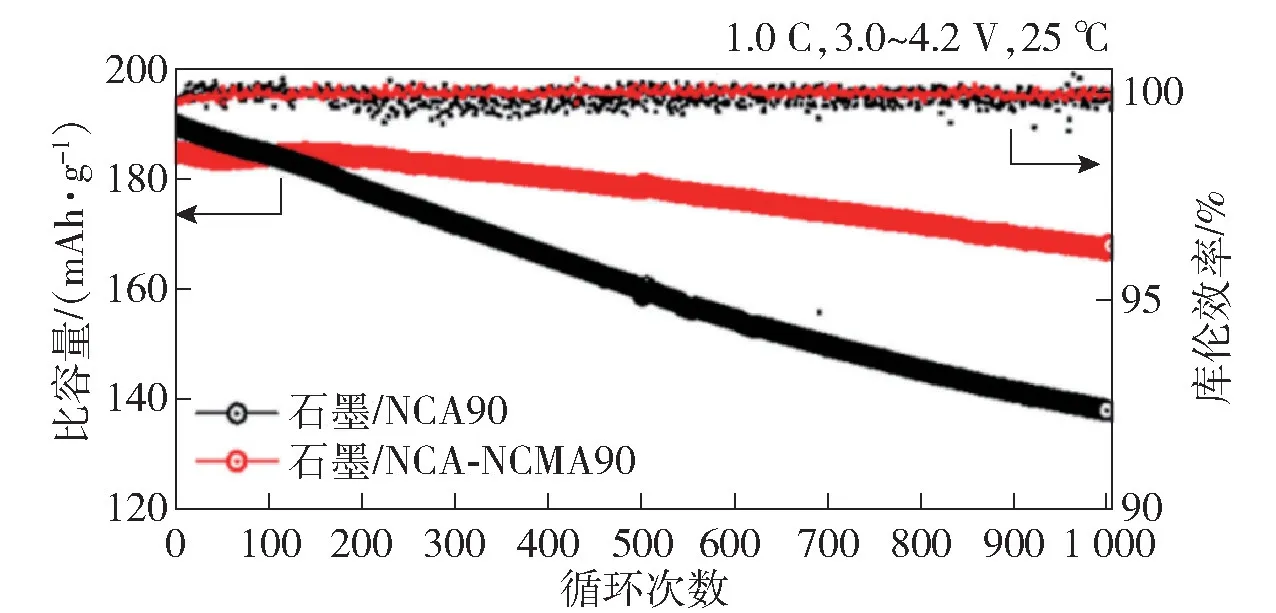
图8 在1C、3.0~4.2 V、25℃下NCA90与NCA-NCMA90在全电池中循环1 000圈的性能曲线[28]Fig.8 Performance curves of NCA90 and NCMA90 after 1 000 cycles in the whole battery at 1C,3.0~4.2 V and 25℃
3.4 晶体设计
据研究报道[29],氧化物正极在高压充电时可以适当提高比容量,但电压的增加会加剧材料的分解,严重影响电池的安全性能。一般认为,富镍阴极材料从层状结构向尖晶石或完全无序的岩盐结构的转变以及过渡金属的溶解与结构重建,导致了容量衰减。试验可以观察到,非均匀应力会在循环过程中引起晶粒内裂纹,从而加剧超高镍正极材料结构的坍塌和容量损失[29]。普遍的改性方法包括掺杂和涂层,其可以抑制锂镍混排和界面副反应,但过量的涂层和不受调节的掺杂可能会阻碍Li+的迁移,从而影响电池的电化学性能。为了解决以上问题,可以采用普遍适用的策略来提高正极的结构稳定性。单晶化的出现,为超高镍正极材料的商业化提供了另外一种方向。
单晶材料具有较高的结晶度、更稳定的层状结构,因此有良好的循环性能和热稳定性能。Ni等[30]通过熔融盐辅助法制备83单晶、88单晶、95单晶。Ni含量大于88%后,锂镍混排和H2→H3相变加剧,导致高速率循环中结构严重坍塌和容量下降,95单晶正极在5C下250次循环后的容量保持率较差,仅为51.8%,而83单晶为78.2%,88单晶为68.3%。Ryu等[31]将镍含量分别为70%、80%和90%的NCM三元正极材料分别制备成单晶与多晶,通过对比性能试验,发现多晶正极材料与单晶正极材料容量衰落的机制不同:多晶正极材料容量的快速衰落主要归因于微裂纹的形成,因电解质的渗入导致岩盐相积累;相对于多晶材料,单晶锂离子扩散途径有限,避免锂离子浓度在循环过程中趋于不均匀,对比掺杂与包覆,单晶化未引入其他元素,降低了成本与工艺的难度。
4 结论与展望
4.1 结论
本文简要分析了超高镍正极材料容量衰退机理,并结合国内外文献,对元素掺杂、表面包覆、形态设计及晶体设计等改性手段进行了总结。
1)导致超高镍正极材料容量衰退的机理主要包括:Li+/Ni+混排造成不可逆容量增加;材料表面残余锂发生副反应导致正极力学性能恶化,形成绝缘层阻止Li+离子的扩散,LiOH和Li2CO3分解,导致比容量下降;H2→H3不可逆相变导致岩盐区形成;微裂纹的形成导致阻抗增加和活性物质减少。
2)掺杂改性方法包括单元素掺杂和多元素掺杂。单元素掺杂方法中,Al元素可以有效抑制晶格畸变与活性物质的溶解,极大提高循环稳定性,对电池的性能影响较为显著;锆掺杂对于晶格氧的稳定性起到了较大作用,也是最为常用元素之一。多元素掺杂的协同作用对于提升电池稳定性能更为显著。
3)表面包覆可以提高材料电子导电性,减少正极材料与电解液之间的直接接触面积,防止正极材料被腐蚀导致晶体结构坍塌,提升材料的电化学稳定性能。
4)形态设计方法目前的主要技术是核壳结构,本质上还是在颗粒表面包覆一层保护膜,能够保护内部材料免受与电解质发生副反应,保障正极材料的容量和稳定性。
5)晶体设计主要是指将高镍正极材料通过熔融盐辅助法制备成单晶材料,来提高结构稳定性。
4.2 展望
上述提到的改性手段在一定程度上会提高超高镍正极材料的循环稳定性,但仍然存在能量密度与结构稳定不匹配问题以及如何从实验室阶段到大规模产业化生产等问题。因此,未来超高镍材料的研究还需在以下几方面开展。
1)通过引入其他元素来降低钴离子含量。深入探究替代元素影响机制、掺杂量范围及其掺杂工艺,以改善能量密度与结构稳定不匹配问题。
2)有机结合多种改性方法,如掺杂与包覆、掺杂与核壳结构、包覆与单晶化等;提出可靠的复合改性机理与失效机理,解决产业化的可行性问题。
3)紧密联系生产实践,改性后超高镍材料需通过小试、中试及试生产阶段,各过程中要逐步调控、优化生产参数,最后出具详细可行的标准文件。
