魔芋花叶病毒衣壳蛋白的原核表达和多克隆抗体制备
2022-11-28唐国亮张玉宝王若愚王亚军苏学思金卫杰
唐国亮,张玉宝,王若愚,王亚军,赵 霞,苏学思,金卫杰
(1.中国科学院 西北生态环境资源研究院 皋兰生态与农业综合试验站,甘肃 兰州730000; 2.甘肃省生态农业综合试验野外科学观测研究站,甘肃 兰州730000; 3.中国科学院大学,北京100049)
魔芋花叶病毒(Konjacmosaicvirus,KoMV)是1990年由Shimoyama等[1]在日本的魔芋(AmorphophalluskonjacK. Koch)中首次发现的一种新病毒。该病毒是马铃薯Y病毒科(Potyviridae)马铃薯Y病毒属(Potyvirus)成员,在电子显微镜下可观察到弯曲杆状的病毒颗粒,其大小长为800~900 nm,宽为13 nm[2]。KoMV基因组由一条正义单链RNA组成,长度为9 544 nt,编码一个大小为350 ku(3 087 aa)的多聚蛋白质,在蛋白酶的作用下被加工成多种蛋白质,分别为P1蛋白、HC-Pro蛋白、P3蛋白、6K1蛋白、CI蛋白、6K2蛋白、Nia蛋白、Nib.VPg蛋白、Nib.Pro蛋白以及CP(capsid protein,CP)蛋白[2]。研究表明,马铃薯Y病毒属的CP蛋白具有较强的免疫原性,这对于病毒生存和侵染寄主的过程中发挥着重要的作用[3]。魔芋花叶病毒与日本金鱼藻花叶病毒(Japanesehornwortmosaicvirus,JHMV)、马蹄莲花叶病毒(Zantedeschiamosaicvirus,ZaMV)同为马铃薯Y病毒科马铃薯Y病毒属成员,根据国际病毒分类委员会(ICTV)第8次报告关于马铃薯Y病毒科的分类标准,KoMV、JHMV、ZaMV属于同种病毒的不同分离物[4]。
根据已报到文献和GenBank数据库中的信息显示,KoMV的宿主主要为天南星科和伞形科的植物,如天南星科的马蹄莲和魔芋,伞形科的鸭儿芹、明日叶和大阿米芹[5-7]。目前KoMV已经在日本、印度、匈牙利等多个国家出现[8-10]。我国于2007年在水半夏中首次检测到KoMV病毒[11],随后在当归中也检测到,不过甘肃岷县当归中该病毒以JHMV分离物的形式出现[4,12]。KoMV是当归重要的病害之一[12],受KoMV侵染的当归,前期症状主要表现为花叶、斑驳、黄化、皱缩等,后期叶片出现深褐色斑点以及生长缓慢、植株矮化、严重坏死等症状(图1)。

图1 健康(A)及感染Konjac mosaic virus的田间当归植株(B , C)Fig.1 Healthy Angelica sinensis plants (A) and Angelica sinensis plants infected by Konjac mosaic virus (B and C)
KoMV主要通过蚜虫以非持久性的方式进行传播,病毒颗粒积累在球茎当中,不仅对已感染的作物造成严重的危害性,同时加速病毒向其他作物的传播[5]。为有效控制KoMV的危害以及加强KoMV病毒在田间诊断和监测的防治措施,迫切需要开发出快速、高效、特异、灵敏的病毒检测技术。目前,国内外对KoMV的检测多采用RT-PCR法[11,13],该方法具有特异性强、灵敏度高的特点,但是操作复杂、需要专业的技术人员和昂贵的仪器设备限制了该方法的推广应用。酶联免疫吸附法(ELISA)在KoMV病毒检测中也有应用[14],该方法操作简单,可以在田间快速检测大批量样品。相比于将直接纯化的病毒粒子作为抗原,通过构建目的基因原核表达载体制备的抗原,有效提高了抗原的浓度和纯度,并且制备的抗体具有更高的特异性和效价[15-16]。与传统的植物病毒检测方法相比,小RNA测序技术(small RNA sequencing,sRNA-seq)不仅可以同时鉴定出多种RNA或DNA病毒,还可以发现新病毒或新的分离物[17-20]。
本研究应用小RNA测序技术分析了甘肃省榆中县疑似病毒感染的当归样品,结合RT-PCR验证测序结果,克隆了KoMVcp基因并进行序列分析,构建了KoMVcp基因的原核表达载体,转化E.coliRosettaTM(DE3)菌株诱导表达,在Ni-NTA重力柱层析作用下纯化CP融合蛋白,并以此为抗原制备了特异性良好的多克隆抗体,以期为KoMV的血清学检测技术和CP蛋白的功能研究提供一定的参考。
1 材料与方法
1.1 材料
2020年7月10日在甘肃省榆中县马坡乡阳屲村(35°46′N,104°1′E,海拔2 422 m)、马坡村(35°47′N,103°59′E,海拔2 601 m)、趟窑村(35°47′N,103°58′E,海拔2 730 m)、河湾村(35°46′N,104°00′E,海拔2 514 m)、羊上村(35°47′N,103°57′E,海拔2 653 m)和银山乡(孙家湾村(35°51′N,103°50′E,海拔2 096 m))采集疑似感染病毒病的当归样品24份,将采集的样品分别取少量混合进行小RNA测序,其他样品放于-80 ℃保存备用。
本实验所用的逆转录试剂盒(PrimeScriptTMRT Reagent Kit)、TaqDNA聚合酶、DNA回收试剂盒(Agarose Gel DNA Fragment Recovery Kit)、T4 DNA连接酶和克隆载体pMDTM19-T均购自宝生物工程(大连)有限公司(TaKaRa);植物总RNA提取试剂盒(RNAprep Pure Plant Kit)购自天根生化科技(北京)有限公司;BCA蛋白定量试剂盒和植物蛋白提取试剂盒购自上海贝博生物科技有限公司;质粒微量抽提试剂盒购自Omega公司(E.Z.N.A.®Plasmid DNA Mini Kit Ⅰ);Ni-NTA预装重力柱(Ni-NTA Pre-Packed Gravity Column)、NBT/BCIP碱性磷酸显色试剂盒(蓝色)购自生工生物工程(上海)股份有限公司;限制性内切酶购自NEB(北京)有限公司;E.coliDH5α、E.coliRosettaTM(DE3)购自北京全式金生物技术(TransGen Biotech)有限公司;表达载体pET-28a(+)由本实验室保存;其他化学试剂均为国产化学纯。
1.2 方法
1.2.1 当归小RNA测序
小RNA测序及分析委托生工生物工程(上海)股份有限公司完成。采用Total RNA Extractor(Trizol)试剂盒提取疑似感染病毒混合样品的总RNA(具体方法参照试剂盒说明书),并应用Qubit2.0检测RNA浓度,琼脂糖凝胶检测RNA完整性以及基因组污染情况,获得满足后续文库构建的RNA样本。根据小RNA具有3′端羟基及5′端磷酸基的结构特点,利用相关酶催化反应及分子生物学技术对当归叶片的小RNA进行3′端和5′端接头连接,合成cDNA单链。之后通过文库扩增、文库质检及定量混合获得满足Illumina平台测序的文库。通过小RNA测序及分析确定混合样品中可能存在的病毒种类。
1.2.2 植物总RNA提取与病毒RT-PCR验证
为验证小RNA测序结果,根据测序得到的KoMVcp基因序列,采用Primer Premier 5设计如下序列的特异性引物(下划线表示引入的酶切位点EcoRⅠ和HindⅢ):F:5′-GAATTCAATGGGGAAGAGGAAAAGG-3′;R: 5′-CAAGCTTGATAGCGCGCACACCCAT-3′。以上引物均由生工生物工程(上海)股份有限公司合成。
以疑似感染KoMV病毒的当归叶片为材料,用植物总RNA提取试剂盒提取总RNA。用提取的总RNA为模板,参照逆转录试剂盒说明书合成KoMV第一条cDNA链,再以所得cDNA链为模板PCR扩增KoMVcp基因。PCR反应体系为:2.5 μL 10×PCR Buffer,2.0 μL dNTPs(各2.5 mmol·L-1),上下游引物各0.5 μL(10 μmol·L-1),0.2 μLTaqDNA聚合酶(5 U·μL-1),2.0 μL cDNA,ddH2O补充体积至25 μL。PCR反应程序为:94 ℃预变性4 min;94 ℃变性30 s,60 ℃复性50 s,72 ℃延伸1 min,循环扩增35次;最后72 ℃延伸7 min。PCR产物以1.5%的琼脂糖凝胶电泳进行检测,通过DNA回收试剂盒纯化目的片段。
1.2.3 重组克隆载体的构建
纯化的目的片段连接pMD19-T克隆载体,转化E.coliDH5α感受态细胞。用质粒微量抽提试剂盒提取重组质粒,经PCR和酶切验证正确后送北京擎科生物科技有限公司进行测序。获得的序列应用BLAST进行序列比对,证实序列正确后命名为pMD19-T-KoMV。应用MEGE 5软件对KoMV病毒的不同分离物采用ClustalW进行多序列比对,以邻接法(N-J法)构建系统进化树。
1.2.4 原核表达载体的构建
将pMD19-T-KoMV质粒和pET-28a(+)质粒分别用限制性内切酶EcoRⅠ和HindⅢ双酶切,酶切产物在T4 DNA连接酶作用下16 ℃过夜连接。连接产物转化E.coliDH5α感受态细胞,涂布于含有氨苄青霉素的LB平板。PCR筛选阳性克隆,然后扩大培养阳性菌落。用质粒微量抽提试剂盒提取重组质粒,经限制性内切酶EcoRⅠ和HindⅢ双酶切、1.5%琼脂糖凝胶电泳检测正确后命名为pET-28a-KoMV。
1.2.5 KoMV CP蛋白的原核表达
取pET-28a-KoMV重组阳性质粒转化E.coliRosettaTM(DE3),PCR鉴定阳性菌落。挑取阳性菌落接种于20 mL含50 μg·mL-1Kana的LB液体培养基中,37 ℃,180 r·min-1摇床振荡培养过夜。次日按1∶100接种3个相同的培养基,37 ℃培养至D600达到0.6,之后分别加入至终浓度为0.5 mmol·L-1的IPTG诱导剂,在16、28和37 ℃分别诱导20、10、4 h收集菌体,超声破碎分别取上清和沉淀进行SDS-PAGE电泳,鉴定KoMV CP融合蛋白可溶性以及不同温度对诱导蛋白表达量的影响。
为获得纯化的KoMV CP融合蛋白,16 ℃大量诱导1.2 L菌体。收集的菌体经0.1 mol·L-1PBS溶液悬浮、超声破碎、离心等步骤后,取沉淀按照Ni-NTA重力柱操作指南纯化目的蛋白。纯化后的目的蛋白经SDS-PAGE电泳后做蛋白质谱鉴定,鉴定由北京华大蛋白质研发中心有限公司完成。
1.2.6 KoMV CP多克隆抗体的制备
选择饮食正常、皮毛光泽、检疫健康的新西兰大耳白兔进行免疫。具体免疫过程为:将纯化的KoMV CP融合蛋白(2.5 mg·mL-1)作为免疫抗原与弗氏完全佐剂(基础免疫)或弗氏不完全佐剂(加强免疫)充分乳化后分别在兔的背部皮内多点注射。共免疫4次,免疫量为每次每只1 mg,每次免疫的时间间隔为21 d,第4次免疫后14 d 取全血,分离得到兔抗血清。通过间接ELISA测定抗体效价,并取5 mL兔抗血清,用Protein A亲和层析柱纯化,获得兔抗KoMV多克隆抗体IgG。
1.2.7 KoMV CP多克隆抗体的鉴定
分别取100~200 mg健康当归叶片、感染百合无症状病毒(Lilysymptomlessvirus,LSV)、黄瓜花叶病毒(Cucumbermosaicvirus,CMV)、车前草花叶病毒(Plantagoasiaticamosaicviris,PLAMV)和百合斑驳病毒(Lilymottlevirus,LMoV)的百合叶片、感染莴苣坏死黄化病毒(Lettucenecroticyellowsvirus,LNYV)的生菜叶片、感染马铃薯Y病毒(PotatovirusY,PVY)的马铃薯叶片、感染KoMV的当归叶片于研钵中加入液氮研磨至粉状,用植物总蛋白提取试剂盒提取蛋白。取80 μL不同病毒叶片的提取蛋白和KoMV CP的纯化蛋白于1.5 mL EP管中,并分别加入20 μL 5×上样缓冲液,煮沸变性后做SDS-PAGE电泳,切胶并采用湿转法15 V恒压25 min将目的蛋白转移至PVDF膜,后用封闭液于4 ℃封闭过夜。以制备的兔抗KoMV CP多克隆抗体作为一抗(1∶2 000),AP标记的羊抗兔IgG作为二抗(1∶5 000),将膜放入加厚的一次性PE手套中,分别加入一抗和二抗于室温摇床上孵育1.5 h,后通过NBT/BCIP碱性磷酸显色试剂盒(蓝色)进行显色。
2 结果与分析
2.1 当归小RNA测序结果与RT-PCR验证
应用SPAdes序列拼接软件对小RNA测序结果的reads片段进行拼接,结果显示,拼接共得到291个contigs且序列长度均大于110 nt。根据比对结果,有23个contigs可以比对到2种病毒序列,其中有1个contigs可以比对到KoMV病毒序列,序列长度为6 287 nt,同源性为99.14%,另外22个contigs比对到另外一种病毒。
根据小RNA测序及分析结果显示,测序的混合当归样品中可能含有KoMV病毒。为验证小RNA测序结果的可靠性,以疑似感染病毒样品的总RNA为模板,RT-PCR扩增KoMVcp基因序列。电泳结果显示,疑似样品中扩增到了KoMV病毒的核酸片段,扩增到的片段大小为750~1 000 bp,与预期(840 bp)大小一致(图2)。
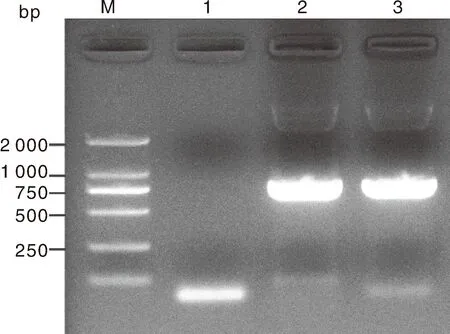
M,DNA 2000 marker;1,阴性对照;2、3,KoMV cp基因M, DNA marker; 1, Negative control; 2-3, KoMV cp gene图2 KoMV cp基因PCR扩增Fig.2 PCR amplification of KoMV cp gene
2.2 KoMV cp基因的序列分析
将克隆于pMD19-T的KoMVcp序列经PCR后送北京擎科生物科技有限公司进行测序。测序结果显示,KoMVcp序列的编码框为840 bp,编码280个氨基酸的CP蛋白。将测序所得的KoMVcp序列经BLAST同源性比对,从GenBank中筛选出16条同源性较高的序列,发现所得序列与KoMV、JHMV、ZaMV 3种病毒的同源性较高,各分离物间核苷酸序列的相似性为85.58%~99.41%,氨基酸序列相似性为89.32%~99.29%;核苷酸和氨基酸同源性最高的均为KoMV(KF150747)。因此,将甘肃省榆中县分离所得的病毒命名为KonjacmosaicvirusDG(KoMV-DG)。
为进一步明确KoMV-DG与分离物之间的进化关系,以邻接法(N-J法)构建了基于KoMV-DGcp序列的系统进化树(图3)。基于核苷酸序列的系统进化树将来自不同国家和地区的分离物分成3个类群,其中来自日本的6个分离物(AB302326、AB181353、AB498939、AB181352、AB181354、MN369533)聚为第一个大的类群;匈牙利分离物(MH979038)、新西兰分离物(EU544542)、韩国分离物(AB081519)和日本分离物(LC114489、LC114492)聚为第二个大的类群;本研究获得的KoMV-DG分离物与云南昆明分离物(KF150747、KF150746)、甘肃岷县分离物(EF157843)和日本分离物(AB251346、AB081518)组成第三个大的类群,其中KoMV-DG分离物与云南昆明分离物先聚为一个分支,而后与甘肃岷县分离物和日本分离物进一步相聚成簇。表明KoMV种群分布呈现明显的区域性差异,地理位置较近的分离物要比地理位置较远的分离物序列相似性高。3个类群分离物的宿主植物也不尽相同,类群一分离物的宿主主要为鸭儿芹、大阿米芹、明月叶;类群二分离物的宿主主要为马蹄莲、魔芋;类群三分离物的宿主主要为当归。表明不同宿主KoMV的分离物序列差异明显,病毒种群呈现寄主差异。

图3 基于KoMV cp基因核苷酸序列系统进化树的构建Fig.3 The phylogenetic tree of KoMV isolates based on the nucleotide sequences of cp genes
2.3 KoMV CP蛋白的表达与纯化
将鉴定正确的重组表达载体pET-28a-KoMV转化到E.coliRosettaTM(DE3),经IPTG在不同温度诱导下,收集菌体超声破碎后分别取上清和沉淀进行SDS-PAGE电泳分析,观察到有明显的诱导表达条带,且与融合His标签的KoMV CP重组蛋白分子量预期大小(36 ku)基本一致。不同温度诱导的目的蛋白几乎都存在于沉淀中,说明KoMV CP蛋白在E.coliRosettaTM(DE3)中是以包涵体的形式存在(图4-A)。纯化后的KoMV CP融合蛋白经SDS-PAGE电泳蛋白呈现上下两组蛋白(a蛋白和b蛋白),其中a蛋白与KoMVCP融合蛋白预期分子量大小一致,而b蛋白是新出现的一组不符合预期大小的蛋白。为验证b蛋白与a蛋白是否为同种蛋白,将两组蛋白在SDS-PAGE电泳后切下,送北京华大蛋白质研发中心有限公司完成蛋白质谱分析。采用LC-MS的质谱分析方法,将切好的蛋白样品用胰蛋白酶Trypsin酶解为肽段混合物,各肽段通过高效液相色谱分离后对各组分进行分析获得两组蛋白的质谱图(图4-B、图5)。应用蛋白质组学鉴定软件MaxQuant,根据对应的Enzyme、Fixed modification、Variable modification等质谱参数打开质谱图进行检索,蛋白质数据库的检索结果显示,纯化后出现的a蛋白和b蛋白均为马铃薯Y病毒的KoMV CP蛋白,匹配显著,成功鉴定。

A,KoMV CP蛋白的原核表达:M,蛋白质marker;1,pET-28a空载体对照;2,未经IPTG诱导的重组载体;3~5,16、28、37 ℃分别诱导20、12、4 h目标蛋白表达产物的上清;6~8,16、28、37 ℃分别诱导20、12、4 h目标蛋白表达产物的沉淀。B,KoMV CP蛋白的纯化:M,蛋白质marker;1,pET-28a空载体对照;2,未经IPTG诱导的重组载体;3,16 ℃诱导20 h目标蛋白表达产物的上清;4~5,纯化的重组KoMV CP蛋白。A, Prokaryotic expression of recombinant KoMV CP:M, Protein marker; 1, Negative control of pET-28a without cp gene inserted; 2, Recombinant plasmid not induced by IPTG; 3-5, The supernatant of target protein expression product induced at 16, 28 and 37 ℃ for 20, 12 and 4 h, respectively; 6-8, The pellet of target protein expression product induced at 16, 28 and 37 ℃ for 20, 12 and 4 h, respectively. B, Purification of recombinant KoMV CP:M, Protein marker; 1, Negative control of pET-28a without cp gene inserted; 2, Recombinant plasmid not induced by IPTG; 3, The supernatant of target protein expression product induced at 16 ℃ for 20 h; 4-5, Purified recombinant KoMV CP protein.图4 KoMV CP重组蛋白的SDS-PAGE分析Fig.4 SDS-PAGE analysis of recombinant KoMV CP

A,a蛋白质谱鉴定。B,b蛋白质谱鉴定。A, Identification of protein a by mass spectrometry. B, Identification of protein b by mass spectrometry.图5 KoMV CP蛋白SDS-PAGE所分离蛋白的质谱图谱Fig.5 Mass spectrum of proteins isolated from KoMV CP protein by SDS-PAGE
2.4 ELISA测定抗血效价
将纯化的KoMV CP融合蛋白免疫新西兰大耳白兔获得抗血清,用间接ELISA的方法测定抗血清效价。结果显示,制备的抗血清效价大于1∶32 000(表1),表明用纯化的KoMV CP融合蛋白作为免疫原制备的多克隆抗体具有很高的效价。
2.5 Western blot免疫印迹
将制备的抗KoMV CP蛋白的多克隆抗体分别与健康当归叶片、感染LSV、CMV、PLAMV和LMoV的百合叶片、感染LNYV的生菜叶片、感染PVY的马铃薯叶片、感染KoMV的当归叶片的总蛋白以及纯化的KoMV CP蛋白进行Western blot分析,结果显示,抗体与感染KoMV的当归叶片以及纯化的KoMV CP蛋白发生特异性反应,而与同属的LMoV、PVY及不同属的LSV、CMV、PLAMV、LNYV感病叶片均未发生任何反应,说明制备抗KoMV的多克隆抗体具有良好的特异性,适用于KoMV的免疫学检测(图6)。

M,蛋白质marker;1,健康当归样品;2~4,分别感染LSV、CMV和PLAMV的百合样品;5,感染LNYV的生菜样品;6,感染LMoV的百合样品;7,感染PVY的马铃薯样品;8,感染KoMV的当归样品;9,纯化的KoMV CP蛋白。M, Protein marker; 1, Negative control of healthy Angelica sinensis; 2-4, Extracts from lily samples infected with LSV, CMV and PLAMV, respectively; 5, Extracts from lettuce samples infected with LNYV; 6, Extracts from lily samples infected with LMoV; 7, Extracts from potato samples infected with PVY; 8, Extracts from Angelica sinensis samples infected with KoMV; 9, Purified KoMV CP protein.图6 Western blot鉴定KoMV CP多克隆抗体Fig.6 Western blot analysis of KoMV CP using rabbit polyclonal antibody
此外,抗体与感染KoMV的当归叶片以及纯化的KoMV CP蛋白发生免疫反应后均出现了上下两条带(图6)。其中,两个样品的上条带均符合预期大小,而下条带与预期大小不一致。由于纯化的KoMV CP蛋白样中含有b蛋白,因此b蛋白与抗体发生反应后出现了下条带。而感染KoMV的当归与抗体免疫反应后出现下条带的原因可能是KoMV CP蛋白在翻译后被植物细胞中的蛋白酶酶切产生的亚蛋白与抗体发生了反应。
3 结论与讨论
植物病毒素有植物癌症之称,能够对作物的生长带来严重的危害性[21]。为有效预防KoMV病毒的传播,迫切需要开发出一种快速、高效、特异、灵敏的病毒检测技术。目前,植物病毒主要的检测技术有血清学方法和分子生物学方法,基于核酸检测的分子生物学方法由于操作复杂、需要专业的技术人员和专门的设备不易普及,血清学方法克服了提取核酸的困难,操作简便,可用于田间样品的大批量检测[3,22]。相较于早期纯化病毒粒子制备抗原的方法,通过构建原核表达载体获得目的蛋白,不但可以降低实验难度和提高抗原的浓度和纯度,同时制备的抗体也具有更好的特异性和效价[16]。本研究通过小RNA测序技术鉴定了甘肃省榆中县当归样品中含有KoMV病毒,结合RT-PCR验证了测序结果。构建KoMVcp基因的原核表达载体,经IPTG诱导蛋白表达,并以纯化的KoMV CP融合蛋白作为免疫原制备了多克隆抗体,这些工作对CP蛋白的功能研究及建立快速、灵敏、特异的血清学检测方法都有一定的参考意义。
克隆的KoMVcp序列经测序后与GenBank中16条同源性较高的序列进行比对分析,结果显示,所得序列与KoMV、JHMV、ZaMV 3种病毒的同源性较高,各分离物核苷酸与氨基酸序列相似性均超过85%,这一结果与国际病毒分类委员会第八次报告认为KoMV、JHMV和ZaMV属于同种病毒的不同分离物的结论一致[2]。克隆所得序列与KoMV(KF150747)的同源性最高,核苷酸与氨基酸的相似性分别为99.41%和99.29%。基于KoMV-DGcp基因建立的系统进化树将来自不同国家和地区的分离物形成3个类群,从地理位置上看,类群一和类群二均为国外分离物,类群三为中国和日本的分离物,地理位置较近的分离物序列相似性要比地理位置较远的分离物序列相似性要高,这可能与KoMV病毒通过蚜虫以非持久性的方式传播有关[5],说明KoMV的种群分布存在着一定的区域性差异,且最早期KoMV病毒可能是由日本传入我国的作物当中;从宿主差异上看,3个类群分离物的宿主植物也不尽相同,感染我国的作物主要为云南和甘肃的当归,表现出较强的寄主特异性。
KoMVcp基因序列中含有27个稀有密码子(GGA、CGG、CUA、CCC、ACG、AGA、AGG、AUA),所占总密码子的比例为9.64%,在初次实验中,将鉴定正确的重组表达载体pET-28a-KoMV转化E.coliBL21(DE3),经IPTG诱导,SDS-PAGE电泳没有观察到目的蛋白的表达条带。后将鉴定正确的表达载体pET-28a-KoMV转化E.coliRosettaTM(DE3),经IPTG诱导,SDS-PAGE观察到明显的目的条带,这可能是由于稀有密码子的偏好性引起的。研究表明,不同物种的基因在大肠埃希菌原核表达时对同一氨基酸不同密码子的使用具有偏好性,如果表达的外源蛋白中含有较多的稀有密码子,则会影响外源蛋白的表达[15,23,24]。为提高目的蛋白的表达量,初步探索了温度对KoMV CP融合蛋白表达量的影响。分别设置16、28、37 ℃的诱导表达温度,结果表明,不同温度诱导下均能观察到明显的表达条带,但温度对蛋白表达量没有显著影响。在不同温度诱导下,KoMV CP蛋白均以包涵体的形式在大肠埃希菌中表达,这可能与蛋白在菌体中缺少相关的修饰酶等有关[25]。蛋白质谱鉴定是一种研究蛋白质的技术,具有操作简单、灵敏度高、快速、通量高、准确性强的优点[26]。纯化后的KoMV CP融合蛋白经SDS-PAGE结果显示,出现了2组蛋白,通过蛋白质谱鉴定确认出现的2组蛋白均为KoMV CP融合蛋白。原核表达的KoMV CP蛋白超声破碎后蛋白电泳只出现了一条与预期大小一致的蛋白条带,而纯化后却出现了另外一条不符合预期大小的蛋白条带,这可能是由于纯化过程中,KoMV CP蛋白中的二硫键被具有还原性的尿素所打断,因此,出现了新的条带[27]。Western blot实验结果显示,从感染KoMV的当归样品中提取的植物总蛋白与制备的抗体发生免疫反应后也出现了上下两条带,其中下条带不符合预期大小,这可能是由于植物对外源表达的蛋白质翻译后进行加工,翻译后的KoMV CP蛋白被植物体内的蛋白酶消化或剪切所致[28-29]。
多克隆抗体具有制备成本低、稳定性好、能识别多个表位、制备周期短、技术要求低等优点,因此,在科研领域被广泛使用[30]。CP蛋白作为病毒的结构蛋白,具有较好的免疫原性,通常被作为抗原来制备抗体[31-32]。本研究以原核表达的KoMV CP蛋白作为免疫原制备的多克隆抗体,其效价超过32 000,Western blot结果显示,制备的多克隆抗体能够与感染KoMV的当归叶片和纯化的蛋白特异性反应,而与同属的PVY、LMoV及不同属的CMV、LSV、LNYV、PLAMV感病叶片均未发生任何反应,说明制备的抗体具有良好的特异性。
