颅内血管周细胞瘤综合治疗1例并文献复习
2022-11-25闵现华牟福玲张垚孙鹏飞
闵现华 牟福玲 张垚 孙鹏飞
作者单位:730030 兰州 兰州大学第二医院放疗科
血管周细胞瘤(hemangiopericytoma,HPC)又称血管外皮细胞瘤或孤立性纤维性肿瘤,好发于下肢、后腹膜和盆腔,也可发生在头颈部、躯干、上肢软组织、内脏及神经系统。其中,颅内HPC少见,约占原发中枢神经系统肿瘤的0.4%,易发生局部复发和颅外转移,预后较差[1]。目前,针对颅内HPC尚无标准治疗方案。本文报道1例颅内HPC患者的综合治疗效果并复习相关文献,以期提高对该病的诊治水平。
1 病例资料
患者,女性,43岁,藏族,因“间断性头痛1月余”于2016年9月18日就诊,颅脑MRI示额部皮下和额叶见椭圆形肿物、邻近颅骨骨质破坏、T1WI增强明显强化、可见脑膜尾征(图1A~B);结合临床表现诊断为脑膜瘤,后行脑肿瘤切除术,肿瘤大小约4.5 cm×4.0 cm×3.0 cm。术后病理检查诊断:恶性血管周细胞瘤,瘤组织侵犯脉管及骨组织,WHO Ⅲ级;Vimentin(+)、CD34(灶+)、CD99(+)、Bcl-2(灶+),CKp(+)、Ki-67 45%(图2A)。术后未行放化疗,未定期复查。1年后因额部肿物再次就诊,颅脑MRI示额部皮下软组织肿物并额叶圆形病灶(图1C~D)。临床诊断肿瘤复发,于2017年10月18日行额部皮下肿物切除术,但未切除颅内复发病灶。术后病理示恶性血管周细胞瘤复发,WHO Ⅲ级,伴坏死(图2B)。术后1个月行颅脑MRI示右额叶圆形病灶,T1WI明显强化(图3A);右额叶镰旁椭圆形病灶,T1WI增强呈不均匀强化(图3B)。考虑肿瘤残留,给予放疗(剂量为64.2 Gy/30 f),及口服替莫唑胺同步化疗,放化疗期间无明显副反应。放疗后行颅脑MRI示颅内病灶完全消退(图3C~D),后续行4周期替莫唑胺单药维持化疗。2018年7月9日患者末次化疗后复查颅脑MRI示颅内病灶维持完全缓解状态,胸部CT示双肺转移(图4B、4E),更改治疗方案为安罗替尼单药靶向治疗。2019年3月1日患者突发胸闷、气短,复查胸部CT示右侧胸膜转移、右侧右肺不张并胸腔积液并肺不张(图4C、4F),后患者自行停药,经随访于2019年9月死亡。患者自初诊到去世生存期为3年。
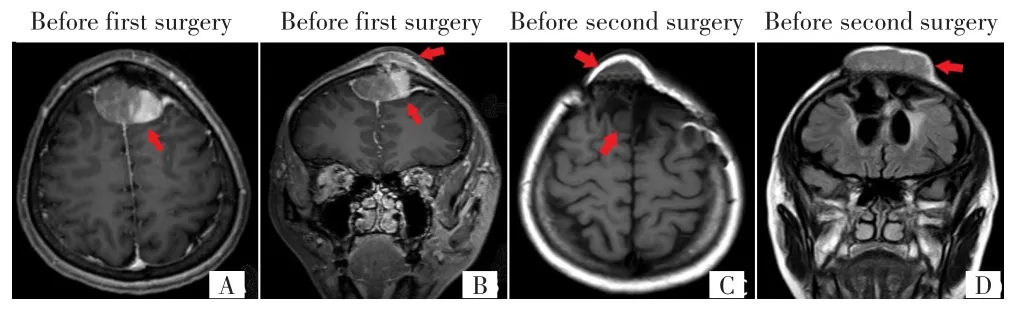
图1 患者两次手术前MRI表现Fig.1 MRI results of before two operations

图2 患者两次术后病理结果Fig.2 Pathological results of patient after two operations
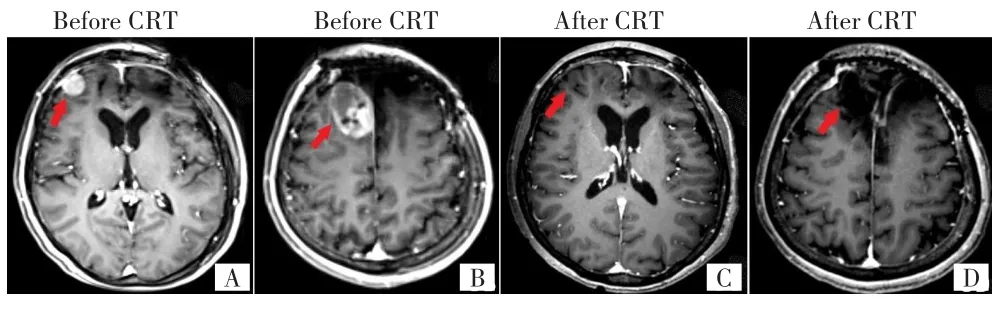
图3 同步放化疗治疗前后MRI表现Fig.3 MRI results before and after concurrent chemoradiotherapy
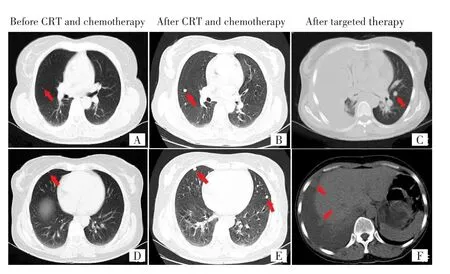
图4 化疗前后和靶向治疗后胸部CT表现Fig.4 Chest CT results before and after chemotherapy and after targeted therapy
2 讨论
颅内HPC起源于脑膜间质组织,病因不明,发病率低,组织学上呈低-中度恶性(WHO Ⅰ~Ⅲ级),病理基础为NAB2-STAT6基因融合,临床表现无特异性,影像学易误诊为脑膜瘤,常通过病理学检查明确诊断。颅内HPC中,WHO Ⅱ~Ⅲ级具有明显侵袭性,有复发和转移倾向,常见转移部位为肺/胸膜、肝脏和骨骼[2-3]。既往有长期随访研究报道HPC术后1年、5年复发率分别为15%和65%,术后10年、15年转移率分别为33%和64%[4]。目前颅内HPC尚无标准治疗方案。
手术是颅内HPC的主要治疗手段,手术全切更是提高患者总生存期(OS)和延长复发的关键[5]。有研究报道,与次全切相比,颅内HPC患者接受手术全切的5年局部控制率显著提高(84%vs 38%)[6],OS也有明显延长[7]。但颅内HPC血供极其丰富,且部分病灶邻近重要器官,手术全切存在困难。有研究报道肿瘤大小≥6 cm、静脉窦受侵和病灶位于颅骨外与肿瘤复发相关[1]。本例患者首诊时病灶跨越颅骨向内外生长,肿瘤位置特殊,可能与术后1年颅骨内外均短期局部复发有关。
放疗在颅内HPC治疗中存在一定争议。RUTKOWSKI等[8]报道在全切和次全切颅内HPC患者中,术后放疗并不能降低局部复发率和提高OS。而在JEON等[9]报道中全切和次全切颅内HPC患者接受术后放疗均可减少肿瘤局部复发,但不能改善OS和无远处转移生存期。也有回顾性研究提示术后放疗可显著提高局控率并延长OS,单纯手术组局部复发率为88%,手术联合放疗组为12.5%[10]。关于放疗剂量,有既往研究表明50~60 Gy的放疗剂量可获得更长的无复发生存[11]。DUFOUR等[10]报道2例接受30 Gy的患者均出现肿瘤复发;GUTHRIE等[4]报道17例接受术后放疗的患者中,3例剂量>51 Gy中未出现局部复发、9例剂量>45 Gy中2例出现局部复发、8例剂量<45 Gy中7例出现局部复发。本例患者经次全切术后因颅内病灶残留,给予X射线调强放疗,采用了较高放疗剂量(64.2 Gy),放疗后颅内病灶完全消退且无明显副反应,提示高剂量放疗对颅内HPC是安全有效的。关于放疗方式,除常规放疗外,立体定向放射外科也可用于颅内HPC,其对术后残留、局部复发或寡转移肿瘤安全有效[12]。质子放疗也可明显提高复发间隔时间,但对OS和无远处转移生存无获益[13]。此外,放射性粒子也可用于HPC放疗,如王园园等[14]采用I125治疗HPC肺转移,右胸壁转移灶明显缩小。关于放疗时机,放疗常见为术后辅助,但对于因肿瘤较大或邻近重要器官不能全切的患者,术前新辅助放疗可缩小肿瘤体积、减少肿瘤出血[15]。
在化疗方面,目前传统细胞毒性化疗药物如环磷酰胺、多柔比星和长春新碱以及α-干扰素、异环磷酰胺、顺铂、依托泊苷等药物治疗HPC均有尝试,但疗效均有限[16-17]。WANG等[5]在 SEER数据库中收集并分析1 243例HPC患者资料,发现手术联合化疗患者的临床获益较单纯手术差。目前也有研究探索化疗联合靶向治疗HPC,发现替莫唑胺联合贝伐单抗对HPC治疗有效[18]。本例患者在替莫唑胺同步放化疗,序贯替莫唑胺维持化疗治疗后,颅内病灶完全消退,且无明显副反应,提示替莫唑胺化疗对颅内HPC安全有效。值得注意的是,患者二次术后9个月复查胸部CT示肺转移,但二次术前胸部CT报告未见异常,复阅二次术前CT影像可见右肺同部位微小结节转移,存在肺转移漏诊。患者肺转移病灶经替莫唑胺化疗后进展,提示HPC肺转移可能对替莫唑胺化疗不敏感。近年来,HPC靶向治疗尝试应用帕唑帕尼[19-20]、舒尼替尼[21]、达沙替尼[22]等药物治疗复发和转移性HPC,均观察到一定疗效。然而,KALEY等[23]报道6例HPC经舒尼替尼治疗未获得阳性结果,且3例因毒性反应停药。有既往研究表明,安罗替尼治疗软组织肉瘤肺转移安全有效[24],而HPC本质上是发生于脑膜的高分级孤立性纤维性肿瘤,因此,本例患者肺转移进展后停用替莫唑胺,更换为安罗替尼靶向治疗,结果维持胸部CT影像学稳定7个月,提示安罗替尼可能对颅内HPC肺转移有一定的潜在治疗作用,但后续因患者依从性差,自行停药6个月后死亡,安罗替尼的长远疗效仍需进一步研究证实。
本病例初诊时影像学误诊为脑膜瘤,提示“脑膜尾征”需与HPC鉴别诊断。其次,颅内HPC病灶跨越颅骨时极易局部复发,即便行全切手术,也应积极行术后放疗,降低复发率。另外,本病例微小肺转移漏诊,后续治疗中没有及时再次复查胸部CT,提示应注意HPC患者易发生肺转移,在术后需密切随访胸部CT检查,以及时发现转移病灶、调整治疗计划。
综上所述,颅内HPC局部复发率高且易发生颅外转移,术后应密切影像学随访。术后采用同步放化疗可以提高局控率,且高剂量放疗和替莫唑胺化疗对颅内病灶安全有效。此外,安罗替尼对颅内HPC肺转移有一定的潜在治疗作用,但其有效性有待更多临床试验证实。
