纳米TiO2胶体光催化-磁絮凝回收深度处理造纸废水
2022-11-24林英行陈小泉
林英行 陈小泉
(华南理工大学制浆造纸工程国家重点实验室,广东广州,510640)
造纸废水中有机污染物种类超过300种,多为难降解、高毒性污染物[1]。为使造纸废水达标排放,通常需采用多段处理及多种方法相结合处理,包括物理法、化学法和生物法等[2]。目前,生物法由于良好的经济性及处理效果,成为制浆废水二级处理阶段的主要选择。相较于传统活性污泥法,序批式活性污泥法(SBR)作为生物法的一种,具有独特的优势,在造纸废水处理应用中的发展前景广阔[3]。
生化法可降解造纸废水中大部分的COD、BOD和固体悬浮物,但需结合高级氧化法等工艺才能使造纸废水达标排放[4]。光催化氧化法作为高级氧化法的一种,可无选择性处理难降解有机污染物,将其矿化成无毒或低毒性的小分子物质[5]。纳米TiO2(Nano-TiO2)因低成本、无毒和性能稳定等特点,是目前最常用的光催化剂[6],但与其他纳米光催化剂一样,其存在回收难的问题。传统过滤方法分离和回收Nano-TiO2既费时又不经济。有研究倾向于将Nano-TiO2固定在如陶瓷、玻璃和磁性物质等基材上,但这种固定方式的合成步骤繁琐,成本高昂,而催化剂比表面积的减少也会抑制其光催化性能,同时产生了传质和光照限制等新问题[7]。通过加入磁性絮凝剂以及调节溶液的pH值,不仅能够实现Nano-TiO2重复利用,也能保持Nano-TiO2高效的光催化活性,具有重要的实际应用意义[8]。
因此,本研究采用溶胶凝胶法制备了磁性絮凝剂Fe3O4/SiO2(FS),通过调节溶液的pH值来改变FS和Nano-TiO2的表面电荷,从而实现Nano-TiO2的回收及释放;并探讨了pH值、FS/Nano-TiO2质量比和Nano-TiO2浓度对絮凝回收性能的影响,以及造纸废水的不同预处理方式对Nano-TiO2光催化-磁絮凝回收循环光降解废水性能的影响。
1 实验
1.1 实验原料
实验用废水取自广州市某造纸厂经SBR处理后的造纸废水。废水CODCr为266.82 mg/L,pH值约为7,固体悬浮物(SS)为163 mg/L,色度为1925倍,浊度为98.6 NTU。
1.2实验试剂
硫酸(H2SO4,98.3%)、硝酸(HNO3,68%)、重铬酸钾(K2Cr2O7)、正硅酸乙酯(C8H20O4Si)、无水乙醇(C2H6O,99.7%)、氨水(NH3·H2O,25%),广州化学试剂厂;氢氧化钠(NaOH),福晨(天津)化学试剂有限公司;硫酸银(Ag2SO4),上海精细化工材料研究所;硫酸汞(Hg2SO4),贵州省铜仁银湖化工有限公司化学试剂厂;磁铁(Fe3O4,粒径200 nm),上海麦克林生化科技有限公司。以上试剂均为分析纯。P25 TiO2粉末(P25,粒径20 nm,比表面积55.2 m2/g),赢创特种化学上海有限公司;Nano-TiO2(粒径约8 nm,比表面积284.52 m2/g,固含量20%),钛唐科技有限公司;实验用水为实验室自制去离子水。
1.3 实验仪器
扫描电子显微镜(SEM,Merlin,德国Zeiss);傅里叶变换红外光谱仪(FT-IR,VERTEX70,德国Bruker);纳米粒度电位仪(Zetasizer Nano ZS,英国Malvern);紫外-可见分光光度计(UV-Vis,UV-1900,日本SHIMADZU);消解仪(DRB200,美国HACH);浊度仪(2100N,美国HACH);光催化氧化降解实验装置(自制)。
1.4 实验方法
1.4.1 FS的合成
将1.00 g Fe3O4分散到含400 mL无水乙醇、100 mL去离子水和12 mL氨水的溶液中。超声分散后转移到三口烧瓶中,逐滴加入2 mL正硅酸乙酯,以500 r/min速度搅拌2 h。反应完成后,通过磁铁回收包覆的磁性粒子,并用去离子水和无水乙醇洗涤,然后在真空烘箱中于50℃下干燥5 h[9]。
1.4.2 Nano-TiO2的絮凝沉降实验
将FS与Nano-TiO2按不同质量比加入到200 mL去离子水中,调节溶液的pH值为6,然后转移到250 mL的量筒中,搅拌均匀后静置,开始计时,每隔1 min记录分层界面的下降距离。
1.4.3 溶液残留Nano-TiO2浓度的检测
测试溶液絮凝沉降后的上清液在250、350和400 nm处的吸光度,与已知浓度的Nano-TiO2悬浮液配置的标准曲线进行比较(见图1),可得出溶液中残留的Nano-TiO2浓度。
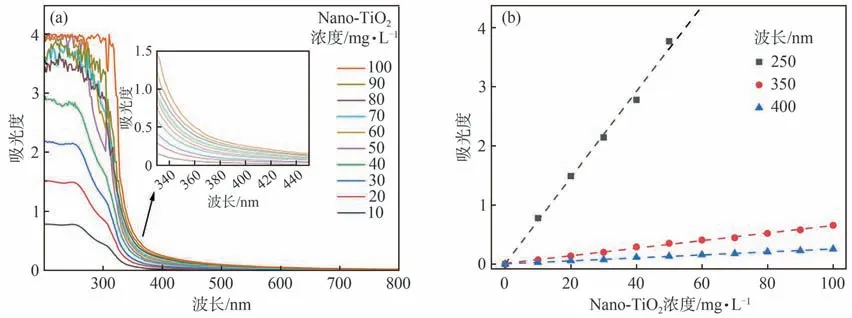
图1 (a)不同浓度Nano-TiO2悬浮液的UV-Vis谱图;(b)根据图1(a)中的UV-Vis谱绘制的标准曲线Fig.1(a)UV-Vis spectra of aqueous suspension of Nano-TiO2 with different concentrations;(b)standard curves drawn according to the spectra in Fig.1(a)
1.4.4 水质指标的测试
分别按照GB 6920—1986《水质pH值的测定玻璃电极法》、GB 11901—1989《水质悬浮物的测定重量法》、GB 11914—1989《水质化学需氧量的测定重铬酸盐法》、GB 11903—1989《水质色度的测定铂钴比色法》、HJ 1075—2019《水质浊度的测定浊度计法》测定造纸废水pH值、SS、CODCr、色度及浊度。
1.4.5 光催化氧化循环降解造纸废水实验
光催化氧化实验:分别量取200 mL经3种不同预处理的造纸废水,包括无处理造纸废水(SBR-P)、5000 r/min离心处理造纸废水(SBR-C)和0.6 g/L Nano-TiO2絮凝处理造纸废水(SBR-T),与0.6 mL Nano-TiO2一同加入到自制光催化氧化降解实验装置(功率为24 W的紫外光,波长为254 nm),在黑暗中搅拌30 min后,进行紫外光照射,每隔一段时间取样2 mL,静置沉降后,测定其CODCr。
循环降解实验:Nano-TiO2光催化-磁絮凝回收循环光降解造纸废水的流程如图2所示。待每次光催化氧化降解实验结束后,添加0.24 g FS,调节废水pH值为6,并充分搅拌,絮凝回收Nano-TiO2。然后通过磁铁将两者形成的絮凝体(FS/Nano-TiO2絮凝体)从水中分离,倒出降解完的溶液,重新加入造纸废水,调节pH值为3以解絮凝释放Nano-TiO2,搅拌分散,再通过磁铁吸引FS到容器底部,使其与Nano-TiO2重新分离,在下一次光催化氧化降解实验结束后,移除磁铁,调节pH值=6并搅拌,FS可以再次吸附絮凝的Nano-TiO2。
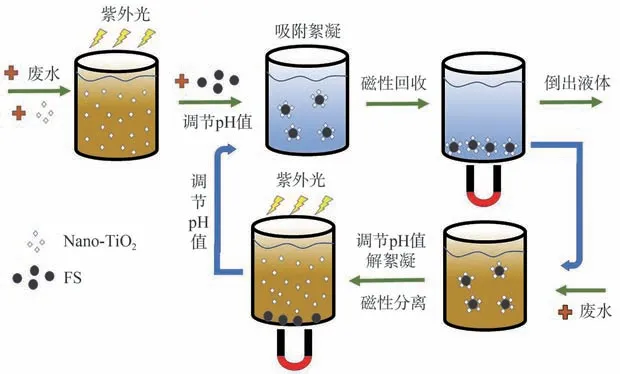
图2 光催化-磁絮凝回收循环光降解造纸废水流程示意图Fig.2 Schematic diagram of the combined cycle of photocatalysis and magnetic flocculation recovery of Nano-TiO2 for photodegradation of papermaking wastewater
2 结果与讨论
2.1 絮凝剂和光催化剂表征分析
2.1.1 Zeta电位分析
等电点(IEP)是表示一个分子表面不带电荷时的pH值,通过测量Zeta电位来获得。有研究测得Fe3O4的IEP为pH值=7.2[10],SiO2的IEP为pH值=2.7[11]。pH值对材料Zeta电位的影响如图3(a)所示。由图3(a)可知,FS的IEP为pH值=3.26,说明Fe3O4表面包覆了SiO2涂层。通过低温液相法得到的Nano-TiO2的IEP为pH值=6.75,与文献[12]所报道相似。
不同pH值下Nano-TiO2磁性絮凝回收的实物图如图3(b)所示(Nano-TiO2浓度为0.6 g/L,FS用量为0.24 g)。当溶液pH值=5、6和7时,FS/Nano-TiO2絮凝体沉淀在烧杯底部,pH值=5和6时,FS和Nano-TiO2的表面电荷相反,因此彼此由于静电作用,相互吸附并絮凝沉淀[13],而pH值=7时,FS和Nano-TiO2表面虽然带有相同电荷,但Nano-TiO2已经接近IEP,表面正电荷非常小,当有足够的絮凝剂吸附在Nano-TiO2表面,可实现电荷中和,且两者之间的静电排斥可忽略[14]。当pH值小于4和大于8时,FS和Nano-TiO2表面带有相同电荷,Nano-TiO2因电荷相斥而重新分散到溶液中。因此,通过调节pH值可以实现Nano-TiO2的絮凝回收与释放。

图3 (a)pH值对材料Zeta电位的影响;(b)不同pH值下Nano-TiO2磁性絮凝实物图Fig.3(a)Effect of pH value on Zeta potential of materials;(b)physical diagram of magnetic flocculation of Nano-TiO2 at different pH values(pH value from left to right:3,4,5,6,7,8,and 9)
2.1.2 FT-IR分析
P25、Nano-TiO2、Fe3O4和FS的FT-IR谱图如图4所示。P25是通过高温气相法制得,制备温度700℃~1000℃[15];而Nano-TiO2则是通过低温液相法制得,制备温度100℃。由图4可知,P25的表面羟基吸收峰相对于Nano-TiO2更加尖锐,强度较小,表明Nano-TiO2比P25含有更多的表面羟基,而表面羟基在一定程度上有利于光催化反应[11]。Ti—O—Ti键出现在400~700 cm-1的范围内,其峰值的锐度随制备温度的升高而增大。此外,Nano-TiO2表面出现了硫酸根离子的特征峰(1215、1137、1049 cm-1),这可归因于其特殊的制备工艺[16]。
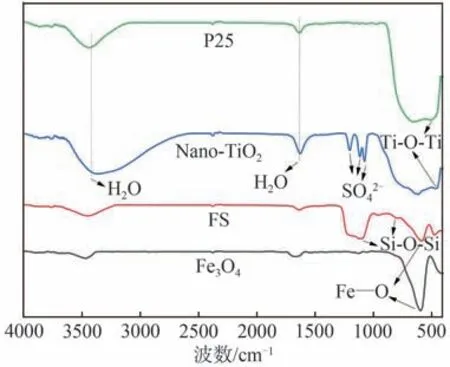
图4 FT-IR谱图分析Fig.4 Analysis of FT-IR spectra
Fe3O4的Fe—O特征峰出现在580 cm-1处,且只有少量的羟基和吸附水的特征峰,说明Fe3O4表面未经任何改性。FS的Fe—O特征峰在包覆SiO2后锐度变小,795 cm-1处的吸收峰归因于Si—O—Si对称振动,1080~1100 cm-1处的吸收峰归因于Si—O—Si不对称伸缩振动,说明SiO2成功包覆在Fe3O4表面。
2.1.3 SEM分析
Nano-TiO2的SEM图如图5(a)所示,其原始粒径即一次粒径约为8 nm。由于过大的比表面能会导致体系不稳定,细小的晶粒会通过弱的相互作用结合形成二次粒径[17],为30~150 nm,总体分散性较好。Fe3O4的SEM图如图5(b)所示,其由球形和方形等结构的粒子组成,粒径200~300 nm,颗粒表面不平整,部分团聚,可能是表面没经过任何改性,导致Fe3O4分散性较差。FS的SEM图如图5(c)所示,相对于Fe3O4,FS表面变得光滑,粒径增大,表面出现一层致密的涂层,说明SiO2成功包覆在Fe3O4表面上。FS/Nano-TiO2絮凝体的SEM图如图5(d)所示,FS原本光滑的表面结合了大量的Nano-TiO2,形成了尺寸更大的絮凝体,这有助于其在溶液中快速沉淀或更加容易被磁性吸引。

图5 (a)Nano-TiO2、(b)Fe3O4、(c)FS、(d)FS/Nano-TiO2絮凝体SEM图Fig.5 SEM images of(a)Nano-TiO2,(b)Fe3O4,(c)FS,and(d)FS/Nano-TiO2 flocs
2.2 Nano-TiO2絮凝性能分析
2.2.1 FS/Nano-TiO2质量比对磁性絮凝体沉降速率的影响及Nano-TiO2残留分析
FS/Nano-TiO2质量比对FS/Nano-TiO2絮凝体沉降速率的影响如图6(a)所示。Nano-TiO2在接近IEP时,其稳定性会被破坏,开始絮凝团聚,但其絮凝过程缓慢,且在形成界面后,上层清液仍有细小白色絮体残留,需经过很长的时间才能完全沉淀,与加入FS相比,其絮凝体十分松散。调节pH值并加入FS后,由于静电吸附作用,体系中可快速形成FS/Nano-TiO2絮凝体并沉降,且其前5 min平均沉降速率随FS/Nano-TiO2质量比增大而提高,在FS/Nano-TiO2质量比为1.5∶1时的沉降速率增幅最大,沉降速率为25.09 mm/min。
FS/Nano-TiO2质量比对Nano-TiO2回收性能的影响如图6(b)所示。由图6(b)可知,不同FS/Nano-TiO2质量比下,Nano-TiO2回收率都能达到99%以上。根据静电诱导絮凝机理可知,表面带正电的Nano-TiO2被吸附到表面带负电的FS上后会发生电荷中和,在电荷中和时,可忽略FS表面上Nano-TiO2颗粒之间的静电排斥,因此可以不断吸附Nano-TiO2并凝聚成更大的絮凝体[18]。但较低FS/Nano-TiO2质量比不利于磁性回收,过多的Nano-TiO2结合会降低FS/Nano-TiO2絮凝体的磁性强度,分离时,在磁力作用下,FS/Nano-TiO2絮凝体会相互摩擦,结合力较弱的Nano-TiO2会被重新释放。由图6(c)可知,FS/Nano-TiO2质量比为1.5∶1时,经底部磁铁吸引,FS/Nano-TiO2絮凝体被固定在烧杯底部,没有白色絮体析出(左图);而FS/Nano-TiO2质量比为0.5∶1时,FS/Nano-TiO2絮凝体在附加磁性后,有大量白色的絮体从FS表面脱离(右图),表明在固液分离后会损失部分Nano-TiO2。因此,根据沉降性能及成本考虑,FS/Nano-TiO2质量比为1.5∶1最佳。
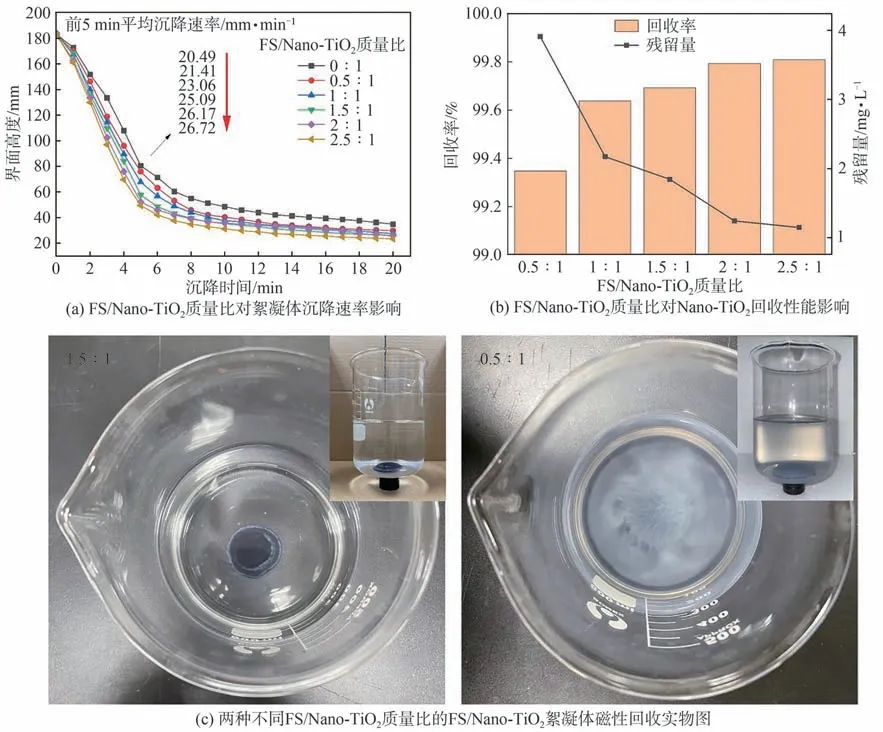
图6 FS/Nano-TiO2质量比不同的FS/Nano-TiO2絮凝体絮凝沉降性能分析Fig.6 Analysis of flocculation and sedimentation performance of FS/Nano-TiO2 flocs with different mass ratio of FS and Nano-TiO2
2.2.2 Nano-TiO2浓度对FS/Nano-TiO2絮凝体絮凝沉降性能的影响
Nano-TiO2浓度对FS/Nano-TiO2絮凝体絮凝沉降性能的影响如图7(a)所示。由图7(a)可知,当Nano-TiO2浓度为0.2 g/L时,絮凝沉降效果很差,没有清晰的界面出现,经过20 min沉降,仅有少部分FS/Nano-TiO2絮凝体沉淀,大部分仍悬浮在溶液中(如图7(b)所示)。其原因是Nano-TiO2浓度较低时形成的絮凝体太小,重力作用不足以让其快速沉降,需相当长时间才能完全沉降。当Nano-TiO2浓度为0.6 g/L时,FS/Nano-TiO2絮凝体沉降速率相对于Nano-TiO2浓度0.4 g/L时提高显著,继续提高Nano-TiO2浓度,絮凝体沉降速率增幅不明显。此外,Nano-TiO2浓度越大,20 min时沉降的絮凝体的体积也更大。

图7 Nano-TiO2浓度对FS/Nano-TiO2絮凝体絮凝沉降性能的影响Fig.7 Effect of Nano-TiO2 concentration on flocculation and sedimentation of FS/Nano-TiO2 flocs
综上,Nano-TiO2浓度通常取决于降解某种物质时的最佳浓度,浓度越大越有利于磁性絮凝沉降,当其浓度过低时,可以在充分搅拌后,直接在底部用磁铁吸引,使漂浮的絮凝体更快被收集,从而实现固液分离。
2.2.3 Nano-TiO2的磁性絮凝回收及反絮凝释放性能研究
对浓度为0.1 g/L的Nano-TiO2悬浮液进行磁性絮凝回收及解絮凝释放的循环测试,以溶液中残留的Nano-TiO2浓度(C)与其初始浓度(C0)的比值作为测试指标,循环次数为5次,结果如图8(a)所示。从图8(a)可知,在5次循环结束时,重新释放的Nano-TiO2浓度只有初始的85.7%,一部分原因是Nano-TiO2还被吸附在FS表面没有释放,而主要原因则是每次絮凝和解絮凝操作,溶液都需要进行酸碱度调节,会稀释溶液,导致在每次循环后的Nano-TiO2浓度变小。但每次絮凝回收后,上清液残留的Nano-TiO2浓度都接近于0,这与图6(b)的结果一致。
图8(b)是一个循环过程的实物图。回收前,Nano-TiO2在溶液中有着良好的稳定性及分散性;回收时,加入FS并调节pH值为6,絮凝沉淀后,通过磁铁可以实现固液分离;释放时,调节pH值为3,充分搅拌,通过磁铁可将FS和Nano-TiO2分离,Nano-TiO2重新分散在水溶液中,并恢复其原来的分散性。因此,在溶剂为去离子水及没有其他杂质干扰时,对Nano-TiO2进行5次絮凝及解絮凝循环操作,其絮凝性能基本保持不变。
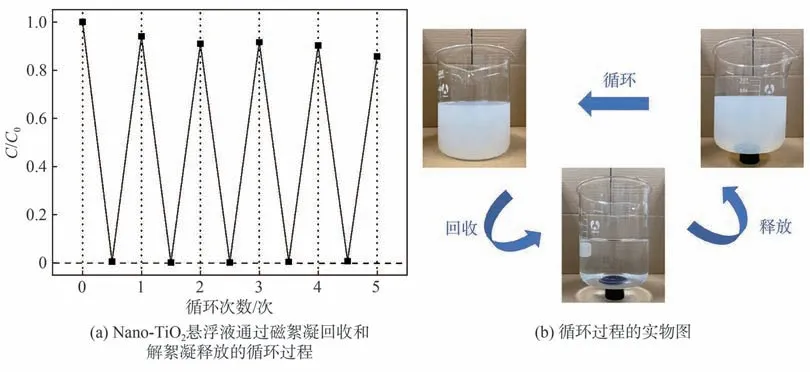
图8 Nano-TiO2磁絮凝回收及释放性能研究Fig.8 Study on magnetic flocculation recovery and release properties of Nano-TiO2
2.3 Nano-TiO2磁性絮凝循环处理造纸废水性能分析
2.3.1 造纸废水预处理对Nano-TiO2光催化氧化降解性能的影响
Nano-TiO2光催化氧化降解不同预处理造纸废水的效果如图9所示。由图9可知,3种预处理造纸废水的光催化氧化降解都基本遵循Langmuir-Hinshelwood模型,反应速率随着污染物浓度的降低而降低[19],其中前30 min的造纸废水CODCr降解幅度较大,反应30 min时取出的Nano-TiO2呈淡黄色黏稠状,而反应180 min后取出的Nano-TiO2则恢复其纯白色的胶体状态,因此除了正常的光催化氧化降解之外,CODCr的降低一部分是Nano-TiO2与造纸废水中的部分污染物相互凝聚沉淀所导致。
造纸废水经过不同处理后的水质指标见表1。由表1可知,SBR-P呈中性,其CODCr、SS、浊度和色度分别为266.8 mg/L、163 mg/L、98.6 NTU和1925倍。结合图9可知,SBR-P在光催化氧化降解180 min后的CODCr仍然很高,而经过预处理去除大部分SS后的SBR-C和SBR-T,其在光催化氧化降解后出水的CODCr较低。通常废水中SS都含有大量难降解物质,且易与Nano-TiO2结合,不仅影响Nano-TiO2的分散性,还会导致其出现中毒失活的现象[20],从而影响系统的光催化氧化降解效果、Nano-TiO2回收以及重复利用等性能。

表1 造纸废水经过不同处理后的水质指标Table 1 Water quality index parameters of papermaking wastewater after different treatment

图9 不同预处理对Nano-TiO2光催化氧化降解造纸废水性能的影响Fig.9 Effect of different pretreatment of papermaking wastewater on photocatalytic oxidation degradation of Nano-TiO2
在光催化氧化降解180 min后,相较于SBR-P,SBR-T光催化氧化降解出水的CODCr、色度、SS和浊度分别降低了89.2%、99.3%、98.2%和99.3%,基本达到了深度处理造纸废水的目的。
2.3.2 光催化-磁絮凝回收循环光降解SBR-C和SBR-T的性能分析
Nano-TiO2光催化-磁絮凝回收循环光降解SBR-C的效果如图10(a)所示。离心处理可去除废水中大部分的SS,但经过一段时间静置后,溶解在废水中的部分污染物又会重新凝聚形成SS。有研究证实,水中天然悬浮固体的存在对于磁絮凝是一种竞争性干扰,对其实际应用存在很大限制[21]。因此,对SBR-C进行絮凝及解絮凝操作时,由于SS干扰,会不可避免损失部分Nano-TiO2。经过5次循环降解后,其CODCr降解率从78.3%降至58.6%,系统光催化氧化降解性能下降了25.2%。
Nano-TiO2光催化-磁絮凝回收循环光降解SBR-T的效果如图10(b)所示。絮凝处理可大幅降低造纸废水中SS等水质指标,更有利于废水的深度处理,且造纸废水中会与Nano-TiO2结合的表面带负电的SS已被预先除去,在后续过程中可以很大程度上避免SS的干扰,从而减少Nano-TiO2流失。经过5次循环降解后,其CODCr降解率从73.6%降至65.2%,系统光催化氧化降解性能仅下降了11.4%。
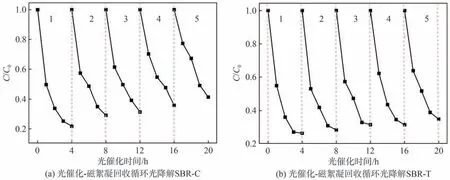
图10 Nano-TiO2光催化-磁絮凝回收循环光降解造纸废水性能Fig.10 Papermaking wastewater performance after photocatalysis and magnetic flocculation recovery of Nano-TiO2 combined with cyclic photodegradation
3 结论
本研究采用溶胶凝胶法制备了磁性絮凝剂Fe3O4/SiO2(FS),通过调节溶液pH值来改变FS和TiO2的表面电荷,从而实现纳米TiO2(Nano-TiO2)的回收及释放;并探讨了pH值、FS/Nano-TiO2质量比和Nano-TiO2浓度对磁絮凝回收性能的影响,以及造纸废水的不同预处理方式对Nano-TiO2磁絮凝回收循环光催化氧化降解造纸废水性能的影响。
3.1 通过调节pH值可实现Nano-TiO2的磁絮凝回收及解絮凝释放,不同FS/Nano-TiO2质量比下,Nano-TiO2回收率都能达到99%,但高质量比的絮凝体絮凝沉降速率更快,且在磁性回收过程中不会释放Nano-TiO2;而相同FS/Nano-TiO2质量比下,Nano-TiO2浓度越高,越有利于絮凝体的自然沉降。
3.2 Nano-TiO2在去离子水中经过5次回收和释放后,系统依然保持良好的絮凝性能,每次回收率都能达到99%,而在释放Nano-TiO2并通过磁性分离出FS后,Nano-TiO2能重新分散在溶液中,从而进行下一次的光催化氧化降解。
3.3 经过絮凝处理的造纸废水(SBR-T),固体悬浮物去除率达94.5%,且在经过5个循环降解后,相较于离心处理的造纸废水(SBR-C)的光催化氧化降解性能下降了25.2%,SBR-T的光催化氧化降解性能仅下降了11.4%,因此,预处理可降低造纸废水的固体悬浮物等指标,有利于保持Nano-TiO2在多次循环使用后的光催化性能。
