艾尔巴韦/格拉瑞韦治疗基因1b型慢性丙型肝炎患者疗效研究*
2022-11-21许海玲
许海玲,秦 刚,薛 红,章 颖
慢性丙型肝炎( chronic hepatitis C,CHC) 是由丙型肝炎病毒( hepatitis C virus,HCV) 感染导致的慢性传染性肝病,可进一步向肝硬化、肝衰竭或肝癌等发展[1]。流行病学调查研究显示[2],目前全球HCV感染率在2.8%左右,且每年CHC新发病例达到3.5万例以上。临床上,积极进行抗病毒清除治疗可降低相关并发症发生率,改善预后[3]。利巴韦林联合聚乙二醇α-干扰素治疗方案被广泛应用于治疗CHC患者,相较于普通α-干扰素,其半衰期长且有效率高[4]。我国HCV感染基因类型主要为1型为主,占比达56.8% ,在这其中又以 1b 型更为常见。然而,与其它基因型比较,1b 型往往发展为肝癌的风险更大,而对标准抗病毒治疗的效果不甚理想[5]。近年来,临床治疗CHC患者的药物研究取得了较大的进展,直接抗病毒药物( directly acting antivirals,DAAs)发展迅速,趋向于成为临床治疗的主流方案之一[6]。在2018年,新型抗HCV药物艾尔巴韦/格拉瑞韦被批准在我国上市,该药包括格拉瑞韦100 mg和艾尔巴韦50 mg,可用于治疗1型和4 型HCV感染的非肝硬化或处于代偿期肝硬化患者[7]。本研究应用艾尔巴韦/格拉瑞韦治疗CHC患者,观察了疗效情况,现报道如下。
1 资料与方法
1.1 病例来源 2018年6月~2020年12月我院收治的基因1b型CHC患者68例,男36例,女32例;年龄为28~57岁,平均年龄为(41.7±6.3)岁;体质指数为18.8~26.7 kg/m2,平均为(23.1±0.8)kg/m2。符合《丙型肝炎防治指南》[8]的诊断标准,经基因芯片法检测为HCV基因1b型感染。纳入患者既往未接受过抗HCV治疗。排除标准:合并甲型、乙型肝炎病毒感染或HIV感染;合并酒精性肝炎;处于失代偿期肝硬化;合并其它严重的器质性病变;合并恶性肿瘤或血液系统疾病。入组对象签署知情同意书,本研究得到我院医学伦理委员会批准。
1.2 治疗方法 采用随机数字表法将患者分为观察组34例和对照组34例。给予对照组利巴韦林(国药集团国瑞药业,国药准字H20020317)300 mg口服,3次/d,聚乙二醇干扰素α-2a注射液(上海罗氏制药,国药准字S20040007)180μg皮下注射,1次/w;给予观察组艾尔巴韦/格拉瑞韦(MSD International GmbHMSD,批准文号H20180017)150 mg口服,1次/d。两组均连续治疗24 w,随访24 w。
1.3 疗效评估 参照《丙型肝炎防治指南》[8],将治疗效果分为快速病毒学应答(rapid virological response,RVR):治疗4 w血清 HCV RNA检测阴性;早期病毒学应答( early virological response,EVR) :治疗12 w血清HCV RNA检测阴性;治疗结束时病毒学应答(end-of-treatment response,ETVR) :治24 w血清HCV RNA检测阴性;持续病毒学应答( sustained virological response,SVR) :治疗结束后随访24 w时血清HCV RNA检测阴性。
1.4 指标检测 使用美国ABI7500型实时荧光定量PCR分析仪检测血清HCV RNA载量;采用ELISA法检测血清 L-选择素(L-selectin)、C反应蛋白(C-reactive protein,CRP)、白细胞介素6(interleukin- 6,IL-6)和肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α,深圳普门试剂);使用希森美康XE-2100型全自动血细胞分析仪检测血常规。
2 结果
2.1 两组病毒学应答比较 观察组RVR、EVR、ETVR和SVR显著高于对照组(P<0.05,表1)。

表1 两组病毒学应答率[n(%)]比较
2.2 两组血清HCV RNA水平比较 在治疗4 w、12 w、24 w和随访24 w时,观察组血清HCV RNA水平显著低于对照组(P<0.05,表2)。

表2 两组血清HCV RNA水平比较
2.3 两组肝功能指标比较 在治疗24 w结束时,观察组血清ALT和AST水平显著低于对照组(P<0.05,表3)。
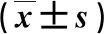
表3 两组肝功能指标比较
2.4 两组血清炎性指标水平比较 在治疗24 w末,观察组血清L-selectin、CRP、IL-6和TNF-α水平显著低于对照组(P<0.05,表4)。
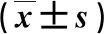
表4 两组血清炎性指标比较
2.5 两组血常规指标比较 在治疗24 w末,观察组外周血白细胞、红细胞、血小板计数和血红蛋白水平显著高于对照组(P<0.05,表5)。
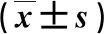
表5 两组血常规指标比较
2.6 两组不良反应发生率比较 在治疗期间,对照组发热和白细胞减少发生率显著高于观察组(P<0.05,表6)。

表6 两组不良反应发生率[n(%)]比较
3 讨论
CHC是致终末期肝病、肝癌及其它肝脏相关性死亡的重要因素之一。临床上,约55%~85%HCV感染者将进展为CHC患者,10%~20%患者在感染发生后的20~30年发展成为肝硬化,并在肝硬化发生后,约有1%~5%进一步进展为肝癌[9]。我国感染HCV基因型以1b 型为主。1b基因型HCV感染患者慢性化率较整体感染者高,往往更易进展为肝硬化或肝癌[10]。因此,对CHC患者予以有效的抗病毒治疗,对于延缓疾病进展极为重要。
利巴韦林联合聚乙二醇干扰素-α是治疗CHC患者的标准方案,但临床应用研究发现,对于相当一部分基因1b型CHC患者治疗应答效果差。DAAs是近年来发展起来的治疗CHC的新型药物,可靶向作用于HCV蛋白酶等位点,有效抑制病毒复制[11]。艾尔巴韦/格拉瑞韦是一种新型治疗HCV感染药物,属于NS3/4A蛋白酶抑制剂(格拉瑞韦)和NS5A蛋白酶抑制剂(艾尔巴韦),主要针对1型和4型HCV感染的CHC患者[12]。应用艾尔巴韦/格拉瑞韦治疗CHC患者,每日仅需口服给药1次,较为方便,有利于提高患者的依从性。自从2018年艾尔巴韦/格拉瑞韦在我国上市以来,取得了良好的治疗效果。
一项多中心临床研究发现[13],亚太地区人群基因1b型CHC患者在接受艾尔巴韦/格拉瑞韦治疗3个月后,病毒学应答率高达90%以上。本研究观察组RVR、EVR、ETVR和SVR分别达到70.6%、91.2%、97.1%和94.1%,显著高于对照组。同时,患者血清HCV RNA载量也显著低于对照组,提示应用艾尔巴韦/格拉瑞韦治疗基因1b型CHC患者疗效确切,病毒学应答率高。艾尔巴韦/格拉瑞韦口服后进入血液,经肝脏代谢。药物与肝细胞膜相结合,发挥抑制病毒复制的作用[14]。本研究在治疗后,观察组血清ALT和AST水平显著低于对照组,表明相较于利巴韦林联合聚乙二醇干扰素-α,应用艾尔巴韦/格拉瑞韦治疗可更有效改善CHC患者肝功能,减轻肝功能损伤,即在病毒学应答效果好的同时,生化学应答率也较高,艾尔巴韦/格拉瑞韦有效降低了HCV患者血清HCV RNA载量,减轻病毒复制导致的肝损伤,机体炎性反应轻,促进了肝功能的恢复,其效果显著优于利巴韦林联合聚乙二醇干扰素-α治疗[15]。
CHC患者体内慢性炎症反应在肝硬化和肝癌发生进程中发挥重要作用。在感染HCV后,巨噬细胞被激活,分泌多种细胞因子,在这其中IL-6参与炎性细胞因子的活化;TNF-α可加强中性粒细胞趋化性,从而损伤肝细胞,促进成纤维细胞增殖,推进肝纤维化发生和发展;CRP可活化T 细胞和巨噬细胞等,通过免疫应答损伤肝细胞,而L-selectin属细胞黏附分子,机体在被炎症刺激时,L-selectin介导白细胞沿血管内皮移动,其水平在一定程度上反映机体免疫功能水平和肝损伤程度[16-18]。本研究治疗后观察组血清IL-6、TNF-α、CRP和L-selectin水平均显著低于对照组,提示应用艾尔巴韦/格拉瑞韦治疗后患者机体炎性反应得到有效控制。艾尔巴韦/格拉瑞韦抑制细胞色素P450合成过程,加强氧自由基清除,减轻氧化应激,抑制肝细胞凋亡,有效减轻机体炎症反应[19]。进一步分析应用艾尔巴韦/格拉瑞韦治疗的安全性,发现在治疗期间观察组白细胞、红细胞、血小板计数和血红蛋白水平均显著高于对照组,提示相较于利巴韦林联合聚乙二醇干扰素-α治疗,应用艾尔巴韦/格拉瑞韦对机体血细胞的影响比较小。本研究还发现,在治疗期间,观察组不良反应发生率相对较少,仅出现一些头晕、恶心和疲劳现象,提示应用艾尔巴韦格拉瑞韦治疗无明显的不良反应,患者耐受性较好[20]。
综上所述,应用艾尔巴韦/格拉瑞韦可有效抑制CHC患者HCV复制,病毒学应答率高,有利于肝功能的恢复,机体炎性反应轻,不良反应小,显示出良好的治疗前景。
