地西他滨、阿扎胞苷治疗高危骨髓增生异常综合征的疗效分析
2022-11-21唐琳洁罗泉芳朱世为王薇
唐琳洁 罗泉芳 朱世为 王薇
541800 广西壮族自治区南溪山医院血液内科,广西桂林
骨髓增生异常综合征(MDS)属于异质性髓系克隆性疾病的一种,与造血干细胞具有密切关系,是老年人最常见的恶性血液病。MDS 具有高度异质性,患者的自然病程和预后差别极大,故个体治疗方案不同[1]。去甲基化药物属于一线化疗药物,其强度较弱,在很大程度上可缩短病程时间,减少病情转化率。目前去甲基化药物主要有阿扎胞苷和地西他滨两种,临床治疗选择何种药物在不断探索[2]。本研究对高危MDS 患者分别采用阿扎胞苷和地西他滨治疗,分析比较两种药物临床治疗效果,旨在探讨更有效治疗MDS的方法,为MDS患者选择治疗方案提供依据。现报告如下。
资料与方法
选取2020年3月-2021年12月广西壮族自治区南溪山医院收治的高危MDS患者28例,随机分为两组,各14例。对照组男9例,女5例;年龄50~80岁,平均(71.2±2.5)岁;骨髓原始细胞检查比例6.8%~16.3%,平均(11.23±2.52)%。观察组男7 例,女7 例;年龄51~80岁,平均(70.5±2.3)岁;骨髓原始细胞检查比例6.5%~15.8%,平均(11.51±2.44)%。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。
纳入标准:①患者符合MDS的诊断标准;②患者及家属详细阅读本研究手册,了解研究的目的、流程,并自愿签署知情同意书;③本研究经医院伦理委员会审批通过。
排除标准:①排除恶性肿瘤疾病患者;②排除全身感染性疾病、免疫功能障碍患者;③排除不配合治疗患者;④排除存在重要靶向器官功能障碍疾病患者。
治疗方法:对照组采用阿扎胞苷(生产厂家:商品名:维达莎,Baxter Oncology GmbH,国药准字:H20170238,规格:100 mg)进行治疗,每次使用剂量为75 mg/㎡,皮下注射,连续用药7 d,28 d为1个治疗周期,共治疗4 个周期。观察组采用地西他滨(生产厂家:杭州中美华东制药有限公司;批准文号:国药准字H2016324)进行治疗,每次使用剂量为20 mg/㎡,静脉滴注,连续用药5 d,28 d为1个治疗周期,共治疗4个周期。
观察指标:观察两组患者治疗效果、不良反应发生率、生存质量、血常规指标情况。不良反应包括骨髓抑制、肺部感染、消化道反应。生存质量利用生存质量中心调查量表(EORTC QLQ-C30)评估,包括躯体功能、角色功能、认知功能、情绪功能、社会功能,各项评分为10 分,分数越高表示生存质量越好[3]。血常规指标包括血红蛋白、白细胞计数、中性粒细胞计数。
疗效判定标准:根据《血液病诊断及疗效标准》[4]对临床疗效进行评估。①完全缓解:治疗后,患者体征、临床症状基本消失,骨髓原始细胞比例≤5%;②部分缓解:治疗后,患者体征、临床症状好转,骨髓原始细胞比例>5%,但与治疗前相比下降程度>50%;③未缓解:未达到以上疗效标准。总有效率=(完全缓解+部分缓解)例数/总例数×100%。
统计学方法:数据采用SPSS 20.0 统计学软件处理,计量资料采用(±s)表示,进行t检验;计数资料以[n(%)]表示,采用χ2检验。P<0.05为差异有统计学意义。
结 果
两组患者临床疗效比较:两组患者治疗后,观察组总有效率为71.4%,对照组为57.1%,两组差异有统计学意义(P<0.05)。见表1。
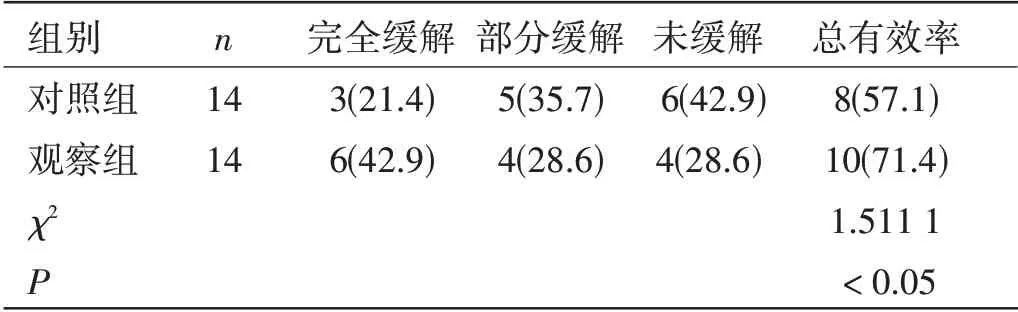
表1 两组患者临床疗效比较[n(%)]
两组不良反应发生率比较:观察组不良反应发生率为42.9%,对照组为35.7%,两组差异无统计学意义(P>0.05)。见表2。

表2 两组不良反应发生率比较[n(%)]
两组生存质量比较:观察组患者治疗后生存质量评分与对照组比较均明显升高,差异有统计学意义(P<0.05)。见表3。随访1年后,观察组生存率为85.7%(12/14),明显高于对照组的64.3%(9/14),两组差异有统计学意义(P<0.05)。
表3 两组患者治疗后生存质量评分比较(±s,分)

表3 两组患者治疗后生存质量评分比较(±s,分)
组别n躯体功能角色功能认知功能情绪功能社会功能对照组146.6±1.37.8±1.66.1±1.97.5±1.57.9±1.8观察组147.6±1.58.0±1.37.9±1.48.6±1.89.2±0.2
两组患者治疗前后血常规指标比较:两组患者治疗前血红蛋白、白细胞计数、中性粒细胞计数比较,差异无统计学意义(P>0.05)。治疗后,观察组各指标改善情况明显优于对照组,两组差异有统计学意义(P<0.05)。见表4。
表4 两组患者治疗前后血常规指标比较(±s)

表4 两组患者治疗前后血常规指标比较(±s)
注:与同组治疗前比较,*P<0.05;与对照组治疗后比较,#P<0.05
组别n时间血红蛋白(g/L)白细胞计数(×109/L)中性粒细胞计数(×109/L)对照组14治疗前74.18±4.122.61±1.121.05±0.05治疗后82.16±4.20*2.97±1.09*1.25±0.13*观察组14治疗前74.18±4.152.62±1.051.04±0.09治疗后88.62±4.09*#2.85±1.11*#1.32±0.11*#
讨 论
高危MDS 患者很容易发展成为急性白血病,对患者的生命安全造成极大威胁[5-6]。MDS 发病机制非常复杂,目前主要采用支持治疗或者化疗以延长患者生命。近年来,临床研究发现表观遗传学修饰治疗对MDS 疾病的缓解具有积极作用,将去甲基化药物应用于MDS 治疗中可提升临床疗效,改善患者的生存质量[7-9]。本研究针对地西他滨和阿扎胞苷治疗高危MDS 的效果进行分析,两种药物均为去甲基化药物,其中阿扎胞苷属于抗肿瘤药物之一,可有效调控异常细胞的分化与凋亡,能够直接作用于患者骨髓中异常的造血细胞,也可以作为DNA 甲基转移酶抑制剂的一种[10-11]。地西他滨则是经过磷酸化后,直接作用于DNA,有效减少DNA 甲基化转移酶的产生,抑制细胞分化、凋亡,逆转DNA 甲基化。除此之外,地西他滨还能够诱导肿瘤细胞向正常细胞分化,或促进肿瘤细胞凋亡[8]。通过本次研究分析,地西他滨的疗效更加显著,但不良反应发生率较高,干预后血常规指标改善情况优于阿扎胞苷,因此医生需要评估两种药物的远期疗效与患者的耐受性进行选择。目前众多文献研究表明[12],地西他滨和阿扎胞苷治疗MDS 的疗效无明显差异,但地西他滨适用于年轻患者,阿扎胞苷的不良反应较小,适用于老年患者。
综上所述,与阿扎胞苷相比,地西他滨治疗高危MDS 的效果更加理想,但是该药物的不良反应发生率较高,因此医生在进行药物选择时,需根据患者病情慎重考虑,以保障患者的生存质量。同时本研究也存在一定的问题,如样本量较少,研究存在局限性,所以还需要加大样本量以进行后期进一步研究。
