3,5-二氯苯甲酸的合成
2022-11-18袁勇军丁钰涵陈秋平
袁勇军,丁钰涵,陈秋平,杨 华,曾 礼
(1.浙江万里学院,浙江 宁波 315100;2.大连大学医学院,辽宁 大连 116622;3南昌大学化学学院 江西 南昌 330031)
3,5-二氯苯甲酸为一重要中间体化合物[1-5],可广泛应用于涉及到酰基引入的反应,如合成信号分子酰基高丝氨酸内酯衍生物。
传统的3,5-二氯苯甲酸合成有两条路线,路线一是以3,5-二氯甲苯(3,5-dichlorotoluene)为原料,具体工艺为在185℃下,向3,5-二氯甲苯中通入氯气经过光照的催化生成3,5-二氯三氯苄。再向生成物中加入发烟硫酸后再搅拌反应30 h,将产物先进行冷却再通过加入强碱生成盐后再酸化的方法进行纯化。合成路线如图1所示:
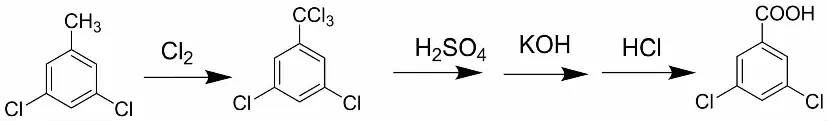
图1 3,5-二氯苯甲酸合成路线一Fig.1 One of The Synthesis Routes of 3,5-Dichlorobenzoic Acid
此法反应步骤长,原料3,5-二氯甲苯难得且其价格甚至远远高于目标产物的价格。而且此法需运用大量的酸碱,会产生大量废液,无论从经济角度还是环保角度,此法都不适合如今的工业化生产。
第二条传统的3,5-二氯苯甲酸合成路线是以3,5-二氯乙苯(3,5-dichloroethylbenzene)为原料,具体工艺为在75 ℃~80 ℃下,3,5-二氯乙苯在碱性条件下经次氯酸钠的氧化得到对应盐,再经过酸化得到3,5-二氯苯甲酸。合成路线如图2所示:
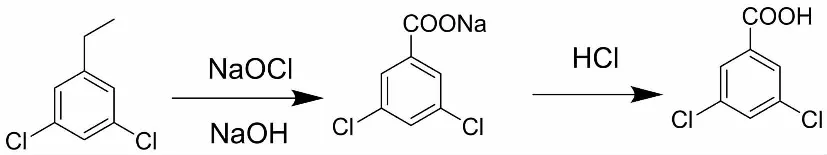
图2 3,5-二氯苯甲酸合成路线二Fig.2 The Second Synthesis Route of 3,5-Dichlorobenzoic Acid
此法较路线一进行了优化,简化了反应步骤,但总体来说原料依旧昂贵且产生大量废液,并不适用于工业化生产[6-8]。
为解决传统合成路线原料不易获得,收率低,工艺污染大等问题[9-11]。本文研究了一条新的合成路线,以期为3,5-二氯苯甲酸合成提供更环保,简洁高效的方法。
1 材料方法
1.1 试剂
2-硝基苯甲酸、锌粉、氯化铵、盐酸,亚硝酸钠,硫酸铜等均购自阿拉丁(上海阿拉丁生化科技股份有限公司)。所有试剂均为分析纯级。
1.2 方法
1.2.1 邻氨基苯甲酸的合成
该工艺中原料为硝基苯甲酸,通过锌粉在氯化铵溶液中,将其硝基还原成氨基,得到邻氨基苯甲酸。反应方程式如图3所示:
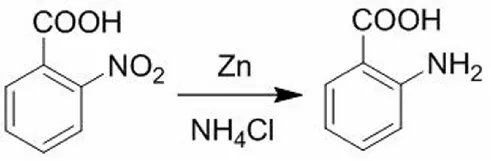
图3 邻氨基苯甲酸的合成反应方程式Fig.3 The Synthetic Reaction Equation of Anthranilic Acid
具体操作如下:称取8.4 g(0.05 mol)邻硝基苯甲酸,14.6 g(0.225 mol)活化的锌粉以及18.7 g(0.4 mol)氯化铵于250 mL的三口烧瓶中,加入100 mL蒸馏水,加热至回流,2 h反应完毕。用布氏漏斗趁热抽滤,过滤掉未反应的锌粉,然后待滤液自然冷却至室温,有大量黄白固体析出。再将滤液进行抽滤,得到黄白色固体,干燥后称量,测其熔点测为141 ℃~142 ℃。谱图为:1H-NMR (600 MHz,DMSO-d6)δ:12.58(s,1H),7.20~7.15(m,1H),7.11(t,J=7.6 Hz,1H),7.07~7.08(m,,1H),6.75~6.77(m,1H),5.32(s,2H);ESI-MS m/z(%):138.0566([M+H]+)。
1.2.2 2-氨基-3,5-二氯苯甲酸的合成
该工艺中,原料为上述所得邻氨基苯甲酸,将其与氯气进行取代反应,得到2-氨基-3,5-二氯苯甲酸。反应方程式如下图所示:

图4 2-氨基-3,5-二氯苯甲酸的合成反应方程式Fig.4 The Synthetic Reaction Equation of 2-Amino-3,5-Dichlorobenzoic Acid
具体操作如下:取13.7 g(0.1 mol)邻氨基苯甲酸以及200 mL醋酸、50 mL蒸馏水于500 mL四口烧瓶中,并加入0.1 g三氯化铁作为催化剂,升温至30 ℃后,约3 h内向烧瓶中缓慢通入15.6 g(0.22 mol)氯气,不断搅拌反应。此反应需严格检查装置气密性并做好尾气吸收工作,3.5 h反应结束后通入氮气将未反应的氯气以及氯化氢气体吹出。将反应液抽滤,取滤饼在真空干燥箱中干燥,干燥后得到白色固体16.2 g,测其熔点为242 ℃~244 ℃(文献值240 ℃)。谱图为:1H-NMR(600 MHZ,DMSO-d6)δ:13.34(s,1H),7.69(d,J=2.5 Hz,1H),7.64(d,J=2.5 Hz,1H),6.92(s,2H);ESI-MS m/z(%):203.965 3([M-H]-)。
采用正交实验设计对影响反应的4个参数,即温度,氯气量,反应时间,溶剂含水量进行优化,每一个因素设计3个水平。正交设计表头如表1:1.2.3 3,5-二氯苯甲酸的合成该工艺中,原料为上步所得2-氨基-3,5-二氯苯甲酸,先与亚硝酸钠反应生成对应重氮盐,再被异丙醇还原脱氨基得到所需产物。反应方程式如图5所示:

表1 合成2-氨基-3,5-二氯苯甲酸的正交实验因素水平Tab.1 Orthogonal experimental factor levels for the synthesis of 2-amino-3,5-dichlorobenzoic acid

图5 合成3,5-二氯苯甲酸的反应方程式Tab.5 The reaction equation for the synthesis of 3,5-dichlorobenzoic acid
具体操作如下:取3.8 g(0.055 mol)亚硝酸钠配置成35%的溶液。称取10.3 g(0.05 mol)2-氨基-3,5-二氯苯甲酸和0.1 g硫酸铜于三口烧瓶中,再加入30 mL异丙醇15 mL浓盐酸20 mL蒸馏水作为溶剂,升温至80 ℃后溶液开始回流,在剧烈搅拌下向2-氨基-3,5-二氯苯甲酸溶液中缓慢滴加配置好的亚硝酸钠溶液,保温反应3 h。反应结束后,将反应液倒入100 mL冰水中,有棕色固体析出,抽滤,干燥后得灰白固体,测其熔点为181 ℃~182 ℃(文献值为186 ℃~188 ℃)。谱图为:1H-NMR(600 MHZ,DMSO-d6)δ:13.72(s,1H),7.91(t,J=2.0 Hz,2H),7.86(d,J=2.0 Hz,2H);ESI-MS m/z(%):188.943 8([M-H]-)。
采用响应曲面法对影响反应的3个参数即浓盐酸的量,亚硝酸钠的量,硫酸铜的量进行优化,采用中心组合设计,如下表所示:

表2 响应曲面实验因素水平及编码Tab.2 Response Surface Experiment Factor Levels and Coding
3 结果
3.1 锌粉和氯化铵添加量对邻氨基苯甲酸合成的影响
采用单次单因素实验设计分别考察反应中锌粉和氯化铵的添加量。通过固定其他反应条件即0.05 mol邻硝基苯甲酸,0.4 mol氯化铵,100 mL水,恒温100 ℃,考察不同锌粉添加量对反应得率的影响。通过固定其他反应条件即0.05 mol邻硝基苯甲酸, 0.225 mol锌粉,100 mL水,恒温100 ℃,考察不同氯化铵添加量对反应得率的影响。
此步反应中的原料邻硝基苯甲酸以及产物邻氨基苯甲酸都能溶解于热水中,故溶剂直接选用水。反应随着温度上升反应速率和转化率都有所升高,控制反应温度为100 ℃即可。锌粉还原反应需在酸性条件下进行,但如果直接使用盐酸溶液会使反应过于剧烈,同时锌粉会和盐酸反应造成大量无谓消耗。常采用廉价高效的氯化铵作为提供质子的物质。故锌粉以及氯化铵的用量为此反应的重要参数。
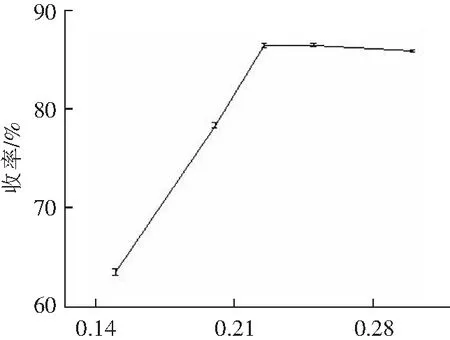
锌粉的量/mol图6 锌粉添加量对反应收率的影响Fig.6 Effect of zinc powder addition on reaction yield

锌粉的量/mol图7 氯化铵添加量对反应收率的影响Fig.7 Effect of ammonium chloride addition on reaction yield
理论上还原1 mol的硝基成氨基所消耗的锌粉量为3 mol,不过此反应是固液两相反应,为使反应更加充分需增大反应接触面积,锌粉的用量往往要大于理论值。由上图可以看出,锌粉量少时反应进行不够彻底,量过多后期处理时也可能造成一定的损失,取4.5当量时收率达到最大值86.4%。
此反应要使得硝基被还原成氨基,则反应需要在酸性条件下进行才能生成目的产物。氯化铵的加入既是为了维持酸性条件同时也为此反应提供质子使反应能顺利进行,理论上还原1 mol的硝基成氨基需要消耗6 mol的H+,但实际氯化铵的用量也需过量。由上图可以看出,氯化铵用量为9当量时收率达到最大值88.7%,继续加大量无意义。
根据以上单因素实验结果,此反应中反应温度100 ℃,反应时间2 h,n(2-硝基苯甲酸):n(锌粉):n(氯化铵)=1:4.5:9时,收率最大为88.7%。
3.2 不同变量对2-氨基-3,5-二氯苯甲酸合成的影响
苯环上卤素的亲电取代反应活性在较强的极性溶剂以及三氯化铁这类路易斯酸或者金属铁的催化下能够被大大加强[12,13]。该工艺中反应本质是苯环上发生亲电取代。首先氯气在催化剂的作用下生成了带正电的亲电试剂Cl+,再与苯环反应生成σ络合物,最后σ络合物失去H+得到一氯取代产物。因为此反应中原料邻氨基苯甲酸含有氨基能极大活化苯环,因此一氯取代物还能进一步发生亲电取代生成二氯取代物[14],从而得到目的产物氨基-3,5-二氯苯甲酸。
此反应是邻氨基苯甲酸中苯环上的氯化反应。其中氨基是第一类定位基,羧基是第二类定位基,所以理论上本氯化反应会优先取代三号位以及五号位的氢[15]。
溶剂方面,原料邻氨基苯甲酸在醋酸中溶解性良好,并且目的产物2-氨基-3,5-二氯苯甲酸不溶于醋酸,这样利于产物的分离,因此选醋酸为反应溶剂。此反应的副产物是氯化氢,可以通过溶剂中加入少量水来溶解生成的氯化氢从而调节pH以使转化率达到最大。其他影响反应的条件经正交实验结果如表3:
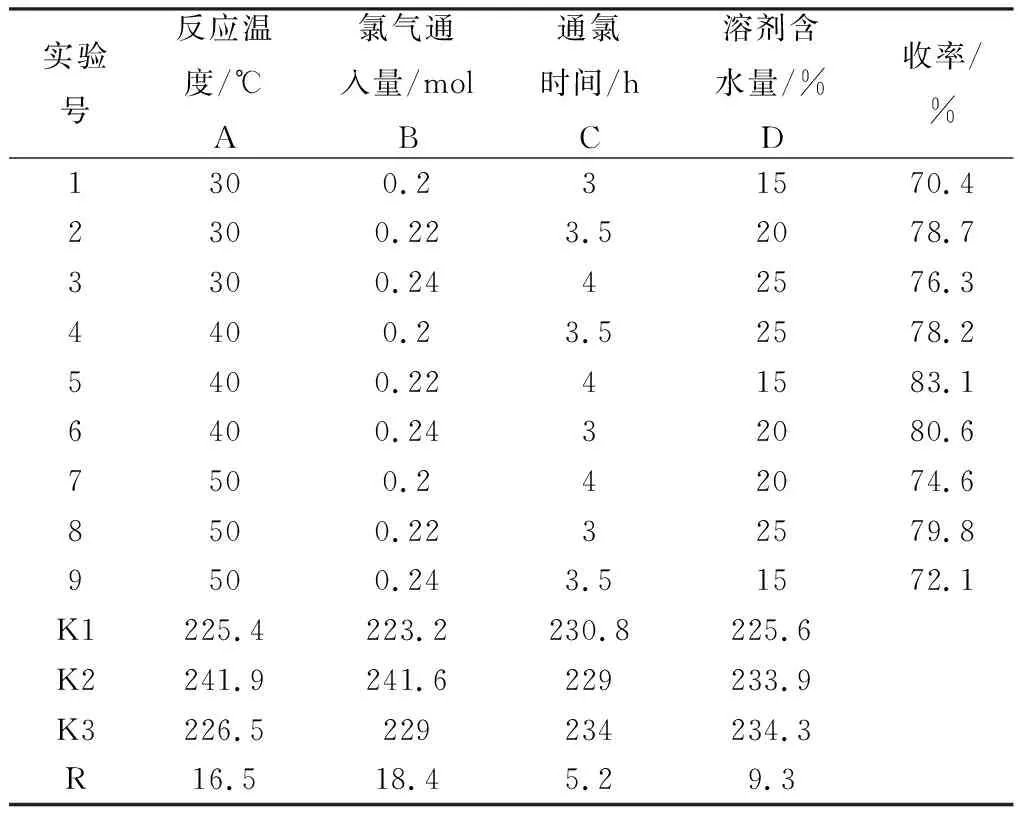
表3 合成2-氨基-3,5-二氯苯甲酸的正交实验结果Tab.3 Orthogonal Experimental Results for The Synthesis of 2-Amino-3,5-Dichlorobenzoic Acid
从上表可知,依据各因素的R值的大小(RB>RA>RD>RC),对此反应影响最大是通氯量,其次是反应温度,含水量以及通氯时间影响较小。综合来看,本实验中收率较高的方案为:反应温度为40 ℃,氯气通入量为2.2当量,通氯时间为4 h,溶剂含水量为25%。以此参数再进行实验,最后反应收率达到84.3%。
3.3 不同变量对3,5-二氯苯甲酸合成的影响
上述所得2-氨基-3,5-二氯苯甲酸经重氮化脱氨基生成3,5-二氯苯甲酸,但同时生成2-氨基-3,5-二氯苯甲酸的重氮盐也能与2-氨基-3,5-二氯苯甲酸中的氨基发生反应形成偶氮化合物。因此需要加入少量硫酸铜来起到转移电子的作用,使生成的重氮盐更容易被还原从而减少副反应的发生。
重氮化反应一般在低温下进行[16-18],但2-氨基-3,5-二氯苯甲酸呈酸性且不溶于水,它难以在常温甚至低温下与盐酸形成对应盐酸盐,也就难以在低温下与亚硝酸钠反应生成对应重氮盐。不过这同时也说明了2-氨基-3,5-二氯苯甲酸的重氮盐有着一定的稳定性,它不会过快地发生分子间的耦合或者被氧化。所以此反应采用了高温重氮法,在较高温度下2-氨基-3,5-二氯苯甲酸能溶于异丙醇中,易于与盐酸反应生成对应的盐酸盐[19,20]。所以主要影响因子是盐酸、亚硝酸钠、催化剂硫酸铜的投料量。
表4中,试验组1~14是析因试验,试验号15~20是中心试验,中心试验重复六次,用以估计实验误差。通过Design Expert软件对表中数据进行多元回归拟合,得收率对各自变量之间的多元回归模型方程为方程(1)。
Y=72.74-1.65X1-2.41X2+3.67X3-2.32X12-4.28X22+4.77X32+16.25X1X2+1.13X1X3-0.75X2X3
(1)
通过对该模型方差分析和显著性检验,且该模型的相关系数R2=0.979,校正决定系数AdjR2=0.961,预测相关系数PredR2=0.846。显著性分析中,当P<0.05时,即表示该项指标显著,本模型对产率所建立的回归模型是显著的(P<0.000 1),失拟项不显著(P=0.050 6)。说明,此模型与实验数据拟合度较好,试验失拟项小,因此可用该回归方程代替真实点对实验结果进行分析。各因子的一次项和二次项都显著,交互项中只有X1X2显著(P<0.000 1),说明盐酸和硝酸钠的添加量之间存在交互作用,因为他们在体系中都能起到酸的作用,表示二者交互作用的3D响应面图如图8所示:

表4 响应曲面优化试验设计及其结果Tab.4 Response Surface Optimization Experimental Design and Results
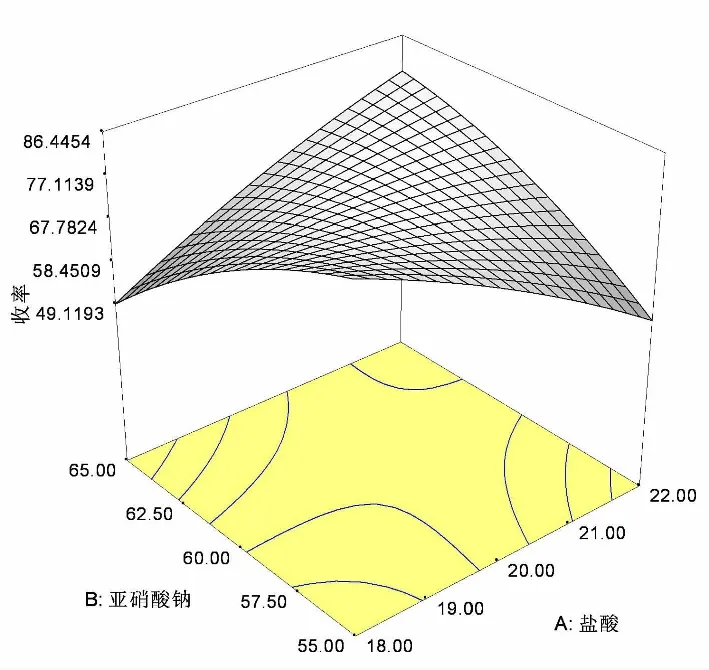
图8 盐酸和亚硝酸钠添加量对反应收率的相应曲面图Figure 7 Corresponding surface plots of hydrochloric acid and sodium nitrite additions to reaction yields
利用Design expert软件,对方程(1)进行分析,求得收率的最大预测值为92%,各主要因素的最佳反应条件为盐酸(37%,w/w)18.11 mL,亚硝酸钠55.3 μmol,硫酸铜添加量为97.52 mg。按上述最佳条件开展了3组验证实验,通过验证实验得到收率的实测值和预测值相似,证明该模型合理有效。
4 讨论
4.1 还原法合成邻氨基苯甲酸的反应机理
此反应是硝基在酸性条件下被锌粉还原成氨基,反应历程为有着电子转移得失的还原反应。Zn(还原剂)在此反应中一直提供着电子,而氯化铵在此反应中不断提供H+,Zn失去的电子转移到硝基的N上,得到了离子自由基后再与H+结合,然后再接受电子生成新的离子自由基而后再和H+结合,如此往复直至硝基完全被还原成氨基。具体反应历程如图9。
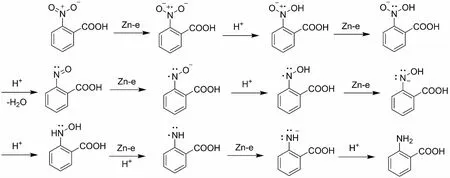
图9 还原法合成邻氨基苯甲酸的反应机理Fig.9 Reaction Mechanism of Reduction Synthesis of Anthranilic Acid
4.2 合成2-氨基-3,5-二氯苯甲酸的反应机理
此反应的本质是苯环上发生亲电取代。苯环上卤素的亲电取代反应活性在较强的极性溶剂以及邻氨基苯甲酸的反应机理FeCl3这类路易斯酸或者金属铁的催化下能够被大大加强。首先氯气在催化剂的作用下生成了带正电的亲电试剂Cl+,再与苯环反应生成σ络合物,最后σ络合物失去H+得到一氯取代产物。此反应中原料含有氨基能极大活化苯环,因此一氯取代物还能进一步发生亲电取代生成二氯取代物。具体反应历程如图10。
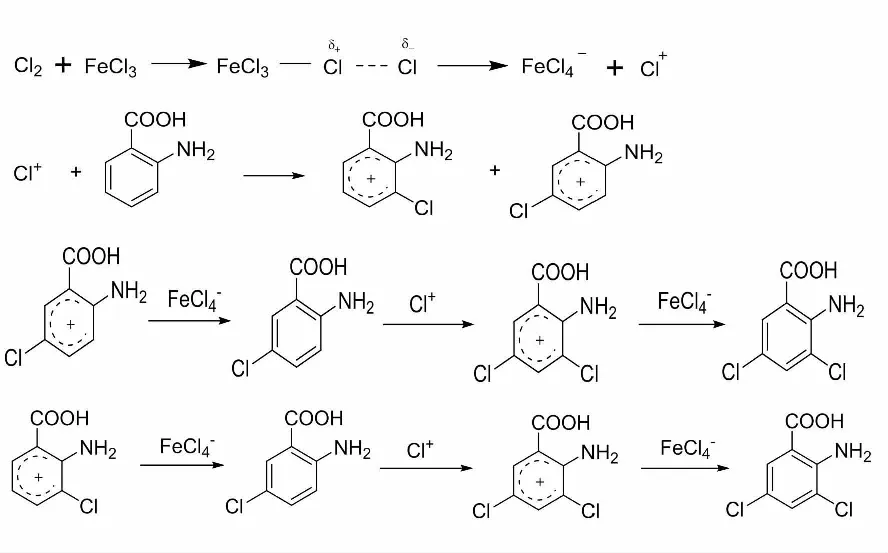
图10 合成2-氨基-3,5-二氯苯甲酸的反应机理Fig.10 Reaction mechanism for the synthesis of 2-amino-3,5-dichlorobenzoic acid
4.3 合成3,5-二氯苯甲酸的反应机理
2-氨基-3,5-二氯苯甲酸经重氮化脱氨基生成3,5-二氯苯苯甲酸,同时反应中生成的重氮盐也能与2-氨基-3,5-二氯苯甲酸中的氨基发生反应形成偶氮化合物。反应中加入少量硫酸铜起到转移电子的作用,能使得生成的重氮盐更容易被还原从而减少副反应的发生。具体反应历程如图11。
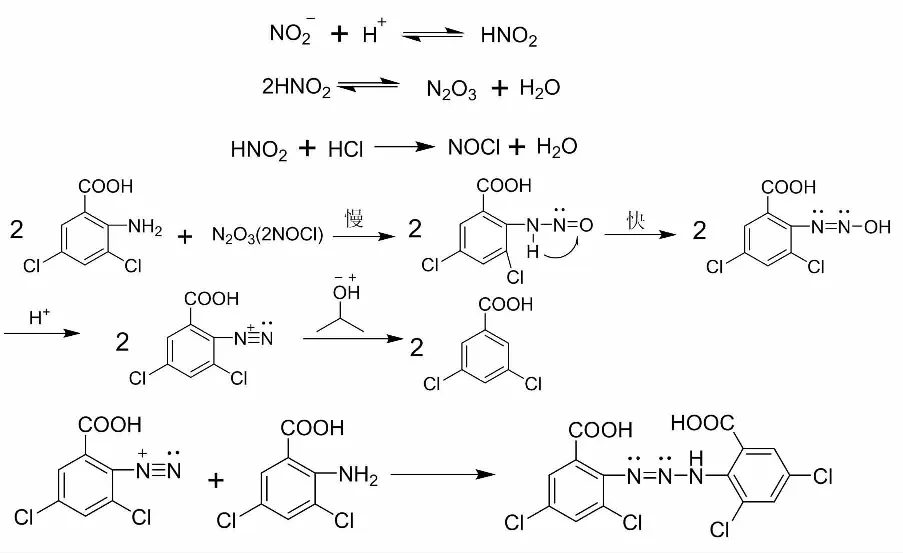
图11 合成3,5-二氯苯甲酸的反应机理Figure 11 Reaction mechanism for the synthesis of 3,5-dichlorobenzoic acid
5 结论
(1)以2-硝基苯甲酸为原料合成邻氨基苯甲酸,经单次单因素条实验结果,此反应中反应温度为100 ℃,反应时间为2 h,n(2-硝基苯甲酸):n(锌粉):n(氯化铵)=1:4.5:9时,收率最大为88.7%。
(2)以邻氨基苯甲酸为原料合成2-氨基-3,5-二氯苯甲酸,经正交优化本工艺中最佳反应温度为40 ℃,氯气通入量为2.2当量,通氯时间为4 h,溶剂含水量为25%本步骤收率可达84.3%。
(3)以2-氨基-3,5-二氯苯甲酸为原料合成3,5-二氯苯甲酸,经响应曲面法优化最佳反应条件为盐酸(37%,w/w)18.11 mL,亚硝酸钠55.3 μmol,硫酸铜添加量为97.52 mg,本步骤收率可达92%。
(4)该路线总收率可达到68%以上。与传统的合成方法相比,该合成方法原料丰富易得,溶剂可回收利用,产生三废较少,适于工业化生产。
