固态电池中的正极/电解质界面性质研究进展
2022-11-18张安邦汪晨阳赵尚骞常增花王建涛
张安邦,汪晨阳,赵尚骞,常增花,王建涛*
(1 有研科技集团有限公司 国家动力电池创新中心,北京 100088;2 国联汽车动力电池研究院有限责任公司,北京 100088;3 北京有色金属研究总院,北京 100088)
锂离子电池已经成为生活的必需品,在消费电子、电动汽车、航空航天等领域发挥着重要作用[1]。然而,含有液态电解液的锂离子电池由于使用易燃的有机溶剂,极易着火甚至爆炸[2]。与目前使用的有机液体电解质不同,无机固态电解质是不易燃的,而且在热失控方面具有更高的起始温度[3]。因此,使用不易燃的固态电解质代替易燃的液态电解液作为锂离子传输的载体,可以极大地提高电池的安全性[4]。此外,由于固态电解质的高机械强度,固态电池有望在一定程度上抑制锂金属电池中枝晶的过度生长,从而使得金属锂作为负极的应用成为可能,这将大大增加电池的能量密度[5]。因此,固态电池被认为是未来的关键电池技术之一,近年来引起极大的关注。
固态电池的研究始于寻找适合作为固态电解质的材料,即同时具有高离子电导率和低电子电导率的材料。最近,硫化物固态电解质的离子电导率已经接近或高于传统的液态电解质,例如Li7P3S11(17 mS·cm-1),Li10GeP2S12(12 mS·cm-1),Li9.54Si1.74P1.44S11.7Cl0.3(25 mS·cm-1)[6-8]。目前开发出的固态电池已经具有与液态电池相当的能量密度,各种类型的固态电池也得到了迅速的发展,简单总结如表1[9-17]所示。
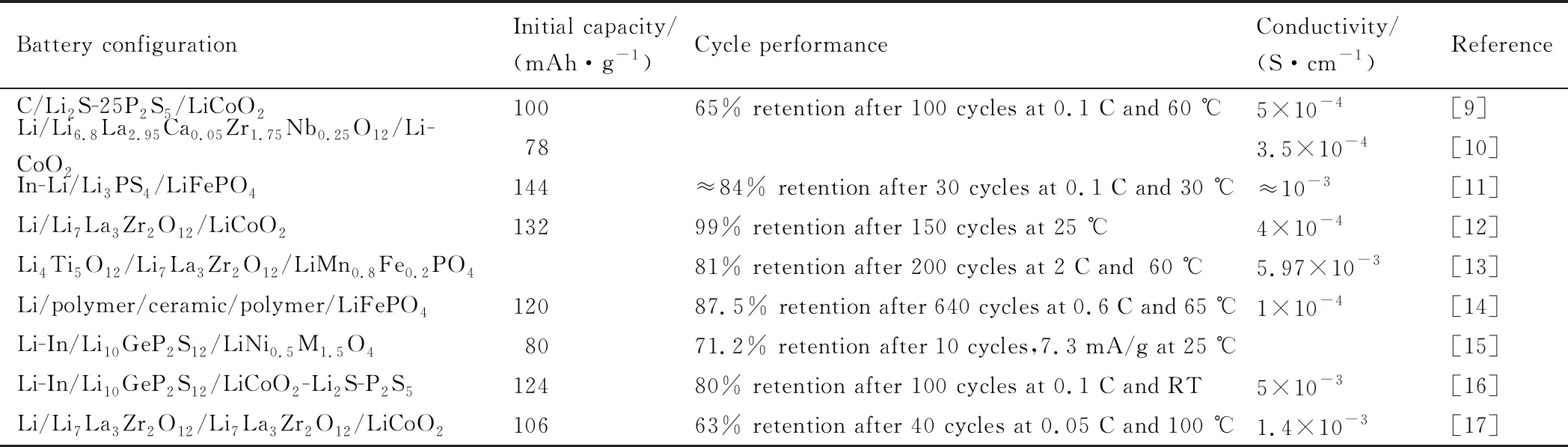
表1 使用各种固态电解质的固态电池的性能
但是,固态电池在研究与应用上仍然存在一些严重问题,例如循环寿命短、性能下降快等,其原因很大程度上与不稳定界面的存在有关,例如空间电荷效应、过渡金属向固态电解质中的扩散、固态电解质的分解等[18]。为了抑制副反应并稳定正极材料/固态电解质界面,就需要进一步探明固态电解质的潜在失效机制,进而开发出高性能的固态电池。
从目前的研究中来看,计算和实验的方法都有助于探索固态电池中界面的复杂性。例如,密度泛函理论(DFT)计算和分子动力学(MD)模拟可以为界面原子相互作用提供理论观点[19]。LiCoO2(LCO)和Li2S-P2S5的界面被计算为热力学不稳定的,因为Co和P可以在界面上进行离子间的扩散反应[20]。尽管理论计算可以预测稳定性和分解产物,但通过实验确定产物的存在及其分布仍然是必要的并且具有挑战性。
鉴于人们对高比能、高安全性的固态电池的需求和研究兴趣日益增长,而界面问题是当前固态电池研发的首要攻关难题。而正极材料相比于负极材料,其物理、化学性质更加复杂,与电解质之间的界面反应尤其难以研究,因此,本文旨在关注当前固态电池各种界面相关研究中的正极/电解质界面的研究进展,综述了固态电池中正极侧的各种界面类型,从物理接触、化学反应、电化学反应等方面分别讨论了正极/电解质界面的特征,针对不同的界面问题,总结了目前主流的解决方案。
1 固态电解质/正极界面的体积效应
在正极活性材料脱锂或嵌锂过程中,其晶胞参数将不可避免地发生缩小或扩大,造成材料颗粒体积形变[21]。尤其在固态电池中,固态电解质与电极颗粒为刚性接触,对电极材料的体积变化更为敏感,循环过程中容易造成电极颗粒之间以及电极颗粒与电解质接触变差,或应力积累造成电解质力学性能失效,进而导致电池电化学性能的衰减[22]。电池循环过程中电极材料不可避免发生体积变化,这将会导致电解质/正极材料颗粒界面处产生应力集中,甚至可能会导致裂缝出现。
体积效应的变化导致接触减少甚至产生裂纹,在锂离子电池中,大多数正极电极材料在嵌锂/脱锂过程中会经历相变、晶格膨胀/收缩和结构变化,导致充放电后材料的体积会有所变化,表2[23-28]简要总结了这些体积变化值。
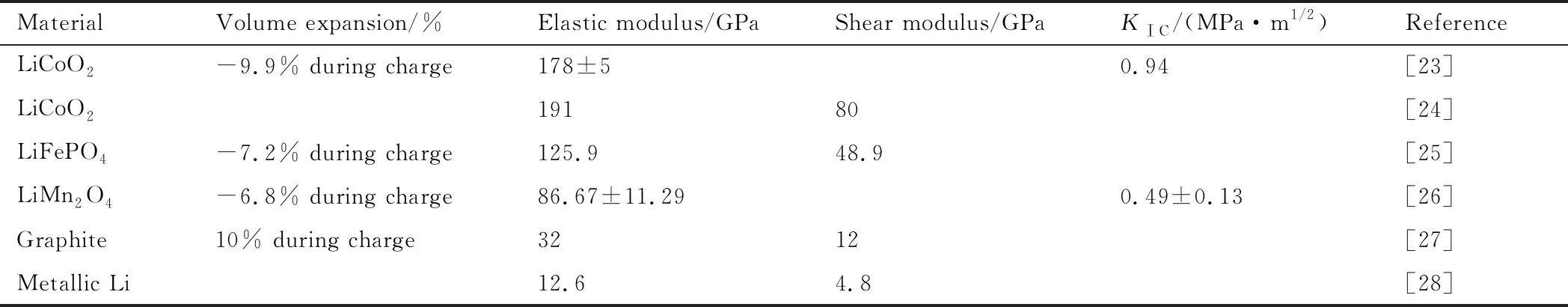
表2 各种正极材料充放电过程中的体积变化和力学性能
反复的膨胀和收缩导致界面接触的不稳定,将会发生如变形、粉化、集流体与电极颗粒之间脱落等现象,从而导致容量衰减。因此,良好的界面机械稳定性同样是获得高性能固态电池的关键,然而到目前为止,在固态电池中此类的研究还较少。由于体积变化引起的应力不能转化为均匀的压力,而压力变化集中由固态电解质承担,这将导致电解质内部出现应力集中。此外,固态电池的正极通常由正极活性材料、导电添加剂、黏结剂和固态电解质组成,在复合正极中,固态电解质的质量分数通常高达50%,因此,固态电池中的应力不仅发生在电极和固态电解质界面处,而且也发生在正极材料和电解质复合材料内部。
例如,Koerver等[21]原位监测了NCM811/β-Li3PS4/Li全固态电池循环过程中的界面接触情况和内部压力,如图1(a)所示,50周次循环后的NCM811与β-Li3PS4界面产生了明显的缝隙。此外,图1(b)[29]中的压力监测数据显示,随着电池充电/放电的进行,其内部压力发生增大/减小的变化,并且变化的程度随充放电深度而改变,电池对应的充放电容量也发生迅速衰减,表明电极材料在循环过程中的体积变化对电池性能有重要的影响。图1(c)为Ma等[29]采用同步辐射得到的三元材料在不同脱锂量下的晶胞体积变化,可以发现在脱出60%(摩尔分数)的Li+前后,其晶胞体积急剧减小。他们认为这主要是因为在三元材料的六方晶系层状结构中,脱锂时过渡金属阳离子会发生氧化,其离子半径减小导致a轴参数减小;而晶格氧和M—O共价键之间的库仑排斥则导致c轴先增大再急剧减小,总体积变化ΔV则为二者叠加造成。除了“零应变”材料Li4Ti5O12(ΔV=0.2%),目前在固态电池中常用的正极材料包括LiCoO2(ΔV=5.56%),LiMnO2(ΔV=3.78%),LiNixCoyMn1-x-yO2(ΔV=6%),LiFePO4(ΔV=6.8%)等都存在明显的体积形变,从而造成电池内部接触情况改变和产生压力应变。图1(d)[30]显示了在首次充电后LiCoO2/Li10GeP2S12/In全固态电池中电解质截面的弯曲情况。由于在充电时,LiCoO2体积减小,而负极In嵌入Li+形成合金体积增大(ΔV=105.6%),这导致电解质在正负界面不均匀受力,弯曲与裂纹应变在其内部会明显生成,也会导致电池性能不佳。为了进一步理解硫化物电解质全固态电池的机械性质,Pervez等[30]测量了LiCoO2,Li2S-P2S5及金属锂的杨氏模量(Young’s elastic modulus,E),硬度(H)以及断裂韧度(KⅠC),如图1(e)所示。他们认为较低的杨氏模量使Li2S-P2S5可以适应循环过程中电极的收缩膨胀,但同时低的断裂韧度会导致其在很低的应力下发生脆性断裂。此外,Pervez等[30]通过电化学-力学模型对固态电解质的机械性质进行定量分析,结果表明,当电解质的杨氏模量为15 GPa时,如果其断裂能Gc≥4.0 J·m-2且电极颗粒的总体积变化ΔV≤7.5%时,则不发生断裂。但是Li2S-P2S5的断裂韧度KⅠC大约为0.23 MPa·m-2,对应的断裂能大约为2.8 J·m-2,小于所要求的最低断裂能值,所以无法避免脆性断裂的发生。需要说明的是,虽然氧化物电解质的杨氏模量高达150 GPa(石榴石结构氧化物),但同样易发生脆性断裂。
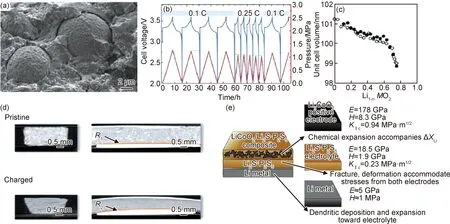
图1 正极界面的体积效应
这些研究表明,电极结构的不稳定性主要表现在正极/电解质界面以及电解质内部,因此,在电池组装过程中,施加外部压力增加各种成分间的接触是必需的,另外,开发具有更高延展性的固态电解质也可在一定程度上适应电极的可逆体积变化,降低体积效应对电池性能的影响。
2 化学稳定性
一般认为,界面相的形成同时受到化学和电化学过程的驱动[31],需要注意的是,化学驱动形成界面的过程无需外加电压,可以看作是一个缓慢的反应过程[3]。化学反应产生的界面分为电子导电层、离子导电层、混合导电层和电子离子双重绝缘层,而界面是否是钝化层取决于界面反应产物的离子电导率和电子电导率[32]。例如,Li3PO4是电子绝缘体和离子导体,允许锂离子在界面上传递[33],而过渡金属硫化物通常是电子导电的,在化学生成的界面上同时存在离子和电子混合导电层会促进固态电解质的电化学分解,从而导致界面的持续增长,不利于电池的性能发挥[34]。一般情况下,电极/电解质界面的化学反应都会消耗一部分锂离子,导致电池在静置过程中初始性能的下降[35]。因此,全面了解固态电池中材料和界面的化学稳定性是十分必要的。
在电池充放电过程开始前,正极/电解质界面保持初始成分和结构的能力对实际电池的设计和制造具有重要意义。Jung课题组[36]用三元材料NMC622和Li6PS5Cl硫化物电解质匹配,组装全固态电池进行电化学性能测试,对照组电池在静置48 h后开始充放电循环,而另一个电池没有进行静置,组装完成后直接进行充放电测试,结果显示没有静置的电池相比于静止48 h的电池,其初始容量较高,而且极化较低(如图2(a)所示),但在循环过程中,未静置的电池的容量保持率较差(图2(b)),这意味着即使不施加任何电压,正极活性物质和Li6PS5Cl之间也存在化学反应。为了验证这一点,他们在不施加任何偏置电压的情况下测量了LiNbO3包覆前后NCM正极材料与电解质的界面阻抗与时间的函数(图2(c)~(e)),结果显示未包覆样品与电解质界面阻抗在48 h内增加了4倍,如图2(d)所示,而包覆后的正极侧界面阻抗几乎没有发生变化,如图2(e)所示。体积阻抗的增加可能是由Li6PS5Cl的降解所导致的,而界面阻抗的增长则是由于离子阻塞层的形成所致,值得注意的是,这种离子阻塞层的形成是由正极材料与电解质在未施加任何电压的情况下发生反应导致的。
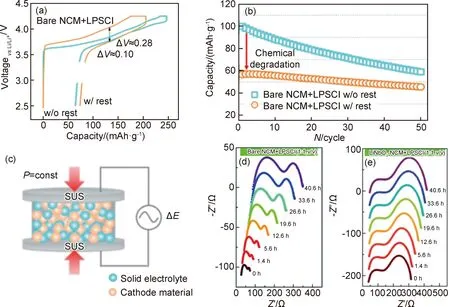
图2 正极/电解质界面的化学不稳定性对电化学性能的影响[36]
对于硫化物电解质来说,如果正极材料和固态电解质颗粒只是简单地混合在一起,则不易在界面上观察到分解产物[37],说明当接触不足时,两者的化学反应是缓慢进行的[38]。然而,由于氧化物电解质具有较高的硬度和较低的表面能,在氧化物基的固态电池制造过程中,需要在高温下使得正极与氧化物电解质颗粒之间的接触变得紧密,容易引发不必要的化学反应,从而产生离子阻塞或电子阻塞层,导致正极侧电荷转移阻抗升高[39]。例如,通过LiCoO2/LLZO[40]和LiCoO2/Li3PS4[41]电极的透射电镜图可以分别观察到100 nm和50 nm的界面反应层。Woo等[42]报道,在LLZO和LiCoO2薄膜阴极之间形成了界面反应产物La2CoO4。Gulin等[43]用XPS,XRD,TEM和XAS对LCO/LLZO的界面产物进行了详细的研究,结果表明,退火温度为250 ℃时的界面厚度约20 nm,500 ℃时的界面厚度约100 nm,并且在界面处均检测到了Li2ZrO7,LaCoO3和Li2CO3,这是由La和Co在高温下的相互扩散,并且与CO2反应引起的。需要注意的是,通常情况下不含锂的分解产物会阻碍离子传输,导致界面电阻升高,从而引发更大的极化现象,降低电池性能[39,44-46]。因此,基于氧化物电解质的全固态电池的体系结构仍需进一步研究,实现低温下的紧密接触。
另外,空间电荷层的存在也会引起正极/电解质界面的电阻升高[47-49],尤其是氧化物正极与硫化物电解质接触时,两者形成的空间电荷层现象更加明显。这是因为硫化物比氧化物更容易被氧化,电子可以很容易地从硫化物电解质迁移到带电的正极材料,而为了平衡电荷,锂离子将离开这个区域,通过自扩散迁移到带电的正极,最终在正极与电解质的界面处形成一个锂离子的耗尽层,因此,正极/电解质界面产生了局部静电势,降低了电解质界面的化学势,最终导致正极/电解质界面的电解质侧的锂离子浓度较低,抑制了锂离子在界面上的传导[1,3,31-32]。虽然空间电荷层可以用来解释初始的高界面电阻,但这一现象的化学性质尚不清楚,目前大多研究只是通过数值模拟来进行解释,还没有对空间电荷层进行直接实验研究的报道。近年来,原位开尔文探针和电子全息摄影实验越来越得到重视,通过这些方法,研究者可以探测到整个界面上的局部静电势,或许可以用来观察空间电荷层现象。此外,正极/电解质的界面行为可能随着外部电位的施加而变得更加复杂。
3 电化学稳定性
大多数固态电解质具有较窄的电化学稳定性窗口,不能在正极和负极材料的全电压范围内工作。如果固态电解质与电子导电材料有足够的接触,则会在高电压下被氧化或在低电压下被还原,这些电子导电材料包括正极/负极材料、集流体和各种导电添加剂[32,50-51],因此,电解质的氧化或还原反应通常发生在与其接触的各种材料的界面处,从而形成复杂的固体电解质界面膜,增加电荷转移阻抗。
在正极侧,充放电过程中会发生由电化学驱动的界面形成,不同电解质与不同的正极材料发生的反应行为不同,而且电池预处理条件的不同也会影响反应的发生,因此,各种电解质与正极材料的电化学反应更加复杂。
3.1 硫化物电解质/正极界面
对于硫化物电解质,研究者进行了大量的实验和理论工作,如图3[52-55]所示,通过TEM与EDS观察到了初始充电过程中Co和S的相互扩散[52],反映到阻抗谱上为初始过程界面阻抗的增大。Hao等[52]运用拉曼成像技术,分析了硫化物/正极界面反应产物为Co3O4,在传统液态电池中,Co3O4通常在LiCoO2过充时出现,不利于电池性能的发挥(图3(a))。此外,Co3O4的分布不均匀,这表明在复合电极中局部极化过大,发生了过电荷的现象。有研究对硫化物侧的反应行为也进行了测试,同样观察到了硫的氧化,在加入导电碳等添加剂时反应更明显。通过俄歇电子能谱测定出Li6PS5Cl可以被氧化成S,LiCl,P2S和LiCl(图3(b)[53]),硫化物在界面上的累积阻碍了离子和电子的传输,一定程度上抑制了之后的氧化过程[53],而在含导电碳的系统中,由于其强电子导电性,电化学分解更加严重[54-55]。
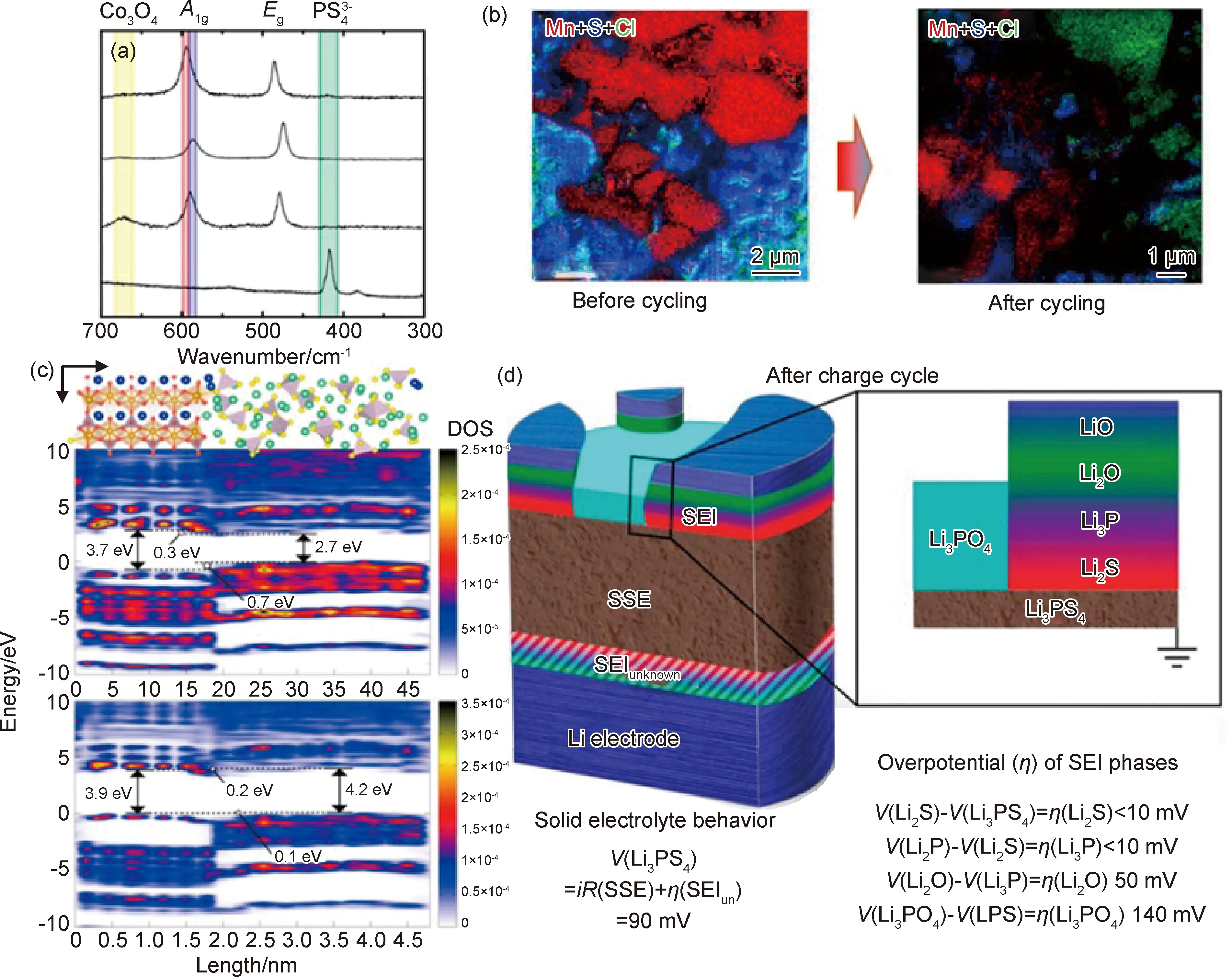
图3 充放电过程中正极/电解质界面的化学和结构演化
此外,在正极/电解质界面上的电化学反应也会受到正极材料类型的影响。研究发现,正极采用LiCoO2时,电化学分解产物通常具有良好的电子电导率,这会导致反应的持续进行。而对于LiFePO4,Kasemchainan等[54]报道,由于硫化物的价电子带最大值高于氧化物(图3(c)),硫化物电解质和LiFePO4在完全放电状态下的反应会受到限制,此时硫化物电解质将会进行电荷补偿,使得与正极材料接触处的电解质更具反应活性,最终形成锂耗尽区,而且由于S—S键的形成和PS4的聚合,锂耗尽区将会进一步扩大[56-57]。Monroe等[58]报道在硫化物固态电池的充放电过程中,S—S键的形成是可逆的,表明即使在相对较低的电压下,硫化物电解质也会发生电化学氧化分解。因此,硫化物电解质要获得超过5 V的高电化学稳定性是相当困难的,硫化物在正极侧的电化学氧化分解是不可避免的。
3.2 氧化物电解质/正极界面
与硫化物相比,氧化物电解质具有更宽的电化学稳定性窗口和更高的氧化稳定性。然而,氧化物电解质的室温离子电导率一般低于硫化物,其较大的晶界电阻也限制了其离子电导率的发挥[21,59]。另外,较高的烧结温度可能导致正极活性物质的降解,从而使得正极/电解质界面的反应更加复杂[60-63]。
与硫化物相似,较早的报道主要通过平面电极的循环伏安测试,发现氧化物的电化学稳定性窗口(0~5 V)明显大于DFT预测值(0.05~2.9 V,LLZO)[64]。为了更精确地判断氧化物电解质的稳定窗口,研究者们通过在正极使用导电碳和氧化物电解质的混合物以模拟电池环境下的电解质电化学行为[65]。例如Han等[66]用在Ar气氛中制备的Li|LLZO|LLZO+C|Pt固态电池进行循环伏安测试,发现LLZO电解质在4 V即开始发生氧化。同样,在Li|Ta-LLZO(LLZTO)|LLZTO+C电池的循环伏安测试中同样检测到低至3.7 V的氧化现象(图4(a))[61]。
在电池循环过程中,因为许多带电正极的电压超过了氧化物电解质的氧化稳定性极限,经过烧结的正极/电解质在界面处可能发生氧化分解[63],在图4(b)[64]中,研究者计算了不同正极与LLZO或LLTaO之间化学反应的驱动力,并将其绘制为电压的函数。在2.5~4.5 V充放电范围内,LLZO与三种常见正极(LiCoO2,LiMnO2和LiFePO4)的反应中,LLZO/LiCoO2界面的反应驱动力最低(<50 meV/atom),而LLZO/LiFePO4界面反应驱动力最高[64]。然而,在电池实际充放电循环过程中,目前的研究仍然不能完全确定氧化物电解质在正极侧的反应产物。例如,LiCoO2|LLZO|Au|Li固态电池在电压为2.7~3.8 V范围内循环时,电池每周都有约5 mAh·g-1的不可逆容量,与LLZO发生氧化的计算结果一致。然而,LiCoO2|Nb-LLZO(LLZNO)|Li固态电池在2.5~4.2 V电压范围内循环,首周库仑效率为99%,100周次后的容量保持率仍为98%,说明LLZNO/LiCoO2界面在更大的电压范围内的电化学反应反而较小,或者充放电过程中界面发生钝化,氧化反应不能持续进行[67]。因此,需要对电池实际运行条件下的电解质/正极界面进行更直接的实验观察与分析,以确定该界面在长期循环下是否是电化学稳定的。
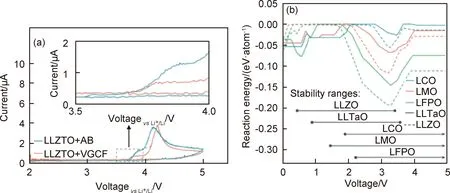
图4 氧化物固体电解质的电化学稳定性
3.3 聚合物电解质/正极界面
以聚合物为主体,与不同锂盐混合制成的聚合物电解质因其柔韧性好、与电极界面接触好、成本低、易于量产等优点而备受关注。自1973年开发出基于固体聚环氧乙烷(PEO)的电解质[68]以来,各种聚合物主体都得到了不同程度的开发与利用,包括聚碳酸酯、聚酯、聚腈(例如聚丙烯腈(PAN))、多胺(例如聚乙烯亚胺)和聚偏氟乙烯(PVDF)等。PEO具有非常低的玻璃化转变温度(约-64 ℃),与其他聚合物相比,是一种良好的锂离子络合剂[69-70]。另外,聚偏氟乙烯(PVDF)及其共聚物也已广泛应用于凝胶电解质中[71],作为聚合物主体,其具有较低的玻璃化转变温度和高介电常数,有利于促进离子解离。
在聚合物电解质中,PEO基电解质因其与电极界面优异的相容性[69-70,72-73],是目前研究最广泛的电解质,然而,室温下的PEO电解质的离子电导率在10-7~10-5S·cm-1范围内,低于固态电池在实际应用时的要求。另一个问题是聚合物电解质在高压下的电化学不稳定性,例如PEO基电解质的电化学稳定性窗口小于3.8 V(vsLi/Li+)[74],这都限制了它们与高压正极材料的匹配和应用[75-76]。
综合来看,聚合物和无机固体电解质不能同时满足高离子电导率、高电极稳定性、成熟的制造工艺和低成本的所有要求。因此,将聚合物和无机物的优势互补并结合起来的无机-聚合物复合固体电解质(inorganic-polymer composites,IPCs)已成为满足要求的更好选择,并得到了较快的发展[36,77-81]。由于聚合物与无机电解质之间的协同作用,这种复合电解质可同时具备较高离子导电性和界面稳定性。值得注意的是,在复合电解质中,聚合物组分可以起到缓冲层的作用,防止无机电解质与固态电池中各组分间发生剧烈反应,例如对于含有被聚合物包裹的硫化物颗粒的硫化物基复合电解质,硫化物颗粒和正极颗粒之间的界面反应可以被有效抑制[82-86]。
复合电解质的电化学稳定性如图5所示,较宽的电化学窗口决定了它们与高压正极和锂金属负极良好的相容性,这对实现高能量密度的固态电池非常重要。例如,常见的PEO基聚合物电解质在>3.8 V的电压下即发生氧化[87],限制了其在高能量密度电池中的应用,而无机电解质具有较宽的电化学稳定性窗口,其电压上限超出了单一的聚合物电解质的上限[88]。无机填料的引入使得复合电解质的电化学稳定性窗口比聚合物电解质更宽[85-90]。因此,通过合理设计聚合物基体、锂盐和无机电解质填料可以进一步拓宽电化学稳定性窗口。又例如腈基聚合物PAN,由于其具有含氮官能团而表现出良好的抗氧化性能,使用PAN作为聚合物基体可以进一步提高复合电解质的氧化电位[91]。另外,电解质与电极之间的界面反应决定了体系的实际电化学稳定性,除了合理设计复合电解质的各种组分比例外,还可以通过设计电解质-电极界面来扩展实际的电化学稳定性窗口。
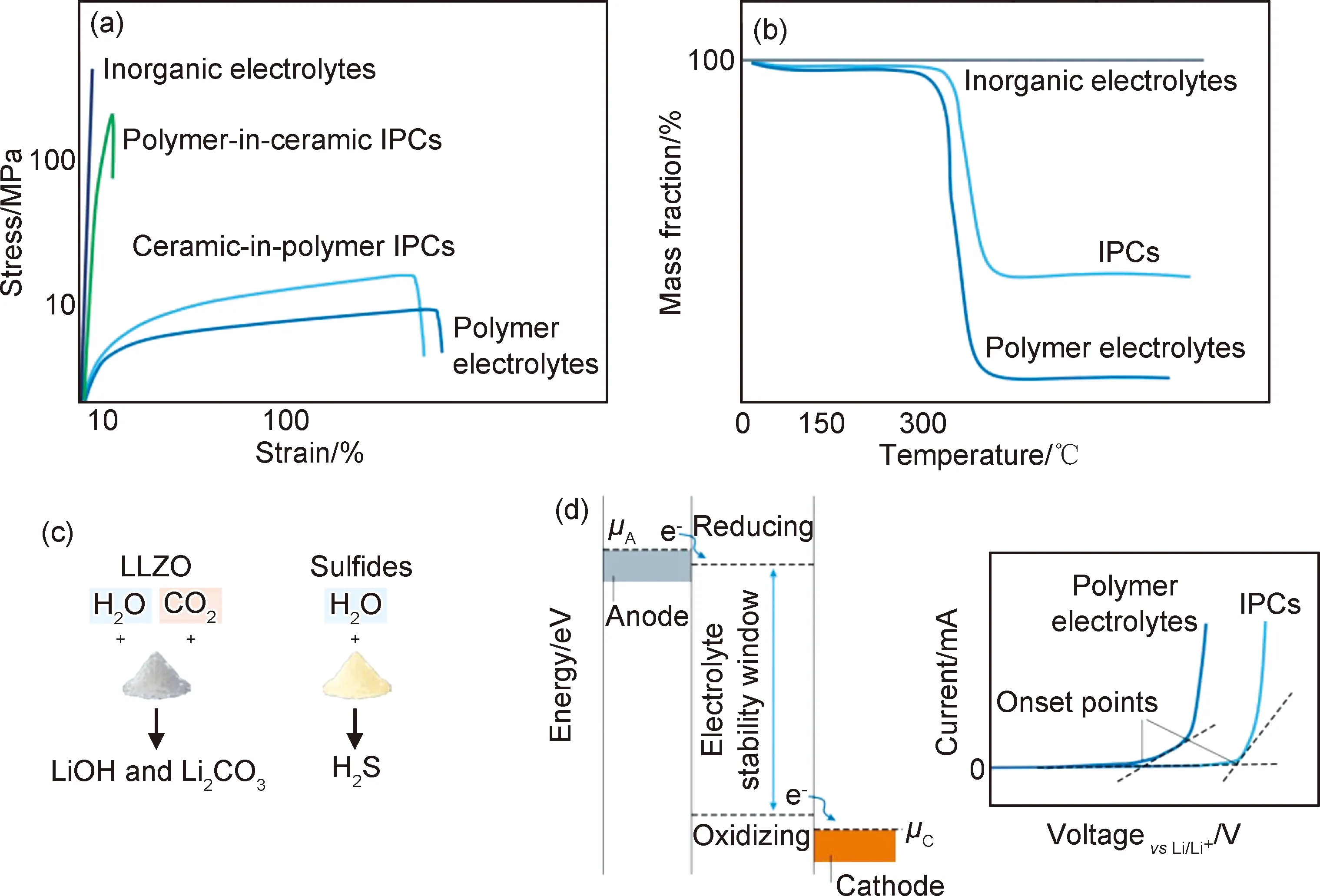
图5 无机-聚合物复合电解质的稳定性
3.4 卤化物电解质/正极界面
氧化物固态电解质合成过程以及随后的电池制作步骤中都需要较高的烧结温度,以促进电极材料与固态电解质之间的紧密接触,导致增加电池制造成本,并且还容易引起界面反应。对于硫化物固态电解质,它们与氧化物正极材料之间的直接接触容易导致形成空间电荷层,而且硫化物的电化学稳定性窗口很窄,在与氧化物正极材料进行匹配时,人工添加界面保护层是非常必要的[47,92-95],但这会使制造过程更加复杂并增加成本。为了解决这些问题,近年来,卤化物固态电解质(Li-M-X三元化合物,M=阳离子,X=F,Cl,Br,I,O和S)成为非常有吸引力的替代品[96]。
基于稀土元素的卤化物固态电解质均显示出较宽的电化学窗口,氧化极限电压均大于4 V,还原电压极限约为0.6~0.9 V,明显宽于许多硫化物和氧化物(如LGPS(1.72~2.29 V),Li3PS4(1.71~2.31 V),LISICON(1.44~3.39 V))[96]。根据现有的实验和理论结果,在大多数情况下,卤化物电解质对氧化物正极材料表现出良好的化学稳定性。目前虽然还未有关于卤化物电解质和正极材料之间电化学稳定性的确切报道,但良好的循环性能可以直接从应用的角度说明卤化物电解质在各种固态电池系统中均有良好的兼容性。例如,在关于Li3YCl6和Li3YBr6电解质的报道中,Asano等[97]以LiCoO2为正极活性材料,在这两种卤化物电解质的基础上分别组装了固态电池,两种电池的初始库仑效率分别为94.8%和94.2%,首周充电后的正极/电解质界面阻抗分别为6.6 Ω·cm-2和16.8 Ω·cm-2,而作为对比,以硫化物Li3PS4作为电解质的固态电池的初始库仑效率仅为84%(图6(a)),而正极/电解质界面阻抗高达128.4 Ω·cm-2,从电化学结果中可以推断出Li3YCl6/Li3YBr6对LiCoO2具有良好的电化学稳定性。Li等[98]使用Li3InCl6电解质分别与LiCoO2和NMC811正极材料进行匹配,在不同充电状态下测试In的L3边和Cl的K边的X射线近边吸收光谱,结果表明,在不同的荷电状态下,LiCoO2-Li3InCl6阴极复合材料的特征峰均保持不变,说明Li3InCl6和LiCoO2即使在充电至高电压下也不会发生反应。
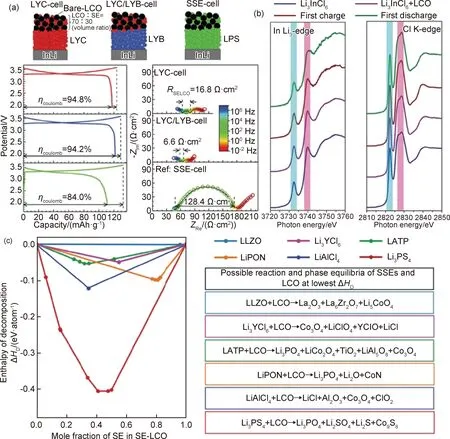
图6 卤化物电解质物理性质的理论计算与实际实验结果
目前对于卤化物电解质的研究多集中在提高其离子电导率[99-100],但是其化学/电化学稳定性同样值得更多关注,迫切需要进一步的实验和分析,以深入了解卤化物电解质的实际电化学稳定性窗口,以及其与具体正极活性物质的具体反应特征。
由于固态电池中固态电解质与电极之间的接触是直接的物理接触,因此界面浸润性较差,而不理想的界面浸润性严重影响了固态锂离子电池的容量,这种不利影响在高倍率情况下尤为突出。同时,电极-电解质界面处发生的化学或电化学的副反应对固态锂离子电池的性能有进一步的影响,而且随着电压或温度的升高,这些副反应会进一步降低固态电池的实际容量。
4 正极/电解质界面问题的解决方案
尽管新开发的卤化物电解质相比于其他电解质来说是一种高电位稳定的电解质,但应注意的是,固态电解质的氧化源于其阴离子的不稳定性,这使得难以只通过调节电解质的组成来达到抑制反应的发生,因此,需要对正极侧的界面进行修饰。
表3[13-14,17,101-115]总结了在不同正极和电解质之间引入的界面改性层,除Nb外,大多数界面修饰层都是离子导电而电子绝缘材料,这种明显的差异源于不同正极/电解质界面的不同设计原则。显然,为聚合物和硫化物基电解质设计的所有界面层都是良好的电子绝缘体。聚合物和硫化物在正极材料和电解质之间会发生化学或电化学反应,因此,良好的两相间的性质应满足以下要求:(1)对正极的高电化学稳定性,以防止形成新的钝化层,即界面层在高压下是稳定的;(2)离子导电和电子绝缘性质,如LiNbO3。引入的界面层在不阻碍锂传输的情况下保护电解质免受氧化,以此提高固体聚合物和硫化物基固态电池的性能。例如,基于LiNbO3或Li3PO4包覆层策略,工作电压为5 V的LiNi0.5Mn1.5O4材料被成功应用于硫化物基固态电池。
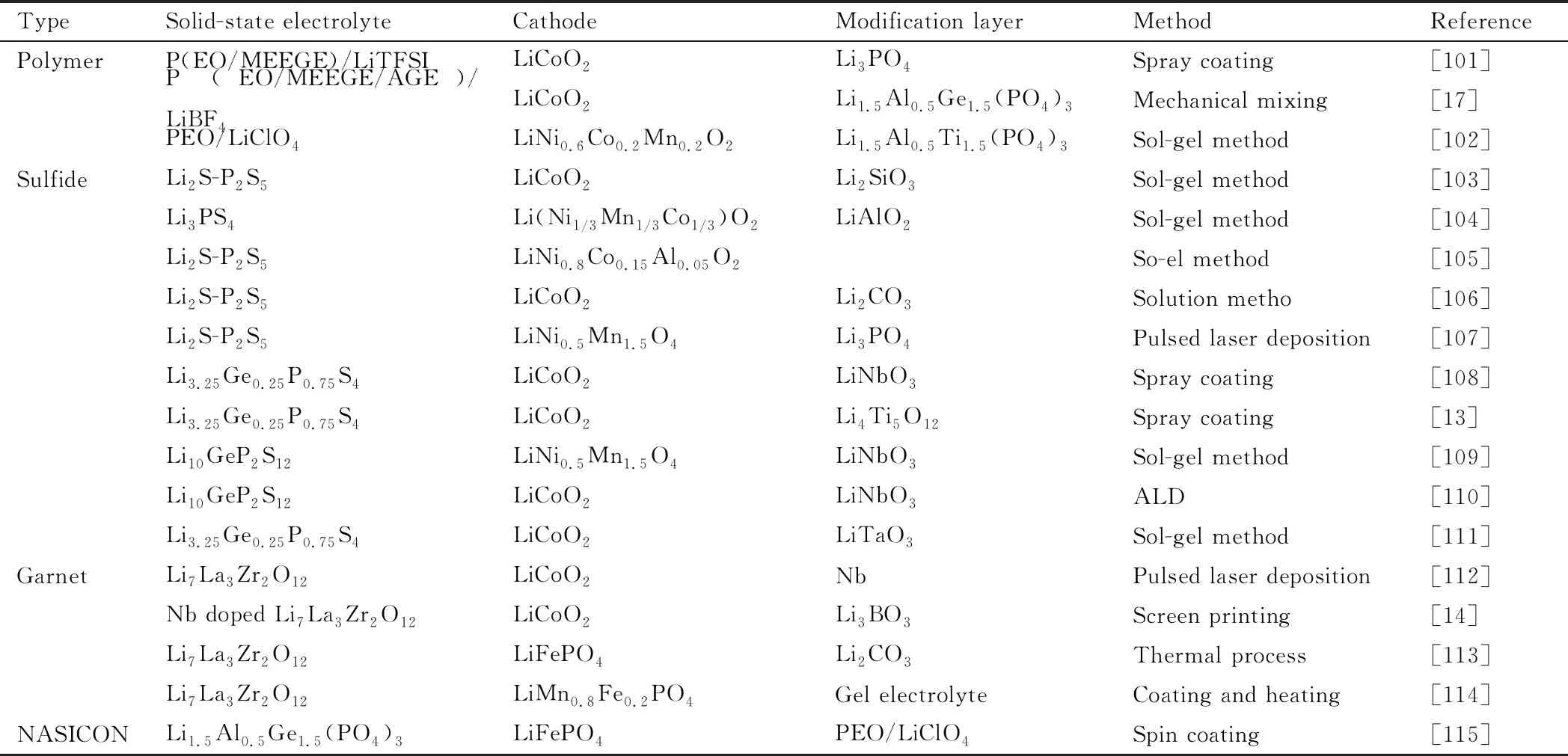
表3 电解质/正极界面修饰改性方法
然而,基于氧化物电解质的固态电池的情况可能不同,其高电阻主要来自接触不良,这对于聚合物和硫化物来说并不明显,因为后两种电解质足够软,简单施加压力即可以获得正极材料和电解质的紧密接触。然而,在基于氧化物的固态电池中,固体-固体接触的巨大动力学势垒可能在很大程度上抑制化学或电化学过程,因此,界面修饰的原则应首先解决接触问题。研究者将Nb,Li3BO3,凝胶电解质,甚至液体电解质引入固态电池应用中,并且都有效地改善氧化物电池的电化学性能。Han等[17]通过引入Li2.3C0.7B0.3O3实现了LLZO/LiCoO2界面的紧密接触,电池的性能显著提高。此外,目前研究者对正极/电解质的改性主要集中在聚合物、硫化物和石榴石基固态电池系统,而对钙钛矿型和NASICON型电解质的研究相对较少,这可能是由于该系统的最主要问题是负极Li侧的严重降解,使得负极侧界面的挑战更加突出。
在生产工艺方面,溶胶-凝胶、喷涂等技术可以很好地实现均匀的界面修饰层,可以有效地减轻界面处的副反应。然而,过于复杂的操作和高昂的生产成本可能是其大规模生产的实际障碍。同时,简单的机械搅拌虽然不能提供理想的保护层,但同样可以在一定程度上改善界面的稳定性,而且该方法制备简单、成本低廉,是界面改性的一种替代方法,具有很好的应用前景。
具体来说,针对固体与固体间刚性的且不完全的物理接触,中科院化学所的郭玉国团队在正极NCM622颗粒表面引入了一种柔性的聚丙烯腈-丁二烯(PAB)包覆层[116],由于柔性材料质地较软,可以改善固体颗粒间的刚性接触,从而增大接触面积,实现界面改性的目的。图7(a)的TEM图揭示了PAB层已经均匀地沉积在NCM颗粒的表面上,且厚度小于10 nm,通过性能测试,PAB界面改性的固态电池具备优异的电化学性能,包覆聚合物PAB后,NCM正极材料可以提供173 mAh·g-1的稳定容量,NCM和NCM@PAB在固体电解质中的倍率性能如图7(d),(e)所示,在0.2 C~3 C的电流密度下,NCM@PAB的放电容量从173 mAh·g-1降低到99 mAh·g-1,即使在5 C的高电流密度下,包覆的正极材料仍显示出57 mAh·g-1的比容量。相比之下,纯NCM在0.2 C时可以提供相同的放电容量,而在3 C时只能保持64 mAh·g-1的比容量,而在5 C时几乎没有容量。实验结果说明,在三元NCM正极材料表面引入柔性的聚合物包覆层,不仅有效抑制了电池在循环过程中的副反应,而且这种柔性的包覆层增加了电极颗粒-硫化物电解质之间的接触面积,使得更多的锂离子参与到充放电反应中,从而提高了电池的性能。
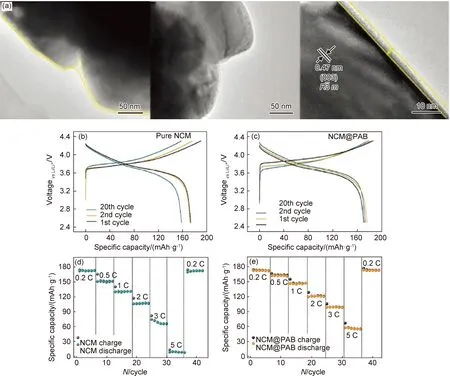
图7 NCM和NCM@PAB形貌及电化学性能对比[116]
除了引入柔性的界面包覆层来达到提高接触性的目的,也有研究者采用在正极材料表面原位生长固态电解质的方法来增加两者的接触面积[47,92,117-119]。Wang等[120]报道了一种直接在水溶液中使用卤化物电解质Li3InCl6原位包覆电极材料LiCoO2(LCO)的包覆方法(图8),通过X射线光电子能谱分析(XPS)和离散傅里叶变换(DFT)计算,发现LCO表面的O与Li3InCl6的Cl配位,这种界面相互作用有助于LIC在LCO表面的生长,从而形成良好的固-固接触,从而使得LIC在LCO上均匀分布。在电化学性能测试中,LIC@LCO电极的初始放电容量为130.1 mAh·g-1,在0.1 C时初始库仑效率为92%,150周次循环后,容量仍保持在95.9 mAh·g-1,由于LIC和LCO之间的界面电阻极小,因此可以实现高倍率性能(4 C下为28.5 mAh·g-1)。该项工作中,研究者没有引入额外的表面过渡层,而是使固态电解质在正极材料表面原位生长,从而实现出色的界面接触,在室温下实现了高能量密度和高功率密度的固态锂离子电池的应用。这种简便的方法为克服固态电池长期存在的界面挑战提供了新的思路。

图8 合成方法(a)和SEM表界面形貌(b)[120]
针对界面化学或电化学副反应的问题,目前的解决方案多集中在引入惰性的界面缓冲层,隔绝正极活性物质与电解质的直接接触,减少甚至避免副反应的发生。例如,加拿大西安大略大学孙学良、天津理工大学罗俊课题组合作采用X射线近边吸收光谱法(XANES)结合透射电子显微镜(TEM)和电子能量损失光谱(EELS)等表征方法,研究了高镍层状正极材料LiNi0.8Mn0.1Co0.1O2(NMC811)与硫化物固态电解质Li10GeP2S12(LGPS)之间的界面行为[121],又通过原子层沉积(ALD)法将LiNbOx用作三元材料NMC811的包覆层,旨在稳定界面并改善固态锂离子电池的电化学性能。将没有包覆层的NMC811正极材料和有包覆层的NMC811正极材料进行比较,在充电过程中,LGPS处于亚稳定的中间状态会与裸露的NMC811反应形成副产物Li2S。此外,该项工作还发现了固态电池中高镍层状正极材料的表面重构和微观裂纹现象。这项工作中运用细致的XANES表征分析,与TEM手段结合,清晰地阐述了界面副反应的详细情况,更重要的是,它提供了在固态锂离子电池研究中表征方法的实际价值。
将缓冲过渡层引入固态电解质和正极材料之间的界面中也可以起到减轻空间电荷层效应和抑制元素相互扩散的作用。例如,Ohta等[47]使用喷涂法在LCO表面包覆厚度1.1~38.9 nm的Li4Ti5O12(LTO)薄膜。与未包覆的样品相比,LTO包覆的样品在LCO/Li3.25Ge0.25P0.75S4固态锂离子电池体系中显示出较小的界面电阻。作者认为,LTO包覆层抑制了电子从Li3.25Ge0.25P0.75S4到LCO的转移及电解质中Li+自扩散到LCO,从而降低了空间电荷层效应,进而减小了界面阻抗。对于氧化物正极材料与氧化物固态电解质之间的界面,各种缓冲层主要用于阻止它们的直接接触,这样可以增强氧化物固态电解质对正极材料的稳定性。如当使用LLZO作为固态电解质时,使用Nb作为掺杂剂,可以抑制杂质的产生并稳定LLZO/LCO间界面,另外,Nb薄层也可以抑制相互扩散,并且形成的非晶Li-Nb-O层具有Li+导电性[92]。
在薄膜电解质体系中,为了降低LCO/LiPON电解质界面处的电阻,可以在LCO上沉积一层薄的Al2O3层形成固溶体LiCo1-yAlyO2,以此来增强电池的电化学性能[45]。当用高电位正极材料如LiCr0.05Ni0.45Mn1.5O4-δ(LNM)代替LCO时,同样观察到很大的界面电阻。这是因为LNM和固态电解质之间存在严重的空间电荷层效应[46],即LNM和LiPON之间存在巨大电势差,这在LiPON电解质侧造成了严重的锂缺乏层。为了解决这个问题,Yada等[103]将BaTiO3纳米颗粒沉积到LNM颗粒上,其中BaTiO3纳米颗粒中的电偶极子可以减小LNM和LiPON之间的大电势差,重新排列锂离子分布并产生锂离子通道,从而减轻空间电荷层效应,提高固态电池的电化学性能。
5 结束语
综上所述,由于固态电解质与正极材料之间存在复杂多样的界面问题,目前固态电池的性能与液态电池相比还有一定的差距。在固态电池的诸多界面之中,固态电解质/正极界面主要存在以下三方面问题:(1)电极材料循环过程中的体积效应所带来的界面接触变差和应力积累造成的电解质破碎问题;(2)正极活性物质和固态电解质物理化学性质差别较大,在充放电前即发生各种界面反应,消耗了一部分锂离子,即正极活性物质与电解质发生化学反应;(3)正极材料的工作电位高于固态电解质稳定窗口,导致正极/电解质界面发生电化学反应,使得电池库仑效率低、循环性能变差。另外,“固-固”接触不良带来的锂离子脱嵌不完全、高温制造过程中正极与电解质中元素的相互扩散等问题也会导致电极活性物质的性能不能完全发挥,电池性能下降。
通过上述的分析与总结,本文认为界面问题的解决方案可以从以下的界面改性方面入手:(1)引入惰性包覆层抑制界面副反应的发生,或者在正极材料颗粒上原位生长固态电解质来实现两者的充分接触;(2)对于电化学窗口不匹配的问题,一方面,可以通过离子掺杂等手段对固态电解质进行改性,提高其耐高压的能力,另一方面,可以在正极材料与电解质之间引入一层较薄的不导电子的过渡层,从而起到电压过渡的作用;(3)卤化物电解质因为具有较宽的电化学窗口以及与氧化物正极材料的良好相容性,与过渡金属氧化物正极匹配时不需要额外的界面修饰,很大程度上降低了固态电池的制造成本,值得进一步的关注与研究。
另外,由于目前测试手段的限制,人们对固态电池中各种界面的具体反应特征的了解不够细致和深入,未来可以设计各种先进的表征手段,例如原位的X射线吸收精细结构、原位透射电镜等,来对界面处具体的反应进行直接且详细的分析。
最后,通过表面修饰改性等手段,有针对性地对正极/电解质界面进行界面结构调控,对于实现高能量密度、高安全性的全固态电池的目标具有重要的研究价值和现实意义。
