废塑料裂解油加氢脱有机氯化物复杂反应体系的热力学分析
2022-11-16郝清泉刘宗鹏武本成朱建华
郝清泉,刘宗鹏,武本成,朱建华
(中国石油大学(北京)化学工程与环境学院,北京 102249)
我国近期实施的垃圾分类,极大地提高了资源化利用程度,但在实施垃圾分类后,由于末端处置能力不足而导致一些垃圾“无路可走”,是现有垃圾分类体系存在的一大“痛点”[1-4]。在城镇垃圾中,废塑料的占比排名第二,所占比例约为13%[5-6],长期占据处理场地且处理困难。垃圾分类后得到的废塑料质量普遍较差,通常无法通过再生造粒回收利用,而填埋、焚烧等常规处理方式也难以实现无害化处理并将对环境造成二次污染,因此将垃圾分类得到的废塑料进行热裂解或催化裂解已成为劣质废塑料减量化和资源化利用的最佳选择[7-9]。
目前文献中针对废塑料油化技术的报道较多,但由于废塑料中掺杂的聚氯乙烯或使用的一些含有氯化物的添加剂而导致裂解油中氯含量严重超标的问题却少有提及[10-12]。尤其是垃圾废塑料中不可避免地会混入少量的聚氯乙烯,致使其裂解得到的油品变成总氯质量浓度高达数千甚至上万mg/L的“毒油”而无法正常使用。若采用吸附法对废塑料裂解油进行脱氯处理,由于吸附剂的氯容较低而易达到饱和,造成脱氯成本居高不下。因此,采用加氢方法对废塑料裂解油中的氯化物进行脱除处理是一种优选的方法。该方法效率较高且经济节能,在加氢脱氯过程中,同时会发生不饱和烃加氢饱和以及脱硫、脱氮、脱金属等反应,可有效提升裂解油品的质量及收率[13-18]。本课题通过对废塑料裂解油加氢脱氯反应体系进行热力学分析,考察各种有机氯化物在指定反应条件下加氢反应自发进行的可能性;并通过计算加氢反应的平衡组成,确定难以加氢脱除的有机氯化物种类;进而考察氢油比、反应温度和压力等因素对该加氢反应体系平衡组成的影响,并探究氢气与各种有机氯化物的先后反应顺序,从热力学角度给出加氢脱氯反应的适宜条件,以期为废塑料裂解油加氢脱氯技术的开发提供指导。
1 废塑料裂解油中有机氯化物的形态及含量分析
1.1 试剂及原料
氯乙烯、偏二氯乙烯、三氯乙烯、氯苯、1,2-二氯苯、1,4-二氯苯、1,2,4-三氯苯、2-氯乙苯、1,1,2,2-四氯乙烷,均为分析纯,上海阿拉丁生化科技股份有限公司产品;2,2-二氯丙烷、四氯化碳、四氯乙烯、2-氯甲苯,均为分析纯,北京伊诺凯科技有限公司产品;环己烷,分析纯,北京鑫葆海化学科技有限公司产品。废塑料裂解油,沧州市某环保科技有限公司生产,其性质如表1所示。

表1 废塑料裂解油的性质
1.2 试验仪器
废塑料裂解油中有机氯化物的定性及定量分析在配备有电子捕获器的气相色谱仪(GC-ECD)上进行,仪器型号为北分SP-3000,生产厂家为北京北分瑞利分析仪器有限公司,采用30 m×0.32 mm×0.25 μm的HP-5色谱柱。
1.3 试验方法
气相色谱的操作条件[19]:初始温度40 ℃,保持5 min;随后以10 ℃/min的升温速率将温度升至250 ℃,保持2 min;采用相同升温速率将温度升至260 ℃,保持1 min;最后将温度升至300 ℃,保持2 min。分流比为80∶1,柱前压力为0.107 MPa,柱流速为3 mL/min,尾吹气流量为30 mL/min,进样器和检测器温度均为300 ℃,进样针规格为0.2 μL。
有机氯化物定性及定量分析方法:以环己烷为溶剂,分别取上述有机氯化物试剂配得相应标准溶液,然后用进样针注入气相色谱仪中,从而得到不同有机氯化物标准物质在色谱图中的保留时间;取废塑料裂解油切割后的68~200 ℃,200~230 ℃,230~300 ℃馏分,并用环己烷稀释后注入气相色谱仪中,通过与上述有机氯化物标准物质的保留时间进行对比,即可完成馏分油中的有机氯化物定性分析。定量分析采用外标法,分别配制不同浓度的有机氯化物标准溶液,建立该有机氯化物标准曲线,将样品的峰面积对照标准曲线即可得到相应的有机氯化物浓度。
1.4 试验结果
通过上述方法,得到废塑料裂解油各馏分的气相色谱,如图1所示,各馏分中有机氯化物的种类、含量及保留时间如表2所示。

图1 废塑料裂解油不同馏分的气相色谱
由表2可知,从该废塑料裂解油68~300 ℃馏分中鉴定出的有机氯化物总质量浓度高达2 846.7 mg/L,且大多分布在68~200 ℃馏分,以低沸点氯代烃为主,其中氯代烯烃约占54.1%,氯代芳烃约占35.0%,氯代烷烃约占10.9%。
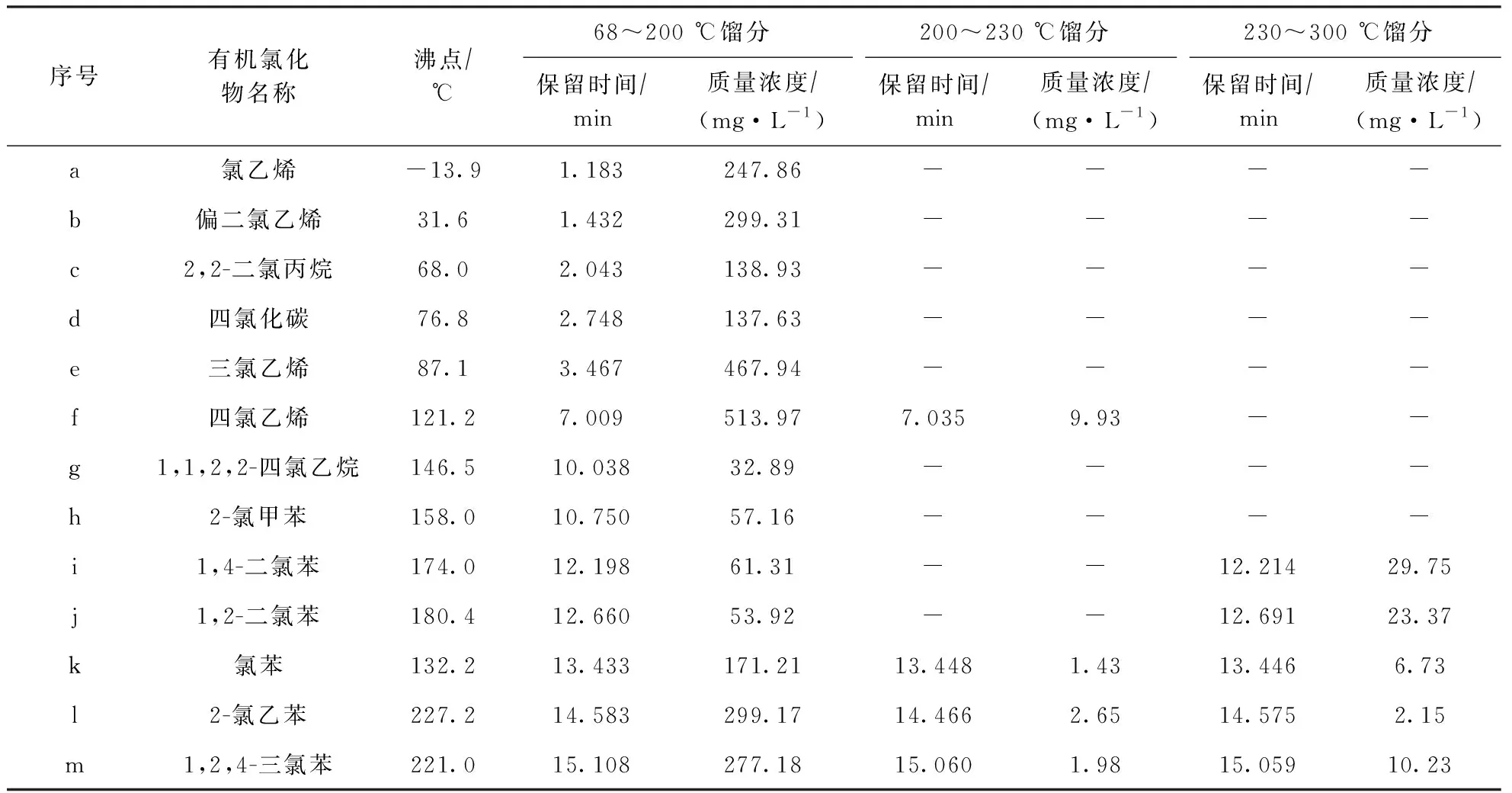
表2 各馏分中有机氯化物的种类、含量及保留时间
2 废塑料裂解油加氢脱氯反应体系的热力学分析
在对废塑料裂解油加氢脱氯反应体系进行热力学分析的过程中,需要对该反应体系中的平衡组成进行计算。较为常用的方法为平衡常数法[20-21],即通过原子系数矩阵确定出一组独立反应,并计算出各独立反应在指定反应条件下的吉布斯自由能变及平衡常数,之后采用单纯形法[22-23]等优化方法求解由各独立反应平衡常数表达式组成的高度非线性方程组,得到该复杂反应体系的平衡组成。该方法原理简单,适用于独立反应数不太多的复杂反应体系,原因是独立反应数量过多时会导致结果不易收敛。废塑料裂解油的加氢脱氯反应体系是一个涉及多组分的复杂反应体系,经组成分析可知,该反应体系的主要组分除上述鉴定出的有机氯化物外,还有甲烷、乙烷、丙烷、环己烷、氯化氢和氢气等共18种组分,对原子系数矩阵进行计算后共得到15个独立反应,如式(1)~式(15)所示,其中ΔrHθm表示标准摩尔反应焓变。在求解过程中发现由这15个独立反应组成的高度非线性方程组不仅初值难于赋值,并且难于收敛,因此需选择更为简便的计算方法。

(1)

(2)

(3)

(4)

(5)

(6)

(7)

(8)

(9)

(10)

(11)

(12)

(13)

由表1可以发现,工程建设中,全过程造价管控具有深远意义,实施有效工程造价管控,在计划额内控制项目投资,提高资源分配率,特别是是利用造价管理有效协调施工各参与方,提高建筑项目管理的效益,以此为建筑企业创造更大的社会与经济效益。
(14)

(15)
与平衡常数法相对应的是吉布斯自由能最小法[24-26],该方法基于吉布斯自由能最小化原理,即当一个体系处于平衡状态时,该体系的吉布斯自由能最小,这一准则同时适用于化学平衡和热力学相平衡体系。该方法的核心是将平衡计算问题转化为最优化问题,然后以组分的平衡摩尔分数或平衡反应进度为变量计算平衡时体系的吉布斯自由能,并通过求解数学最优化问题获得平衡组成,无需确定复杂反应体系中发生的具体化学反应[27-28]。
因此,为简化计算过程,本课题采用Aspen Plus软件中的Gibbs反应器对废塑料裂解油中有机氯化物的加氢脱氯复杂反应过程进行模拟分析,Gibbs反应器是基于吉布斯自由能最小化原理的平衡反应器。同时,使用Aspen Plus软件中自带的灵敏度分析工具,考察氢油比、反应温度和压力等因素对复杂反应体系平衡组成的影响。采用Gibbs反应器对废塑料裂解油中有机氯化物加氢反应的分析流程如图2所示。

图2 利用Gibbs反应器分析加氢脱氯反应的流程
由于本研究使用的废塑料裂解油较为劣质,除氯含量超标外,硫、氮、氧化物等杂质的含量也较高。因此为消除其他杂质的影响,在模拟时仅考虑从样品油中鉴定出的有机氯化物与氢气进行的加氢反应,且假设均在较为理想的反应条件下进行。假定废塑料裂解油的进料流量为1 L/min,根据气相色谱对各种有机氯化物含量的定量分析结果,定义进料中各有机氯化物的初始流量,结果如表3所示。
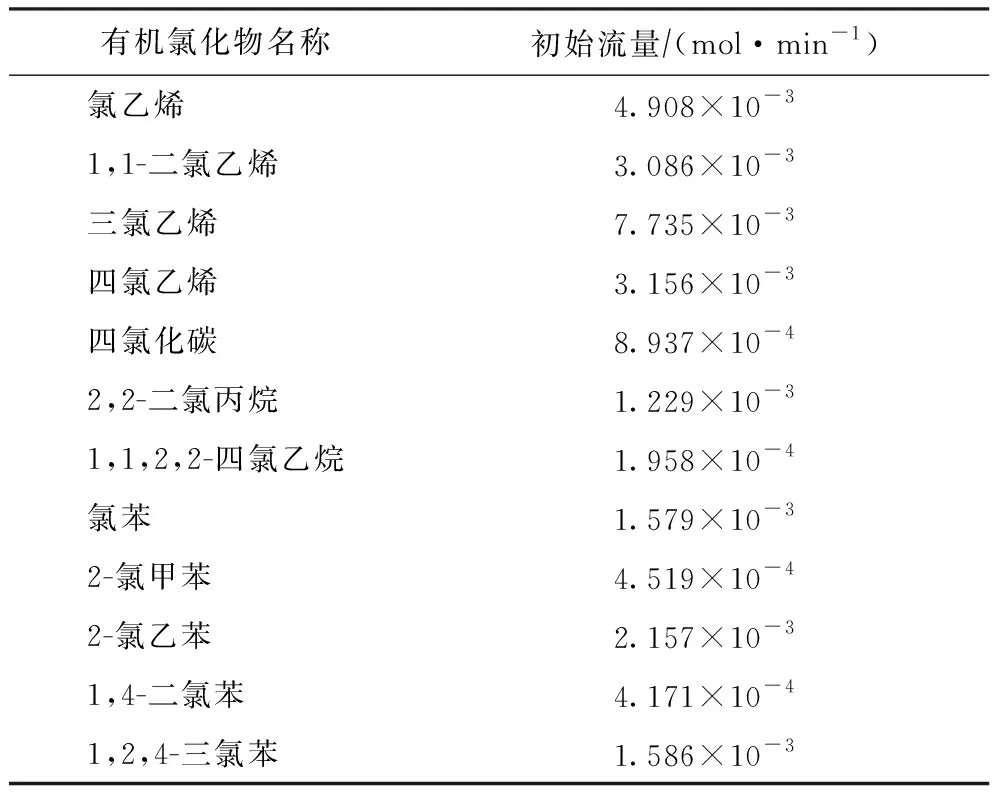
表3 参与加氢反应的各种有机氯化物的初始流量
3 加氢脱氯热力学影响因素分析
3.1 反应温度及压力的影响
采用Aspen Plus软件中的灵敏度分析模块,在保证进料氢气过量的情况下,考察反应温度、压力对各种有机氯化物加氢反应平衡组成的影响。由于本次拟考察各种有机氯化物在指定加氢反应条件下的反应规律,因此将反应温度变化范围设置为300~380 ℃,增幅为10 ℃;反应压力变化范围设置为0.1~5 MPa,增幅为0.5 MPa。使用Matlab软件对经Aspen Plus灵敏度分析得到的数据进行三维绘图,以便直观地展示各种有机氯化物的平衡组成随反应温度及压力的变化趋势。作图后发现部分有机氯化物的三维图形状及变化趋势相似,并存在一定的规律性。对其进行分类整理,发现三维图走势相似的有机氯化物可分为氯代烯烃、氯代烷烃和氯代芳烃3类,反应温度及压力对各类有机氯化物平衡组成的影响分别如图3~图5所示。
由图3可知:各种氯代烯烃的平衡摩尔分率随反应温度、压力变化的趋势较为相似,在360~380 ℃及0.1~2 MPa的反应条件下,氯代烯烃的平衡摩尔分率较高,呈峰状突起,表明在该反应条件下各种氯代烯烃的加氢反应进行得不完全,说明在相对高温下,低压反应条件并不利于氯代烯烃的加氢反应;在360~380 ℃及4~5 MPa的范围内,氯代烯烃的平衡摩尔分率下降并形成一个明显的低谷,且出现数值为负的现象,这是因为此时氯代烯烃的平衡摩尔分率在数值上已趋近于零,由于衰减速率较快,尚未达到图形的边界,Matlab软件根据自身算法进行了优化,故出现了负值,表明在该反应条件下各种氯代烯烃的加氢反应较为完全,脱氯效果较好。因此,在相对高温下,高压反应条件有利于氯代烯烃加氢反应。

图3 反应温度及压力对不同氯代烯烃平衡组成的影响
然而,值得注意的是,在300~320 ℃、3~5 MPa的范围内,氯代烯烃的平衡摩尔分率也出现了一个明显的低谷,虽然在该反应条件范围内氯代烯烃平衡摩尔分率的衰减速率低于在360~380 ℃及4~5 MPa范围内的衰减速率,但此处氯代烯烃的平衡摩尔分率也趋近于0。这说明,在相对高压下较低反应温度也可获得较好的加氢效果。考虑到升高温度会增大过程能耗,确定氯代烯烃加氢的适宜反应条件为温度300~320 ℃、压力3~5 MPa。
由图4可知,各种氯代芳烃的平衡摩尔分率随反应温度、压力的变化趋势与氯代烯烃近似,但通过对比图3与图4中的颜色深浅可知,氯代芳烃的加氢反应程度低于氯代烯烃,表明与氯代烯烃相比,氯代芳烃的加氢反应较难进行。综合考虑氯代芳烃的加氢脱除效果,确定适宜的反应条件仍为300~320 ℃、3~5 MPa。

图4 反应温度及压力对不同氯代芳烃平衡组成的影响
由图5可知,各种氯代烷烃的平衡摩尔分率随着反应温度及压力的变化趋势较为一致,但与氯代烯烃和氯代芳烃差异较大。其中,反应温度为影响氯代烷烃加氢反应的主要因素,当温度在300~350 ℃范围内时,氯代烷烃的平衡摩尔分率较低,加氢反应较为完全,且在310 ℃附近出现一个低谷,此时平衡摩尔分率达到最小值;当温度超过350 ℃后,氯代烷烃的平衡摩尔分率随反应温度升高而增大,且在380 ℃时达到最大值。氯代烷烃的平衡摩尔分率基本不随反应压力变化而改变,表明反应压力对氯代烷烃的加氢反应影响不显著,这是因为各种氯代烷烃的加氢反应均为等分子反应,理论上讲压力对其反应平衡并无影响。综上所述,氯代烷烃加氢反应的适宜条件为低压、300~320 ℃。
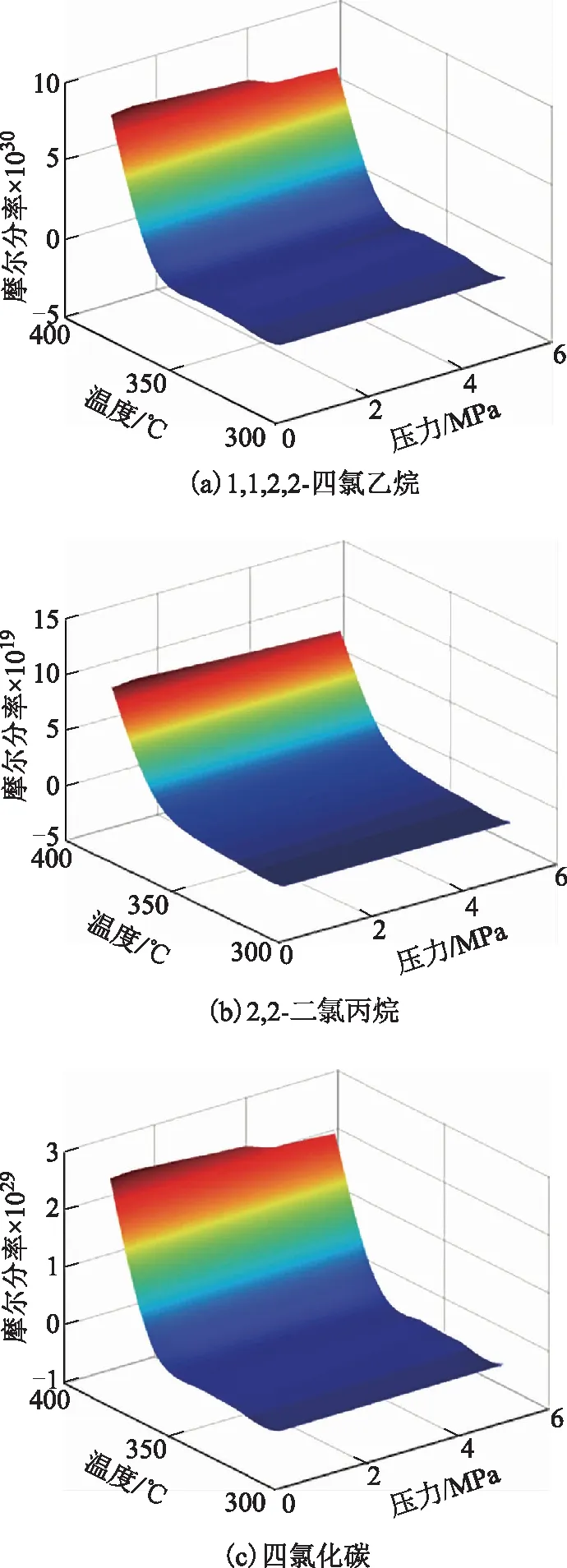
图5 反应温度及压力对不同氯代烷烃平衡组成的影响
3.2 氢油比的影响
考虑到部分有机氯化物中存在不饱和键,采用氢氯比作为考察氢气进料量对废塑料裂解油中有机氯化物脱除效果影响的指标时并不严谨。因此,将氢气进料量转换为标准状况下的氢气量,进而考察氢油比的变化对废塑料裂解油中有机氯化物脱除效果的影响。
为忽略其他杂质的影响,模拟中氢油比的计算仅考虑氢气与废塑料裂解油中的有机氯化物进行加氢反应,而在实际加氢过程中,氢气首先会与油品中烯烃、硫化物、氮化物等进行反应,且内、外扩散作用的影响也会导致氢气需求量增加,因此实际加氢过程中的氢油比会远大于利用Aspen Plus软件得到的模拟结果。
采用脱氯率作为考察氢油比对复杂反应平衡组成影响的指标。通过改变氢油比,考察废塑料裂解油中有机氯化物脱除率的变化趋势。脱氯率是以产物氯化氢的生成量为依据,即假设废塑料裂解油中有机氯化物的氯原子加氢后转化为氯化氢。在反应温度为320 ℃、压力为3 MPa、氢油体积比为0~7时,废塑料裂解油脱氯率的变化趋势如图6所示。
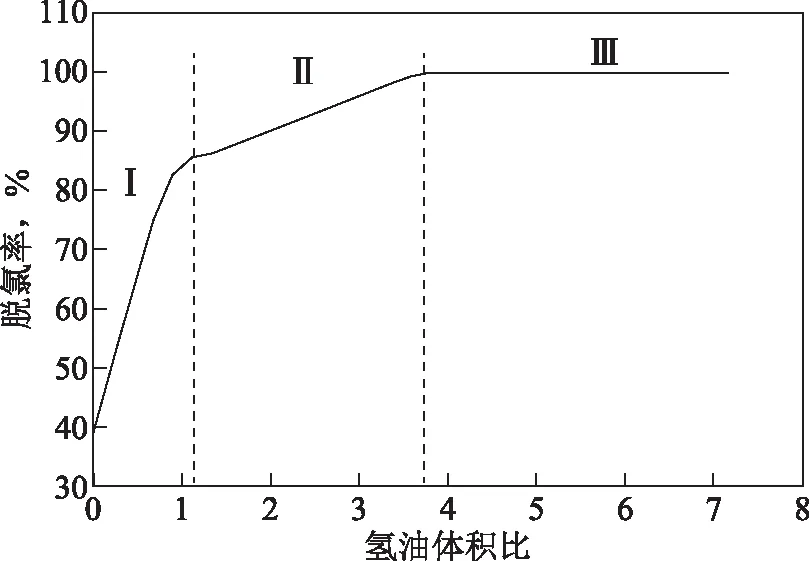
图6 氢油比对废塑料裂解油脱氯率的影响
由图6可知:当氢油体积比在0~1.12范围内时,脱氯率随氢油比的增加迅速升高;当氢油体积比大于1.12时,脱氯率随氢油比的增加持续升高,但增幅趋缓;当氢油体积比大于等于3.7时,脱氯率达到最大值后基本保持不变,最大脱氯率接近100%。值得注意的是,当氢油体积比为0时,脱氯率约为40%,表明各种有机氯化物在指定反应条件下混合时亦可生成氯化氢。
3.3 氢气与有机氯化物的反应顺序
由图6可知,废塑料裂解油中有机氯化物的加氢反应过程大致可分为3个阶段,在保持反应条件恒定的情况下,分别从上述3个阶段中各取3个点的氢油比,通过对比每阶段不同氢油比条件下各种有机氯化物的平衡流量,探究各种有机氯化物与氢气反应的先后顺序。其中,阶段Ⅰ和阶段Ⅱ为氢气未过量进料阶段,分别取氢油体积比为0.3,0.6,0.9和2,2.5,3;阶段Ⅲ为氢气过量进料阶段,取氢油体积比为5.5,6,6.5。以有机氯化物的平衡流量数值大小为依据,对模拟后各种有机氯化物的平衡流量进行降序排列,发现阶段Ⅰ的数据杂乱、规律性较差,但总体上看是氯代烯烃优先发生加氢反应;阶段Ⅱ和阶段Ⅲ的数据变化较为规律,因此以阶段Ⅱ、阶段Ⅲ中的数据为依据,分别对氢气未过量进料和过量进料阶段的反应情况进行分析。具体软件模拟数据分别如表4和表5所示。
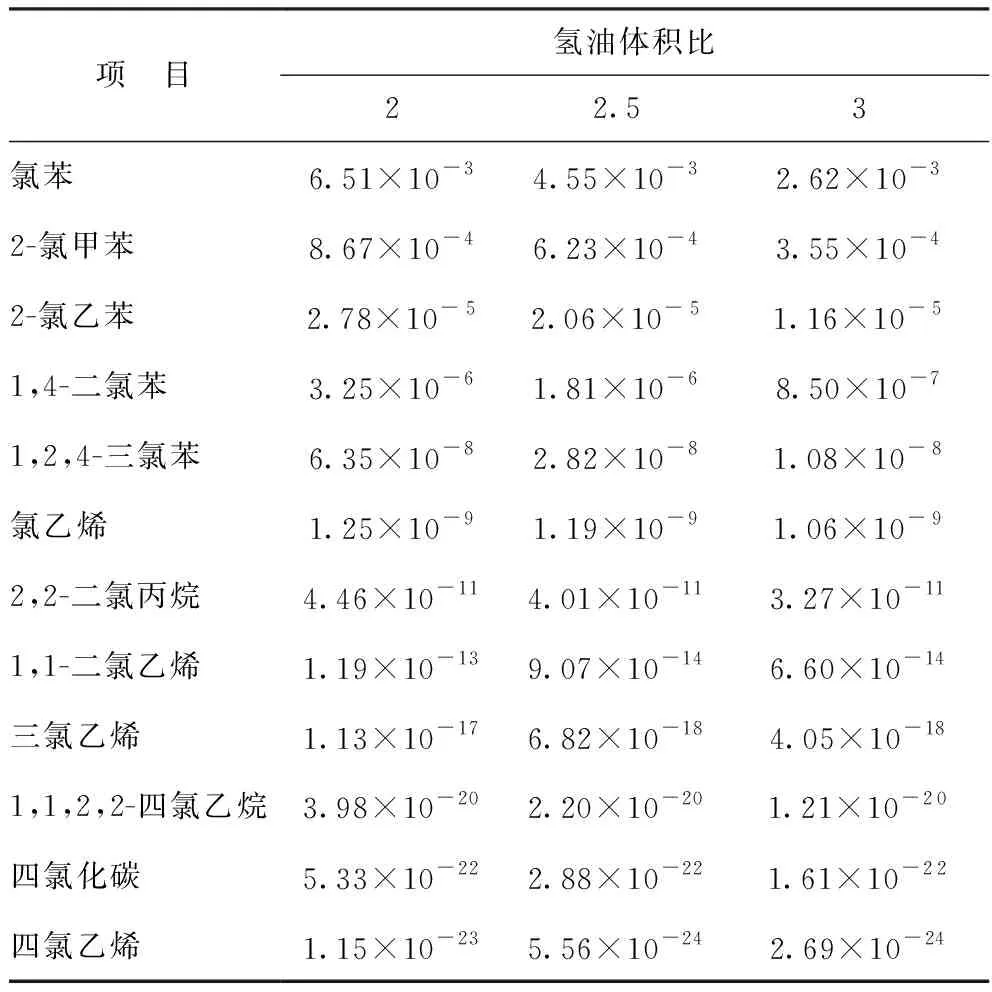
表4 氢气未过量进料时各种有机氯化物的平衡摩尔流量 mol/min
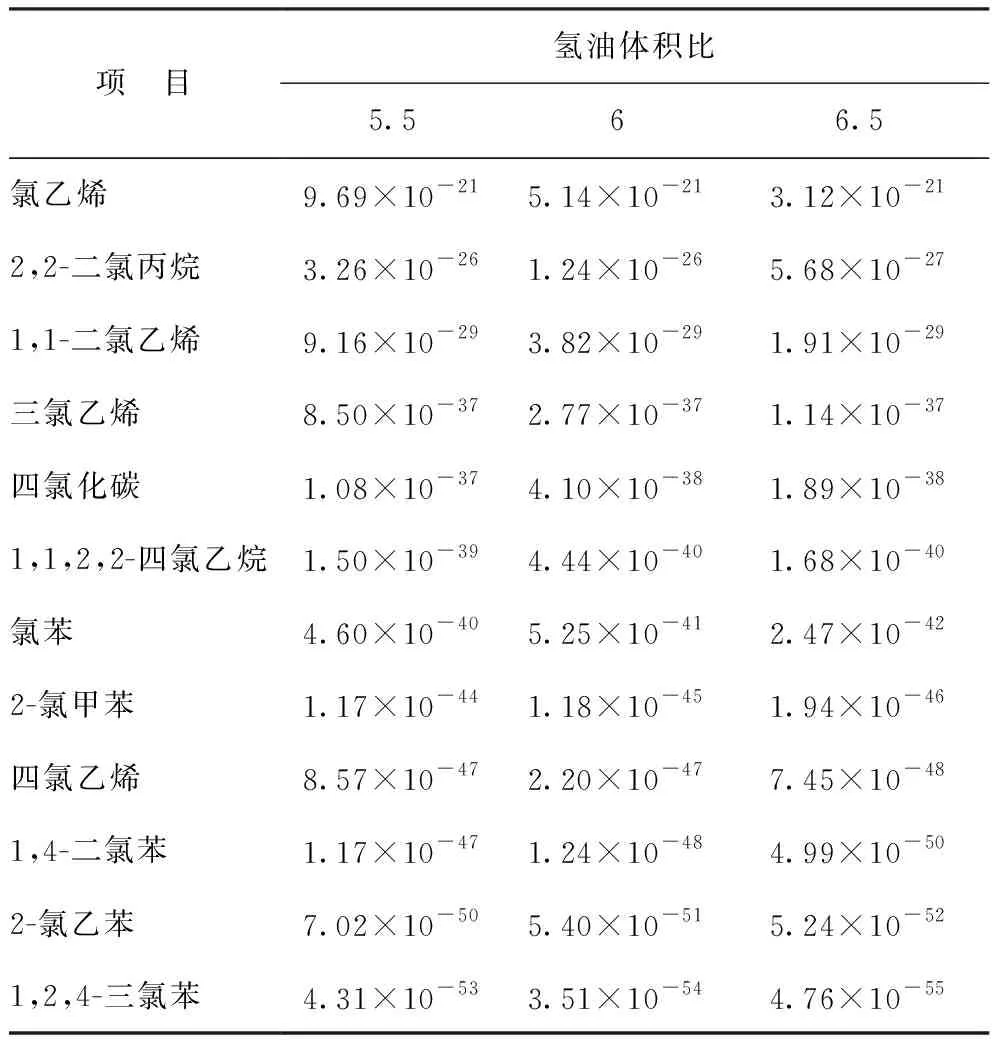
表5 氢气过量进料时各种有机氯化物的平衡摩尔流量 mol/min
由表4可知:在氢气未过量的情况下,各种有机氯化物的平衡流量均随氢油比的增加而减少;氯代烯烃和氯代烷烃的平衡流量较小,表明在反应初期氢气先与二者反应,准确地讲是氢气先将不饱和烃加氢饱和后再进行加氢脱氯反应,这从相同氯取代基数量的氯代烯烃的平衡流量低于氯代烷烃的平衡流量即可得知;平衡流量按数值从大到小的前5位均为氯代芳烃,其中以氯苯、2-氯甲苯最大,说明在反应初期氯代芳烃与氢气进行加氢反应的优先程度要排在氯代烯烃和氯代烷烃之后,原因是氯代芳烃的结构与氯代烯烃和氯代烷烃相比更为复杂和稳定。
由表5可知,与氢气未过量进料时相比,氢气过量进料时各种氯代芳烃的平衡流量显著降低,说明在氢气过量进料的情况下,氯代芳烃的加氢反应可以进行得较为彻底;多氯代烃的平衡流量远低于单氯代烃,说明多氯代烃更容易与氢气进行反应,原因是多氯代烃分子中的氯原子数目多,与氢气发生反应的概率要高于单氯代烃。综合表4和表5中的结果可知,一般情况下,氢气与有机氯化物的加氢反应由易到难的顺序为氯代烯烃>氯代烷烃>氯代芳烃。
此外,有机氯化物与氢气的反应顺序也可根据C—Cl键能的大小进行判断。各种有机氯化物的C—Cl键能如表6所示。

表6 各种有机氯化物的C—Cl键能[29]

3.4 氢气与有机氯化物的反应程度
通过探究氢气与有机氯化物的反应程度,可确定加氢脱氯反应后期难以脱除的有机氯化物种类。而表4和表5中的数据无法用来考察各种有机氯化物的加氢反应程度,原因如下:一是各种有机氯化物的初始进料组成不同,例如在进料中氯代烯烃的初始氯含量约占总氯含量的74%,这也可能是导致表5中加氢反应后期氯代烯烃的平衡摩尔流量相对较高的原因;二是上述模拟过程仅考虑有机氯化物加氢一步生成最终产物,并没有考虑到反应过程中氯代烃中间体的生成情况,而从废塑料裂解油中鉴定出的有机氯化物多为多氯代烃,加氢脱氯过程一般分多步进行,在反应过程中生成的多种氯代烃中间体之间可能会相互影响,因此需改进模拟方法。
为解决上述问题,重新设定有机氯化物的进料初始组成,按照氯代烯烃、氯代烷烃和氯代芳烃的分类方法,每类各选取一种典型的有机氯化物作为代表进行模拟,充分考虑反应过程中氯代烃中间体的生成情况,并保证生成的各种中间产物之间互不影响;设置废塑料裂解油的进料流量为1 L/min,各种有机氯化物的初始进料流量均为0.01 mol/min,尽可能地保证各种有机氯化物的初始氯含量相同。采用上述相同的反应条件和模拟方法,得出在氢油体积比为3.8时该体系的脱氯率达到最大值(接近100%),在不同脱氯率下这3种有机氯化物及其中间产物的平衡流量模拟数据如表7所示。表7中氯代烯烃的中间产物用氯代烯烃而不用氯代烷烃表示,是因为氯代烯烃加氢生成氯代烷烃并热解脱除氯化氢是一个非常快速的过程,在模拟过程中很难捕捉到氯代烷烃的生成踪迹。
由表7可知,在进料中氢气过量、氢油体积比为3.8时,该体系的脱氯率达到最高(99.99%),氯原子取代个数相同的有机氯化物及其中间产物的平衡流量由大到小的顺序为氯代烷烃>氯代芳烃>氯代烯烃,因此在氢气过量进料的条件下,各种有机氯化物的加氢脱氯反应程度由高到低的顺序为氯代烯烃>氯代芳烃>氯代烷烃。

表7 在不同脱氯率下各种有机氯化物及其中间产物的平衡摩尔流量 mol/min
事实上在氢油体积比为1.3时,该体系的脱氯率已达到了99%,此时反应体系中的氯代烯烃基本已反应完全,但氯代烷烃及氯代芳烃的平衡摩尔流量相对较大,尤其是氯代芳烃的平衡摩尔流量比氯代烯烃高几个数量级,表明在加氢脱氯反应的后期,部分氯代芳烃较难脱除;继续增大氢气的进料量,剩余的氯代芳烃可进一步脱除,而氯代烷烃基本不再发生反应。当氢油体积比由1.3增至3.8时,该体系的脱氯率由99%增至99.99%,增加不足1百分点。考虑到废塑料裂解油的氯质量浓度一般高达数千甚至上万mg/L,若按本次使用的废塑料裂解油有机氯化物质量浓度接近3 000 mg/L计算,即使在脱氯率达到99%的情况下,加氢处理后油品中的氯质量浓度仍接近30 mg/L,高于油品中氯化物质量浓度不大于20 mg/L的标准。虽然继续增大氢气用量可使脱氯率得到进一步的提升,但提升这不足1百分点的代价却是约99%脱氯率时3倍的氢气进料量,显然其经济性较低。因此如何在保持低氢耗的同时,将这约1百分点的“顽固”有机氯化物有效脱除,从而使油品中的氯含量达标,成为后续研究中值得思考的问题。
4 结 论
(1)从废塑料裂解油中鉴定出的13种有机氯化物在该复杂加氢反应体系中均可自发进行反应,且基本可反应完全。
(2)氯代烯烃及氯代芳烃的加氢反应平衡组成随着反应温度及压力变化的趋势基本相似,氯代烷烃的加氢反应平衡基本不受压力影响;对于给定的有机氯化物初始组成,在氢油体积比为3.7时脱氯率达到最大值;从热力学角度分析,该废塑料裂解油加氢脱氯的适宜反应条件为300~320 ℃、3~5 MPa,可为废塑料裂解油加氢脱氯技术的开发提供一定的指导。
(3)一般情况下,氢气与有机氯化物的加氢反应由易到难的顺序为氯代烯烃>氯代烷烃>氯代芳烃;在进料中氢气过量的条件下,各种有机氯化物的加氢反应程度由高到低的顺序为氯代烯烃>氯代芳烃>氯代烷烃;如何在保持低氢耗的情况下,将有机氯化物深度脱除,是后续研究过程中值得思考的问题。
