心肺联合超声目标导向液体管理在ICU心脏术后患者中的临床应用研究
2022-11-14赖军华马华怡
李 霞, 赖军华, 马华怡
心脏手术后患者常出现血流动力学不平稳的情况,需密切监测,输注液体过多或者过少都有可能对心脏术后患者造成不可逆的影响,包括各器官功能障碍,甚至死亡。容量管理的方法有中心静脉压(central venous pressure,CVP)监测、被动抬腿(passive leg raising,PLR)试验、脉搏指示连续心输出量(pulse-indicated continuous cardiac output,PICCO)监测、肺动脉漂浮导管以及超声监测等。目前比较常用的监测手段是CVP监测,其他监测手段各有利弊。床旁超声具有无创、便捷、可重复等优点,近年来已逐渐应用于临床[1]。已有研究表明超声测定下腔静脉直径及下腔静脉塌陷率与患者CVP有良好的相关性[2]。目标导向超声治疗方案是近年来出现的指导液体用量的新方法,主要应用于感染性休克、急性呼吸窘迫综合征、脓毒血症、急性肾功能衰竭患者的液体管理[3-6],但其在心脏手术后患者的管理中应用较少。鉴此,本研究旨在探讨心肺联合超声目标导向液体管理在重症加强护理病房(intensive care unit,ICU)心脏术后患者中的临床应用效果,现报告如下。
1 对象与方法
1.1研究对象 选择2020年6月至2021年3月我院ICU收治的心脏术后患者50例,采用随机数字表法将其分为研究组和对照组,每组25例。排除有下列情况之一者:(1)年龄<18岁;(2)心功能Ⅳ级[参照美国纽约心脏病学会(New York Heart Association,NYHA)标准];(3)存在高腹腔压;(4)超声提示右心功能不全;(5)不能进行超声检查;(6)存在明确外科原因所致的大出血、心脏破裂、心脏骤停。所有纳入对象知情同意参与本研究并签署知情同意书。本研究获医院伦理委员会批准(KY2020069)。两组进入ICU时的年龄、性别、急性生理学及慢性健康状况评分系统Ⅱ(Acute Physiology and Chronic Health Evaluation Ⅱ,APACHE Ⅱ)评分、平均动脉压(mean arterial pressure,MAP)、疾病种类等基线资料比较差异无统计学意义(P>0.05)。见表1。
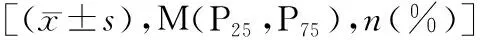
表1 两组基线资料比较
1.2方法 研究组采用心肺联合超声目标导向液体管理方案,对照组采用CVP指导液体管理方案。两组治疗过程中可根据患者病情调整血管活性药物,使用强心药物或进行利尿治疗。若患者出现严重并发症需要使用连续性肾脏替代治疗(continuous renal replacement therapy,CRRT)或体外膜肺氧合治疗时则退出本研究。
1.2.1 心肺联合超声目标导向液体管理方案[7]采用迈瑞M5便携式彩色多普勒超声诊断仪(深圳迈瑞生物医疗电子股份有限公司),进行心脏超声和肺部超声评估。(1)心脏超声:使用心脏超声探头探查心尖四腔心切面、胸骨旁长、短轴切面了解心脏情况;探查右侧肝切面检查下腔静脉直径,并进行心脏前负荷评估,明确心腔大小、亲吻征、左心室流出道速度时间积分((velocity-time integral,VTI)、下腔静脉塌陷(<1 cm)或充盈(>2.1 cm)情况。下腔静脉塌陷指数=(IVC呼气期-IVC吸气期)/IVC呼气期。(2)肺部超声:使用腹部探头,以胸骨角水平线分为上、下2个区,再将每一个区以腋前线和腋后线为界分为前、中、后3个区,两侧肺部共划分为12个区域。肺部超声主要观察彗星尾征(B线)、火箭征、肺实变或肺不张、胸腔积液发生情况。治疗过程中以出现心腔扩大(目测明显增大或左室内径变化率<25%)、下腔静脉直径增宽>2.1 cm、下腔静脉塌陷率<40%、肺水增加(出现B线、火箭征或胸腔积液)中任何一项为补液终止指征[8]。所有患者床旁超声由同一名经过专业培训的重症医师进行操作。
1.2.2 CVP指导液体管理方案 通过CVP指标指导液体管理,维持CVP在8~12 cmH2O,若CVP<8 cmH2O则加快输液速度,若CVP>12 cmH2O则限制液体输注速度。
1.3观察指标 (1)术后24 h心率、呼吸频率、MAP、氧合指数(PaO2/FiO2)、血乳酸、左室射血分数。其中MAP应用迈瑞监护仪进行监测;氧合指数及血乳酸应用罗氏公司cobas b 123血气分析仪进行检测;左室射血分数应用迈瑞MS便携式彩色多普勒超声诊断仪测量。(2)术后24 h内患者肾上腺素、多巴胺的使用量。(3)术后24 h内总输液量、输血量。(4)术后24 h呼吸机使用时间、住ICU时间、住院时间。(5)术后二次手术率、28 d病死率。

2 结果
2.1两组术后24 h生物学指标及药品、液体、血液输入量比较 在术后24 h,研究组呼吸频率、心率低于对照组,MAP、PaO2/FiO2水平高于对照组,差异有统计学意义(P<0.05)。在术后24 h内,研究组肾上腺素用量、多巴胺用量、总输液量和输血量均低于对照组,差异有统计学意义(P<0.05)。见表2。

表2 两组术后24 h生物学指标及药品、液体、血液输入量比较
2.2两组术后24 h呼吸机使用时间、住ICU时间、住院时间比较 研究组术后24 h呼吸机使用时间、住ICU时间、住院时间均短于对照组,差异有统计学意义(P<0.05)。见表3。

表3 两组术后24 h呼吸机使用时间、住ICU时间、住院时间比较
2.3两组预后情况比较 研究组二次手术1例,对照组2例,均因活动性出血导致血流动力学不平稳,血红蛋白进行性下降,需二次开胸探查止血治疗。两组二次手术率差异无统计学意义(χ2=0.000,P=1.000)。对照组术后28 d死亡1例,原因为出现恶性心律失常,积极治疗效果不佳,抢救无效死亡。研究组术后28 d无死亡病例。两组术后28 d病死率差异无统计学意义(χ2=0.000,P=1.000)。
3 讨论
3.1液体管理与危重症患者预后具有关联,液体不足或液体过量都会影响危重症患者的救治效果,尤其是对于心脏术后患者,患者可能因手术失血、血容量重新分布等导致血容量不足,或由于心脏收缩功能的原因导致心脏前负荷过重,此时是需进行补液还是利尿治疗,这对于临床医师而言是一个难题。目前评估机体容量状态以及容量反应性的方法包括CVP监测、PLR试验、PICCO监测以及肺动脉漂浮导管等。但它们也各有缺点:CVP受心脏的收缩-舒张功能、瓣膜功能、胸腔顺应性等因素的影响;腹腔压力增高会影响PLR试验的结果,而PICCO监测及漂浮导管费用昂贵且有创。床旁超声目前已广泛应用于临床各科室,具有方便、无创、快捷及可重复等优点,可以用于评估患者容量状态以及容量反应性。
3.2根据美国超声心动图学会(American Society of Echocardiography,ASE)和美国急诊医师学会(American College of Emergency Physicians,ACEP)的共识[9],床旁心脏超声是为了解决某个特定的问题而进行的针对性检查。重症超声在心脏外科围手术期的应用包括以下几个方面:(1)超声指导下的容量管理;(2)超声评估心脏瓣膜病患者术后心功能,及早发现术后低心排血量;(3)床旁超声探查术后低氧血症原因,指导早期拔管。
3.3心脏病术后患者因为经历了体外循环、长时间呼吸机支持、有创操作等,是感染性休克的高危人群,而且,心脏病患者的补液一直是危重医学的难题之一。常用的脓毒症患者液体复苏方案是给予30 ml/kg的晶体液扩容[10]。但是这种方法未必适用于心脏病术后患者,这是因为心脏病患者围手术期常常合并多种干扰因素,如感染所致的心肌抑制[11-12]、心脏病导致的心功能障碍、高龄、心肺功能不全、急性肾功能不全等因素,均对患者的围手术期液体管理造成一定困扰。床旁超声可以通过监测每搏量(stroke volume,SV)和心输出量(cardiac output,CO)、下腔静脉直径以及塌陷指数、锁骨下静脉直径及塌陷指数、上腔静脉直径及塌陷指数、股静脉等指标来评估患者的血容量情况[13]。下腔静脉是顺应性良好的薄壁容量血管,吸气时胸廓内压下降,下腔静脉回流至右心房的血液增加导致下腔静脉管径减小,而呼气时胸廓内压升高,回流至右心房的血量减少,下腔静脉管径扩张[14],不受容量丢失后动脉收缩代偿机制的影响,这就使得床旁超声可较依赖动脉系统的监测方法更好地反映患者的即时血容量。当患者有效循环血容量减少时,下腔静脉管径随呼吸变化的幅度可用下腔静脉呼吸变异指数(即塌陷指数)来表示,此时下腔静脉管径随呼吸运动的变化幅度增加[15]。这种方法已被美国超声协会推荐为快速、便捷、无创的容量评估方法[16-17]。
3.4床旁超声也可用于监测肺水。有研究结果显示,床旁肺超声检查监测血管外肺水的灵敏度和特异度分别达90%和86%[18];若超过三个区域检测到B线,其监测血管外肺水的灵敏度和特异度可达100%和70%[19]。提示肺超声可以较好地监测血管外肺水及肺水肿的发生,结合心脏超声可以鉴别心源性肺水肿或非心源性肺水肿。此外,超声还可用于指导外科术后二次开胸探查,及早发现潜在的出血、心包填塞等问题。
3.5本研究结果显示,在心肺联合超声目标导向液体管理方案下,研究组患者呼吸频率、心率、动脉压、氧合指数等指标均明显好转且优于对照组,提示此方案指导下液体管理能够改善患者肺部状况,减轻心脏负荷,避免器官进一步损害,改善患者预后。有研究表明,控制总液体摄入量与降低毛细血管静水压及改善心肺顺应性具有关联[5],且早期液体负平衡有利于改善心脏术后患者的预后[20],这与本研究结果相符。本研究中研究组的二次手术率以及28 d病死率低于对照组,但两组比较差异无统计学意义(P>0.05),考虑与纳入研究对象病情相对较轻以及纳入研究对象数量相对较少有关。
3.6本研究结果显示,研究组与对照组术后24 h血乳酸水平比较无显著差异。心脏术后患者血乳酸因体外循环、心脏收缩功能等因素,出现不同程度的升高,可分为早发型高乳酸血症和迟发型高乳酸血症。早发型高乳酸血症与体外循环导致微循环障碍有关;迟发型高乳酸血症发生在术后6~12 h[21]。本研究中纳入的研究对象主要为心功能相对较好的患者,术后血乳酸值高峰在术后6 h左右出现,并在术后6~12 h达到清除峰值,大部分患者在术后24 h就已恢复至正常水平。另外,本研究结果还显示两组术后24 h左室射血分数比较差异无统计学意义(P>0.05)。分析原因可能与本研究纳入的对象心功能情况较好有关,且已排除严重心功能障碍、心功能不全的患者,因此患者术后早期液体管理对其影响较小,而血管活性药物的调整也会影响患者的心功能。本研究中,研究组术后24 h内的肾上腺素用量、多巴胺用量、总输液量、输血量均显著低于对照组,表明心肺联合超声目标导向液体管理在心脏术后患者取得较好的效果,能够改善组织灌注,减少血管活性药物使用,具有临床应用价值。
3.7本研究也存在一些不足之处,主要包括:(1)研究对象心功能情况较好,未能评估该管理办法对心功能严重异常者的效果;(2)纳入的研究病例数相对较少,且均为单中心数据;(3)本研究仅对比了术后24 h的血流动力学变化情况,但对术后早期各时间点的血流动力学变化以及液体出入量变化未能详细记录。
综上所述,心肺联合超声目标导向液体管理可有助于改善患者心肺情况,减少血管活性药物使用和输注量,对ICU心脏术后患者液体管理具有临床价值,但研究结论尚需进一步验证。
