UPLC-MS/MS法研究联苯双酯对葛根素大鼠血浆药代动力学的影响*
2022-11-11张国哲何姝颖
张国哲,张 周,何姝颖
(江苏医药职业学院药学院,江苏 盐城 224005)
葛根素是葛根解酒保肝的主要活性成分之一[1-3],还可用于防治心脑血管疾病[4]、急性肝肾损伤[5],并对高血压[6]、骨质疏松症[7]、炎症、高脂血症和糖尿病有治疗作用[8]。联苯双酯是由五味子素C合成的保肝化合物[9],对氯仿、乙醇及其他化学试剂引起的化学性肝损伤显示出明显的保护作用[10-12],广泛用于治疗慢性肝炎[13-14]。但联苯双酯口服生物利用度仅为10%~30%,故由于水溶性差和口服生物利用度低而限制了其临床应用[15]。单体成分给药经常出现耐药性、毒副作用等问题,且联苯双酯停药后存在谷丙转氨酶回升问题,通常称为“反跳”现象[16]。因此,考虑是否可以通过药物的联合使用解决上述的问题。有报道称联苯双酯与某些药物联合使用可以降低这些药物的血药浓度,并且联苯双酯与某些药物联合使用可以降低药物性肝损伤的发生率,同时也可以增强治疗效果[17-19]。药物的联合使用过程中,药代动力学参数的考察是必要的。本研究考察了联苯双酯对大鼠口服葛根素药代动力学的影响,旨在为两种保肝药物的联合使用提供动物实验依据。葛根素和联苯双酯结构式见图1。
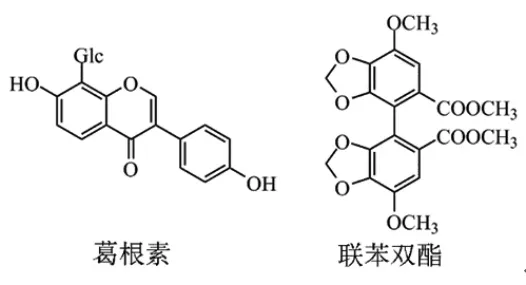
图1 葛根素和联苯双酯结构式
1 材 料
1.1 药物与试剂 葛根素标准品(批号:G008-180426,纯度>98%)购自成都瑞芬思生物科技有限公司;盐酸小檗碱标准品(批号:20170708,纯度>98%)购自上海金穗生物科技有限公司;联苯双酯滴丸(批号:17060)购自北京联合制药有限公司;乙腈(色谱级)和甲酸(色谱级)均购自美国赛默飞世尔科技公司;超纯水采用Milli-Q水净化系统制备。
1.2 仪器Waters Xevo TQD三重四极杆液质联用仪(美国沃特世科技有限公司);AL104型电子天平(梅特勒-托利多仪器有限公司);SB-5200D型超声波仪(宁波新芝生物科技股份有限公司);TGL-16K型低温离心机(湖南湘仪离心机仪器有限公司);MIX-2500混合振荡器(上海启前电子科技有限公司);Milli-Q超纯水仪(法国密理博公司)。
1.3 实验动物SPF级雄性健康Wistar大鼠12只,体质量为250~270 g,7周龄,购自斯贝福(北京)生物技术有限公司,动物生产许可证号:SCXK(京)2019-0004。饲养条件:标准饲料,自由饮食和进水,环境温度23~27℃,相对湿度45%~55%。实验方案经江苏职业技术学院医学实验动物管理委员会批准,批准号:XMLL-2021-045。
2 方 法
2.1 标准溶液的配制 精密称取葛根素和盐酸小檗碱标准品各5 mg,分别置于25 mL容量瓶中,用甲醇溶解并定容。取一定量葛根素母液用甲醇稀释制备质量浓度为200 μg/mL的葛根素储备液。随后将储备液用甲醇稀释制备一系列标准品溶液(4 000、1 000、400、200、100、40 ng/mL)。同时用甲醇制备100 μg/mL的内标储备液,并用甲醇稀释储备液制备质量浓度为100 ng/mL的内标工作液。按照上述相同步骤制备了低、中、高浓度(8、80、720 ng/mL)的葛根素质量控制样品。
2.2 色谱、质谱条件 色谱条件:使用Acquity UPLC系统(Waters)进行样品分离。采用HSS T3色谱柱(50 mm×2.1 mm,1.8 μm),流动相A为0.1%甲酸-水,流动相B为0.1%甲酸-乙腈。梯度洗脱如下:0~0.5 min,10%B~15%B;0.5~2 min,15%B~40%B;2~4 min,40%B~80%B;4.1~5 min,80%B~99%B;5.1~7 min,99%B~10%B。流速为0.3 mL/min,柱温为40℃,样品室温度为10℃,进样量为2 μL。
质谱条件:使用Waters TQD串联质谱电喷雾电离(ESI)源进行质谱检测。采用多反应监测(MRM)的正离子模式测试样品,并使用以下母离子>子离子对进行定量:葛根素(m/z)417.1>297.0,盐酸小檗碱(m/z)336.0>320.0。葛根素和盐酸小檗碱的锥电压均为35 V,碰撞能为30 eV,氩气用作碰撞气。毛细管电压设定为2.8 kV,源温度设定为500℃,氮气流量为850 L/h。锥孔气流速为50 L/h。葛根素和盐酸小檗碱的质谱碎片图见图2。使用MassLynx4.1进行数据采集和仪器控制,并使用TargetLynx进行定量分析。
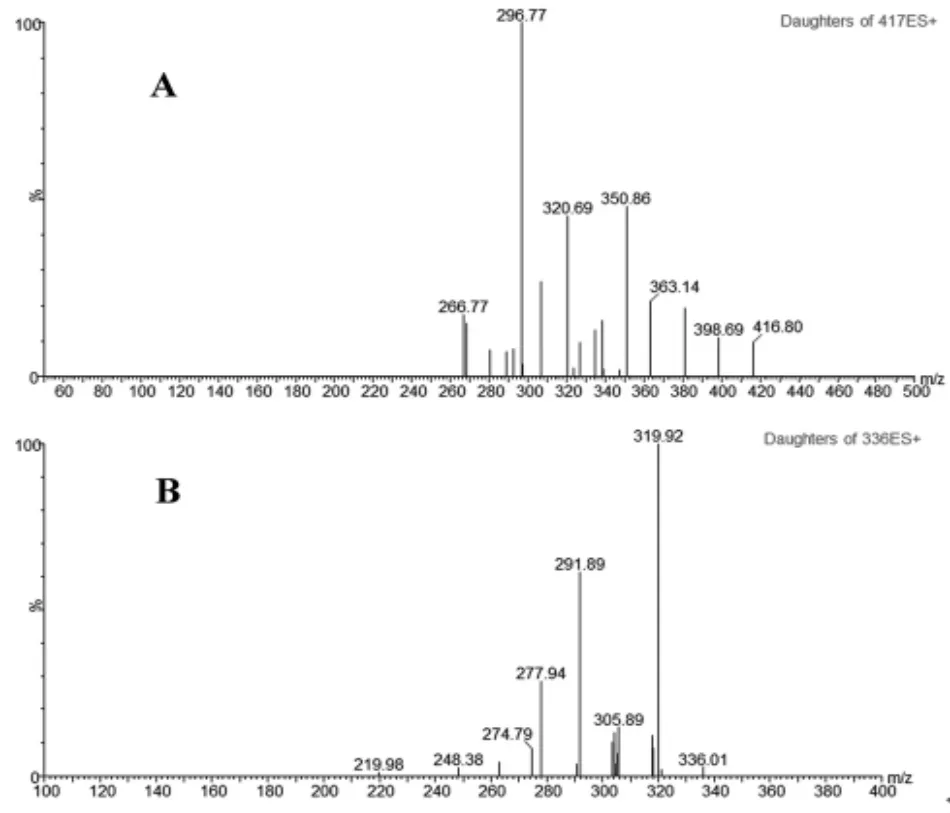
图2 葛根素(A)和内标盐酸小檗碱(B)质谱离子碎片图谱
2.3 大鼠分组及给药 将12只雄性Wistar大鼠随机分为葛根素组和葛根素+联苯双酯组,每组6只。葛根素+联苯双酯组大鼠按葛根素100 mg/kg与联苯双酯30 mg/kg剂量单次灌胃给药(葛根素和联苯双酯均溶于0.5%羧甲基纤维素钠制备成混悬液,质量浓度分别为10 mg/mL和3 mg/mL);葛根素组大鼠灌胃给予葛根素(质量浓度为10 mg/mL),100 mg/kg。
2.4 血浆样品的采集与处理 分别于给药前及给药后的0.25、0.50、0.75、1.00、1.50、2.00、3.00、4.00、6.00、8.00、12.00、24.00、36.00、48.00 h,眼眶后静脉采集全血,4℃下以3 500 r/min离心10 min分离血浆,于-80℃冰箱保存。
取100 μL大鼠血浆和20 μL的内标工作液(100 ng/mL)加入1.5 mL EP管中,涡旋混合30 s,加入500 μL乙腈沉淀蛋白。涡旋混合2 min,并以10 000 r/min离心10 min。将上清液移至另一EP管中,室温下用氮气吹干。残余物用复合溶液[V甲醇∶V水=80∶20]以13 000 r/min离心10 min,取2 μL上清液进样分析。
2.5 统计学方法 数据采用SPSS 25.0软件进行统计分析,两组间计量资料比较采用t检验,P<0.05为差异有统计学意义。
3 结 果
3.1 方法学考察
3.1.1 线性关系考察 取空白大鼠血浆100 μL,加入20 μL不同浓度的葛根素标准溶液,使样品中葛根素的质量浓度分别为800、200、80、40、20、8 ng/mL。按上述“2.4”项下的方法进行样品处理和质谱检测。采用加权(1/χ2)最小二乘法用于线性回归方程计算。以葛根素与内标的峰面积比为纵坐标(y),以相应的葛根素质量浓度为横坐标(x,ng/mL),得回归方程为:y=1.099x+2.985,判定系数(R2)为0.996 1。表明大鼠血浆葛根素浓度在8~800 ng/mL范围内线性关系良好。葛根素的定量下限(LLOQ)为校准曲线上最低浓度,即8 ng/mL。
3.1.2 专属性试验 使用大鼠的空白血浆样品考察内源性成分的潜在干扰。量取100 μL空白血浆(不加内标),按照“2.4”项下处理样品,并进行质谱分析。取100 μL空白血浆并加入内标和LLOQ浓度的葛根素,按相同处理方法处理并进样分析。取100 μL大鼠口服葛根素后0.25 h血浆样品,按相同方法处理并进样分析。结果显示多反应监测(MRM)的专属性强,内源干扰少,在样品和空白血浆中未观察到葛根素和内标的干扰峰。(见图3)3.1.3精密度和准确度试验 取100 μL的空白血浆,分别加入低、中、高浓度(8、80、720 ng/mL)的葛根素标准品溶液,每个浓度5份,按照“2.4”项下血浆样品处理步骤进行处理并分析,连续3 d。计算日内、日间精密度和准确度。结果显示精密度的RSD为6.59%~14.91%,准确度的RE为-11.25%~12.55%,符合生物样品分析要求。
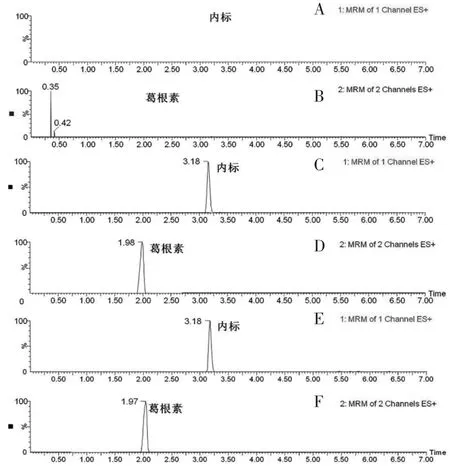
图3 血浆中葛根素多反应监测(MRM)图

表1 准确度、精密度结果 (n=5)
3.1.4 提取回收率和基质效应试验 精密量取100 μL的空白血浆,按“2.4”项下方法处理,制备低、中、高3个浓度的血浆样品各5份,进样分析,得到对应的峰面积A1;另取空白血浆100 μL,加入500 μL乙腈沉淀蛋白,按“2.4”项下方法处理后,在上清液中分别加入低、中、高3个浓度的葛根素对照品溶液20 μL,进样分析,得到对应的峰面积A2;相同分析条件下测定相应的低、中、高3个质量浓度对照品溶液各5次,得到对应的峰面积为A0,提取回收率计算公式为A1/A2,基质效应计算公式为A2/A0。结果如表2所示,葛根素的提取回收率为85.65%~93.42%。葛根素的基质效应范围为108.82%~113.21%。结果均符合生物样品分析要求。
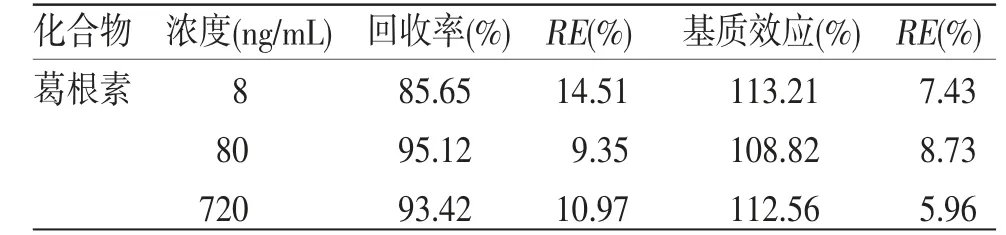
表2 提取回收率及基质效应结果 (n=5)
3.1.5 稳定性试验 通过分析3种不同储存条件下的QC样品研究葛根素在大鼠血浆中的稳定性,包括3个冻融循环,室温放置24 h和-20℃持续30 d考察稳定性。在3种试验条件RE均在±15%范围内,表明葛根素具有较好的稳定性。(见表3)

表3 葛根素在大鼠血浆中的稳定性结果 (n=5)
3.2 葛根素在大鼠体内的药代动力学 药代动力学参数通过DAS2.0软件进行评估,选择2室模型,权重1单次给药,分析主要药代动力学参数。数据用SPSS18.0软件进行统计分析,使用t检验比较两组间Cmax、Tmax、t1/2、AUC0-inf、AUC0-t、MRT0-t、CLz/F和Vz/F参数。葛根素在两组大鼠体内的平均血浆浓度-时间曲线,见图4。主要药代动力学参数见表4。结果显示,大鼠口服葛根素联合联苯双酯后,葛根素的最大血药浓度(Cmax)从(101.64±41.82)ng/mL增加到(124.75±51.47)ng/mL(P>0.05),葛根素的Tmax从(1.46±1.08)h降低至(0.46±0.10)h(P<0.05)。但是,浓度-时间曲线下面积(AUC0-t)从(213.09±61.91)μg·h/L降低到(201.65±53.68)μg·h/L(P>0.05)。两组药代动力学参数比较,差异无统计学意义(P>0.05)。
表4 两组大鼠药代动力学参数比较 (±s,n=6)
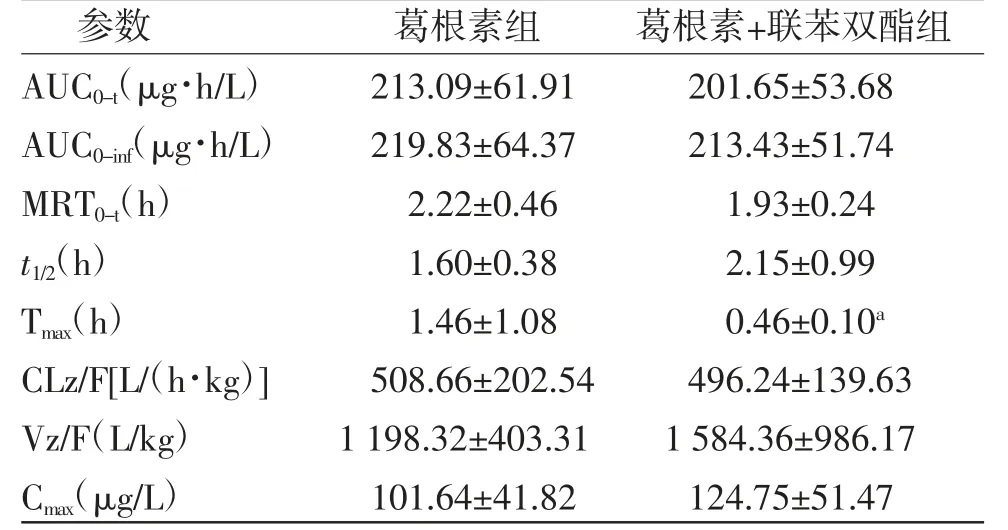
表4 两组大鼠药代动力学参数比较 (±s,n=6)
注:与葛根素组比较,aP<0.05
参数 葛根素组 葛根素+联苯双酯组AUC0-t(μg·h/L) 213.09±61.91 201.65±53.68 AUC0-inf(μg·h/L) 219.83±64.37 213.43±51.74 MRT0-t(h) 2.22±0.46 1.93±0.24 t1/2(h) 1.60±0.38 2.15±0.99 Tmax(h) 1.46±1.08 0.46±0.10a CLz/F[L/(h·kg)] 508.66±202.54 496.24±139.63 Vz/F(L/kg) 1 198.32±403.31 1 584.36±986.17 Cmax(μg/L) 101.64±41.82 124.75±51.47
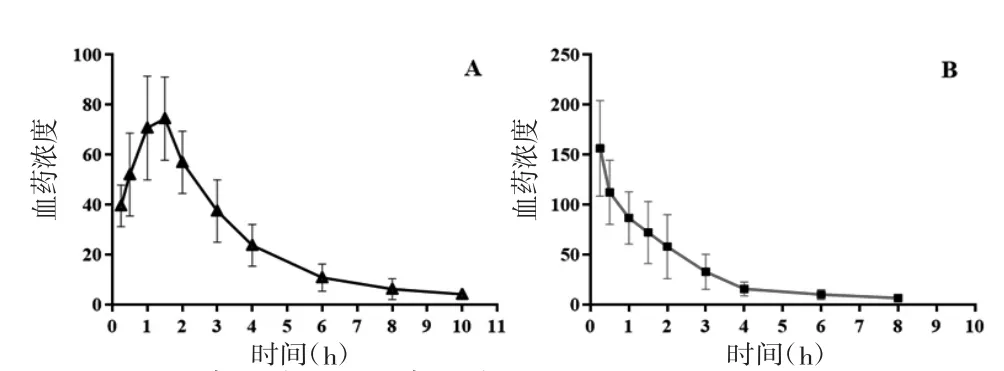
图4 两组大鼠血浆中的血药浓度-时间曲线图
4 讨 论
葛根素为异黄酮成分,文献报道主要采用正离子模式进行质谱检测[20-21]。本实验对正负离子模式均进行了比较,正离子模式响应更高,色谱峰形更好,因此实验选择正离子模式进行质谱数据采集。通过查阅文献及实验条件摸索,本实验选择常用的(m/z)417.1>297.0作为葛根素定量母子离子对,因为此离子对背景干扰少,而且响应较高。本实验将碰撞能从20~50 eV进行优化,最终选择30 eV。由于葛根中存在大量异黄酮成分,而且大鼠口服葛根素后,会发生系列代谢反应。因此,试验排除了大豆异黄酮和尼泊尔鸢尾异黄酮内标,而选择盐酸小檗碱为本试验内标,即没有内源及潜在代谢物的干扰,同时又有较好的质谱响应。
有研究显示,某些药物的联合使用也会影响葛根素的药代动力学参数,如甘草甜素和黄芪甲苷Ⅳ均可显著降低葛根素的Tmax、Cmax和AUC0-t,表明甘草甜素、黄芪甲苷Ⅳ与葛根素联合用药时的药物相互作用不可忽视[22-23]。也有研究显示:联苯双酯与某些药物联合使用会使该药物的血药浓度降低,如联苯双酯可以降低他克莫司胶囊(FK506)的血药浓度;当联苯双酯与他林洛尔联合使用时,也会使他林洛尔的血药浓度降低;联苯双酯还能降低CYP3A4控制的环孢霉素的血药浓度[24-25]。其原因可能是联苯双酯可以诱导肝细胞色素P450中的特定酶,从而加速药物的代谢,降低其血药浓度,同时也使药物半衰期缩短。如联苯双酯可以加速诱导CYP2B1的作用,而CYP2B能催化底物加速代谢,形成易于排泄的药物代谢物。此外,联苯双酯可以抑制特定细胞色素酶的活性,影响联合使用药物的代谢,从而降低药物的血药浓度。中医学认为肝炎的发生与外感六淫、疠气、七情内伤、饮食劳倦失常、瘀血、痰饮有形之邪阻滞等多种因素有关。使用联苯双酯时结合中医的辨证施治,发挥中医的优势配合选用对证的方剂治疗,可以有效提高疗效,减轻联苯双酯的停药“反跳”现象。
本研究结果表明,联苯双酯虽然可以增加大鼠血浆中葛根素的Cmax并缩短Tmax,说明联苯双酯可以在一定程度上促进葛根素的吸收。然而,除Tmax有明显差异以外,葛根素组和葛根素+联苯双酯组之间其他药代动力学参数无明显差异,联苯双酯和葛根素联合使用时的药物间的相互作用不会影响葛根素的药代动力学参数,临床两种药物可以联合用于酒精性肝损伤的预防和治疗。
5 结 论
本研究建立并验证了一种简便、快速、准确的UPLC-MS/MS方法测定大鼠血浆中葛根素含量,并比较了大鼠灌胃给予葛根素及联合灌胃给予葛根素和联苯双酯后大鼠血浆中葛根素的血药浓度。结果表明:与葛根素组比较,除了Tmax明显缩短外,两组间的其他药代动力学参数无明显差异。联苯双酯和葛根素联合使用时的药物间的相互作用不会影响葛根素的药代动力学参数,临床可以同时使用两种药物用于酒精性肝损伤的预防和治疗。
