锰氧化物-海藻酸钠凝胶微球材料的制备及其在偶氮染料废水处理中的应用
2022-11-10何怡静刘嘉润石玉青
何怡静,乔 宇,刘嘉润,石玉青,梁 杰
(上海师范大学化学与材料科学学院,上海 200234)
0 引言
染料废水含有多种污染物质,包括各种纤维材料、化学药剂、染料、浆料和各种整理剂,其中30%以上的染料被直接排放进入水体,包括大量难于脱色、组分复杂、难以生化降解的污染物.所以,染料废水是中国最具危害和难处理的工业废水之一[1-6].偶氮染料的使用量在所有染料使用量中占比最高,高达三分之二,该产品可用于各种纤维的染色和印花.约有10%~15%以上的偶氮染料被释放到水环境中,在特定情况下,偶氮染料可分解生成具有致癌作用的芳香胺.偶氮染料抗光、抗氧化能力强,即使较低的浓度进入水中,仍然可以产生明显颜色,从而影响光照摄入量,影响水生生物活动,进而破坏生态平衡.另外,偶氮染料中的“三致”作用和生物抵抗性,进一步对自然生态环境和人体健康构成了威胁[7].
高级氧化技术(AOPs)可以通过光辐射、超声波、过渡金属氧化物等多种方式产生自由基,并以自由基为活性物种,该技术中产生的过硫酸根自由基氧化能力强,与污染物反应速率快,可降解大多数有机污染物.近年来,越来越多的学者关注了以过一硫酸盐(PMS)作为氧化剂的非均相类Fenton技术,主要是因为与传统的Fenton技术相比,非均相类Fenton技术中过硫酸根(SO4-)可以在更广泛的pH值范围内发挥出较好的氧化能力,其中PMS具有稳定的化学性能,以及易于储存和运输等优点[8-9].与其他的催化剂相比,锰氧化物(MnOx)因其低毒性、储量大、绿色环保等优势,也被越来越多地应用到污染物处理中.而海藻酸钠(SA)作为一种天然多糖,其主要成分为海藻酸的钠盐.SA溶液可以与钙离子(Ca2+)、钡离子(Ba2+)等多种金属阳离子反应形成性能稳定的凝胶[10].废水降解过程中,金属氧化物可能会产生聚集等问题,与SA结合形成复合凝胶材料后,不仅机械强度增大,不易破损,而且化学性质更加稳定,减少了聚集的可能,提高了适用性.
因此,本研究采用水热法制备MnOx,与SA结合形成一种锰氧化物-海藻酸钠凝胶微球(MnOx@MABs)材料,并对其进行X-射线衍射(XRD)、场发射扫描电镜(FE-SEM)和红外光谱(FT-IR)表征,将其应用于活化PMS降解偶氮染料废水的代表污染物日落黄.同时,考察了MnOx@MABs材料的投加量、废水的pH值、废水温度、日落黄初始浓度对其吸附性能的影响.最后,结合材料的微观结构和对日落黄的降解效能,分析了MnOx@MABs材料的使用情况.
1 实验部分
1.1 主要试剂和仪器
主要试剂:氢氧化钠(NaOH)、无水氯化钙(CaCl2)、硫酸(H2SO4)、硫酸锰一水合物(MnSO4·H2O)、无水硫代硫酸钠(Na2S2O3),均采购于国药集团化学试剂有限公司;过硫酸氢钾(KHSO5)、日落黄,均采购于上海麦克林生化科技有限公司;次氯酸钠(NaClO),采购于上海氯碱化工有限集团公司;SA,采购于上海阿达玛斯试剂有限公司;模拟废水,用日落黄溶液模拟印染废水,进行降解实验;本实验中,若无特别说明所用水均为超纯水.
主要仪器:FE-SEM,Hitachi S4800;FT-IR测试仪,PK-60000;XRD,Dmax-2000X;磁力搅拌器,MSH280-Pro;加热套,ZNCL-TS-C250ML;旋转蒸发仪,RE-2000A;真空干燥箱,DZF-6053;恒温振荡水槽,DKZ-2B;紫外分光光度计,DU730;pH计,5B-3C.
1.2 制备方法
1.2.1 MnOx材料的制备
称取1.0 g一水合硫酸锰(MnSO4·H2O),加入40 mL蒸馏水,搅拌均匀至澄清.取适量NaClO溶液(按不同的MnSO4与NaClO物质的量之比:1∶1.0,1∶1.5,1∶2.0,1∶2.5,1∶3.0),缓慢滴加到上述澄清溶液中,溶液逐渐变浑浊,反应过程中,维持pH值在7左右(用稀H2SO4和NaOH溶液调节pH值),室温下搅拌30 min.将制得的混合溶液转移至水热反应釜中,控制温度为140℃,反应时长为12 h[11].反应完成后,待反应釜冷却至常温,收集所得到的黑色沉淀物.将其离心过滤,用蒸馏水洗涤2~3次,得到不同的MnOx产物.
1.2.2 MnOx@MABs材料的制备
将上述不同的MnOx产物加入到50 mL质量分数为2.5%的SA溶液中,于室温下持续搅拌2 h左右,得到混合均匀的液体.然后将该悬浮液用注射器逐滴加入到200 mL 1 mol·L-1的CaCl2溶液中,滴加完成后,持续搅拌12 h,使其继续凝胶化,制得MnOx@MABs.经蒸馏水清洗后的凝胶颗粒贮存于4℃冷柜中备用.
1.3 MnOx@MABs材料降解偶氮染料废水的实验方法
取200 mL 200 mg·L-1的日落黄溶液模拟偶氮染料废水,将其转移到250 mL的烧杯中,放到恒温磁力搅拌器中,加入一定量的MnOx@MABs材料和PMS,开始计时,每间隔10 min取少量日落黄溶液,利用滤膜分离杂质,加入微量Na2S2O3终止反应进行,测定日落黄的质量浓度.
1.4 日落黄溶液质量浓度的测定
根据日落黄在482 nm处有最大吸收波长,采用紫外分光光度法测定日落黄的吸光度.根据朗伯-比耳定律:吸光度与吸光物质的质量浓度成正比.在波长482 nm处绘制日落黄标准曲线,其降解率为:

其中,C0为日落黄初始质量浓度(mg·L-1);C为取样测定时的日落黄质量浓度(mg·L-1).
2 结果与讨论
2.1 MnSO4与NaClO的物质的量之比对日落黄降解的影响
在废水温度40℃、200 mL 200 mg·L-1日落黄和30 g·L-1MnOx@MABs的条件下,考察了MnOx材料制备过程中不同的MnSO4与NaClO的物质的量之比对MnOx@MABs材料影响,结果如图1所示.随着NaClO加入量的增加,日落黄降解效果逐渐提升,在MnSO4和NaClO物质的量之比n(MnSO4)∶n(NaClO)是1∶2.5时,呈现最佳降解效果;当MnSO4和NaClO物质的量之比是1∶3.0时,降解效果和1∶2.5相比没有明显提高.这是因为NaClO越多,锰元素的价态也会逐渐增加,并表现出多种价态MnOx混合的状态,不同价态之间的电子转移有利于产生更多的羟基自由基,从而降解日落黄;当NaClO的量继续扩大达到一定值时,锰元素的价态已经不能再进一步提高,无法产生更多的羟基自由基.所以选取最佳制备条件为n(MnSO4)∶n(NaClO)=1∶2.5.
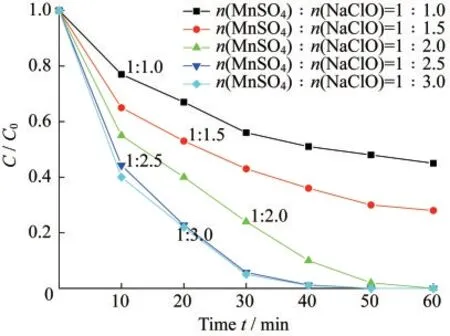
图1 不同MnSO4和NaClO物质的量之比下制备的MnOx@MABs降解日落黄效果
2.2 MnOx@MABs材料的表征
2.2.1 MnOx@MABs材料的FE-SEM分析
MnOx@MABs颗粒的表面形态可通过FE-SEM检测.从图2(a)可以看出,凝胶状态下的MnOx@MABs颗粒表面光滑,珠粒为黑色球形,直径约为2 mm,平均质量为55 mg.图2(b)为一个完整的MnOx@MABs颗粒,可以看出为球形结构,表面粗糙不平,有明显的褶皱.吸附剂表面的褶皱一方面是因为凝胶在干燥条件下脱去自由水分子产生的缩水效应;另外一方面是由于MnOx颗粒进入凝胶球引起分子间作用力的变化.图2(c)和2(d)表示颗粒局部表面放大和截面放大的FE-SEM照片,可以看出,MnOx颗粒已经成功并均匀地嵌入海藻酸凝胶微球颗粒表面/里面.从材料表面粗糙不平、有明显褶皱的表观形貌上来看,MnOx@MABs材料为日落黄的分解以及水分子在其表面的吸附等过程提供了有利的反应平台.
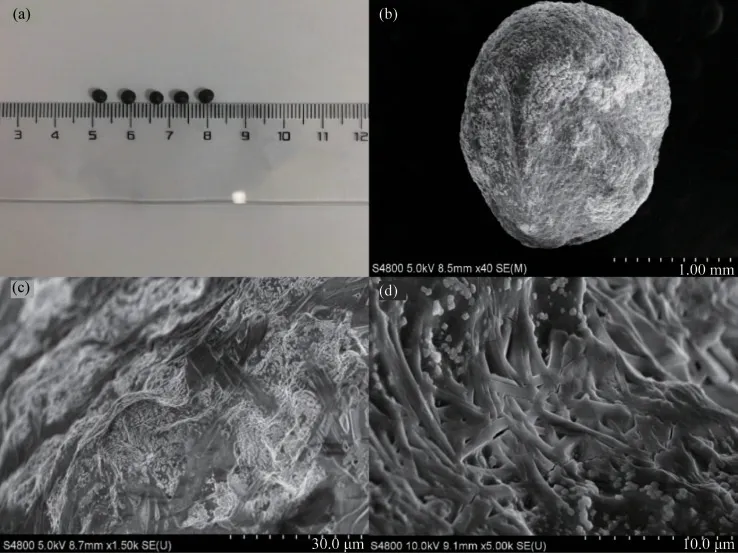
图2 MnOx@MABs凝胶微球的FE-SEM分析.(a)MnOx@MABs凝胶微球的照片;(b)干燥后的MnOx@MABs凝胶微球的FE-SEM图;(c)干燥后的MnOx@MABs表面放大的FE-SEM图;(d)MnOx@MABs凝胶微球截面图
2.2.2 MnOx@MABs材料的XRD分析
MnOx@MABs颗粒和MnOx的XRD谱图如图3所示.从图3中可以发现,MnOx和MnOx@MABs颗粒峰的位置是一致的,这表明MnOx@MABs颗的衍射峰是由MnOx产生的.MnOx在12.65°,17.84°,28.70°,37.50°,41.95°,49.89°和60.20°都出现较为明显的特征峰,证明MnOx@MABs颗粒中MnOx存在的形式主要是MnO2[12].
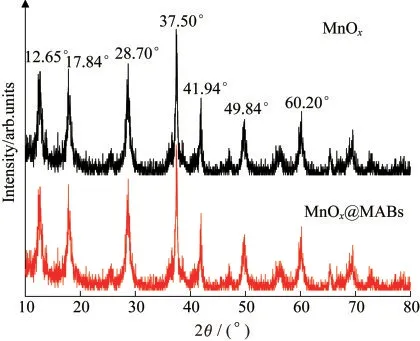
图3 MnOx@MABs颗粒和MnOx的XRD图
2.2.3 MnOx@MABs材料的FI-TR分析
MnOx@MABs颗粒的FT-IR光谱如图4所示.从图4可以看出,除载体和催化剂骨架组成吸收外,在3 432 cm-1附近出现了强而宽的羟基拉伸振动吸收带,这表示MnOx@MABs凝胶球的表面存有足够的羟基基团.此外,1 635 cm-1处的特征峰可能是由于SA分子上吸附—COOH而引起的振动吸收峰.而在1 077 cm-1附近出现的伸缩振动峰则是—CO的伸缩震动而引起的[13],Mn—O基团的吸收峰则位于574 cm-1附近[14].FT-IR表明MnOx成功地分散在了SA凝胶中.
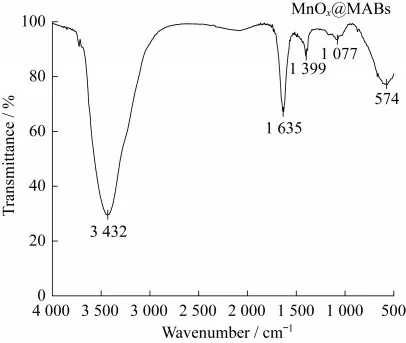
图4 MnOx@MABs颗粒的FT-IR图
2.3 MnOx@MABs材料氧化降解偶氮染料废水
2.3.1 MnOx@MABs用量对日落黄降解的影响
在废水温度40℃、200 mL 200 mg·L-1日落黄和0.5 mmol·L-1PMS的条件下,MnOx@MABs用量对于降解日落黄的影响如图5所示.随着凝胶球用量从0上升40 g·L-1时,日落黄的降解效果也在逐渐提升,这是因为MnOx@MABs用量越多,所能提供的活性位点也就越多,从而活化PMS产生大量的SO4-·,提高了日落黄的降解效果.从实验结果来看,当用量达到30 g·L-1时,日落黄的降解效果已经达到比较好的水平.从经济角度考虑,选择30 g·L-1的MnOx@MABs用量作为最佳用量.
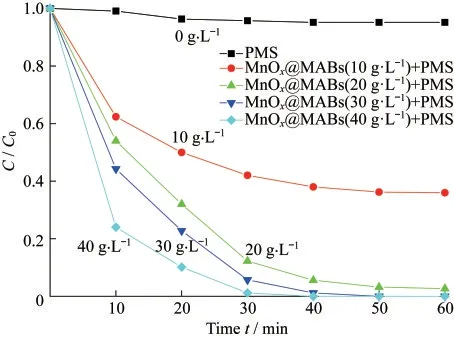
图5 MnOx@MABs用量降解日落黄效果
2.3.2 PMS用量对日落黄降解效果的影响
在废水温度40℃、200 mL 200 mg·L-1日落黄和30 g·L-1MnOx@MABs的条件下,PMS的用量对于降解日落黄废水效果的影响如图6所示.在不加PMS的情况下,单独的MnOx@MABs材料几乎对于日落黄没有任何作用;随着PMS用量的增加,越来越多的PMS分子与凝胶球表面活性位点进行反应,产生了大量的SO4-·,从而提高了日落黄的降解效果.当PMS的物质的量浓度进一步提升,从0.5 mmol·L-1提升至0.7 mmol·L-1时,虽然PMS用量提高了,但是对于日落黄的降解效果已经没有什么改变.这是因为当PMS的量在0.5 mmol·L-1时,吸附在MnOx@MABs材料表面的PMS分子数量已足够多,并趋于饱和,剩余的PMS只能以离子态的形式游离在溶液中,并没有参与到反应中来,从而限制了日落黄降解效果的继续提升.
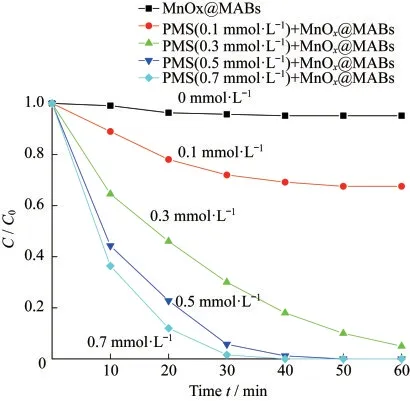
图6 PMS对日落黄降解效果的影响
2.3.3 废水温度对日落黄降解的影响
在200 mL 200 mg·L-1日落黄、30 g·L-1MnOx@MABs和0.5 mmol·L-1PMS的条件下,废水温度对于日落黄降解效果的影响如图7所示.随着废水温度的逐渐提高,日落黄的降解速率在明显提升,当温度升高到40℃时,降解时间大约在40 min左右时,日落黄降解率基本达到100%;而温度在20℃时,经过60 min的降解,其降解率也只能在55%.据文献记载[15-16],基于SO4-·的AOPs属于吸热反应.因此,温度的升高对于活化PMS是有利的,可以产生更多的SO4-·,提高日落黄的降解效率.
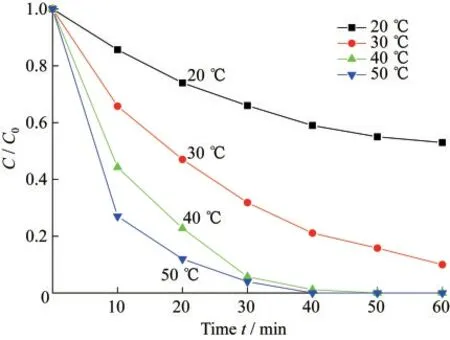
图7 废水温度对日落黄降解效果的影响
2.3.4 废水pH对日落黄降解效果的影响
在废水温度40℃、200 mL 200 mg·L-1日落黄、30 g·L-1MnOx@MABs和0.5 mmol·L-1PMS的条件下,废水的pH值对于日落黄降解效果的影响如图8所示.用稀H2SO4和NaOH溶液调节pH值,经过1 h的降解后,从实验结果可以看出,从酸性环境到碱性环境,MnOx@MABs材料对日落黄均有良好的降解效果.所以MnOx@MABs/PMS体系可以在广泛的pH值范围里降解日落黄,并达到良好的降解效果.
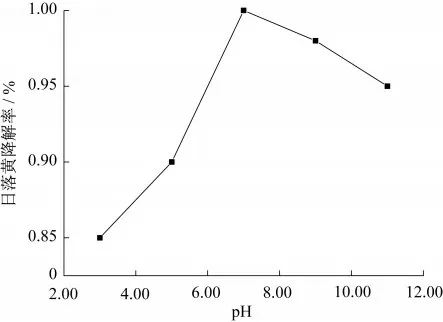
图8 废水pH值对于日落黄降解效果的影响
2.3.5 初始溶液的质量浓度对日落黄降解效果的影响
在废水温度40℃、200 mL 200 mg·L-1日落黄、30 g·L-1MnOx@MABs和0.5 mmol·L-1PMS的条件下,初始溶液的质量浓度对于日落黄降解效果的影响如图9所示.从图9中不难看出,当日落黄的质量浓度在100 mg·L-1和200 mg·L-1时,利用MnOx@MABs/PMS体系可以在1 h内将日落黄完全降解掉.随着日落黄初始的质量浓度从200 mg·L-1增加至600 mg·L-1,降解效果在逐渐减弱;当质量浓度在600 mg·L-1时,日落黄的降解率仅为27.3%.这是由于体系中日落黄的增加,但MnOx@MABs的量不足,不能有效提供足够多的活性位点来活化PMS,从而不能产生足够的自由基,导致日落黄无法降解完全.但是在日落黄初始质量浓度较高的情况下,可以通过增加MnOx@MABs的投入量和PMS的物质的量浓度来提高其降解率.
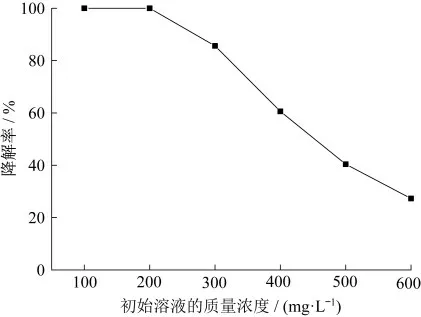
图9 初始溶液的质量浓度对日落黄降解效果的影响
3 结论
采用水热法制MnOx,在尚未烘干的情况下直接加入SA溶液,形成均匀的MnOx@SA凝胶体系,并将其加入到CaCl2溶液中,形成MnOx@MABs凝胶微球材料.将MnOx@MABs作为活化材料,构造MnOx@MABs/PMS体系,用于偶氮染料废水中日落黄的降解.采用FE-SEM、XRD和FT-IR等一系列的表征手段对MnOx@MABs形貌结构、组成成分等进行分析.此外,根据日落黄的降解效果,进一步分析MnOx@MABs材料的性能,得出如下结论:
1)将制备出的MnOx与SA结合,成功制备出符合预期的MnOx@MABs凝胶球材料,并用其来活化PMS,降解偶氮染料废水代表物日落黄.通过调节MnSO4和NaClO的物质的量之比,获得最佳的MnOx制备条件(n(MnSO4)∶n(NaClO)=1∶2.5),将制得的MnOx与SA结合,形成MnOx@MABs凝胶球后,其对降解日落黄效果良好.
2)降解实验表明:MnOx@MABs/PMS体系在酸性、中性、碱性条件下,均可对日落黄废水表现出良好的降解性能,在200 mL 200 mg·L-1的日落黄废水中加入30 g·L-1的MnOx@MABs凝胶球材料和0.5 mmol·L-1的PMS,40℃条件下搅拌60 min可完全降解日落黄.
3)MnOx@MABs材料具有良好的机械强度,且避免了过渡金属氧化物在降解过程中的聚集.同时,MnOx的相对含量、表面羟基在催化降解日落黄中都有作用.所以,MnOx@MABs/PMS体系催化降解日落黄的效果良好.
