超声造影应用于肝移植术后非血管性肝缺血/坏死的早期诊断研究
2022-11-07赵宁波谢晓娟赖宇婷李志艳
赵宁波,谢晓娟,赖宇婷,赵 东,李志艳
超声造影作为一种纯血池显像技术,可实时动态观察肝脏的血流状况,现已被广泛应用于评估肝移植围手术期肝脏血管通畅程度及肝实质灌注情况[1]。肝移植术后非血管性肝坏死是一种特殊的肝坏死类型[2],其表现为移植肝血管通畅,而肝实质表现为大片坏死灶,不明原因的肝功能急剧恶化,其发病隐匿,病情危重,亟需早期诊断。目前对于肝移植术后非血管性肝缺血/坏死的早期诊断多采用CT血管造影(CT angiography, CTA)进行,但肝移植术后早期患者病情较重不宜搬动至CT检查室,且CTA存在着放射线辐射及造影剂肾损伤等缺点。与之相比较,超声造影技术具有安全无辐射,并可在床边动态检查等优势。本研究通过对比分析9例肝移植术后非血管性肝缺血/坏死患者CTA与超声造影图象,证实超声造影可作为一种良好的肝移植术后非血管性肝缺血/坏死的早期诊断工具。
1 对象与方法
1.1 对象 将2017年7月—2021年3月在深圳市第三人民医院接受肝脏移植的9例患者做为研究对象,该组患者经CTA均显示移植肝血管正常增强,而肝实质的无增强(定义为移植肝的外围或中央区域出现无增强,累及范围大于1个肝段)。9例患者中男性8例,女性1例,平均年龄(42.18±17.46)岁。原发疾病中原发性肝癌2例,乙型肝炎肝硬化失代偿期4例,酒精性肝硬化失代偿期3例。术式中8例采用改良背驮术式,1例采用劈离术式。供肝来源全部为脑死亡供体。供受体血型相同8例,血型相容者1例。均采用肝动脉端端吻合。
1.2 仪器与检查方法 采用Mindray昆仑7超声诊断设备,彩色多普勒模式下采用SC6-2U腹部探头,频率(1.2~6.0 )MHz。造影模式下机械指数0.124。Mindray M9超声诊断设备,彩色多普勒模式下采用S5-1s腹部探头,频率(1.5~5.0)MHz,造影模式下机械指数0.067。
1.3 方法 患者均在术中及术后7 d内每日采用Mindray昆仑7超声诊断设备常规扫查移植肝及血管,术后7 d~1月间每3 d检查移植肝及血管,重点观察各血管的通畅性及实质回声分布。当无法观察到血流信号和频谱或肝功能指标急剧恶化时,立刻行超声造影。
超声造影:在彩色多普勒条件对Glisson系统全程走行进行确定,切换至造影模式,造影剂选用SonoVue(Bracco,意大利),抽取5 ml生理盐水注入瓶装冻干粉末内,震荡摇匀后制成混悬液,设备调节完成后,经颈内静脉或肘正中静脉团注声诺维混悬液2.4 ml,同时计时器和向后储存功能,随后5 ml生理盐水冲管,实时动态分段观察Glisson系统内部血管显影情况,并同时观察各血管旁的肝实质灌注情况,最后观察肝静脉显影情况。当第一次造影对血管显示不理想时,可在第一次造影5 min后进行第二次超声造影检查,肝动脉走行区仍未见造影剂充盈可诊断为肝动脉闭塞[3]。肝实质的缺血或坏死被定义为在移植肝的外围或中央区域的楔形,圆形或椭圆形或不规则形状的区域中低/无增强[4]。
2 结 果
2.1 二维超声表现 9例患者二维超声均可见大面积低回声区,范围大于1个肝段,但未累及全部肝脏。回声区内部分布不均匀,边界模糊。以患者5为例,见图1。
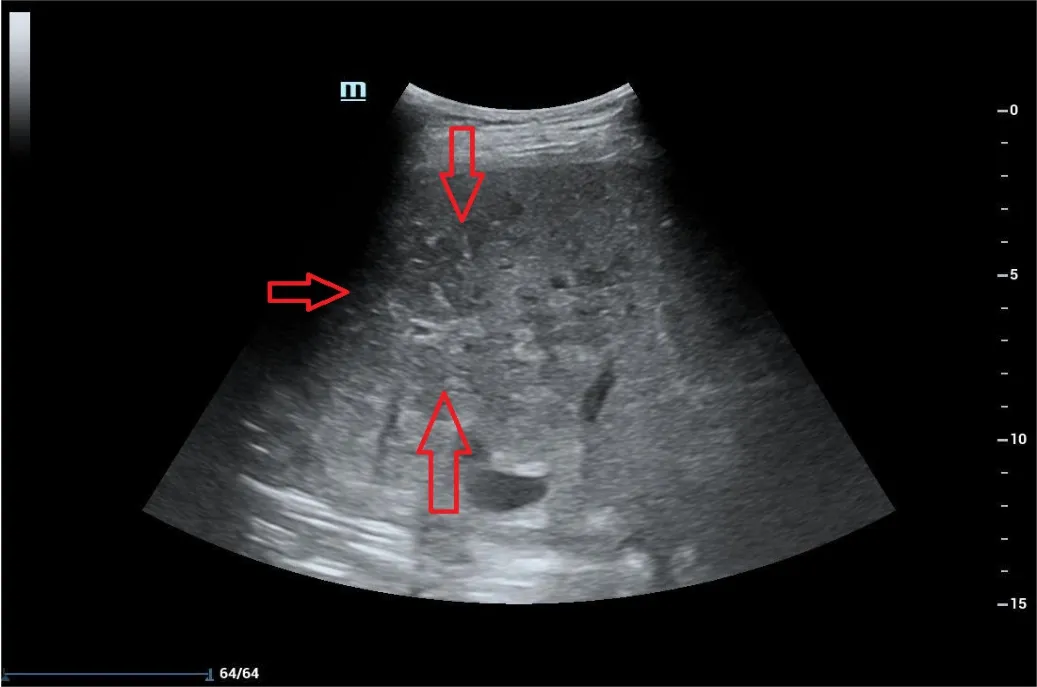
图1 非血管性肝坏死常规二维超声表现S5,S6,S7,S8段区域回声减低Figure 1 Conventional ultrasound findings of non-vascular liver necrosis
2.2 彩色多普勒表现 彩色多普勒及频谱多普勒提示各血管均可见血流及频谱信号,流速正常,但7例患者出现相应肝段肝内动脉阻力指数减低(<0.5),但收缩期加速时间均未见延长(<80 ms)。以患者5为例,见图2所示。

图2 非血管性肝坏死彩色多普勒表现A.右肝动脉血流通畅,血流速度正常,肝内动脉阻力指数减低(<0.5);B.门静脉右支血流通畅,血流速度正常Figure 2 Color Doppler findings of non-vascular liver necrosis
2.3 超声造影表现 超声造影提示肝动脉、门静脉和肝静脉均全程正常增强,低回声区三期均未见增强,但其内仍然可见正常血管走行,低回声区内部增强的血管呈“枯树枝样”特征,与CTA影像特征一致。以患者5为例,见图3。
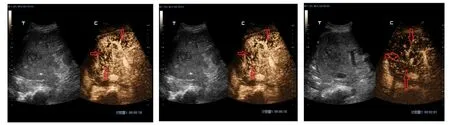
图3 非血管性肝坏死超声造影表现超声造影,肝动脉、门静脉和肝静脉均全程正常增强,低回声区三期均未见增强,但其内仍然可见正常血管走行,低回声区内部的增强的血管呈“枯树枝样”特征(红色粗箭头所示)Figure 3 Contrast-enhanced ultrasonography of non-vascular liver necrosis
2.4 CTA表现 9例患者CTA示移植肝血管起源及走行未见异常。但可见移植肝大片状低密度区三期无强化,范围大于1个肝段,其内仍可见肝动脉及门静脉走行。以患者5为例,见图4。
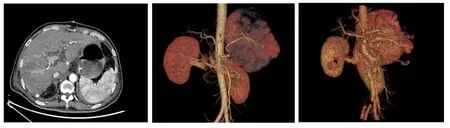
图4 非血管性肝坏死CTA表现患者5的移植肝大片状低密度区无强化(红色粗箭头所示),但其内可见肝动脉及门静脉走行Figure 4 CTA findings of non-vascular liver necrosis
2.5 9例患者具体超声造影资料及临床预后 9例非血管性肝坏死患者中,3例患者术后发生失血性休克;1例患者术后发生感染性休克;1例患者供肝为边缘线供肝;1例患者因供肝体积过大(边缘线供肝)在术后1周行移植肝部分减体积术;1例患者在术中发生心脏骤停;另2例患者术中及术后未见明显异常改变(表1)。
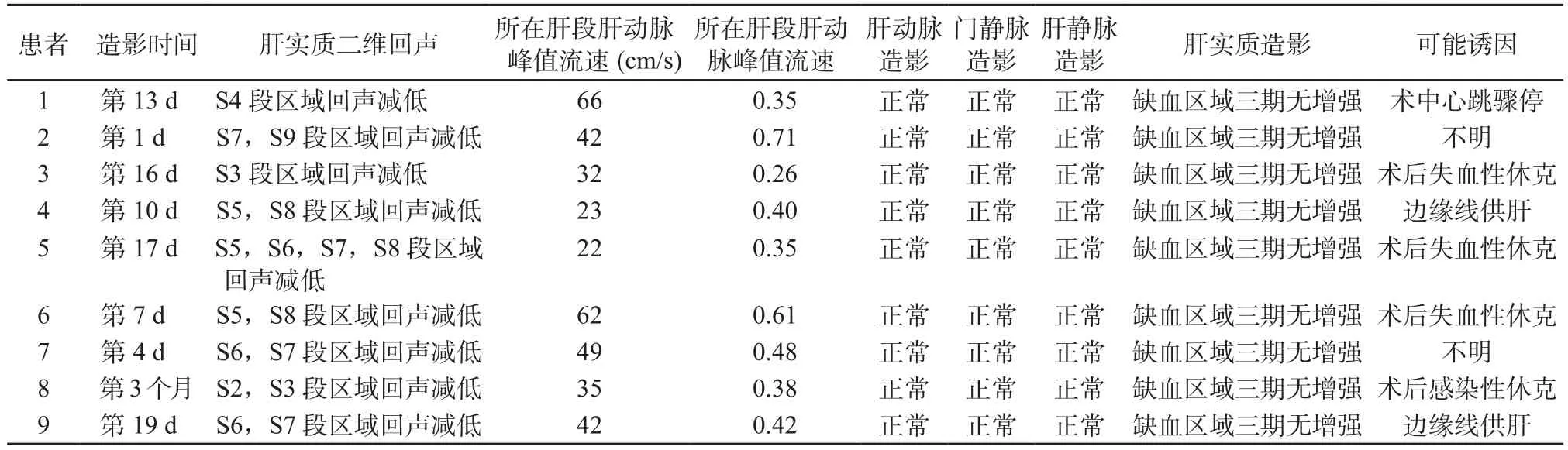
表1 9例患者超声造影资料Table 1 Contrast enhanced ultrasound data of 9 patients
9例患者氨基转移酶及凝血功能指标峰值出现在超声造影前1~3 d,且呈进展趋势。以患者5为例,术后19 d的氨基转移酶及凝血功能趋势见图5~6,提示该患者氨基转移酶及凝血功能在手术当天及超声造影前2 d出现明显波动,超声造影前出现“胆酶分离”现象。9例患者中4例在血浆置换等护肝治疗后肝功能转为正常,其余5例因急性肝功能衰竭死亡。

图5 患者5肝功能指标趋势图Figure 5 Trend chart of liver function indicators of patient 5
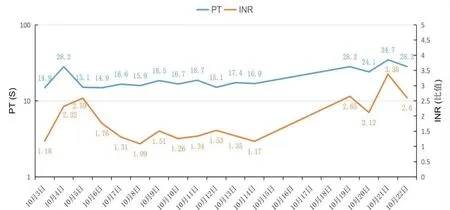
图6 患者5凝血功能指标趋势图Figure 6 Trend chart of coagulation function indexes of patient 5
3 讨 论
肝移植术后非血管性肝缺血/坏死是肝移植术后少见的并发症之一,其发生机制是移植肝实质严重损害导致。肝细胞坏死的原因可能是局部缺血[5]、ABO血型不兼容[6]、病毒或其他原因导致的肝炎[7-8]、严重感染[8-9]、心脏死亡后捐献供肝[2]等。影像学表现为移植肝血管通畅,而肝实质表现为大片坏死灶。临床表现为不明原因的肝功能急剧恶化,氨基转移酶指标呈直线上升。因其多发生于术后早期,部分患者被误诊为移植肝原发性无功能。该并发症早期可通过减轻肝损伤程度和预防继发感染等治疗方案取得良好效果。目前对于该并发症的诊断依赖于CTA,但是肝移植术后早期患者病情较重不宜搬动至CT检查室,且CTA存在着放射线辐射及造影剂肾损伤等缺点限制了其在肝移植的广泛应用。超声因其便携及无损伤等优势已成为肝移植围手术期患者检查的首选。
常规超声能提示血管是否通畅,但对肝实质的灌注状况无法评估。超声造影利用六氟化硫微泡作为对比剂来增强血液的反射信号,提高了对血流信号检测的敏感性。武红涛等[10]认为超声造影诊断血管栓塞的准确性甚至优于增强CT,其成像效果类似数字减影血管造影,可直观并动态观察血管的走行及其通畅性。另有研究证实,超声造影可定量分析肝脏缺血-再灌注损伤后的微循环障碍状况[11]。肝实质的低增强是肝脏缺血的超声造影特征,而无增强则是肝脏坏死的表现[12],且肝脏损伤程度与增强程度呈负相关[13]。超声造影在诊断移植肝大血管和微循环小血管方面是具有一定优势,本研究的中未见血管闭塞病例,移植肝所有血管走形正常。坏死区域以外的肝实质呈均匀一致性增强,与CTA结果一致,这表明超声造影可以鉴别正常肝实质及血管。
本组9例患者中,二维超声均可见大面积肝脏回声减低,累及范围超过1个肝段,最严重的整个肝右叶回声均减低。彩色多普勒可完整探及各血管的血流信号及频谱,7例患者出现相应肝段肝内动脉阻力指数减低。肝脏缺血再灌注损伤可导致大量自由基等有害物质产生[14],肝内小动脉内皮细胞对此类有害物质比较敏感,可使肝内小动脉发生适应性扩张。频谱多普勒表现为阻力指数减低,这种缺血导致肝内动脉的阻力指数减低与肝外动脉狭窄导致的阻力指数减低有着不同的诱因。肝脏坏死的超声特征是周围楔形或圆形低回声区域或中心圆形低回声区域。低回声区内部见树枝状等回声带,这种树枝状等回声带可能是该区域格雷森系统的界面反射所致[15]。树枝状等回声带在超声造影和CTA上表现为增强的血管,而肝脏坏死的低回声区则表现为三期无增强
该表现表明虽然肝实质发生了坏死,供应该区域的血管却是通畅的,进一步证实了该并发症并非由血管因素导致,我们在5例患者的可能诱因中发现,这些患者均有过不同类型的休克打击,休克后肝脏的缺血再灌注损伤可能是导致肝脏坏死的原因[16-17]。这与先前报道的非血管性性肝坏死的CT表现一致[17],本研究首次尝试应用超声造影诊断该疾病并取得良好效果,国内外暂无超声造影在此类疾病中应用的报道[18-21]。
综上所述,本研究中9例患者的超声造影图像特征,均为移植肝血管无异常,大面积肝实质三期却无增强的情况,与CTA表现完全一致,可见其对肝移植术后非血管性肝坏死患者同样具有诊断价值。并且相比于CTA,超声造影具有无辐射及造影剂肾损害等优点,更具有可在床旁动态观察的不可替代的优势。
