四丁基溴化铵-二氧化碳体系中不同结构水合物生成条件测量与模型预测研究
2022-11-04丁宇荣少杰刘青松
*丁宇 荣少杰 刘青松
(中油(新疆)石油工程有限公司设计分公司 新疆 834099)
水合物技术是一种高效、环保捕集、封存二氧化碳(CO2)的一体化技术[1-2]。在一定低温和高压条件下,CO2吸附于由水分子在氢键作用下形成的笼型结构中,实现CO2的捕集与封存[3]。当前水合物生成压力较高限制了水合物的应用与发展,但低毒性、不挥发的阴离子表面活性剂-四丁基溴化铵(TBAB)的开发有效解决了这一问题[4]。
有效生成水合物是水合物法CO2捕集与封存一体化技术的实施前提,必须掌握不同条件下TBAB-CO2水合物临界生成条件,这是制定捕集、封存工艺的基础[5]。通过实验明确TBAB-CO2生成条件,并建立合适的预测模型是实现这一技术工业化的前提。但由于TBAB-CO2有A型(TBAB·26H2O)和B型(TBAB·38H2O)两种结构,两种结构水合物生成热力学条件明显不同,且两种结构水合物生成的相对难易程度会随条件变化而逆转,这使得TBAB-CO2的临界生成压力预测十分困难,难以采用现有技术将多种结构水合物模糊处理成一种结构水合物的方式来解决[6-7]。
本文针对水合物法CO2捕集过程中的强化问题,通过实验研究了含TBAB体系CO2水合物的生成条件,明确TBAB对CO2水合物的强化及促进作用。在试验结果的基础上,将A型和B型两种结构水合物分开计算,根据对A型和B型水合物的计算结果,选取既定条件下更容易生成的结构型的生成条件为体系生成条件,从而将模型进一步贴合于实际,实现了预测准确性的提升。经过本文的研究掌握了TBAB-CO2体系水合物生成条件,定性分析了不同条件下A、B双构型转换和分布规律,为实现水合物法CO2捕集与封存一体化工业应用打下了基础。
1.试验与模型
(1)试验试剂
二氧化碳(CO2),x(CO2)=99.9%,北京永圣气体科技有限公司;四丁基溴化铵(TBAB),ω(TBAB)=99.0%,天津光复精细化工研究所;去离子水,15×106Ω·cm,实验室自制。
(2)试验仪器
活塞式高压反应釜(耐压25MPa,不锈钢,磁力搅拌)海安拓新科研仪器有限公司;手摇泵(调节反应釜内气体压力,刻度范围0~230ml)、空气浴(调节反应釜内温度,控温范围-20℃~50℃,控温精度±0.1℃),海安拓新科研仪器有限公司;温度传感器(Pt100,测温精度±0.1℃),上海实验仪器厂有限公司;压力传感器(0~20MPa,测量精度±0.01MPa),上海实验仪器厂有限公司;电子天平(LQA5003),上海瑶新电子科技有限公司。
(3)热力学实验方法
本实验采用“恒温压力搜索法”测量水合物生成条件,该方法为水合物热力学测量的通用方法。将100ml按照配方量配制所需浓度的实验溶液加入清洗干净的反应釜中。使用CO2气体吹扫反应釜和管线充分置换空气后,向反应釜内通入一定压力的CO2气体。启动空气浴,控制反应温度至指定实验温度,待温度恒定时,启动磁力搅拌并维持实验过程中搅拌速度恒定。通过手摇泵调节反应釜内压力,使反应釜内生成痕量水合物颗粒,并维持4h稳定。则此时的压力即为当前温度条件下的水合物生成压力。改变实验温度、溶液等条件,测定不同实验条件下的水合物生成条件。
(4)热力学模型
本文基于Chen-Guo水合物模型[8-9],结合TBAB水合物构型转换现象,以化学位判据建立了TBAB-CO2水合物生成预测改进模型。根据Chen-Guo水合物模型的描述,首先生成基础水合物,基础水合物不断生长形成联结孔,然后发生气体分子CO2的吸附过程,CO2分子填充于联结孔中,降低水合物化学位能,提高结构稳定性。以化学位能差△μ为判据,<0表示可生成水合物,>0表示不能生成水合物且水合物出现解离,△μ计算式如方程式(1)所示[10-11]。
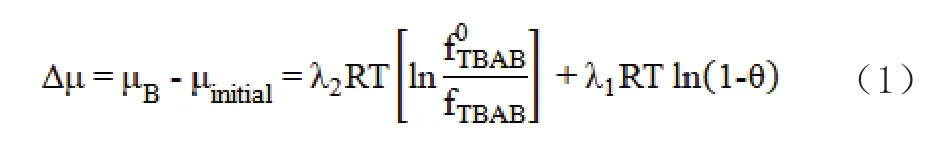
式中,μinitial、μB分别为体系生成水合物前后的化学位能;λ1、λ2分别为联结孔数、气体分子数与水分子数比;R、T分别为通用气体常数、实验温度;fTBAB0、fTBAB分别为TBAB在基础水合物、实验条件下的逸度。fTBAB0由方程式(2)计算:
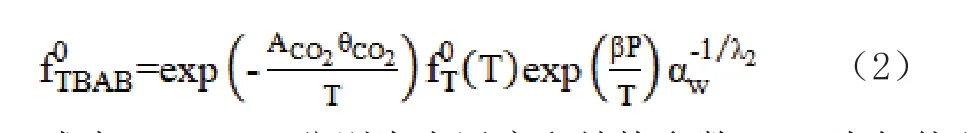
式中,αw、β分别为水活度和结构参数;ACO2为气体分子吸附过程中联结孔CO2分子间相互作用参数。本模型考虑TBAB水合物A、B结构构型转换问题,对ACO2与TBAB浓度进行关联,其中ωTBAB为TBAB质量分数。
TBAB A型水合物关联式如方程式(3)所示:
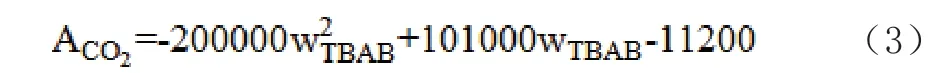
TBAB B型水合物关联式如方程式(4)所示:

2.结果与讨论
(1)TBAB-CO2水合物生成条件。实验测定了7~11℃范围内,不同浓度TBAB溶液(ω(TBAB)=5%,10%,15%,20%,25%)中CO2水合物的生成条件,结果如图1所示,整体趋势为水合物生成压力与温度呈正相关。相比于纯水体系,在相同温度下TBAB溶液中CO2水合物的生成压力明显降低。根据文献[12-13]报道,TBAB在常压下就可生成水合物,阴离子取代一个水分子在氢键作用下与其他水分子形成笼型结构,阳离子占据水合物晶体的大孔穴,气体分子则填充于小孔穴[12-13]。因此TBAB的热力学促进作用已被证实。TBAB的存在可有效促进CO2水合物的生成,降低CO2水合物的生成条件。10℃时,ω(TBAB)=5%溶液中CO2水合物生成压力降低2.74MPa,降幅达63.7%;ω(TBAB)=20%溶液中,生成压力降低4.12MPa,接近常压,降幅达95.8%,这为实现水合物法CO2捕集与封存技术的工业化应用提供了可能。水合物生成压力降低幅度与TBAB浓度呈正相关,浓度越高,促进作用越强。
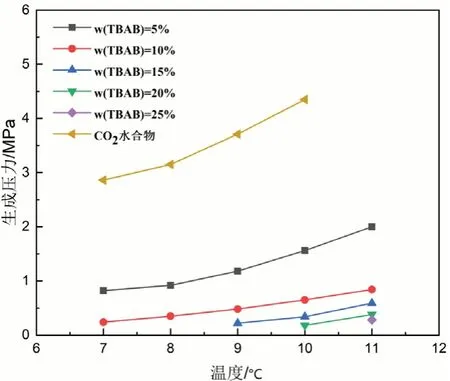
图1 TBAB-CO2体系水合物生成条件
(2)TBAB-CO2水合物热力学模型。表1为采用TBAB A型水合物模型计算所得不同TBAB浓度及不同温度条件下的CO2水合物生成压力。将计算值与实验值对比,可以发现在浓度为ω(TBAB)=5%、10%的溶液中,CO2水合物的生成压力模型预测值经过迭代计算均超过10MPa,远远大于实验值,同时ω(TBAB)=15%的溶液中,CO2水合物的生成压力预测值也远大于实验值。这表明ω(TBAB)=5%、10%、15%的溶液体系中无A型水合物的生成,在ω(TBAB)=20%、25%的溶液中,CO2水合物的模型预测值与实验值基本一致,绝对偏差在0.001MPa,由此表明该体系生成的为A型水合物。
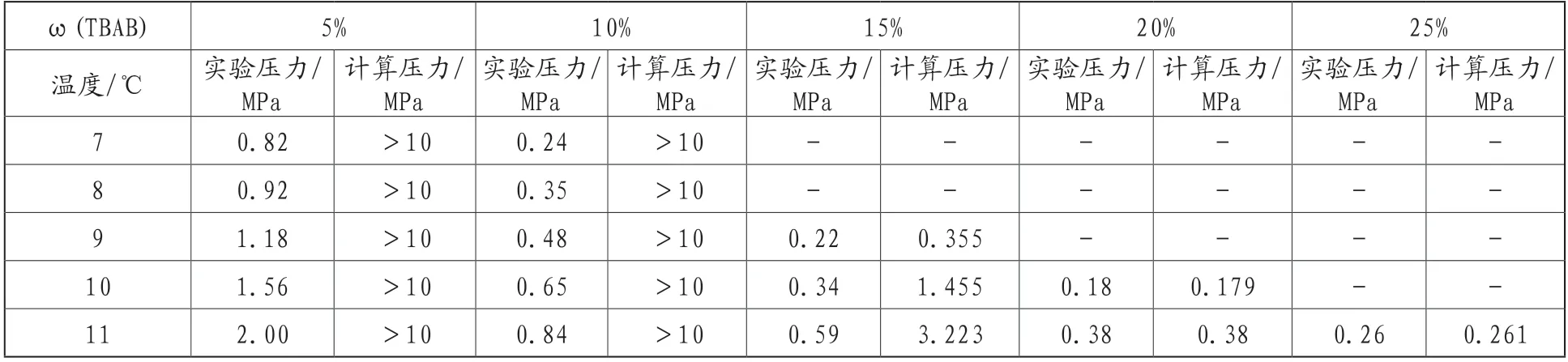
表1 A型水合物生成压力实验值与计算结果
表2为采用TBAB B型水合物模型计算所得不同TBAB浓度及不同温度条件下的CO2水合物生成压力。同样对比计算值及实验值可以发现,ω(TBAB)=5%、10%、15%的溶液中,相同温度下,CO2水合物生成压力预测值与实验值基本一致。这表明在此条件下生成的水合物为B型。同时从表中可知,针对ω(TBAB)=20%、25%的溶液体系,模型预测值与实验值也基本吻合,这表明在该浓度下同样可以生成B型号水合物,但在此两种浓度条件下,以B型水合物模型计算的预测值精度要低于以A型水合物模型计算的预测值。
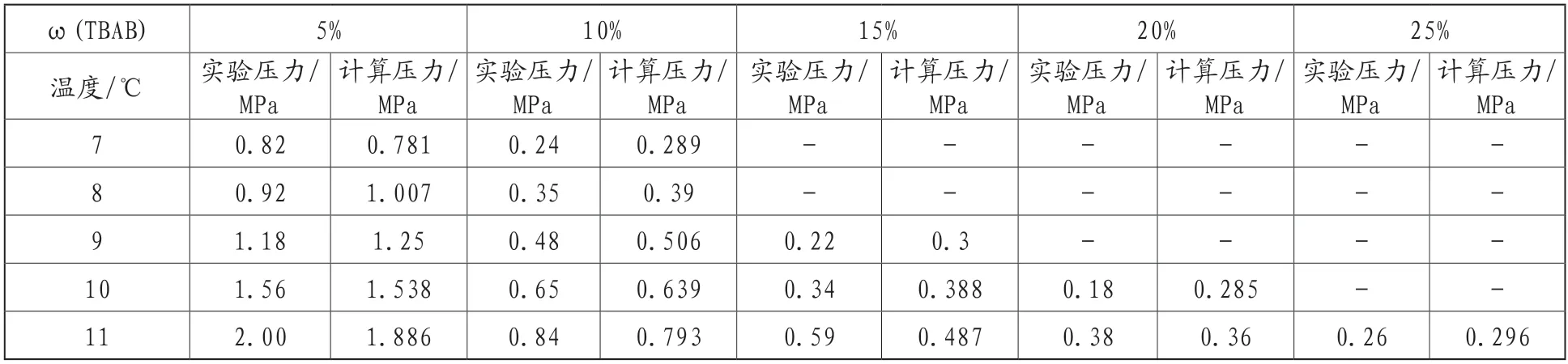
表2 B型水合物生成压力实验值与计算结果
依据模型预测值与实验值接近原则,ω(TBAB)=5%、10%、15%的溶液体系CO2水合物的生成压力预测值选择以B型水合物模型的计算结果,同时ω(TBAB)=20%、25%的溶液体系CO2水合物的生成压力预测值选择以A型水合物模型的计算结果。通过分析可以明确不同浓度的TBAB溶液体系A型和B型水合物构型转变和分布情况,在低浓度时B型水合物是体系中的主要构型,当浓度较高时A型水合物将会出现,A型和B型水合物共生共存。从表3数据可知,模型具有较高的精度,预测值与实验值的绝对误差在0.1MPa以内。
3.结论
水合物CO2捕集与封存一体化技术具有高效、环保的特点,针对该技术中热力学促进剂TBAB的应用及存在A、B构型转变、TBAB-CO2体系模型预测困难的问题,本文通过研究得以有效解决以上问题,并得出以下结论:
(1)本研究实验测定了TBAB-CO2水合物体系的相平衡数据,TBAB可有效降低CO2水合物的生成条件,促进CO2水合物的生成,并且促进作用随着TBAB浓度的增加而增强。
(2)建立了考虑TBAB构型转换的热力学模型,通过定性分析模型计算数据,在ω(TBAB)=5%、10%、15%的溶液体系中,优先生成B型水合物,无A型水合物的存在。而ω(TBAB)=20%、25%的溶液体系中,A型和B型水合物将共同存在。模型预测值与实验值的绝对误差在0.1MPa以内,模型具有较高的精度。为水合物CO2捕集与封存一体化技术奠定基础。
