可见光响应的MoS2纳米花及其光催化性能研究
2022-11-04许相花林正宇赵宇王圣康邵宗涵柴希娟
*许相花 林正宇 赵宇 王圣康 邵宗涵 柴希娟
(西南林业大学云南省木材胶黏剂及胶合制品重点实验室 云南 650224)
在倡导协调发展、绿色发展的今天,半导体多相光技术以其反应条件温和、廉价高效、有机物矿化程度高等优点[1],在处理有机污染物和净水方面发挥着越来越重要的作用。近年来,层状二硫化钼(MoS2)以其独特的二维层状石墨烯结构、优异的可见光吸收能力和较高的反应活性等优点,迅速成为催化领域的研究热点[2]。然而,MoS2的不规则团聚常导致其暴露在外的活性边缘位点较少且导电性能差,故催化性能较差[3]。因此,需要寻找一种有效的途径来优化MoS2的催化活性。
过渡金属掺杂被认为是提高MoS2光电催化性能的有效途径。这是因为,过渡元素掺杂能调整MoS2的电子结构,优化Mo和S的电子密度,从而增加电导率和新的活性中心[4-5]。Xiong等[4]制备了Co掺杂MoS2。结果表明,适量Co掺杂可有效调控MoS2的电子结构,提高其本征电导率,降低MoS2的氢吸附自由能,获得高HER。有效提高其本征电导率,降低MoS2的氢吸附自由能,获得优异的析氢反应活性。Ge等[5]采用单原子Ru和Ni共修饰MoS2。研究发现,Ru和Ni的共掺杂协同作用有效降低了MoS2分解水步骤的中间能垒。Nguyen等[6]采用Co和Nb双掺杂的策略改变了MoS2的电子结构,极大提高了其析氢反应、析氧反应和氧化还原性能。然而,以上研究多采用过渡元素掺杂MoS2进行分解水的研究,用于降解罗丹明B的研究较少。本研究采用一步法制备Co掺杂MoS2,用于降解罗丹明B(RhB),研究Co掺杂量对MoS2光催化性能的影响。
1.实验部分
分别称取1mmol钼酸钠、33mmol硫脲和一定量的六水合硝酸钴,先后溶解于30mL的去离子水中,搅拌均匀后将混合液倒入高压反应釜中,调控反应温度为220℃,反应时间为18h。反应结束后等待反应溶液自然冷却至室温,然后分别用无水乙醇和蒸馏水洗涤产物数次,离心过滤后将产物置于60℃的真空干燥箱中6h,得黑色粉末。按Co掺杂量(0mmol、2.5mmol、3mmol、3.5mmol)分别将样品标记为MoS2、MoS2-2.5Co、MoS2-3.0Co、MoS2-3.5Co。
以350W氙灯为辐照光源。将0.05g样品超声分散在100mL质量浓度为10mg/L的RhB溶液中,于黑暗条件下剧烈搅拌10min,达到吸附解吸平衡后打开氙灯进行光催化反应。每隔15min,抽取3ml上清液,于554nm处测定吸光度。
2.结果与讨论
图1为纯MoS2和不同钴掺杂量MoS2的XRD图谱。如图所示,所有样品在2θ为14.03°、33.39°、39.50°、58.84°附近均出现了衍射峰,与2H型MoS2的标准卡片上(JCPDS 37-1492)的衍射峰位置基本一致,分别对应(002)(100)(103)(110)晶面[6]。纯MoS2图谱中无杂质峰、对应(002)晶面的衍射峰突出且尖锐,表明样品的纯度较高。掺Co后样品的衍射峰强度均出现不同程度的衰减,这说明Co离子掺杂阻碍了层状MoS2内部晶相的形成。在XRD图谱中没有观察到Co的衍射峰,这是由于掺杂量较低的原因。
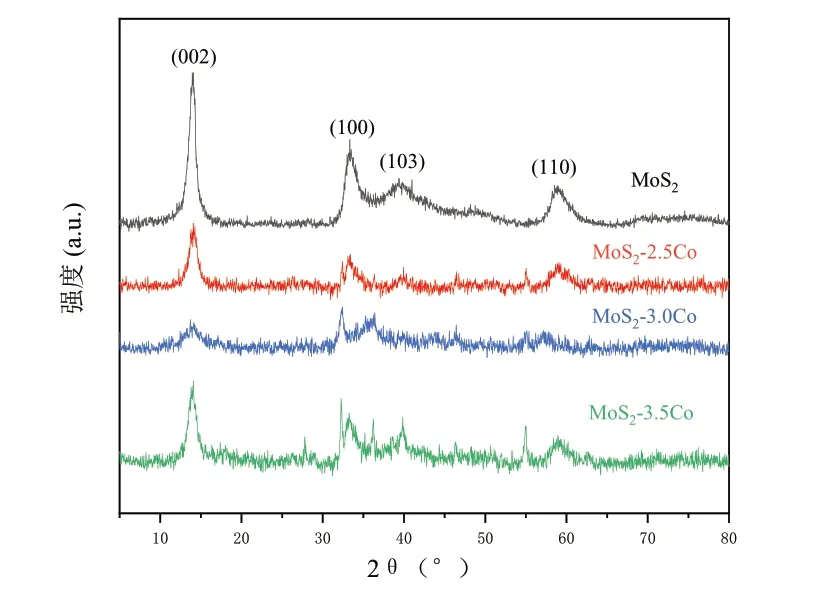
图1 纯MoS2和不同Co掺杂量MoS2样品的XRD图谱
MoS2的SEM(a)及MoS2-3.0Co的SEM(b)、TEM(c)及EDS(d)图像如图2所示。从图2(a)可知,MoS2具有纳米花结构,单个纳米花约为20μm,大小均匀,分散性好。由内插图可知,MoS2纳米花由弯曲纳米片组成。掺Co后,MoS2-3.0Co(图2b)仍保持纳米花结构,但尺寸明显减小,约为2μm。纳米花尺寸减少有利于提高样品的比表面积及活性边缘位点数量,进而提高样品的光催化活性。MoS2-3.0Co的TEM图像(图2c)显示,MoS2呈现相互交叉的层状结构。EDS元素映射图像(图2d)证实,Mo、Co和S元素均匀分布,进一步表明MoS2掺杂了Co。

图2 MoS2的SEM(a)及MoS2-3.0Co的SEM(b)、TEM(c)及EDS(d)
图3(a)为MoS2及掺杂样品的N2吸附-脱附等温曲线。由图可知,所有样品的吸附-脱附曲线等温线均为Ⅳ型曲线和H3型滞后环。曲线在低压端偏X轴,且相对平缓,说明材料与氮气具有较弱的作用力;中压段谱线缓慢抬升,高压段提升明显,说明材料中存在大量孔结构。细长的H3型滞后环表明,样品孔隙多为层状结构引起的狭缝孔。图3(b)显示,所有样品均存在丰富的介孔,掺杂Co后MoS2的最可几孔径变小,孔容增加。这是由于掺杂Co后MoS2的花状微球尺寸减小所致。
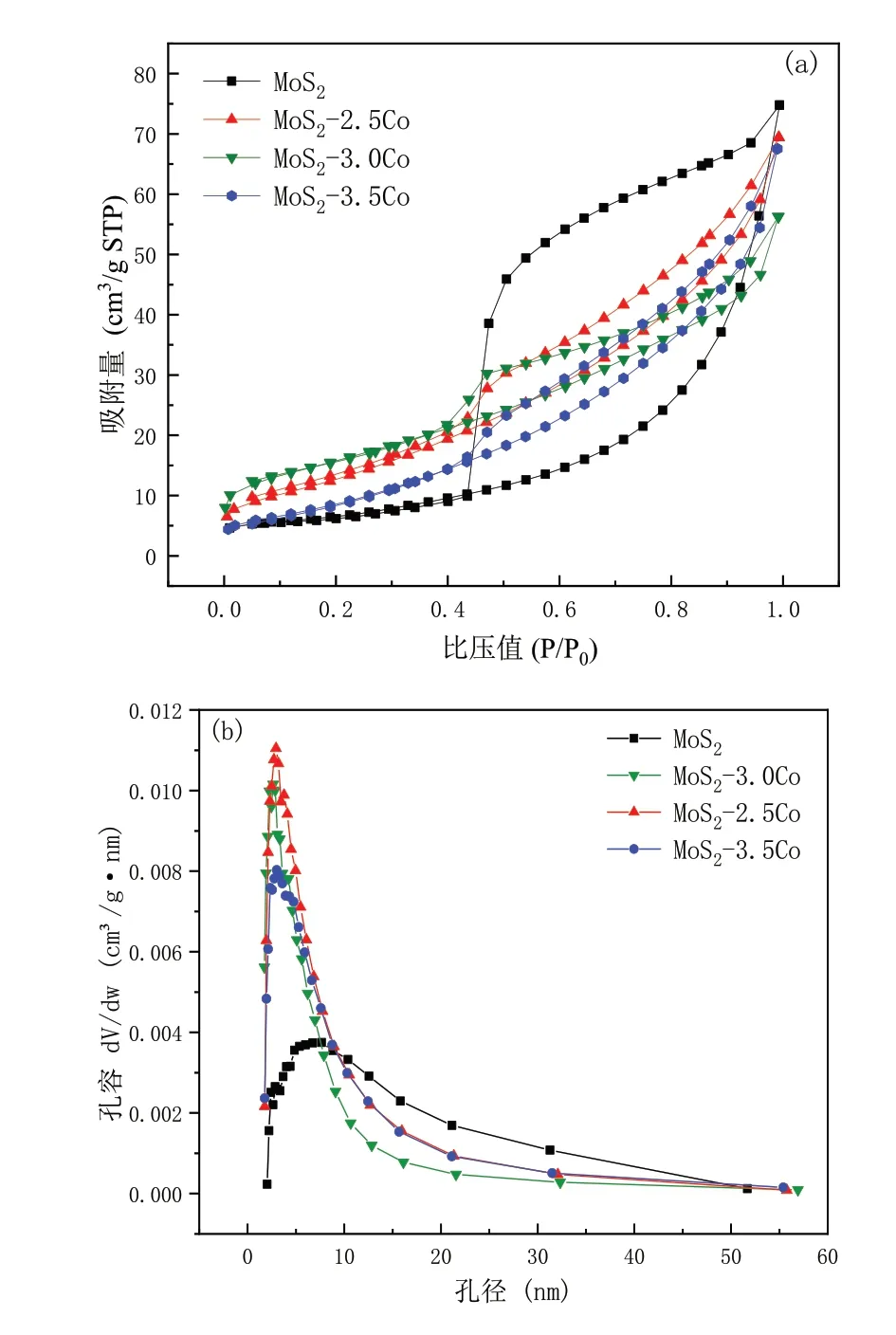
图3 二硫化钼及掺杂样品的N2吸附-脱附等温曲线(a)和孔径分布曲线(b)
BET显示纯MoS2的比表面积为23.7970m²/g,掺杂Co样品的比表面积均有提高。其中,MoS2-3.0Co的比表面积最大,为MoS2比表面积的2.41倍。较大的比表面积在光催化降解过程中可以提供更多的活性位点。
图4(a)为纯MoS2及MoS2-3.0Co的紫外-可见光谱。两个样品在可见光区均显示出较高的吸收强度。掺杂Co后,MoS2-3.0Co在350~800nm的吸收峰增强。图4(b)是在激发光波长为390nm下测得样品的荧光光谱。两个样品均在463nm处具有最强的荧光强度。但MoS2-3.0Co的强度明显低于MoS2。说明Co掺杂提高了样品光生电子和空穴的分离效率。
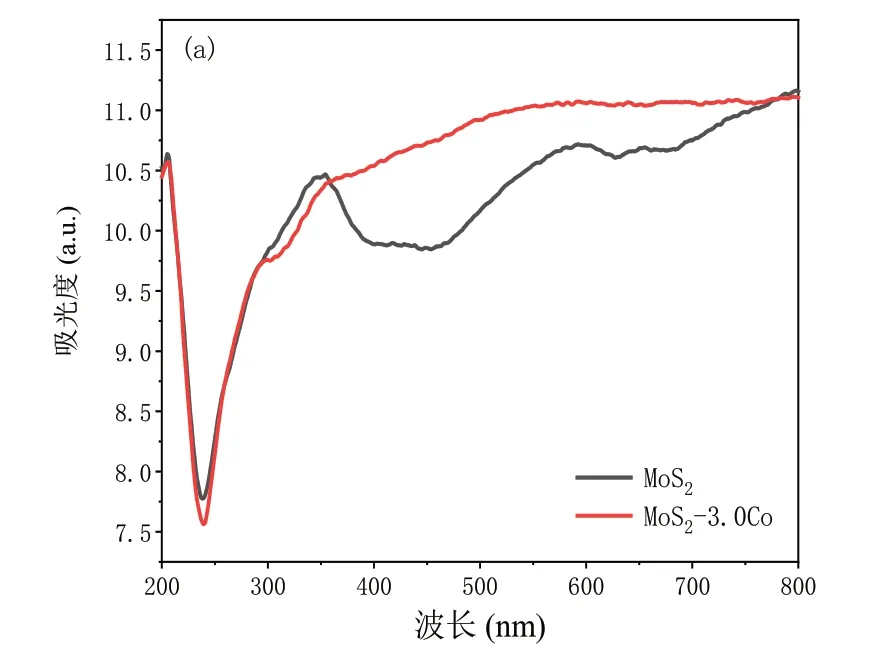
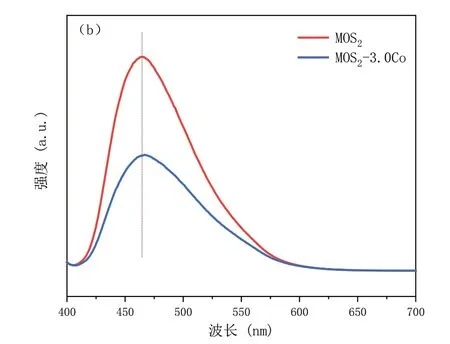
图4 样品的紫外-可见吸收光谱(a)和PL光谱(b)

表1 样品的比表面积和孔结构
图5为纯MoS2及不同Co掺杂样品的光催化降解曲线(a)和一级反应动力学曲线(b)。从图5(a)可以看出,所有掺杂Co的样品对RhB的降解率都高于纯MoS2。其中,MoS2-3.0Co的降解率最高约为97.8%,其一级反应动力学k为纯MoS2的4.46倍。这是因为MoS2-3.0Co具有较高比表面积及更多暴露在外的活性边缘位点的缘故。
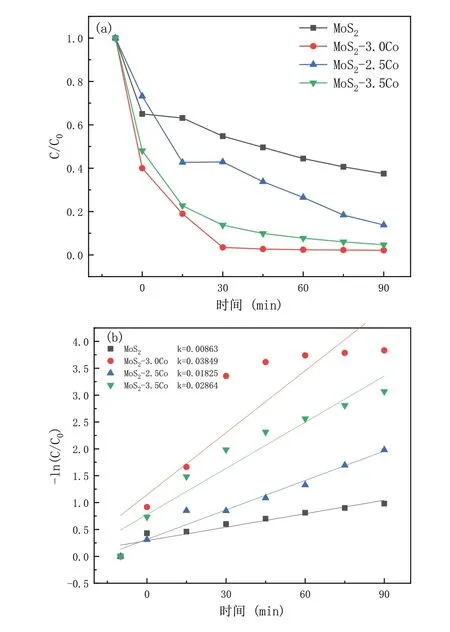
图5 各样品的光催化降解曲线(a)和一级反应动力学曲线(b)
3.结论
(1)采用水热法制备了具有优异光催化性能的MoS2纳米花。SEM分析表明,掺杂Co有利于减小单个纳米花的尺寸。
(2)掺杂Co能显著提高MoS2的光催化性能,MoS2-3.0Co光催化活性最优,其一级反应动力学k为纯MoS2的4.46倍。
(3)光学特性研究显示,掺杂Co有利于提高MoS2对可见光的吸收强度及光生载流子的分离效率。
