白癜风易感基因单核苷酸多态性研究进展
2022-11-03苗钰,张峰
苗 钰,张 峰
哈尔滨医科大学附属第一医院皮肤性病科,哈尔滨 150001
白癜风是一种多基因的色素脱失性疾病,以皮肤和黏膜上的白色斑片为特征。白癜风在世界各地流行,患病人数达世界人口的0.5%~1%。关于其病因与发病机制有许多假说,涉及遗传、自身免疫、细胞凋亡、黑素细胞异常、氧化应激等,其中遗传因素占重要地位[1-2]。已有的研究提示许多易感基因的存在可能对白癜风的发病产生重要的影响。本文对近年关于白癜风易感基因单核苷酸多态性(single nucleotide polymorphism,SNP)的研究进行综述,为明确白癜风的病因提供新思路。
白癜风易感基因的鉴别方法初起是候选基因法,通过检测与疾病表型相关的基因,对病例、对照组等位基因频率进行简单比较。基于此方法至少鉴别出33种不同的白癜风候选基因[3],如主要组织相容性复合体、蛋白酪氨酸磷酸酶非受体型22、血管紧张素转换酶、雌激素受体1、过氧化氢酶、细胞毒性T淋巴细胞抗原4等[4],但由于种族差异、人群分层、多重测试校正不足等因素,部分候选基因的关联尚未得到后续研究的证实,可能是假阳性结果。因此科学家提出了一种新方法,即全基因组关联分析研究(genome wide association study,GWAS)。与候选基因方法不同的是,GWAS可用于鉴定复杂性状的易感基因,控制人群分层,并进行多重测试校正,使得其结果在多项研究中具有可重复性,目前该方法也普遍应用于白癜风遗传方向的研究[2,5]。
白癜风与SNP
SNP是指基因非编码部分(启动子、内含子)或编码部分(外显子)的核苷酸序列变化,某一表型或疾病的变化可能是SNP引起的[6]。人们利用GWAS方法发现了50多个白癜风易感位点[2],研究易感基因SNP与白癜风患病人群的内在联系,使得人们能够更好地理解白癜风人群的遗传结构,了解其发病机制。近几年发现的白癜风易感基因按照其影响机制归纳如下(表1、2)。
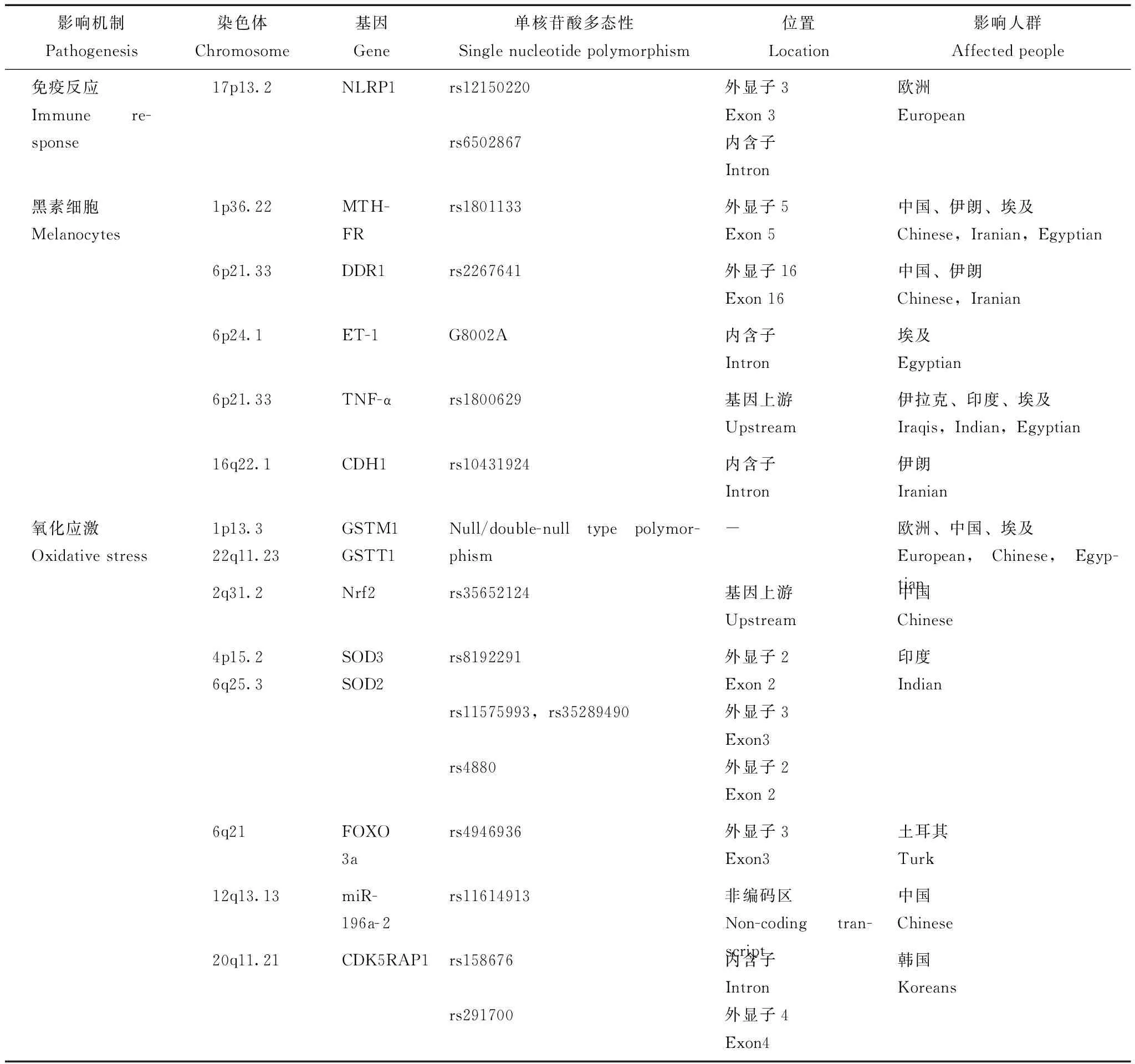
表1 候选基因分析研究检测白癜风易感位点Table 1 Detection of vitiligo susceptibility loci by candidate gene analysis
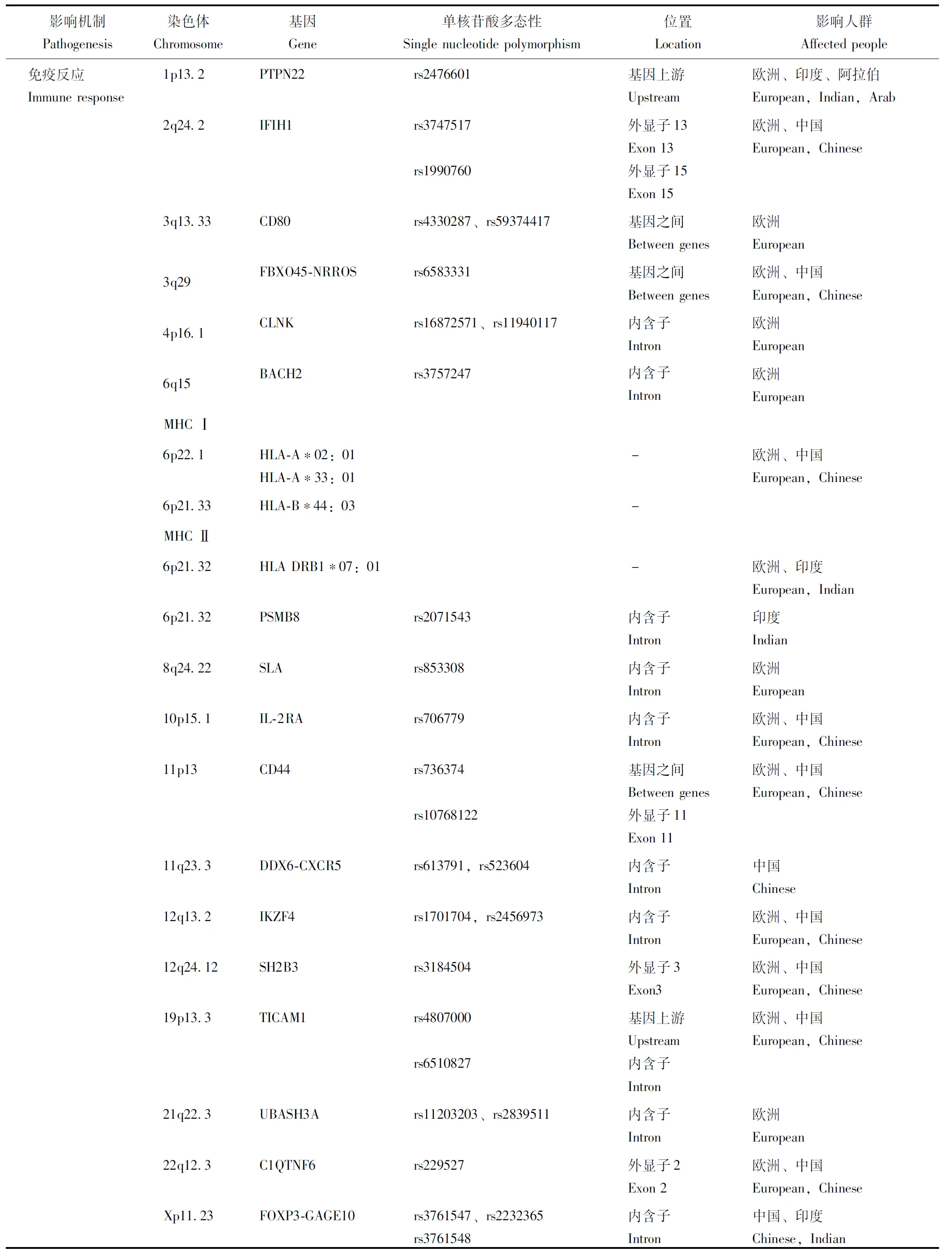
表2 全基因组关联分析研究检测白癜风易感位点Table 2 Detection of vitiligo susceptibility loci by genome-wide association study

续表2
白癜风易感基因
影响自身免疫相关基因
人类白细胞抗原:人类白细胞抗原(human leukocyte antigen,HLA)位于6p,与遗传、免疫密切相关。现已发现HLA参与了白癜风的发展,但HLA等位基因的频率在不同种族之间有所不同。据报道,HLA-A可通过自身抗原介导黑素细胞的免疫反应,导致疾病发生[7-8];位于HLA-DPB1和HLA-DQB1基因座之间的蛋白酶体亚基8外显子2(PSMB8)与白癜风有很强的相关性,可能是通过自身抗原的异常处理和泛素化蛋白的积聚起作用[9]。
干扰素诱导的解旋酶:干扰素诱导的解旋酶(interferon-induced helicase,IFIH1)位于2q24.2,编码MDA5,MDA5可触发自身免疫,也可将寡核苷酸与修饰的解旋酶核心和C端结构域结合,从而导致包括干扰素在内的促炎反应,MDA5还与自身免疫性疾病有关,现已发现该位点多态性与白癜风有关[1,10]。
FBXO45-NRROS:位于3q29,FBXO45编码一种FBXO蛋白,可激活Toll样受体(Toll-like receptor,TLR)和核因子-κB信号通路,介导炎症、免疫。NRROS编码一种富含亮氨酸的跨膜蛋白,负性调节TLR信号通路,影响过敏性疾病和自身免疫性疾病的发生[11]。
BACH2:位于6q15,编码B细胞的转录抑制因子,可对多个免疫细胞进行编程,在维持免疫稳态方面发挥着重要作用。在外周 CD4+T细胞谱系中,显示出抑制T细胞分化。Bach2可直接抑制IL-2R,减弱调节性T细胞(regulatory T cell,Treg)中IL-2R 信号传导[12],现已发现该位点与白癜风发病有关。
CD44:位于11p13,作为重要的T细胞活化分子,参与Th1和Th2分化,CD44 v5 结构域在Th2细胞分化中的作用,抑制的CD44 v5使pSTAT6 和GATA3水平以及IL-4的分泌降低,阻断该结构域可加速IL-4Rα降解,进而诱导Th2细胞抑制[13]。
CXCR5-DDX6:位于11q23.3,CXCR5基因主要表达于滤泡辅助性T细胞(follicular helper T cell,Tfh细胞),在维持表达的同时,Tfh细胞通过细胞间的相互作用和分泌的细胞因子,控制B细胞外周耐受和抗体产生,在自身免疫疾病发病中起着关键作用。作为死亡蛋白盒家族的一员,DDX6编码一种RNA解旋酶,对先天免疫反应和炎症反应的调节有很大影响,而白癜风也是一种与免疫反应有关的疾病[14]。
C1q/肿瘤坏死因子相关蛋白-6(C1QTNF6):位于22q12.3,可参与炎症、免疫、凋亡等多种生物学过程。其编码的糖蛋白可能会影响补体系统,促进细胞因子分泌,进一步发展成白癜风[15]。
FOXP3-GAGE10:位于Xp11.23,Treg参与抑制细胞毒性T细胞并维持对自身抗原的耐受性,从而预防自身免疫性疾病。近期发现由于白癜风患者的Treg中CTLA4、IL10和TGFB表达减少,FOXP3 mRNA和蛋白的减少导致Treg细胞功能的改变[16]。
CD80[10]、IKZF4[3]、UBASH3A[8]、IL-2RA[17]可作为T细胞的激活剂,调控发病;CLNK、SLA[3]可作为信号转导调节剂介导发病;PTPN22可阻止T细胞活化、发育以及使T细胞受体相关激酶及其底物失活而参与自身免疫[8,18-19]。
影响细胞凋亡相关基因
RERE:位于1p36.32,该基因编码含有精氨酸-谷氨酸二肽重复序列的蛋白质家族成员。编码的蛋白质是一种转录抑制因子,可与细胞核中的转录因子共定位,其过度表达引发细胞凋亡[10]。
CASP7:位于10q25.3,该基因可编码半胱氨酸-天冬氨酸蛋白酶(caspase)家族成员。Caspase的顺序激活在细胞凋亡的执行阶段起着核心作用[2]。
颗粒酶B:颗粒酶B(granzyme B,GZMB)位于14q12,可编码半胱天冬酶样丝氨酸蛋白酶,介导两个过程:编码的前蛋白由自然杀伤细胞和细胞毒性T淋巴细胞分泌,并经过蛋白水解处理以产生活性蛋白酶,从而诱导靶细胞凋亡;还可激活辅助T细胞诱导细胞死亡[20]。
影响黑素细胞相关基因
ZMIZ1:位于10q22.3,编码一种与活化STAT(PIAS)蛋白抑制剂相关的蛋白质。PIAS3是 PIAS蛋白家族的相关成员,可以抑制小眼畸形转录因子的转录活性,该因子已被证明是黑素细胞发育、功能和存活的关键调节因子[21]。
OCA2-HERC2:位于15q12-q13.1,OCA2编码黑素体膜转运蛋白8,可造成眼皮肤白化病,并在决定皮肤、头发和眼睛颜色方面发挥重要作用[10]。
黑皮质素1受体:黑皮质素1受体(melanocortin 1 receptor,MC1R)位于16q24.3,编码黑色素细胞刺激素(MSH)的受体蛋白,MSH与其受体的结合激活受体并刺激真黑色素合成,还可作为黑色素生成的调节剂和轻微的白斑自身抗原,与恶性黑色素瘤以及皮肤和头发颜色相关[10]。
亚甲基四氢叶酸还原酶:亚甲基四氢叶酸还原酶(5,10-methylenetetrahydrofolate reductase,MTHFR)位于1p36.22,主要参与同型半胱氨酸(homocysteine,Hcy)的代谢。Hcy对皮肤中的酪氨酸酶活性有抑制作用,影响黑素生成,此外Hcy升高会导致脂质过氧化、活性氧自由基增加,这可能对黑素细胞有毒性作用。在不同人群中被证实与白癜风发病相关[22]。
影响氧化应激相关基因
核因子E2相关因子2:核因子E2相关因子2(nuclear factor erythroid-2related factor 2,Nrf2)位于2q31.2,Nrf2与抗氧化反应元件结合,其下游的抗氧化酶HO-1可以减轻H2O2诱导的人黑素细胞氧化损伤。现已发现白癜风风险降低与rs35652124等位基因C相关,而等位基因T可增加Nrf2的转录活性[23]。
超氧化物歧化酶:超氧化物歧化酶(superoxide dismutase,SOD)清除超氧化物自由基,将其转化为H2O2来降低其毒性,按照金属辅基的不同,大致可将其分为3类,SOD1、SOD2、SOD3。在白癜风患者中,3种亚型活性有所增高,其活性与该位点的多态性及转录水平提高有关[24]。
MiR-196A-2:位于12q13.13,影响酪氨酸酶和酪氨酸酶相关蛋白1(Tyr-Tyrp1)复合体,最终影响活性氧的产生。rs11614913基因型TT、TC可使白癜风易感,等位基因C可下调Tyr的表达,降低细胞内活性氧水平和细胞凋亡率[25]。
其他
与细胞黏附相关:LPP编码的蛋白质参与细胞间黏附和细胞运动,这种蛋白质可穿梭在细胞核中,并可以作为转录共激活剂发挥作用[10]。SMOC2编码一种广泛表达的糖蛋白,在皮肤中,SMOC-2主要存在于表皮的基础水平,并且SMOC-2 可刺激原代角质形成细胞的附着,考虑黑素细胞的丢失可能是由于细胞黏附缺陷导致的慢性细胞分离[26]。
与转录水平相关:PVT1编码一种长的非编码RNA,该RNA嵌入4种微RNA,该位点的SNPs可能通过改变免疫细胞中的转录调节而易患白癜风,也可能是PVT1本身,或者区域中的其他基因[27]。
与其他疾病:通过GWAS发现DNAH5、KIAA1005基因位点SNP与白癜风有关,但目前的研究发现DNAH5突变可导致感觉和运动纤毛的结构和功能缺陷,KIAA1005也与纤毛病有关,与白癜风的关联仍需进一步研究[28]。
易感基因的相互作用
上述易感基因的功能多种多样,但研究发现,这些易感基因也存在相互作用,如抗原加工和呈递、免疫细胞活化、黑素细胞生成、调节T细胞功能等(表3),为进一步了解这些基因导致白癜风的生物学机制提供了重要的见解。
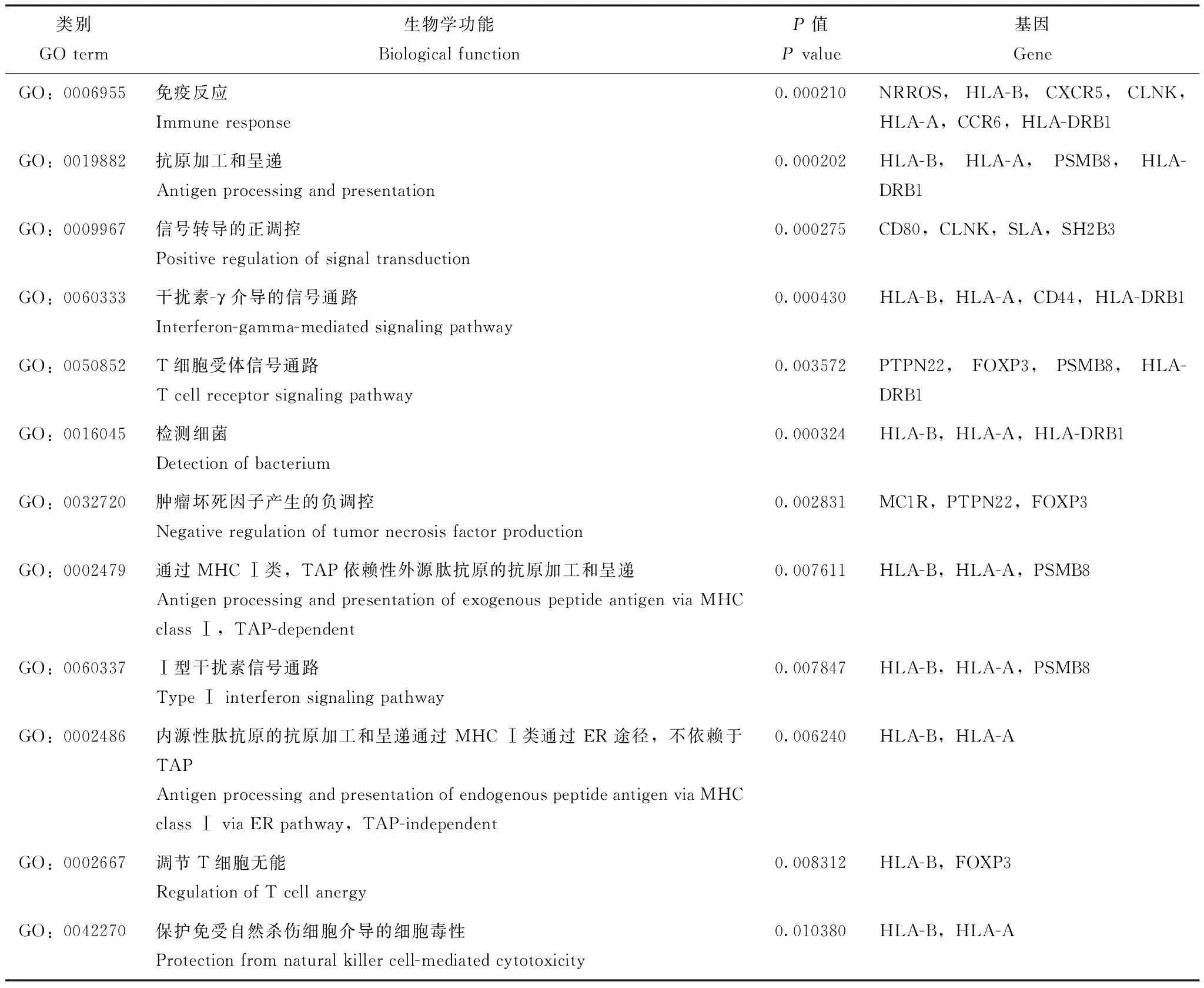
表3 易感基因生物学功能富集分析Table 3 Gene ontology annotation of vitiligo susceptibility genes

续表3
总结与展望
对于白癜风易感基因SNP的研究,可以从微观层面了解白癜风的作用机制,并且从不同的患病人群中找到共通之处,为研究中国白癜风人群提供一定的方向。目前研究虽然取得了一些成果,但也存在一定的缺陷,如研究易感位点有限的SNP;种族不同导致的结果差异;多基因作用及基因与环境共同作用导致表型分布差异等。因此,对白癜风的遗传研究还有待完善。白癜风是由多基因调控的皮肤疾病,随着科技水平的提高,检测方法也从单个基因到全部基因组,但人群分布差异、实验仪器、经费、基因重复验证仍给研究带来不便,希望在未来可以利用大数据进行大样本、多重复、单基因和多基因位点联合检验,最终获得较全面、误差小的结果,为充分理解白癜风的发病机制提供理论依据。
