改性壳聚糖吸附材料吸附水中重金属离子的研究进展
2022-11-02冯思涵赵臣康巩明月王东军
冯思涵,祖 钰,赵臣康,巩明月,辛 颖,姜 伟,王东军
(中国石油天然气股份有限公司石油化工研究院大庆化工研究中心,黑龙江 大庆 163000)
近年来,环境保护和可持续发展问题越来越引起人们的重视,吸附法作为一种绿色的处理回收方法,成本低廉,不会造成二次污染,越来越受到研究人员们的青睐[1~3]。活性炭、无机矿物、聚合物、纳米颗粒等均可作为吸附剂进行使用[4,5]。
在过去的几十年中,来自不同国家的研究人员研究了各种基于生物聚合物的吸附剂,如壳聚糖、纤维素、藻酸盐、木质素等,以实现使用低成本生物材料吸附废水中的重金属。壳聚糖是自然界最丰富且成本最低的生物聚合物之一,具有多种特性,可作为去除废水中污染物的理想吸收剂,同时也是一种天然且可完全生物降解的聚合物材料[6]。壳聚糖的分子结构中包含大量的活性基团,例如氨基和羟基。这些反应性基团使壳聚糖具有很强的化学反应能力并且对废水中金属离子有着很强的结合作用,因此,壳聚糖已被广泛用于去除废水中的重金属离子[7]。
在壳聚糖制备的过程中,甲壳素的乙酰基被水解并转化为游离的氨基。壳聚糖的吸附能力多取决于这时的原料来源及实验条件,这些因素决定了壳聚糖的乙酰化程度(DD)、相对分子质量、结晶度、亲水性等[8]。其中,DD的程度就影响着壳聚糖的吸附能力。壳聚糖基吸附剂对重金属离子的高吸附能力可能是由于其特定的物理化学特性,优异的螯合行为,高反应性和亲水性,同时,壳聚糖中存在的大量吸附位点以及其本身聚合物链的柔性结构也对吸附过程提供了帮助[9]。已经发现基团NH2是吸附金属离子的主要反应基团,—OH 基团也可能有助于吸附。然而,壳聚糖在具备高吸附能力的同时也具有一定的缺陷,例如产量不稳定、尺寸不均匀、缺乏工艺可重复性、机械强度和耐化学性低,限制了其应用。因此,一些研究人员选择对壳聚糖进行改性来进一步增强其对金属离子的吸附性能,本文阐述了壳聚糖主要的制备方法,系统地总结了壳聚糖的主要的物理和化学改性方法。
1 壳聚糖的制备
从甲壳类动物、软体动物、昆虫外骨骼和真菌细胞壁中提取的甲壳素由于乙酰化基团含量高、晶体结构刚性以及其在水溶液中的溶解性差而限制了应用[10]。当甲壳素的乙酰基部分去除后,水溶性增加,生物降解性和生物相容性也会有所增强。一般来说,DD大于50%的甲壳素可以称为壳聚糖[11,12]。
1.1 化学降解法
壳聚糖的化学制备是工业生产中最常用的方法。由原料(如虾壳、蟹壳)经脱钙、脱蛋白、脱色得到甲壳素,再加入40%~50%的NaOH 混合除去乙酰基得到壳聚糖。根据不同的碱溶液浓度、反应时间、温度和甲壳素/碱溶液的比例,可以得到不同脱乙酰度的壳聚糖,Fig.1 展示了由甲壳素到壳聚糖的结构变化。化学降解法简单易行,效率高,且生产过程易于控制[14,15],但该方法能耗大,对环境的污染较为严重。

Fig.1 Schematic for the preparation of chitosan[13]
1.2 酶降解法
酶促脱乙酰是通过甲壳素脱乙酰酶将甲壳素转化为壳聚糖的方法,有效地解决了化学降解法出现的环境污染问题,同时节约能源。然而,优良产酶菌的选择、育种、提取和培养等问题限制了酶降解法的应用[16],选择合适的菌株进行培养来促进高活性甲壳素脱乙酰酶的产生仍是有待解决的问题[17]。
2 改性方法
壳聚糖的改性通常通过物理或化学过程或2 种过程的组合方式进行。物理改性包括混合和转化壳聚糖的形式,通过物理改性可以增加壳聚糖的孔隙率、表面积和吸附位点,提高其力学性能,扩展壳聚糖聚合物链,降低其结晶度并增强其溶胀和扩散性能。化学改性的常用方法是交联和接枝共聚、复合材料制备和掺入取代基等,主要在壳聚糖的官能团(主要是氨基)上进行。目前,已经有许多研究人员使用这些方法对壳聚糖进行加工,以提高其在实际应用中的性能[18,19]。
2.1 壳聚糖的物理改性
2.1.1 功能杂化改性:纯净的壳聚糖为白色或灰白色半透明的片状固体,可以溶于稀酸溶液中,而后与碱混合得到固体壳聚糖。该方法通常用于制备壳聚糖膜、纤维和球形壳聚糖珠,可以增强动力学吸附机制,克服吸附后的固液分离困难等问题[20]。Fig.2 展示了壳聚糖功能杂化改性的几种形貌。一般来说,颗粒状壳聚糖与纤维状和薄膜状壳聚糖相比具有更大的孔隙度,这直接影响到材料的比表面积。而壳聚糖的比表面积是影响壳聚糖吸附能力的重要因素,比表面积越大,吸附容量越大。张宇鑫等[21]以壳聚糖为原料、戊二醛(GA)为交联剂、苯甲醛保护氨基,通过乳化交联法制备了具有吸附功能性的壳聚糖微球(CSM)。对其进行Cr6+的吸附实验,结果表明,CSM 对Cr6+的吸附量随着吸附时间延长和溶液初始浓度增加而增加,当交联剂用量为0.8μL/g,Cr6+溶液初始浓度为320 mg/L 时,CSM 具有较好的吸附效果,对Cr6+的最大吸附量和吸附率可达301 mg/g 和99.8%。Zhang 等[22]制备了壳聚糖微球,然后用锆对其进行改性,以提高壳聚糖对Cr6+的吸附能力,并进行优化实验以获得最佳的吸附条件。研究表明,将锆引入壳聚糖显着提高了其对Cr6+的吸附效果,在pH 4.5、吸附剂用量0.8 g/L 时,改性壳聚糖Zr-CS 对Cr6+的吸附量达到最大,为230.42 mg/g。Zr-CS 对Cr (VI) 的吸附过程符合准二级动力学方程和Langmuir 吸附模型,吸附过程以化学吸附为主。
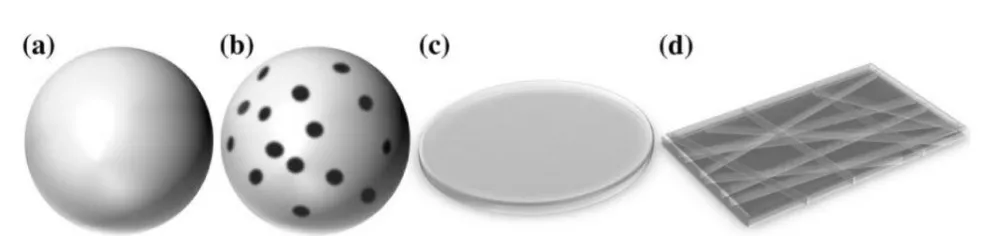
Fig.2 Morphology of physically modified CS composites
2.1.2 无机物修饰改性:以壳聚糖与高岭石、活性炭、粉煤灰等多孔无机物为原料,可以获得集多种吸附材料优点于一体的复合吸附剂[23]。通过共混,可以增加材料的比表面积和内部孔隙度,从而提高复合材料的吸附性能。Jiang 等[24]以壳聚糖和粉煤灰为原料,经乙酸和硫酸交联改性,采用酸浸-包覆法制备了壳聚糖包覆粉煤灰(CWF)。物料配比为壳聚糖:醋酸:酸改性粉煤灰=2 g:3%:15 g。pH=5 时,Cr6+在水中的吸附率可达87%。
2.2 壳聚糖的化学改性
2.2.1 交联改性:交联壳聚糖已被广泛应用于制备各种壳聚糖基材料。通过壳聚糖的交联反应可以将线型的壳聚糖分子相互连接起来,形成具有网络结构的壳聚糖树脂。壳聚糖不溶于高pH 溶液、水和一般有机溶剂中,但是因为NH2基团的存在,壳聚糖在酸性溶液中易被质子化,限制了壳聚糖作为理想吸附剂的应用。为了提高壳聚糖的力学性能,可用环氧氯丙烷、戊二醛和乙二醛等作为交联剂与壳聚糖进行交联反应。当以戊二醛为交联剂时,戊二醛分子与壳聚糖链进行氨基反应,并将壳聚糖分子链联合在一起。
钟少锋等[25]以聚甲基丙烯酸作为共纺和交联试剂,通过静电纺丝制备了形貌良好的交联壳聚糖/聚甲基丙烯酸(CS/PMAA)纤维膜。通过对Cr6+吸附实验发现,在pH =3 时,交联壳聚糖纤维膜的吸附效果最好。Cr6+浓度为6.50 mg/L 时,CS/PMAA 纤维膜的吸附量可以达到4.98 mg/g;Cr6+浓度为3.75 mg/L 时,铬的去除率可以达到81.0%,且提高壳聚糖的含量有利于提高CS /PMAA 纤维膜的吸附性能。研究表明,CS/PMAA 纤维膜对铬离子具有良好的吸附性能。
交联反应虽然可以提高壳聚糖在酸性溶液中的化学稳定性,但氨基、羟基等活性基团与交联剂的结合也使得壳聚糖中的吸附活性点有所减少,进而影响到其吸附能力。为了解决这个问题,寻找合适的材料对交联壳聚糖进行改性,不仅可以提高其在溶液中的稳定性,还可以增加吸附容量。
Şenol[26]以壳聚糖生物聚合物和天然海泡石矿物为原料,使用三聚磷酸盐(TPP) 和环氧氯丙烷(ECH)作为交联剂,合成了一种新型壳聚糖基复合材料,并将其用作吸附剂以去除UO22+离子。研究表明,Ch-Sep 复合微球在25℃,pH=5 下对UO22+离子的最大吸附容量为0.243 mol/kg,Ch-Sep 复合微球表现出对UO22+离子的高吸附能力。
2.2.2 接枝改性:壳聚糖的接枝改性是通过将分子(接枝物)共价结合到壳聚糖主链上来形成功能衍生物。壳聚糖分子骨架上含有大量的—NH2和—OH,可以进行接枝改性,从而增加壳聚糖的吸附位点,达到提高材料吸附选择性和吸附容量的目的。刘海宁等[27]使用三聚氯氰、壳聚糖及硫氢化钠制备了巯基改性壳聚糖树脂,并研究了改性壳聚糖树脂对重金属Cu2+的吸附行为。改性壳聚糖树脂在吸附Cu2+时,吸附量随着pH 升高逐渐增大,在投放量为8 g/L,pH=6.0 时吸附初始浓度为100×10-6的Cu2+10 h 吸附率可达95% 以上。吸附等温线较好地符合Langmuir 吸附等温方程。张润虎等[28]以脱乙酰度95% 的壳聚糖为原料,通过丁二酸酐酰化、氯化钙交联后对壳聚糖的改性,制备了酰化壳聚糖交联微球。并研究了酰化壳聚糖交联微球对Cu2+的吸附性能。结果表明,酰化壳聚糖交联微球对铜离子具有很好的吸附性能,吸附过程符合Langmuir 吸附模型。酰化壳聚糖交联微球对Cu2+的吸附容量为37.88 mg/g,吸附在60 min 后可达平衡。在pH 为6左右时,壳聚糖交联微球的酰化对Cu2+有较好的去除效果。
2.2.3 磁性复合改性:磁性壳聚糖微球是壳聚糖在交联剂的作用下包裹Fe3O4而生成的一种微米级甚至纳米级的球形吸附剂,在磁场的作用下可回收重复利用,具有成本低、易固液分离、吸附效率高等特点。Fe3O4作为磁性内核包覆在壳聚糖内部,壳聚糖作为外壳包覆在磁核表面。壳聚糖由于交联剂的作用形成了一种网状结构,这种结构使其在一定酸性条件下也能稳定存在。周丽莎等[29]将TEMPO 氧化的纤维素纳米纤维与磁性羧甲基壳聚糖纳米粒子交联复合,并将其用于Pb2+的吸附。研究结果表明,在最优吸附条件(pH=5,Pb2+初始浓度为100 mg/L,吸附时间为240 min,常温下进行实验)下,单位质量的TOCNF/MCCN 吸附Pb2+的饱和容量为193.5 mg,比TOCNF 高了近1 倍。复合吸附剂吸附Pb2+的过程更符合准二级动力学方程,说明决定吸附速率的主要是化学吸附。
2.2.4 离子印迹改性:与分子印迹技术一样,离子印迹被广泛用于合成智能聚合树脂材料,这些材料能够在其他干扰物质存在的情况下选择性地与某些特定物质相互作用[30,31]。离子印迹聚合物通常通过单体配体和模板金属离子之间形成络合物,然后将该络合物与交联剂共聚进行制备。制备完成后,使用物理或化学方法将模板离子提取出来,留下空间位点可以选择性地重新捕获这些金属离子[32,33]。作为一种衍生技术,离子印迹在从水性介质中选择性提取和回收特定金属离子方面表现出相当高的效率[34],同时长时间重复使用也不会出现任何明显的效率下降。蔡伟成等[35]利用离子印迹技术对壳聚糖基水凝微球进行改性,制备具有对Cr6+特异识别性能的吸附材料(CTS-IGB),对其在单一Cr6+溶液和模拟电镀废水中的吸附行为特征进行研究。研究结果表明,CTS-IGB 对单一Cr6+溶液和混合溶液中Cr6+的吸附量随pH 值的增大而逐渐减小,在pH值为3 时对Cr6+的吸附量最大。在20 ℃,pH=3 条件下,CTS-IGB 在单一Cr6+溶液和模拟电镀废水中对Cr6+的最大吸附量在180 min 内分别达到37.4 mg/g和44.3 mg/g,半饱和吸附时间仅分别为5.8 min 和23.5 min。相比于未改性壳聚糖水凝微球,CTS-IGB在共存离子溶液中对Cr6+的选择性提高了32%~74%。王可等[36]以空心玻璃微珠为无机载体、壳聚糖为功能单体、铜离子为模板离子,利用戊二醛对其进行交联改性制备了空心玻璃微珠-壳聚糖印迹材料,并且对比研究了交联改性前后的印迹材料在不同条件下的吸附容量。实验结果表明,当初始铜离子浓度为0.3 mmol 时,改性前、后印迹材料的吸附容量均达到最大值,分别为89.88 mg/g 和219.72 mg/g。当pH=5,交联时间2h 时,所制备的改性印迹材料吸附容量达到最大值246.98 mg/g。同时由于改性印迹材料中含有大量Cu2+的有效吸附位点,这些吸附位点具有特定的半径尺寸(即Cu2+的半径尺寸),使得即使在多元吸附的条件下,印迹材料对于Cu2+仍保持较高的吸附能力,可达其他离子的5~15 倍,吸附性能明显优于其他干扰离子。
3 总结与展望
从整理的部分壳聚糖基吸附材料的应用情况来看,研究者们大多采用物理改性与化学改性相结合的方式来提升其吸附能力。与未改性的壳聚糖材料相比,壳聚糖基吸附剂具有较大的吸附容量,选择性高,力学稳定性也有所增强,是未来开发环境友好型吸附剂的重要选择之一。近年来,越来越多的国内外学者开始关注到壳聚糖及壳聚糖基吸附剂优良的吸附性能,但距离其商业化应用还有很长的路要走。今后可能会从以下几个方面开展研究。
(1)深入研究壳聚糖基吸附剂对重金属离子的吸附机理,明确吸附理论体系,有利于更有针对性地研发对某类特定的污染物的高效吸附剂。
(2)将壳聚糖基吸附剂作为商业吸附剂具有良好的商业应用前景,但由于壳聚糖的结构对其进行改性是不可避免的。大多数主要的交联剂、表面活性剂和某些接枝剂具有剧毒,对环境和健康非常有害。因此,还应对交联剂等进行更深入的研究,寻找更安全绿色的改性方法,实现壳聚糖基吸附剂商品化的目标。
(3)从目前的文献来看,很少有研究集中在壳聚糖基吸附剂的再生上。采用高效的解吸方法对壳聚糖吸附剂进行解吸和再生,将重金属离子转移到浓缩形式的洗脱液中,可以进一步处理后回收金属,促进金属的回收再利用以及减少二次污染。同时,研究吸附剂的解吸机制和参数,将有助于壳聚糖基吸附剂工业化工艺设计和经济评估。
