干湿环境对河岸带硝化及反硝化潜力的影响
2022-10-27陈丽慧肖静文冯晶红刘瑛李晗李毅
陈丽慧,肖静文,冯晶红,刘瑛,李晗,李毅
(湖北工业大学土木建筑与环境学院河湖生态修复与藻类利用湖北省重点实验室,湖北武汉 430068)
0 引言
近年来,氮污染逐渐成为地表水和地下水的重要污染源,其主要来自农业非点源污染[1],如合成氮肥的过度使用[2]、畜禽养殖排污[3]、水土流失[4]等。河岸带作为连接陆生生态系统和水生生态系统的生态交错带,可截留过剩的氮素进入河流,硝化与反硝化作用是河岸带氮循环的重要一环[5]。硝化是指在亚硝化细菌、硝化细菌作用下将NH4+转化为NOx-的过程[6],被视为氮循环的限速步骤。反硝化是指在反硝化细菌作用下以NO3-为底物、土壤有机碳为电子供体,将NO3-转化成N2O 或N2的过程,被认为是最佳的脱氮途径[7]。硝化、反硝化过程受多个环境因子的综合影响,如土壤氮素含量及存在形态、土壤有机碳、氧浓度、pH、含水率、温度、盐分等[8,9]。河岸带水位波动会改变土壤理化性质,进而影响硝化、反硝化过程,如王静等[10]研究蓄水期和泄水期三峡库区在沉积物硝化、反硝化速率时发现硝化速率、反硝化速率分别在蓄水期、泄水期达到最高值。邵志江等[11]以丘陵区自然沟渠为研究对象,对比干湿交替和长期淹水沉积物的反硝化速率,发现干湿交替显著促进了沉积物反硝化速率。郭士林等[12]通过探讨人工湿地在不同水位下脱氮效果,发现随水位变动幅度增加,硝化强度减小,而反硝化强度增加。目前诸位学者关于沉积物硝化、反硝化作用对不同水位的响应结论不一,且主要集中在水库、农田、人工湿地等,对河岸带硝化、反硝化作用的研究尚有不足,河岸带作为拦截污染物、净化水质的一道重要屏障,在控制水体面源污染问题方面发挥着重要作用。因此,开展干湿环境下河岸带硝化、反硝化潜力及其影响因素分析研究,对水环境保护和发展具有重要意义。
以夏家寺河河岸带为研究对象,通过室内培养试验研究淹水期、落干期河岸带土壤硝化、反硝化潜力及与其与环境因子的相关性,探讨干湿环境下河岸带土壤氮硝化、反硝化作用的主要环境影响因素,为了更好地认识硝化-反硝化作用在河岸带去除氮素的重要作用,明晰土壤环境因子对硝化-反硝化作用的影响,以期为河岸带氮迁移转化的理论研究提供依据。
1 材料与方法
1.1 研究区概况
夏家寺河(又名长堰河)地处湖北省黄陂区(30°58'N~31°03'N、114°27'E~114°30'E),自北注入夏家寺水库,出库后向南汇入滠水,流程36.43 km,流域面积239 km2(如图1),流域属北亚热带季风性湿润气候,属于季节性河流,年平均气温16.3 ℃。

图1 研究区域示意图Fig.1 Schematic map of the research area
1.2 研究方法
1.2.1 样品采集及测定方法
本研究分别于2021 年5 月的淹水期[图2(c)]、2021 年6 月的落干期[图2(d)]在夏家寺河某河岸带(114°28'E,31°02'N)距河岸5 m×5 m 的样方内随机采集3 个样点的土壤。正式采样前,首先除去土壤表层2 cm 的残枝败叶,再用土壤取样钻机STC-3D 分层采集0~10(表层)、10~20(中层)、20~30 cm(底层)的土壤样品[图2(b)],将土样混合后放入4 ℃密封遮光的保温箱中,运回实验室保存至低温冰箱。取一部分新鲜土样测NH4+-N、NO2--N、NO3--N,其余的土样平铺在通风无尘的室内进行风干过筛,取一部分风干土测定土壤总氮(TN)、土壤总有机碳(SOC)、pH、土壤电导率(EC),另一部分风干土用于硝化潜力、反硝化潜力培养试验[13],每项指标测3次平行样。具体测定方法及仪器见表1。

表1 河岸带沉积物理化性质的测定Tab.1 Determination of physicochemical properties of deposits

图2 采样点分布示意图Fig.2 Schematic diagram of sampling point distribution
1.2.2 室内培养试验
(1)土壤硝化潜力的测定。采用恒温培养法测定土壤硝化潜力。分别称取6 份5 g 过20 目筛的各层风干土壤,为保证实验的准确性,每份测3 个平行样,共54 个待测样品,分别放入100 mL 培养瓶中,加入超纯水至淹没土样,用塑料薄膜密封瓶口,膜上扎2 个小孔以保持通气条件。将样品放置25 ℃培养箱预培养3 d后,各层样品分别取出一份测定NH4+-N、NO3--N计作初始含量,其余45份样品分别加入1.25 mg N 的溶液继续培养,调节土壤水分为最大田间持水量60%,并定期补水保持其含水率,分别于第1、3、6、10、15 d 进行NH4+-N、NO3--N 含量的测定。以单位培养时间内NO3--N 的含量之差表征氮硝化速率,以某培养日NO3--N变化量占(NH4+-N+NO3--N)初始量的百分含量表征硝化活性。
(2)土壤反硝化潜力的测定。采用恒温厌氧淹水培养法测定土壤反硝化潜力。分别称取6 份5 g 过20 目筛的各层风干土壤于100 mL 培养瓶中,共54 份待测样品,加入超纯水至淹没土样,用橡胶塞密闭瓶口。将样品放置25 ℃培养箱预培养3 d后,各层样品各取一份测定NO3--N初始含量,其余样品分别加入1.50 mgN 的KNO3溶液继续培养,调节土壤水分为25 mL,定期补水,分别于第1、3、6、10、15 d 测定NO3--N 的含量。以单位培养时间内NO3--N含量之差表示氮反硝化速率,氮反硝化活性:以某培养日NO3--N 变化量占NO3--N 初始量的百分含量表征反硝化活性。
1.3 数据处理与分析
运用Excle2010 软件整理实验数据,通过SPSS25.0 软件进行正态分布检验、方差分析以及培养15 d 后的土壤硝化潜力、反硝化潜力与土壤理化性质的相关性分析,采用Origin2018 进行绘图及数据拟合。
2 结果
2.1 干湿环境下河岸带环境因子特征
通过对同一河岸带状态下的不同深度下的土壤指标及相同深度下的不同河岸带状态下的土壤指标分别进行了单因素方差分析(one-way ANOVA)及独立样本T 检验,分析结果见表2,淹水期河岸带表层土壤的EC、pH、SOC、NH4+-N、NO2--N、NO3--N、TN 含量达到最大值,各土层深度上EC、SOC、NH4+-N、NO3--N 含量存在显著的差异性(P<0.05,n=9)。落干期SOC、NH4+-N、NO3--N、TN 含量最大值均在土壤表层,而EC 最大值出现在土壤底层,pH、NO2--N 在中层土壤出现最大值,EC、pH、SOC、NO2--N 在不同土层上具有显著差异性(P<0.05,n=9)。研究发现,河岸带EC、pH、SOC、NH4+-N、NO3--N、TN 最大值均出现在淹水期表层土壤,分别为(1 065.42±46.73)μS/cm、6.52±0.08、(26.92±0.15)g/kg、(1.86±0.09)mg/kg、(1.03±0.04)mg/kg、(2.15±0.32)mg/kg,与王静等[10]关于三峡库区小江支流沉积物在蓄水期、泄水期土壤理化性质的研究结果相似,且淹水期、落干期河岸带在同一深度下的EC、SOC、NH4+-N、NO2--N、NO3--N 含量具有显著差异性(P<0.05,n=6)。
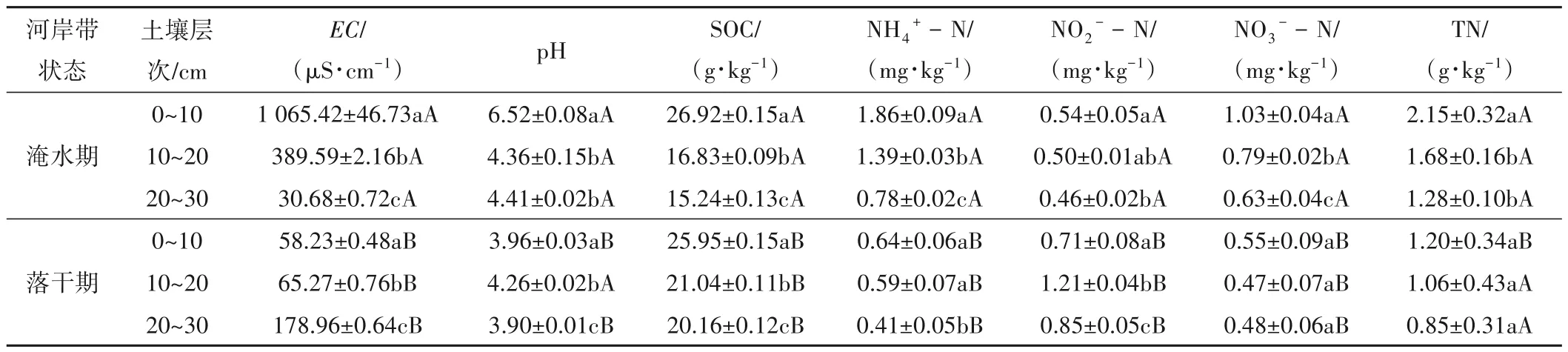
表2 干湿情况下河岸带土壤环境因子统计学特征Tab.2 Statistical characteristics of soil environmental factors in riparian zone under dry and wet conditions
2.2 干湿环境下河岸带沉积物的硝化潜力
2.2.1 干湿环境下河岸带沉积物的硝化速率
干湿环境下河岸带各层土壤的硝化速率随培养时间的变化见图3。无论是淹水期还是落干期,河岸带土壤的硝化速率均呈现随培养时间的增加而增加的趋势。淹水期河岸带的硝化速率变化范围和平均值分别为(-0.03~1.84)mg/(kg·d),其平均硝化速率最高值、最低值分别出现在土壤表层、中层,均值为(0.81、0.22)mg/(kg·d);落干期河岸带的硝化速率变化范围和平均值分别为(-0.05~3.06)mg/(kg·d),各层土壤平均硝化速率表现为表层>中层>底层,分别为(1.14、0.77、0.16)mg/(kg·d)。研究发现,无论是河岸带处在淹水期还是落干期,硝化速率的最大值均出现在表层土壤。此外,通过对平均硝化速率的计算可知,淹水期均值为0.47 mg/(kg·d),落干期均值为0.69 mg/(kg·d),落干期河岸带平均硝化速率大于淹水。

图3 干湿环境下河岸带土壤硝化速率Fig.3 Nitrification rate of riparian soil in dry and flooding period
2.2.2 干湿条件下河岸带沉积物的硝化活性
干湿环境下河岸带各层土壤的硝化活性随培养时间的变化如图4所示。干湿环境下河岸带的硝化活性随培养时间的增加逐渐增加,前6 d 内土壤的硝化活性的变化较为缓慢,淹水期各层土壤增幅仅为16.29%、3.54%、4.13%,落干期各层土壤增幅为4.00%、3.28%、1.25%,从培养6 d 后至培养结束过程中迅速增加,淹水期各层土壤硝化活性分别增长66.73%、17.10%、34.72%,落干期各层土壤分别增加130.13%、92.24%、21.02%,研究发现,落干期河岸带的平均硝化活性显著高于淹水期,且干湿环境下各层土壤的硝化活性变化趋势同硝化速率变化一致:淹水期,表层>底层>中层,落干期,表层>中层>底层。

图4 干湿环境下河岸带土壤硝化活性Fig.4 Nitrification activity of riparian soil in dry and flooding period
2.3 干湿环境下河岸带沉积物的反硝化潜力
2.3.1 干湿环境下河岸带沉积物的反硝化速率
干湿环境下河岸带各层土壤的反硝化速率随培养时间的变化如图5 所示,淹水期和落干期河岸带的反硝化速率变化范围及分别为(5.33~73.76)、(4.15~65.17)mg/(kg·d),均值分别为24.02、24.23 mg/(kg·d),落干期平均反硝化速率大于淹水期。从图5中可知,无论是淹水期还是落干期,各层土壤反硝化速率随深度的增加而减小,表层土壤的反硝化速率在培养初期达到最大值,分别为69.98、63.91 mg/(kg·d)。
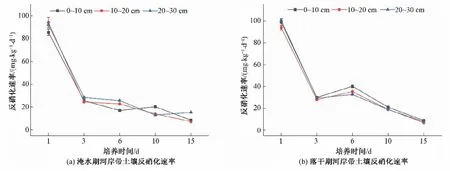
图5 干湿环境下河岸带土壤反硝化速率Fig.5 Denitrification rate of riparian soil in dry and flooding period
淹水期反硝化速率随培养时间的增加而持续下降[图5(a)],各层土壤平均反硝化速率分别为(26.30、24.02、21.75)mg/(kg·d)。落干期反硝化速率在培养1 d 后达到最大值后下降,再于6 d小幅上升后继续下降[图5(b)],各层土壤平均反硝化速率分别(25.50、24.04、23.16)mg/(kg·d)。研究发现,河岸带表层土壤平均反硝化速率表现为淹水期>落干期,而落干期中层、底层土壤反硝化速率均大于淹水期。通过对淹水期、落干期各层土壤与培养时间的拟合发现各层土壤的反硝化速率均随时间增加呈现一阶指数衰减曲线变化,且R2≥90(表3)。

表3 土壤反硝化速率随培养时间变化的模拟模型Tab.3 Simulation model of soil denitrification rate varying with culture time
2.3.2 干湿环境下河岸带沉积物的反硝化活性
干湿环境下河岸带各层土壤的反硝化活性随培养时间的变化如图6 所示,淹水期与落干期河岸带土壤的反硝化活性变化范围及平均值分别为36.18%~102.28%、56.17%、35.19%~105.36%、60.81%,落干期河岸带的平均反硝化活性大于淹水期。淹水期、落干期河岸带各层土壤平均反硝化活性分别为(64.91±23.18、54.38±12.94、49.21±10.27)%、(65.83±27.95、59.78±22.81、56.25±22.77)%,无论河岸带是处于淹水期还是落干期,河岸带反硝化活性均在表层土壤达到最大值。
淹水期、落干期河岸带土壤的反硝化活性均随培养时间的增加呈现先减后增再减的趋势,其中,淹水期在培养10 d 后硝化活性达到最大值,各土层深度上反硝化活性分别为99.07%、68.26%、63.46%[图6(a)],落干期反硝化活性达到最大值在培养后的6 d,各土层深度上反硝化活性分别为101.61%、88.64%、82.59%[图6(b)]。

图6 干湿环境下河岸带土壤反硝化活性Fig.6 Denitrification activity of riparian soil in dry and flooding period
3 讨论
3.1 干湿环境对河岸带沉积物硝化潜力的影响
土壤的硝化潜力与其理化性质密切相关,通过Pearson系数法分析培养15 d 的硝化潜力与土壤理化性质之间的相关性(表4),分析结果表明,淹水期河岸带硝化潜力与pH、SOC呈显著正相关性(P<0.05),与NH4+-N 含量呈极显著正相关性(P<0.01),与EC、NO2--N、NO3--N、TN相关性不显著。硝化潜力随pH 的增加而增加,与国内外研究结果一致[16,17],说明此区域pH 可能是适宜硝化细菌生长繁殖的范围。张青山等[18]发现SOC与硝化潜力呈极显著正相关关系(P<0.01),是影响洼地土壤硝化潜力的主要影响因素之一。另外,NH4+-N 作为硝化作用的底物,底物浓度越高,硝化速率越快。落干期河岸带硝化潜力与TN 含量呈显著正相关关系(P<0.05),与EC、SWC、pH、SOC、NH4+-N、NO2--N、NO3--N 相关性不显著。通过对无机氮占总氮比例的计算可知,无机氮占总氮的0.1%~0.2%,与他人研究结果一致,土壤氮素主要以有机氮的形式存在为主[19],有机氮通过微生物的矿化作用生成无机氮NH4+-N、NO3--N,NH4+-N在硝化细菌的作用下生成硝酸盐。
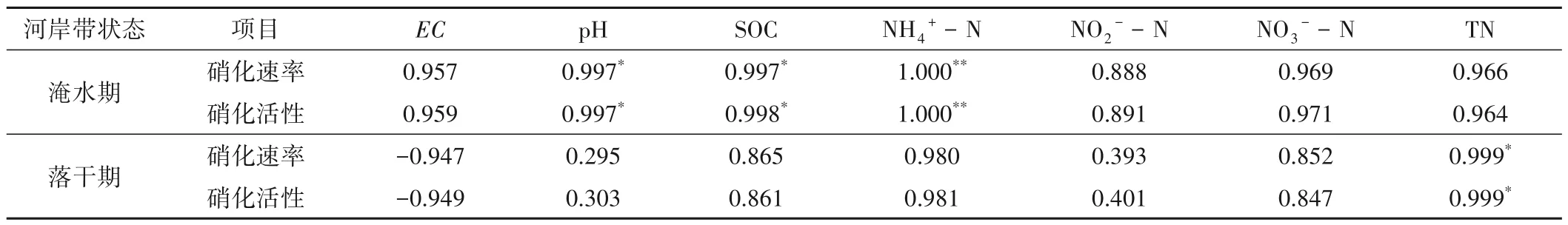
表4 培养15 d时的硝化潜力与土壤理化性质间的相关性结果(n=3)Tab.4 Correlation between nitrification potential and soil physical and chemical properties after 15 days of culture(n=3)
本研究中,淹水期硝化潜力弱于落干期可能是因为一方面氨化细菌、硝化细菌都是需氧型微生物,淹水期河岸带处于滞水状态,土壤颗粒间通气状况较差,不利于O2的扩散,另一方面SOC 的分解过程会造成O2的消耗,硝化作用减弱。淹水期、落干期河岸带硝化潜力最高值均出现在表层土壤,与郭士林等[12]研究结果相似,硝化潜力的大小主要受限于硝化细菌、O2及NH4+-N,表层土壤充分暴露于空气中,土壤氧含量在此区域达到最大值,但随着土层深度的增加,O2及NH4+-N 含量逐渐减少使得硝化潜力减弱。而淹水期底层(20~30 cm)硝化潜力的增加可能是因为此处由于潜流交换作用河水侧向流入土壤河岸带,溶解氧随河水径流作用进入土壤,该层土壤内氧含量增多;也可能与该层硝化细菌的数量及活性有关。
3.2 干湿环境对河岸带沉积物反硝化潜力的影响
通过Pearson 系数法分析培养15 d 的反硝化潜力与土壤理化性质之间的相关性,分析结果见表5,淹水期反硝化潜力与SOC、NH4+-N含量呈显著正相关关系(P<0.05),发现氮源、碳源含量是影响河岸带反硝化潜力的重要因素。河岸带NH4+-N 含量越多,反硝化潜力越大,与吴佳栩等[20]关于淀山湖的研究结果一致,NH4+-N 作为硝化作用的底物在硝化细菌的作用下生成NO3--N,NH4+-N 含量越高,生成的NO3--N 越多,反硝化作用在底物浓度增大的环境下速率加快。反硝化速率随SOC 含量的增加而增加[21],SOC 为反硝化细菌提供电子供体,其分解过程会消耗土壤内部的氧气,形成厌氧环境,从而促进反硝化作用的进程。而落干期反硝化作用与EC、pH、SOC、NH4+-N、NO2--N、NO3--N、TN相关性不显著。本研究中,无论河岸带处于淹水期还是落干期,表层土壤的反硝化潜力高于深层土壤,与其他学者研究结果一致[22,23],如陈紫萱在研究竹林河岸带不同深度土壤对反硝化速率的影响时发现反硝化速率随土壤深度的增加逐渐减小,表明深层土壤的可溶性有机碳含量低,反硝化作用可利用的碳源较少是反硝化速率减慢的原因所在。表层土壤的碳源、氮源在外源的输入下(如动植物腐体、有机肥的施加、大气氮沉降等)达到峰值(表5),使得河岸带表层成为反硝化作用的热点区域。

表5 培养15 d时的反硝化潜力与土壤理化性质间的相关性结果(n=3)Tab.5 Correlation between denitrification potential and soil physical and chemical properties after 15 days of culture(n=3)
4 结论
(1)无论淹水期还是落干期,河岸带EC、pH、SOC、NH4+-N、NO3--N、TN含量最大值均出现表层土壤,且淹水期土壤环境因子的平均含量大于落干期;
(2)淹水期、落干期河岸带硝化潜力随培养时间的增加而增加,且平均硝化速率均呈现在表层土壤:淹水期均值为0.81 mg/(kg·d),分别是中层、底层土壤的3.64 倍、2.19 倍;落干期均值为1.14 mg/(kg·d),分别是中层、底层土壤的1.49 倍、7.20倍,落干期平均硝化速率[0.69 mg/(kg·d)]大于淹水期[0.47 mg/(kg·d)];
(3)淹水期、落干期反硝化速率均于培养初期在表层土壤达到最大值,分别为(69.98、63.91)mg/(kg·d),淹水期反硝化活性在培养后的10 d达到最大值99.07%,落干期反硝化活性在培养后的6 d达到最大值101.91%,落干期河岸带平均反硝化速率[24.23 mg/(kg·d)]大于淹水期[24.02 mg/(kg·d)];
(4)通过河岸带硝化潜力、反硝化潜力与其土壤基本理化性质的相关性结果可知,淹水期硝化潜力、反硝化潜力与SOC、NH4+-N、pH含量呈显著正相关,落干期硝化潜力与TN呈显著正相关,表明SOC、氮素是影响河岸带硝化反硝化潜力的主要因素。
