药食两用中药AHP安全性评价方法构建及分析
2022-10-25揭圣刘恒利詹懿程春雷叶青江西中医药大学计算机学院南昌330004
★ 揭圣 刘恒利 詹懿 程春雷 叶青(江西中医药大学计算机学院 南昌 330004)
药食两用中药是指作为食品且列入《中华人民共和国药典》的物质[1]。在本次新型冠状病毒肺炎预防处方中,药食两用中药被广泛使用。其应用体现了中医学扶正祛邪“治未病”的理念,对疾病防治、日常保健及相关产品的研发具有较高参考价值[2]。当前综合指标评价药食两用中药安全性的研究较少,使用时存在一定的安全隐患,探索药食两用中药的安全评价方法具有现实意义。AHP是由运筹学家萨蒂教授提出,将与决策有关的相关因素分解成目标到决策,决策到选择层次。本文研究的药食两用中药AHP安全性评价具有两点特色:一是药物-分子-人体层次结构,药食两用中药的毒性与其分子结构有关,各药食两用中药在临床上有不同的不良反应,药物分子作用于人体靶细胞,可以标量毒性分子的主要属性包括半数致死量、类药性、口服生物利用度,通过分子、人体与药物层关系共同作为评价因素。二是层次分析+药食两用中药安全性评估,运用层次分析法(analytic hierarchy process,AHP)综合性测评药食两用中药的安全性,选取出关键性评价指标作为打分因素,构建其安全性评价方法。
1 资料与方法
1.1 评价方法
人们普遍认为食源性中药毒副作用小,但近年来,中药引发的不良反应事件时常出现,例如新加坡禁用黄连素和国内的鱼腥草事件[3],所以,加强药食两用中药安全性评价研究势在必行。
目前对药食两用中药的安全性研究大多集中在其加工以后,对保健食品的原料单一保健功能的分析[4],应用综合指标全面评价药食两用中药的研究尚未见报道。在各类排序算法选择上,数据包络[5]、层次分析和模糊综合评价法被广泛用于产业性评价的排名上[6-8],其中,层次分析法对定量数据的需求少、实用性强,通过结合专家的主观性因素,对于药食两用中药评估有很大的适应性。
本研究从药食两用中药的毒性化合物分子层面出发,对药食两用中药进行安全性评价,与专家评价结果存在一致性,为系统性分析药食两用中药的评价方式、推进其适用范围提供支撑,详细的药食两用中药AHP安全性评价方法构建及流程。见图1。

图1 药食两用中药AHP安全性评价方法构建流程
1.2 数据来源
各个指标的数据信息均来自于可靠的数据库,其中:药食两用中药基础信息、半数致死量(LD50)来自于通用数据库;药食两用中药类药性(DL)、口服生物利用度(OB)来自于中药药理学数据分析平台(TCMSP)和中国知识资源总库(CNKI);临床不良反应数来自于中国知识资源总库(CNKI)和中文科技期刊数据库(维普网)。
1.3 数据筛选
数据筛选阶段遵循化学成分的收集和筛选作为标准,按照口服生物利用度OB 30%和类药性DL 0.18的原则选取有效活性成分信息[9],运用Numpy库进行整理获得最终数据,所得药食两用中药部分信息见表1。

表1 部分药食两用中药指标信息表
2 结果
2.1 分析药食两用中药AHP安全性评价模型
2.1.1 三个评价层级和四个评价指标药食两用中药AHP安全性评价模型的构建借鉴中医药产业、健康产业评价研究相关指标[10-11],间接梳理出三层次四指标体系结构。
三层次一方面是指层次分析法的“选择层-决策层-目标层”;另一方面是指“药物-分子-人体”,药食两用中药包含各类毒性分子化合物,毒性分子作用于人体的靶细胞靶器官影响其生理功能。见图2。

图2 药食两用中药AHP安全性评价模型的构建
四指标是指各个毒性分子有众多的特征属性,但这些属性的交集包括了半数致死量(LD50)、类药性(DL)、口服生物利用度(OB),以及每种药食两用中药通过大量临床试验,总结出其确定的临床不良反应数。
通过与药理学专家研讨,借鉴药食两用中药相关行业规范和国家标准的指南[12],制定了评价指标层级。由专家咨询按照层次分析法的一般流程形成决策层到目标层的比较矩阵[13](主观),最终确定各级指标权重;药物对比标准化的方法由计算机自动构建从选择层到决策层的比较矩阵[14](客观),计算二者的组合权重,并通过了一致性检验后,构成了药食两用中药AHP安全性评价方法,主客观因素结合,提高评价模型的准确度。
2.1.2 评价指标与符号说明本文中用到的评价指标和符号所代表的的意义见表2。

表2 评价指标与符号说明
2.1.3 决策层对目标层的成对比较矩阵的确定(主观性)决策层对目标层的成对比较矩阵的确定,由药理学专家根据判断矩阵元素的标度方法进行打分处理[15],判断矩阵的打分方法见表3,以各指标属性相对于药食两用中药安全性的影响程度下,最终确定成对比较矩阵。见表4。

表3 判断矩阵元素Wab的标度方法

表4 标准层对目标层的成对比较矩阵
其中,专家评价的结果如下,半数致死量(LD50)∶类药性(DL)∶口服生物利用度(OB)∶临床不良反应数=7∶1∶3∶9。
比例结果及其代表意义:
LD50∶DL=7∶1(LD50比DL指标强烈重要)
LD50∶OB=7∶3(LD50比OB指标稍微重要)
临床不良反应数∶LD50=9∶7(临床不良反应数比LD50指标稍微重要)
OB∶DL=3∶1(OB比DL指标稍微重要)
临床不良反应数∶DL=9∶1(临床不良反应数比DL指标极端重要)
OB∶临床不良反应数=3∶1(OB比临床不良反应数指标稍微重要)
2.1.4 选择层对决策层的成对比较矩阵的确定(客观性)选择层对决策层的成对比较矩阵的确定依托python程序由计算机自动化建立[16],在本次研究中,每次通过对两类药食两用中药的比较得其安全性权向量,建立的基础是药物A与药物B的对比意义,筛选后标准化处理,将两类药物的属性值的比值、属性比值的倒数,作为构建矩阵的基础。对32种药食两用中药每两类进行比较一次,共需要多次安全性评价比较,每次安全性评价构建5个成对比较矩阵,所以需要进行2 480个成对比较矩阵的打分处理,工作量繁重,由专家进行打分不切实际,所以运用计算机进行自动化操作效果更优,以黄芪和附子为例,选择层-目标层的成对比较矩阵。见表5、表6、表7、表8。

表5 选择层对半数致死量LD50的成对比较矩阵
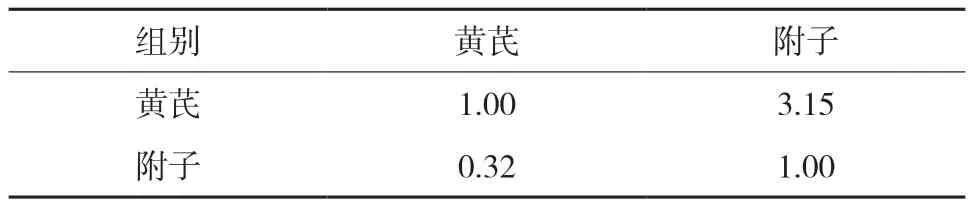
表6 选择层对类药性DL的成对比较矩阵
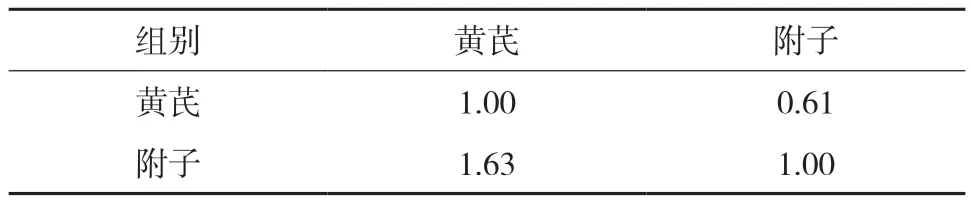
表7 选择层对口服生物利用度OB的成对比较矩阵
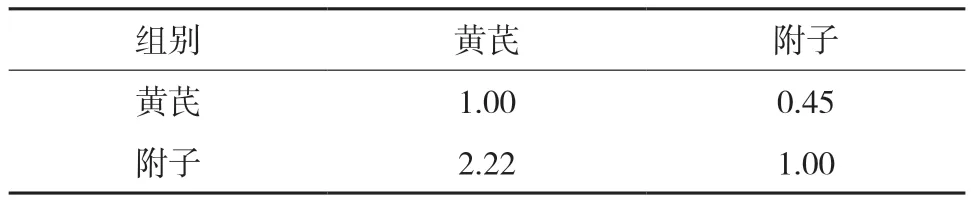
表8 选择层对临床不良反应数的成对比较矩阵
2.1.5 评价信息集结和随机一致性检验评价信息集结就是指利用具体模型将多个评价的指标结果组合权重为一个综合结果,对所要评价的目标进行排序与具体分类。本研究利用线性加权综合法[17],按照安全性评价三层级自底向上的顺序,将指标值与权重乘积,得到药食两用中药的安全性评价结果。
根据成对比较矩阵N得出各个评价元素的相比较重要性排序的权值,首先计算成对比较矩阵最大特征根(λmax),以及其相对的通过归一化处理后特征向量(W):

归一化处理后可以得到特征向量W0=[f1,f2,f3,.....]T,WO代表决策层各评价因素相对于总目标层的权重。
同理,可以根据选择层对决策层的成对比较矩阵获得每两个药物针对单个指标的权向量W1=[n1,m1],W2=[n2,m2],W3=[n3,m3],W4=[n4,m4],分别表示:
W1:药物A与药物B对于半数致死量(LD50)指标的权值向量,其中n1代表药物A对于LD50的权值向量,m1代表药物B对于LD50的权值向量。(下同)
W2:药物A与药物B对于类药性(DL)指标的权值向量。
W3:药物A与药物B对于口服生物利用度(OB)指标的权值向量。
W4:药物A与药物B对于临床不良反应数指标的权值向量。
将特征向量与各指标权值向量进行评价信息集结处理,即:

经过计算得出:
药物A的安全性权值为:Result[0]=n1×f1+n2×f2+n3×f3+n4×f4
药物B的安全性权值为:Result[1]=m1×f1+m2×f2+m3×f3+m4×f4
对决策层到目标层的成对比较矩阵、选择层到决策层的成对比较矩阵进行一致性结果检验。若判断矩阵中的元素具有传递性,被称为一致性矩阵[18]。在现实生活中,由于专家具有主观性的判断,会受到个人思维方式以及其学识能力的局限,判断矩阵往往无法满足一致性,为了进一步确保结论的可信赖性,必须对判断矩阵进行检验,检测矩阵一致性的指标为一致性比率CR。

其中RI为随机一致性指标,n是成对比较矩阵的阶数,当CR<0.1时,一般认为判断矩阵的一致性是可接受的,否则应该修改矩阵使之符合要求。每个矩阵阶数n都对应一个确定的判断矩阵特征值RI。见表9。

表9 一次性检验指标取值表
若所有成对比较矩阵都通过了一致性检验,最终得到结果,药物A与药物B在安全性上比值为:
Result[0]∶Result[1]
如果Result[0]>Result[1],则药物 A 更不安全性,毒性更强。
如果Result[0]=Result[1],则药物 A 与药物B安全性大致相同。
如果Result[0]<Result[1],则药物 B 更不安全性,毒性更强。
2.2 药食两用中药的安全性比较
(1)根据专家给出的决策层对目标层的成对比较矩阵获取权重向量W0,利用Python语言编程进行一致性检验与最大特征值计算,计算出的结果:
W0=[0.45 0.15 0.05 0.35]
(2)以附子和黄芪为例,其指标信息LD50、DL、OB、临床不良反应数见表10。
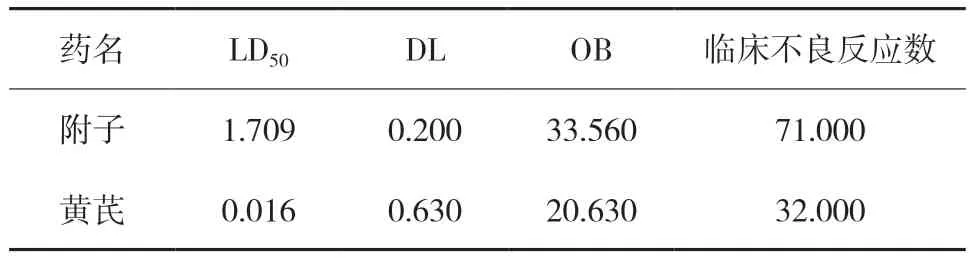
表10 附子和黄芪的相关指标信息
(3)构建4类选择层对决策层的成对比较矩阵,可见表5、表6、表7、表8。并计算其特征值。
LD50指标成对比较矩阵的特征值:
W1=[0.00934729 0.99065271]
DL指标成对比较矩阵的特征值:
W2=[0.75903614 0.24096386]
OB指标成对比较矩阵的特征值:
W3=[0.38069755 0.61930245]
临床不良反应数成对比较矩阵的特征值:
W4=[0.31067961 0.68932039]
同时,对各类矩阵实施一致性结果检验,都满足CR<0.1,是可接受的。
最后,对所得特征值进行评价信息集结,最终得到权重比:
Result=[0.246 0.754]
结果说明:其中药物黄芪毒性占比0.246,附子占比0.754,附子相比较黄芪占比更高,评价结果是附子毒性相对毒性更强,更不安全。
3 讨论
本文研究探讨了药食两用中药AHP安全性评价方法的构建,对药食两用中药安全性评估有一定的参考价值,本次新型冠状病毒肺炎预防处方中,药食两用中药被广泛的应用,对药食两用中药安全性的研究是保障使用人群的基础。
目前,针对药食两用中药安全性体系的研究少,本文在该方面做出尝试,提供一种中医药+计算机交叉学科、“药物-分子-人体”多层面信息融合,开展药食两用中药安全性综合评价的创新思路。本研究借鉴了管理科学领域的层次分析法、Python语言构建的药食两用中药安全性评价方法,对药食两用中药进行安全性比较。
构建药食两用中药安全性评价方法的思路,设计了药食两用中药AHP安全性评价模型。首先确立了三层次四指标,三层次是指药食两用中药AHP安全性评价模型中的“选择层-决策层-目标层”,也是指中药六位一体理论体系结构中的“药物-分子-人体”;四指标是指文献调研以及专家讨论的形式,确立了以半数致死量(LD50)、类药性(DL)、口服生物利用度(OB),以及临床不良反应数为安全性评价结构的决策层指标。
本研究为药食两用中药安全性评价提供原始数据,构建了主客观结合评价药食两用中药的思路,AHP层次分析+药食两用中药安全性评估的方法,开拓了创新性[19]。其中,研究结论可以为使用人群提供有益参考,以及相关科研人员研究药食两用中药提供部分决策依据。
本文的研究有一定的适用价值,但也存在局限性:(1)药食两用中药安全性评价数据参考了保健类、中药类分析结果[20-21],但相关中文文献质量不高,对研究设计方案、评价方法等缺乏详细的描述,各个相应数据库中的实验遵循指标不相同,数据值有所差异,这种不一致造成了统计上的误差与困难。(2)药食两用中药AHP安全性评价指标选取仅停留在“药物-分子-人体”层面,对早期毒理学(细胞层面)、常规毒理学(组织、器官、动物)层面未充分考虑。
综上所述,下一步的工作将从以下几个方面开展:第一,提高药食两用中药安全性评价分析结果的质量、去选择准确权威的评价指标和数据源;第二,开发自动化的药食两用中药安全性评价软件,增大实践性;第三,现国家卫健委公布有101种药食两用中药品种名单,应该扩建数据集提高信息覆盖的范围,满足大批量多品种药食两用中药源料的评价需求。
