基于磁性分子印迹材料的荧光分光光度法测定血液中同型半胱氨酸的含量
2022-10-21信建豪侯巧芝王聪颖张利娟
信建豪,侯巧芝,王聪颖,张利娟,张 蒙
(黄河科技学院 医学院,郑州 450063)
同型半胱氨酸(Hcy)是甲硫氨酸代谢过程中形成的一种非必需的含巯基氨基酸,血液中Hcy浓度水平升高会引起血管功能障碍,导致动脉硬化、心脑血管等疾病[1-2]。目前临床测定Hcy含量大多依赖于色谱-质谱法和免疫分析法[3-5],但这些方法都涉及繁琐的分析过程以及昂贵的试剂和仪器。分子印迹技术具有成本低、分析快速、选择性好、毒性低且模板分子可回收利用等优点[6-8],在分离检测[9]、仿生传感器[10]、食品安全[11]等领域显示出强大的发展潜力。本课题组曾用制备的分子印迹聚合物微球分离血液中的Hcy,采用紫外分光光度法进行检测,但其灵敏度未达到实际样品的检测要求[12]。因此,本工作在前期研究的基础上,通过优化工艺条件,制备了磁性分子印迹材料,用于吸附血液中的Hcy,然后选择灵敏度高、成本低的荧光分光光度法测定Hcy的含量,以该方法代替免疫分析法,对诊断高Hcy血症的相关疾病具有重要意义。
1 试验部分
1.1 仪器与试剂
L9型紫外-可见分光光度计;970CRT型荧光分光光度计;FA1004型电子分析天平;E30-H型电动搅拌器;Quanta FEG250型扫描电子显微镜(SEM)。
Hcy标准储备溶液:1 000 mg·L-1,准确称取DL-Hcy标准品0.1 g,用0.1%(质量分数,下同)氢氧化钠溶液溶解后,转移至100 mL容量瓶中,定容。
乙二醇二甲基丙烯酸酯、3-(异丁烯酰氧)丙基三甲氧基硅烷、硅酸四乙酯、α-甲基丙烯酸、N-(1-芘基)马来酰亚胺标准品的纯度均不小于97%;所用氨基酸标准品的纯度均为98%;其余试剂均为分析纯;试验用水为蒸馏水。
1.2 试验方法
1.2.1 Hcy纳米磁性分子印迹材料的制备
精密称取六水合三氯化铁11.626 g和四水合二氯化亚铁4.351 g于三颈烧瓶中,加入水200 mL,室温下用电动搅拌器以600 r·min-1速率搅拌10 min后,加入氨水30 mL,充入氮气,于62℃水浴加热下搅拌180 min,得到褐色沉淀。用磁铁吸附分离沉淀,再分别用水和乙醇多次洗涤,真空干燥后,得到Fe3O4纳米磁芯。
精密称取Fe3O4纳米磁芯1.609 g,加入乙醇80 mL和水8 mL,超声15 min,缓慢加入硅酸四乙酯4 mL和氨水5 mL,室温下用电动搅拌器以400 r·min-1速率搅拌12 h,产物经磁铁分离,分别用2.5 mol·L-1盐酸溶液和水洗除杂质,真空干燥,得到Fe3O4-@SiO2颗粒。
精密称取Fe3O4-@SiO2颗粒1.003 g,加入甲苯200 mL和3-(异丁烯酰氧)丙基三甲氧基硅烷20 mL,在氮气氛围下于70℃以400 r·min-1速率搅拌12 h,经磁铁分离后,用水多次洗涤,真空干燥,得到Fe3O4-@SiO2-@C=C磁珠。
精密称取Fe3O4-@SiO2-@C=C磁珠0.507 g,α-甲基丙烯酸0.223 g和DL-Hcy标准品0.117 g于三颈烧瓶中,加入乙醇80 mL,于62℃水浴以600 r·min-1速率搅拌12 h,再加入乙二醇二甲基丙烯酸酯1.144 g和偶氮二异丁腈0.010 g,超声15 min,在氮气氛围下继续搅拌24 h。反应结束后,用磁铁分离产物,并真空干燥。
以0.1%氢氧化钠溶液为洗脱液,对上述产物进行洗脱,每隔1 h洗脱一次,至洗脱液在213.5 nm处的吸光度接近0,真空干燥,即得Hcy纳米磁性分子印迹材料。
1.2.2 Hcy纳米磁性分子印迹材料的性能研究
精密量取2 mL Hcy标准储备溶液于100 mL容量瓶中,加入磷酸盐缓冲溶液(pH 3.0)10 mL和Hcy纳米磁性分子印迹材料0.500 g,振荡10 min,用水定容,测定体系在213.5 nm处的吸光度,以考察Hcy纳米磁性分子印迹材料的吸附性能。采用磁铁分离后,加入磷酸盐缓冲溶液(pH 8.0)10 mL和水90 mL,振荡40 min,测定体系在213.5 nm处的吸光度,以考察Hcy纳米磁性分子印迹材料的释放性能。
1.2.3 样品分析
精密量取血液样品1 mL于10 mL容量瓶中,加入磷酸盐缓冲溶液(pH 3.0)1 mL和二硫苏糖醇2.0 mg,混匀,静置5 min,用水定容,再加入Hcy纳米磁性分子印迹材料0.100 g,振荡10 min,磁分离后弃去溶液,接着加入磷酸盐缓冲溶液(pH 8.0)1 mL和水9 mL,振荡40 min,磁分离后,在溶液中加入N-(1-芘基)马来酰亚胺2.4 mg,静置衍生10 min,以365 nm为激发波长,测定体系在378 nm处的荧光强度。
2 结果与讨论
2.1 Hcy纳米磁性分子印迹材料的SEM表征
采用SEM对制备的Hcy纳米磁性分子印迹材料进行表征,结果见图1。

图1 SEM图Fig.1 SEM diagram
由图1可知,该材料粒径约为40 nm。
2.2 Hcy纳米磁性分子印迹材料的性能研究
2.2.1 吸附、释放时间的选择
按照1.2.2节试验方法,绘制吸光度随吸附、释放时间变化的曲线,结果见图2。
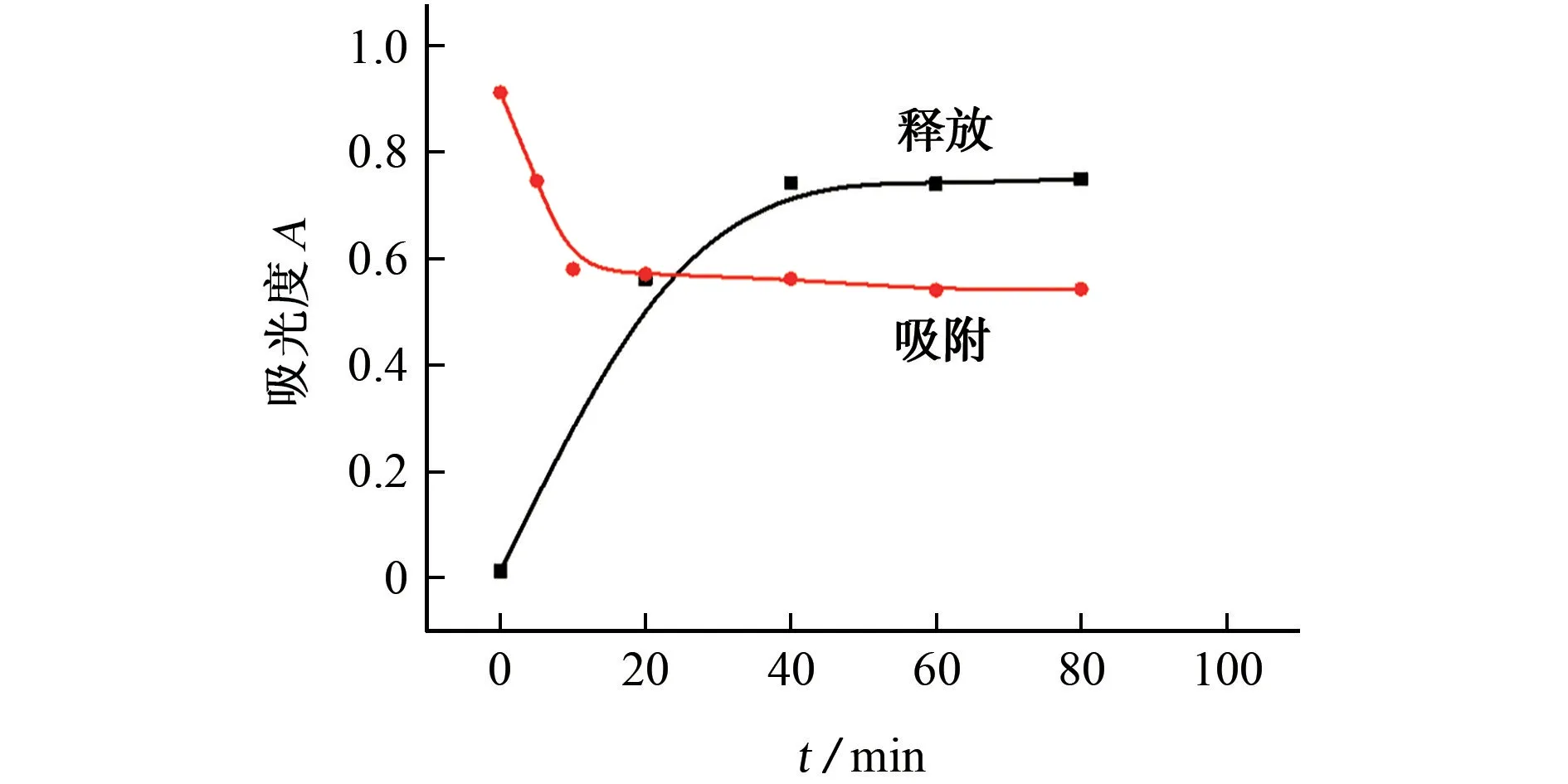
图2 吸附、释放时间对吸光度的影响Fig.2 Effects of the adsorption and release time on the absorbance
由图2可知:该材料与Hcy混合振荡10 min后,吸光度基本不变,即10 min时对Hcy的吸附达到平衡,因此选择吸附时间为10 min;磁分离后,当振荡释放40 min时,吸光度基本不变,因此选择释放时间为40 min。与之前研究相比[13],吸附时间显著缩短,可能是由于材料粒径在纳米级别,吸附速率较大。
2.2.2 吸附、释放时酸度的选择
按照1.2.2节试验方法,考察了吸附时酸度对吸光度的影响,结果见图3。
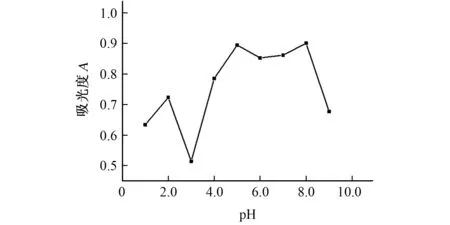
图3 酸度对吸光度的影响Fig.3 Effect of the acidity on the absorbance
由图3可知:当酸度为pH 3.0时,吸光度较小,说明此时Hcy磁性分子印迹材料的吸附量较大,因此选择吸附时的酸度为pH 3.0;当酸度为pH 8.0时,吸光度较大,说明此时材料对Hcy的吸附量较小,便于释放Hcy,因此选择释放时的酸度为pH 8.0。
2.2.3 Scatchard分析
根据Scatchard公式Q/ρ=Qmax/KD-Q/KD(式中,Qmax为最大表观吸附量,mg·g-1;KD为解离平衡常数;Q为实际吸附量,mg·g-1;ρ为Hcy质量浓度,g·L-1),以Q/ρ对Q进行拟合,结果得Q/ρ=-0.034 21Q+1.113,相关系数为0.996 4,则KD=29.4,Qmax=32.4 mg·g-1。
2.2.4 吸附选择性试验
将Hcy标准储备溶液换成相同浓度水平的其他氨基酸的单标准溶液,按照1.2.2节试验方法进行吸附。考察了共存的常见氨基酸对吸附的干扰情况。结果表明,该材料对Hcy的吸附量分别是L-半胱氨酸、L-赖氨酸、L-组氨酸、L-丙氨酸、L-色氨酸、L-天冬氨酸、L-脯氨酸、L-谷氨酰胺的19.3,23.8,31.6,243,213,31.7,39.7,33.4倍,并且振荡吸附10 min时对Hcy吸附明显,对其他8种氨基酸吸附可忽略。
2.2.5 使用次数的选择
按照1.2.2节试验方法分析Hcy磁性分子印迹材料使用1~8次时体系的吸光度,结果见图4。
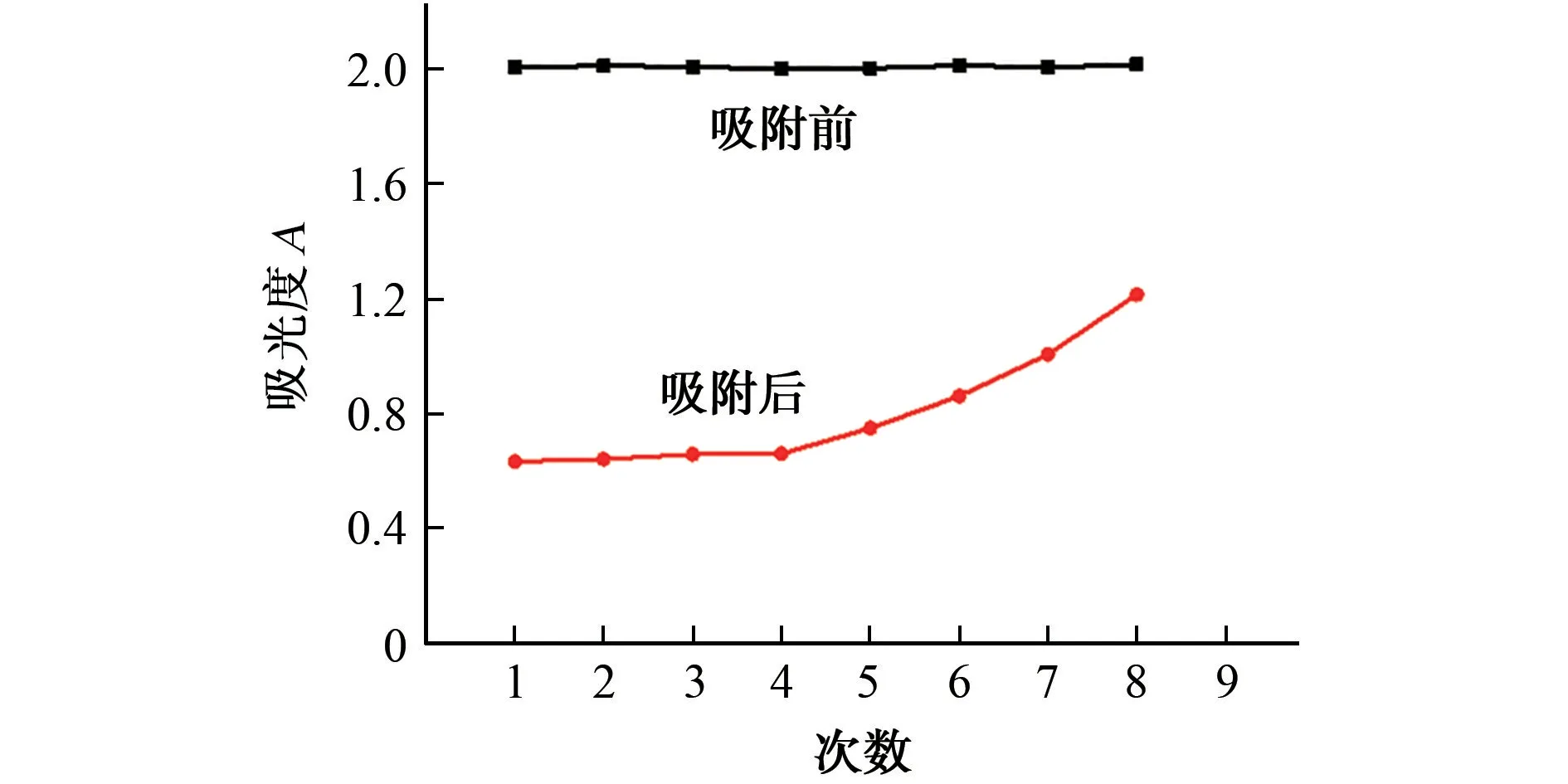
图4 使用次数对吸光度的影响Fig.4 Effect of the using times on the absorbance
由图4可知:该材料使用不超过4次时,吸附前后体系吸光度无明显变化;使用超过4次时,吸附后体系吸光度开始逐渐增大,表明该材料最多可重复使用4次。
2.3 Hcy测定条件的选择
2.3.1 荧光发射光谱图
以365 nm为激发波长,绘制Hcy的荧光发射光谱图,结果见图5。
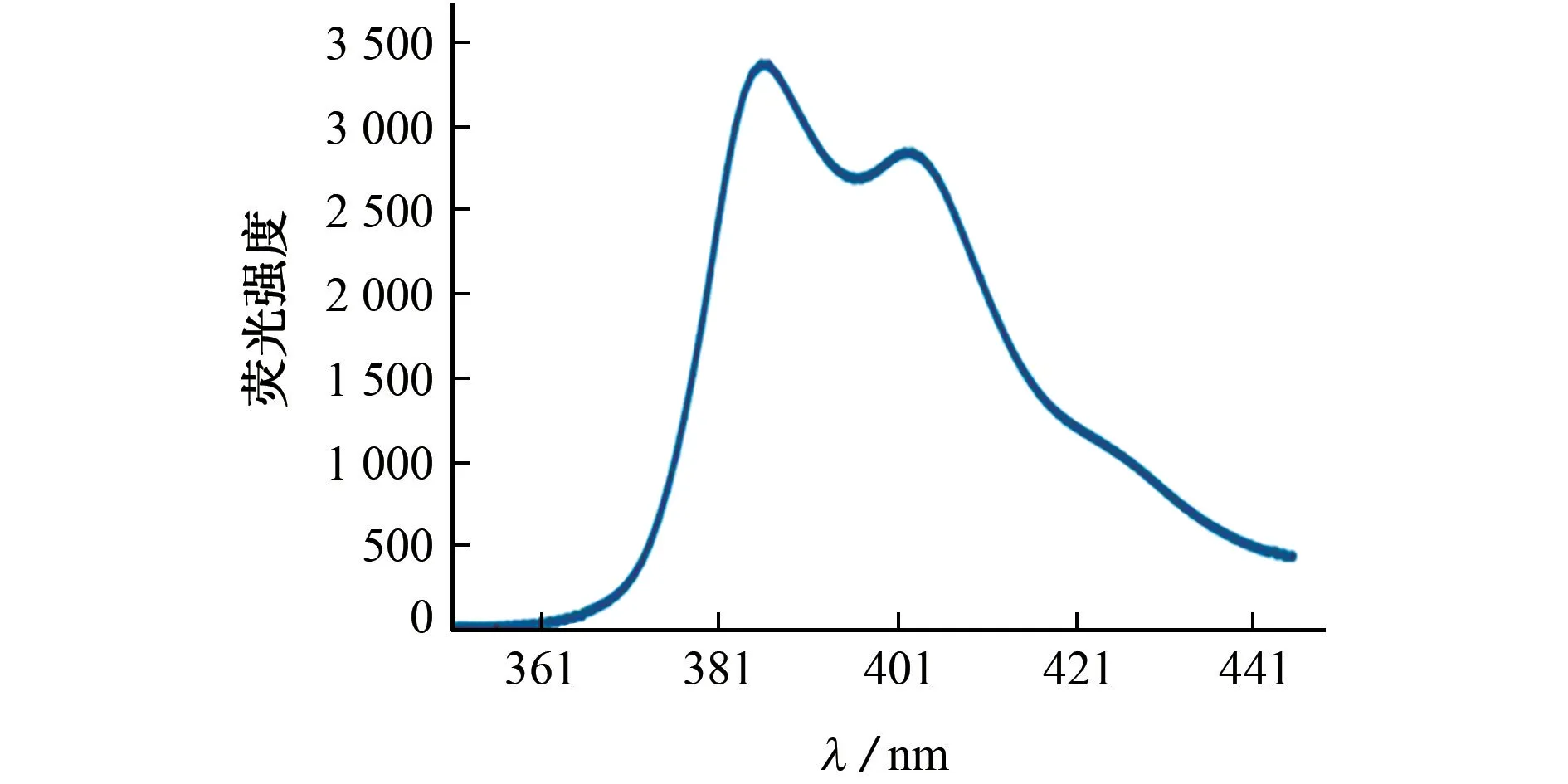
图5 Hcy的荧光发射光谱图Fig.5 Fluorescence emission spectrum of Hcy
由图5可知,Hcy在波长387 nm处有特征发射峰,因此试验测定体系在387 nm处的荧光强度。
2.3.2 酸度
分别用pH 7.5,8.0,8.5,9.0,9.5,10.0的磷酸 盐缓冲溶液配制6份0.04 mg·L-1Hcy标准溶液,各加入N-(1-芘基)马来酰亚胺2.4 mg,考察了酸度对Hcy荧光强度的影响,结果见图6。
由图6可知:在pH 8.0时,Hcy荧光强度最大,pH低于或高于8.0时,Hcy荧光强度均会降低,结合Hcy释放时酸度的选择,最终确定测定Hcy时的体系酸度也为pH 8.0。
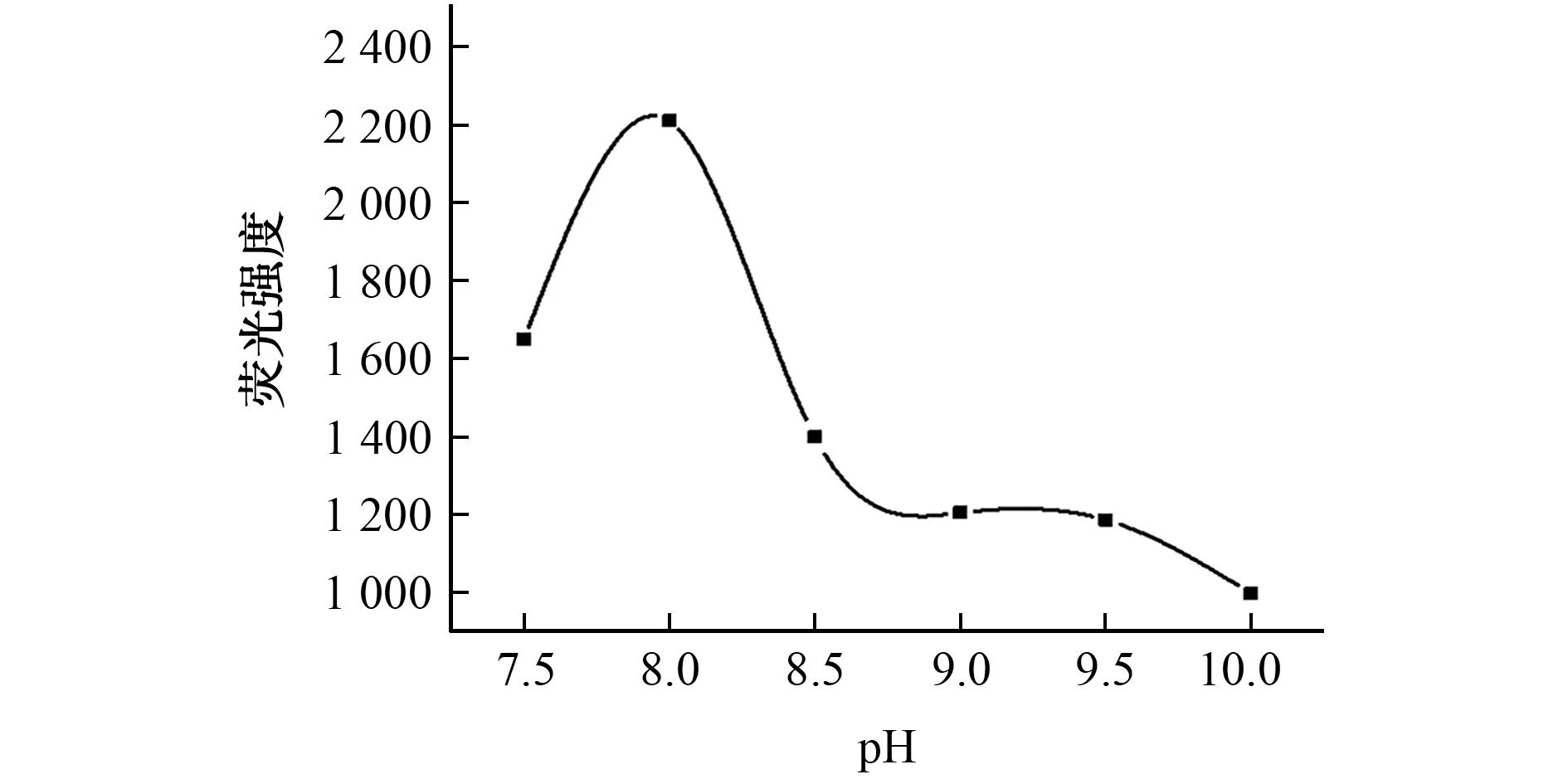
图6 酸度对Hcy荧光强度的影响Fig.6 Effect of the acidity on the fluorescence intensity of Hcy
2.3.3 衍生时间
用磷酸盐缓冲溶液(pH 8.0)配制0.04 mg·L-1Hcy标准溶液,加入2.4 mgN-(1-芘基)马来酰亚胺,在静置衍生1,5,10,15,20 min时用荧光分光光度计测定,结果见图7。
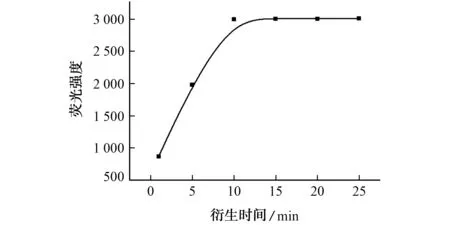
图7 衍生时间对Hcy荧光强度的影响Fig.7 Effect of the derivative time on the fluorescence intensity of Hcy
由图7可知,衍生反应10 min后,体系荧光强度基本不变,因此选择衍生时间为10 min。
2.4 标准曲线和检出限
用磷酸盐缓冲溶液(pH 8.0)配制0.02,0.04,0.06,0.08,0.10 mg·L-1Hcy标准溶液系列,各加入2.4 mgN-(1-芘基)马来酰亚胺,静置衍生10 min,以体系在387 nm处的荧光强度对Hcy质量浓度进行线性回归。结果显示,Hcy质量浓度在0.02~0.10 mg·L-1内与其对应的荧光强度呈线性关系,线性回归方程为y=3.559×104x+2.538×103,相关系数为0.999 6。
对空白样品溶液连续测定11次,以3倍标准偏差与稀释因子的乘积计算检出限,结果得检出限为0.008 mg·L-1。
2.5 精密度和稳定性试验
按照试验方法对0.04 mg·L-1Hcy标准溶液重复测定5次,计算测定值的相对标准偏差(RSD)。结果显示,测定值的RSD为1.8%,表明该方法的精密度较好。
接着将0.04 mg·L-1Hcy标准溶液静置衍生30,60,90,120,150,180 min,然后测定体系的荧光强度。结果得测定值的RSD为3.8%,表明Hcy在180 min内较稳定。
2.6 回收试验
取5只成年家兔,用静脉采血针取血,然后用血细胞过滤器过滤,按照1.2.3节试验方法对兔血中Hcy含量进行测定。结果发现,兔血中均未检出Hcy。
对上述空白样品进行加标回收试验,计算回收率,结果见表1。
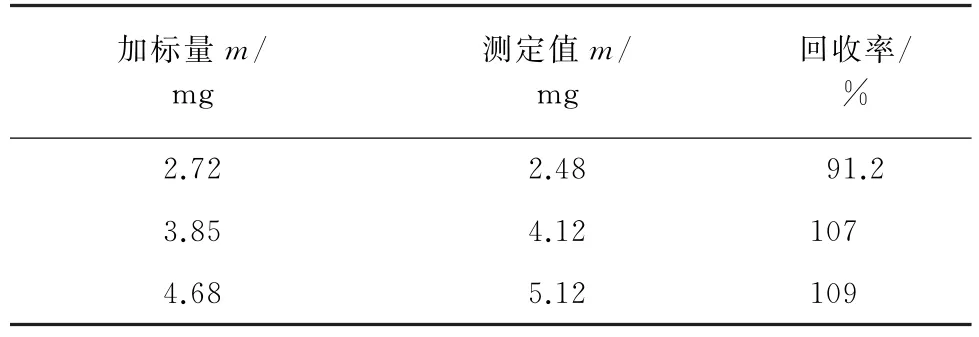
表1 回收试验结果Tab.1 Results of test for recovery
由表1可知,Hcy的回收率为91.2%~109%,方法准确度满足临床分析的要求。
本工作提出了一种基于磁性分子印迹材料的荧光分光光度法测定血液中Hcy含量的方法。该方法分析快速、精密度和稳定性好、准确度高,满足临床分析的要求,所制备的磁性分子印迹材料可替代临床分析中常用的免疫物质,降低了检测成本。
