松香酸钠理化性质及油水分配系数的测定*
2022-10-21刘满军石会丽
刘满军,石会丽,陈 昊,杜 君,高 蓉
(陕西省中医医院,陕西 西安 710018)
从上世纪70年代开始,以松香为原料加工制成的银屑平片在我院皮肤科临床应用至今,经几代临床大夫及药学科研工作者不懈努力,不断改进,使毒副作用不断降低,证明疗效愈来愈确切。通过研究认为活性成分是松香酸,但由于其性质不稳定,药品放置之后,松香酸会产生诸多变异成分,而引起病人恶心、呕吐等不良反应,这样会中断病人服药,引起疾病反复,不仅对病人产生影响,还造成药物浪费。以上原因一直影响着这一药物在临床的推广应用,为此,设想将松香提取松香酸,并通过化学合成制备成稳定性较好的钠盐,再制成直接作用于皮肤的凝胶剂或者口服制剂。因药物的理化性质与其生物膜的渗透性存在着相关性,所以这种相关性有助于预测药物动力学性质,并为剂型设计提供指导[1]。但目前,尚未见测定松香酸钠的油水分配系数和平衡溶解度等理化性质的文献报道,本文旨在通过采用摇瓶法[2-6]和HPLC法测定松香酸钠[7]在不同pH值条件下的平衡溶解度和油水分配系数来推测松香酸钠的体内与皮肤吸收过程,并为其开发新剂型制剂设计提供依据。
1 实验部分
1.1 仪器与试剂
LC-16型高效液相色谱仪(日本岛津);LC-16型泵;SIL-16型进样器;SPD-16型紫外-可见检测器;CTO-16L型柱温箱;DGU-20A型脱气机;Lab-Solution化学工作站;BSA224S型电子天平(上海梅特勒-托利多仪器有限公司);KQ-250DE型数控超声波清洗器(昆山禾创仪器有限公司);DELTA-320型pH计(瑞士Mettler Toledo公司);SHA-BA型水浴恒温振荡器(常州市中贝仪器有限公司)。
松香酸钠原料(自制,批号:20201101,纯度99.0%);松香酸钠对照品(自制,批号:20201201,纯度99.82%);H3PO4(国药化学试剂有限公司);KH2PO4、K2HPO4,西安化学试剂厂;Na2HPO4(天津市科密欧化学试剂有限公司);NaH2PO4、乙醇、丙酮、甲醇、乙酸乙酯、正丁醇、正辛醇,天津市天力化学试剂有限公司;NaOH(汕头市西陇化工厂);HCl、氯仿,四川西陇科学有限公司;NaCl(重庆北碚精细化工厂);30%H2O2,河北建宁药业有限公司,以上试剂均为分析纯;水为纯化水。
1.2 方法与结果
1.2.1 溶液的配制
(1)缓冲液的配制 根据中国药典2020版第四部通则8004[8],配制pH值分别为1.2、2.0、5.0、6.8、7.0、7.4、8的磷酸盐缓冲溶液。
(2)松香酸钠对照品溶液配制 精密称取松香酸钠对照品3.78mg,于50mL的量瓶中,加甲醇溶解,超声10min,定容至刻度,制得75.6μg·mL-1储备溶液,备用。
(3)松香酸钠原料储备溶液配制 精密称取松香酸钠原料10.520mg,于100mL的量瓶中,加甲醇溶解,超声10min,定容至刻度,制得105.2μg·mL-1储备溶液,备用。
1.2.2 色谱条件及系统适用性
色谱柱 岛津Shim-pack GISS C18,(250mm×4.6mm,5μm);流动相:乙腈-0.1%甲酸(60∶40);检测波长:241nm;流速:1.0mL·min-1;柱温:30℃;进样量:10μL。色谱图见图1。

图1 松香酸钠HPLC色谱图Fig.1 HPLC chromatograms of rosin acid sodium
2 结果与讨论
2.1 方法学考察[9]
在上述色谱条件下,流动相和不同pH值缓冲溶液均对松香酸钠的含量测定无干扰。松香酸钠浓度(X)在1.512~378.0μg·mL-1浓度范围与峰面积(Y)线性关系良好,线性回归方程为Y=42659283.50X-102043.18,R2=1.00;将标准曲线末端浓度的样品逐步稀释进样,信噪比(S/N)=3.03时的浓度(8.2ng·mL-1)为检测限,信噪比(S/N)=10.8时的浓度(27.47ng·mL-1)为定量限;低、中、高浓度(37.8、75.6、151.2μg·mL-1)对照品溶液测定结果的RSD分别为0.56%、1.21%、0.99%,说明本方法仪器精密度良好;按照制备标准曲线溶液的方法制备高、中、低(154.0、75.0、9.8μg·mL-1)3个浓度的松香酸钠溶液各3份,测定值与真实值的比值即为回收率。平均回收率为100.03%,RSD为1.92%(n=9)。
2.2 松香酸钠原料样品的含量测定
分别精密称取3份样品,制得含量约50μg·mL-1的甲醇溶液,按1.2项下色谱条件,进样10μL,记录峰面积,以线性方程计算含量,结果均值为99.0%(n=3)。
2.3 松香酸钠在不同溶剂中平衡溶解度的测定
分别精密吸取5mL的不同溶剂(水、0.9%的生理盐水、pH值分别为1.2、2.0、5.0、6.8、7.0、7.4的缓冲液,甲醇、乙醇、丙酮、正丁醇、乙酸乙酯、三氯甲烷),于10mL具塞试管中,加适量松香酸钠药粉末至溶液出现大量不溶性白色粉末,超声处理30min使充分湿润后,将此试管口密封,置于(37±0.5)℃恒温水浴振荡器中(转速150r·min-1),振摇48h,使形成平衡的过饱和溶液;离心(3000r·min-1、10min)后,取上层溶液,用0.45μm微孔滤膜过滤后,用相应的溶媒稀释10倍,进样10μL,按2.2项下色谱条件测定,记录峰面积,计算,得出松香酸钠在水等不同溶剂中的平衡溶解度。平行测定3次,取平均值,结果见表1。

表1 不同溶剂中松香酸钠平衡溶解度测定结果(x±s,n=3)Tab.1 Determination results of rosin acid sodium equilibrium solubility in different solvents(x±s,n=3)
由表1可知,松香酸钠在不同溶剂中的平衡溶解度有很大差异,其大小排序在有机相中为:甲醇>乙醇>正丁醇>丙酮>乙酸乙酯>氯仿;在水相中为:0.9%生理盐水>水>pH值6.8缓冲液>pH值7.0缓冲液>pH值7.4缓冲液>pH值1.2缓冲液>pH值5.0缓冲液>pH值2.0缓冲液。
2.4 松香酸钠稳定性影响因素实验考察[8]
2.4.1 高温试验 依据2020版药典四部通则9001《原料药物与制剂稳定性试验指导原则》,称取适量松香酸钠粉末适量,置于培养皿中,摊成小于5mm厚的薄层,敞口分别放置于在电热鼓风干燥箱中,70℃加热一定时间。精密称取加热后样品一定量3份,用甲醇定容,超声处理10min使充分溶解,配制成约40μg·mL-1的溶液,用0.45μm的微孔滤膜过滤,取续滤液进样10μL,按2.2项下色谱条件测定,记录峰面积,计算。将测定值与称量值进行比较。
2.4.2 强光试验 依据2020版药典四部通则9001,取适量松香酸钠粉末,同上,将摊好样品培养皿敞口置于稳定性实验箱中,用强光(5000Lx)照射一定时间之后,精密称取照射后的样品3份,配成约40μg·mL-1的甲醇溶液,以下同“高温试验”项下。
2.4.3 氧化试验[9]精密吸取105.2μg·mL-1松香酸钠储备溶液1mL和30%H2O21mL置10mL容量瓶中,充分混匀,室温放置1h,然后用甲醇稀释至刻度,摇匀备用。以下同“高温试验”项下。将测定值与储备液浓度进行比较。
2.4.4 强酸破坏试验[9]精密吸取105.2μg·mL-1松香酸钠溶液1mL和6.0M HCl 1mL置10mL容量瓶中,充分混匀,室温放置1h,然后用NaOH 6.0M中和,最后用甲醇稀释至刻度,以下同“高温试验”项下。
2.4.5 强碱破坏实验[9]精密吸取105.2μg·mL-1松香酸钠溶液1mL和6.0M NaOH 1mL置10mL容量瓶中,充分混匀,室温放置1h,然后用6.0M HCl中和,最后用甲醇稀释至刻度,以下同“高温试验”项下。
2.4.6 稳定性实验结果 对于以上不同影响因素下的实验结果,归纳总结见表2。

表2 不同影响因素下松香酸钠的稳定性试验结果(n=3)Tab.2 Stability test results of rosin acid sodium under different influencing factors(n=3)
由表2可知,影响稳定性的因素由大到小排序:强碱>氧化剂>高温>光照>强酸。含量依次下降21.16%、16.35%、13.64%、9.82%、9.41%。
2.5 松香酸钠油水分配系数的测定[9-13]
油、水相选择 本实验选择正辛醇为油相,pH值分别为1.2、2.0、5.0、6.8、7.0、7.4、8.0的缓冲液及蒸馏水为水相。
饱和油、水相的制备 吸取pH值为1.2、2.0、5.0、6.8、7.4、8.0缓冲液及蒸馏水各15mL,分别于同体积的正辛醇混合,在恒温(37±0.5)℃下振摇48h,静置,分层备用。上层作为饱和油相,下层作为饱和水相。
水饱和油相松香酸钠饱和溶液的制备与浓度测定 精密吸取水饱和正辛醇溶液30mL,置具塞试管中,加入过量的松香酸钠,先超声30min,使充分湿润后,置恒温振荡器中,在恒温(37±0.5)℃下振摇48h,取出、离心10min(3000r·min-1),上清液经0.45μm微孔滤膜过滤,取续滤液,稀释5倍,按2.2项下色谱条件测定,进样10μL,记录峰面积,用标准曲线计算松香酸钠在水饱和正辛醇的浓度C0。
油水分配系数测定 精密吸取含松香酸钠的水饱和正辛醇溶液2mL,8份,分别置5mL具塞试管中,分别加入2mL正辛醇饱和的水及正辛醇饱和的pH分别为1.2、2.0、5.0、6.8、7.0、7.4、8.0的缓冲液,将口密封后的试管放入恒温水浴振荡器中,在恒温(37±0.5)℃下振摇48h,取下层水相,0.45μm微孔滤膜过滤,取续滤液10μL进样,按1.2项下色谱条件分析测定,依标准曲线计算松香酸钠分配平衡时水相浓度Cw,依据P=(C0-Cw)/Cw计算油水分配系数。结果见表3。
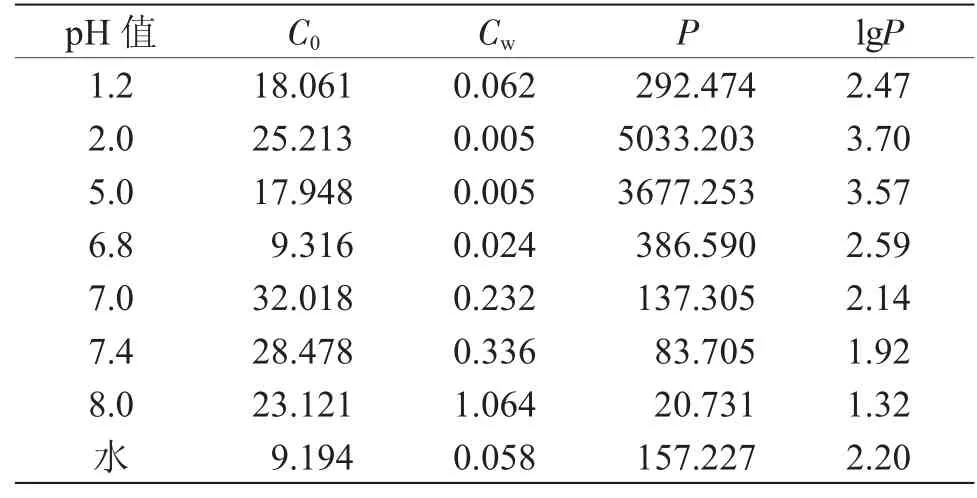
表3 松香酸钠正辛醇在不同pH值溶液中油水分配系数(37℃,n=3)Tab.3 Oil-water partition coefficient of rosin acid sodium in the different pH value solution of octyl alcohol(37℃,n=3)
图2为松香酸钠在37℃正辛醇的不同pH值溶液中油水分配系数。

图2 松香酸钠在37℃正辛醇的不同pH值溶液中油水分配系数Fig.2 Oil-water partition coefficient of rosin acid sodium in 37℃octyl alcohol in different pH value of the solution
由表3、图2可知,在水及pH值为1.2~8.0的磷酸缓冲液介质中,松香酸钠的lgP均大于0,说明其在油相中的溶解度大于水相中的溶解度,表明其具有良好的脂溶性。
3 结论
首次建立了松香酸钠的HPLC分析方法,本方法快速、简单、灵敏度高、精密度、重复性和回收率均符合法规要求,表明该测定方法可行。
松香酸钠的相关物料保存时,应密闭、避光、低温、避强酸强碱及氧化剂。
查阅文献[13,14],测定油水分配系数的方法有:摇瓶法、HPLC法、产生柱法和薄层色谱法等,但属摇瓶法是最为简单,用时短,结果准确,故选用摇瓶法测定。正辛醇与多数有机溶液极性相似,其溶解度参数与生物膜参数一致,可以选用其作为模拟生物膜相的有机溶剂,故选用正辛醇-水体系测定油水分配系数(lgP),结果可知,松香酸钠的lgP随着pH值的增大而减小,将其制成经皮给药制剂时,必须对其供药体系的pH值进行调节,使之具有更好的透皮效果。随着pH值的升高,脂溶性先增大,后减小;当pH值在2~5时达到最大,理论上应该与胃、十二指肠pH值较为接近,提示松香酸钠在十二指肠内可被吸收。
平衡溶解度和油水分配系数与在机体内的溶解、吸收、分布、转运及代谢等过程紧密相关,是体现药物透过生物膜能力的重要参数,对预测药物在皮肤及体内的吸收具有重要意义[14]。因此,本次测定松香酸钠平衡溶解度和油水分配系数,作为新制剂设计时参考。
