低温条件下氯化铌催化果糖有效转化制5-羟甲基糠醛*
2022-10-21王紫微贾松岩
张 恒,王紫微,贾松岩
(沈阳化工大学 化学工程学院,辽宁 沈阳 110142)
我国于2021年正式发布了“碳达峰”和“碳中和”的重大决策,为今后的可持续发展指明了方向。生物质资源被认为是一种非常具有前景的清洁可再生能源,它可通过植物的光合作用将CO2回收与转化,具有“碳中和”属性[1]。以生物质提炼具有高附加值的化学品是未来化学工业的一个重要发展方向。
近20年来,利用生物质转化制备5-羟甲基糠醛(5-HMF)的研究呈几何式增长。5-HMF是一种重要的化工中间体,通过催化氧化、还原、氨基化等处理可制备多种具有高附加值的化学品,为燃料、高分子、医药中间体等领域的替代产品开发提供了广阔的空间[2]。5-HMF可通过以果糖和葡萄糖为代表的生物质资源获得。因此,利用生物质催化合成5-HMF的工艺与“碳中和”以及可持续发展的理念相契合。
果糖是合成5-HMF最具代表性的生物质资源。以果糖制5-HMF较容易,在极性有机溶剂、水/有机溶剂双相体系、离子液体等体系中并在多种酸催化剂的作用下,均能获得较高的产物收率[3]。目前,关于果糖有效转化的研究多数反应条件仍然较为苛刻。近年来,一些研究组针对果糖在低温条件下有效转化制5-HMF取得了一些进展。例如,Jia等[4]在二甲基亚砜体系中采用P2O5与NiCl2为共催化剂,70℃下反应90min,果糖转化为5-HMF的收率为75%。Ray等[5]采用离子液体1-丁基-3-甲基咪唑氯化物(BMIMCl)体系,以P2O5为催化剂,在50℃下反应60min,5-HMF的收率为81%。Zhang等[6]在二甲基亚砜中加入BMIMCl,GeCl4为催化剂,果糖在25℃下反应12h,5-HMF的收率约为70%。结合“碳中和”与“节能”的背景,如何在更温和的条件下实现果糖转化将成为生物质资源高效利用领域的重要课题。
本研究通过催化剂筛选,考察反应影响因素,开展对比实验等研究了果糖在低温下有效转化为5-HMF的反应性能和可能的反应机理,也探索了菊糖的低温转化,为生物质的综合利用提供了有效参考。
1 实验部分
1.1 试剂及仪器
果糖、菊糖、AlCl3·6H2O、ZnCl2、HfCl4、FeCl3、NbCl5、ScCl3·6H2O、TaCl5、CuCl2·2H2O、ZrCl4、CrCl3·6H2O、WCl6、1,3-二羟基丙酮、Nb(OH)5,阿拉丁试剂有限公司;甘油、乙二醇、SnCl4·5H2O、P2O5、二甲基亚砜(DMSO),国药集团化学试剂有限公司;离子液体1-丁基-3-甲基咪唑氯化物(BMIMCl),中国科学院兰州化学物理研究所,以上试剂均为分析纯。
DBS-100型恒温摇匀仪(群安实验仪器有限公司);LC-16型高效液相色谱(HPLC,配RID-20型示差检测器,日本岛津公司);TS-DI10-L/h超纯水设备(陶氏水处理设备工程有限公司)。
1.2 典型实验步骤
称量30mg果糖和催化剂(果糖摩尔量的15%),加入到容积为2mL的反应瓶中,再加入500μL DMSO,密封反应瓶后将其置入恒温摇匀仪,在设定的温度下反应,转速为600r·min-1。达到预设的时间后,取出反应瓶冷却。向反应瓶中加入一定量甘油作为内标物,加水稀释后的样品采用HPLC分析。每个实验均经过平行重复验证。由于二羟基丙酮与甘油在HPLC中的保留时间接近。为此,一些特定对比实验采用乙二醇作为内标物。
1.3 分析方法
HPLC中使用的分析柱和保护柱为安捷伦公司的Hi-Plex H型色谱柱(300mm×7.7mm,8μm)和Hi-Plex H型色谱柱(50mm×7.7mm,8μm),流动相为0.005mol·L-1的H2SO4水溶液,流速为0.65mL·min-1。柱温箱温度设定为65℃,检测器温度设定为50℃。
2 结果与讨论
2.1 果糖低温转化合成5-HMF的催化剂筛选
以一系列金属氯化物作为果糖低温转化的催化剂进行筛选。预设的反应温度为50℃,催化剂的用量为果糖摩尔量的25%,反应时间为180min,果糖转化制5-HMF的反应性能见图1。

图1 不同催化剂催化果糖转化为5-HMF的转化率Fig.1 Conversion rate of fructose into 5-HMF with different catalysts
由图1可知,采用AlCl3·6H2O、ZnCl2、FeCl3、ScCl3·6H2O、CuCl2·2H2O以及CrCl3·6H2O为催化剂时,没有5-HMF生成。虽然文献报道这些催化剂在较高温度下具有促进六碳糖转化为5-HMF的活性[7-10],但它们在低温条件下尚无法催化果糖转化。分别采用HfCl4、SnCl4·5H2O和TaCl5为催化剂时,有少量5-HMF生成。NbCl5、ZrCl4和WCl6作为催化剂展示出较高的催化活性。相比而言,NbCl5展示出更为优异的催化活性,在上述条件下,果糖的转化率为98%,5-HMF的收率为70%。因此,NbCl5被选为适宜的催化剂进行后续研究。
2.2 反应因素对果糖低温转化合成5-HMF的影响
2.2.1 催化剂用量和果糖加入量的影响 图2探究了反应温度为50℃,反应时间为180min时,NbCl5用量和底物用量对果糖转化的影响。
由图2a可知,当加入NbCl5的量为果糖摩尔量的10%时,果糖的转化率与5-HMF的收率分别为65%和48%,与空白实验对比显示出明显的催化活性。当NbCl5的用量提升到果糖摩尔量的15%及以上时,果糖转化率与5-HMF收率不再明显提高,接近达到最高值,因此,该用量被选为优化参数进行后续研究。图2b探究了不同果糖初始加入量对反应转化率的影响。由于是单因素调变果糖加入量,NbCl5的加入量随果糖加入量的变化而变化,而溶剂量并没有改变。因此,当果糖加入量较低时,催化剂的实际浓度也较低,导致反应性能发生下降。随着果糖加入量的增加,反应性能明显提升,但进一步增加果糖的加入量也会导致5-HMF的收率下降,这可能由于果糖浓度过高或催化剂浓度过高而引发果糖与5-HMF或5-HMF分子间发生了缩聚等副反应[11]。因此,选用的果糖加入量为30mg是较为合适的。
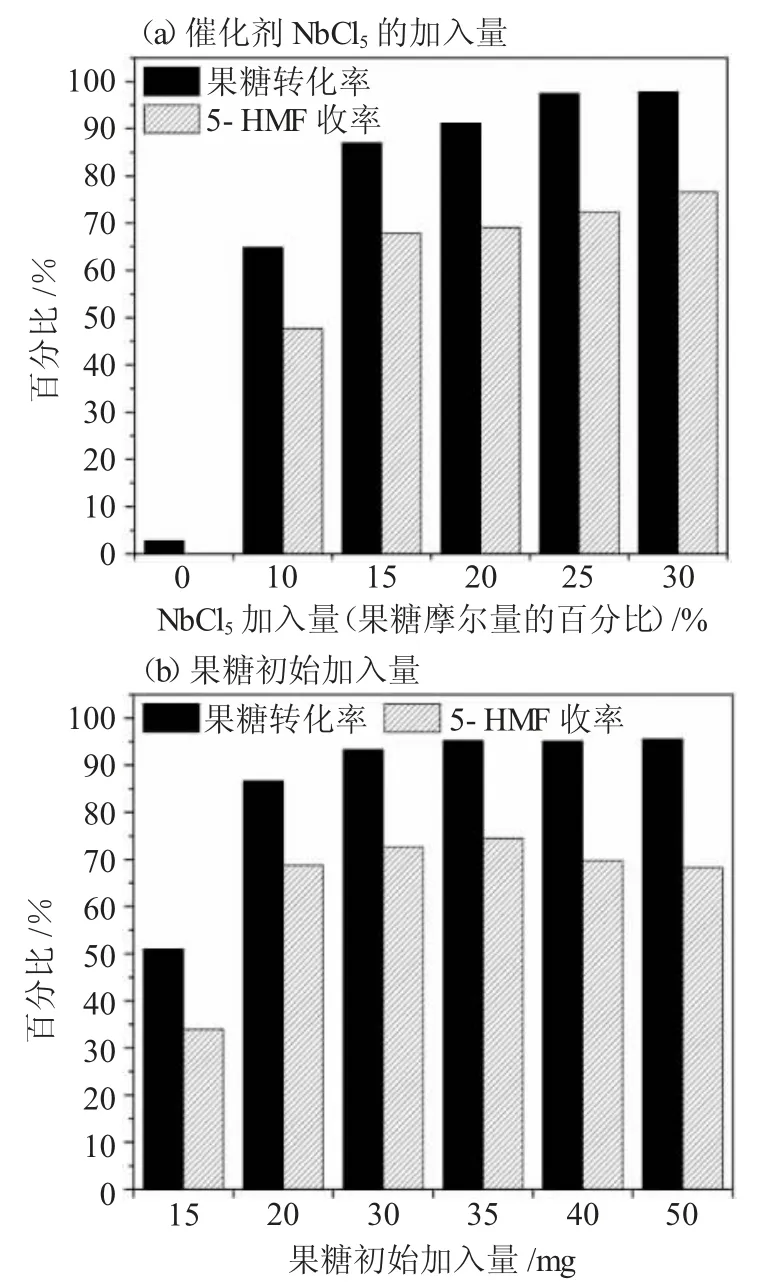
图2 催化剂NbCl5和果糖初始加入量对反应转化率的影响Fig.2 Effect of NbCl5 catalyst loading(a)and initial dosage of fructose on the reaction performance
2.2.2 共催化剂和共溶剂的影响 为提高果糖低温转化的反应性能,考察了共催化剂与共溶剂的影响。据文献报道,当采用P2O5与一些金属氯化物作为共催化剂时,果糖在DMSO中转化为5-HMF的性能明显提升[4]。为此,预期P2O5也能对NbCl5催化果糖转化具有影响。
图3为添加物P2O5和离子液体BMIMCl对果糖转化率的影响。
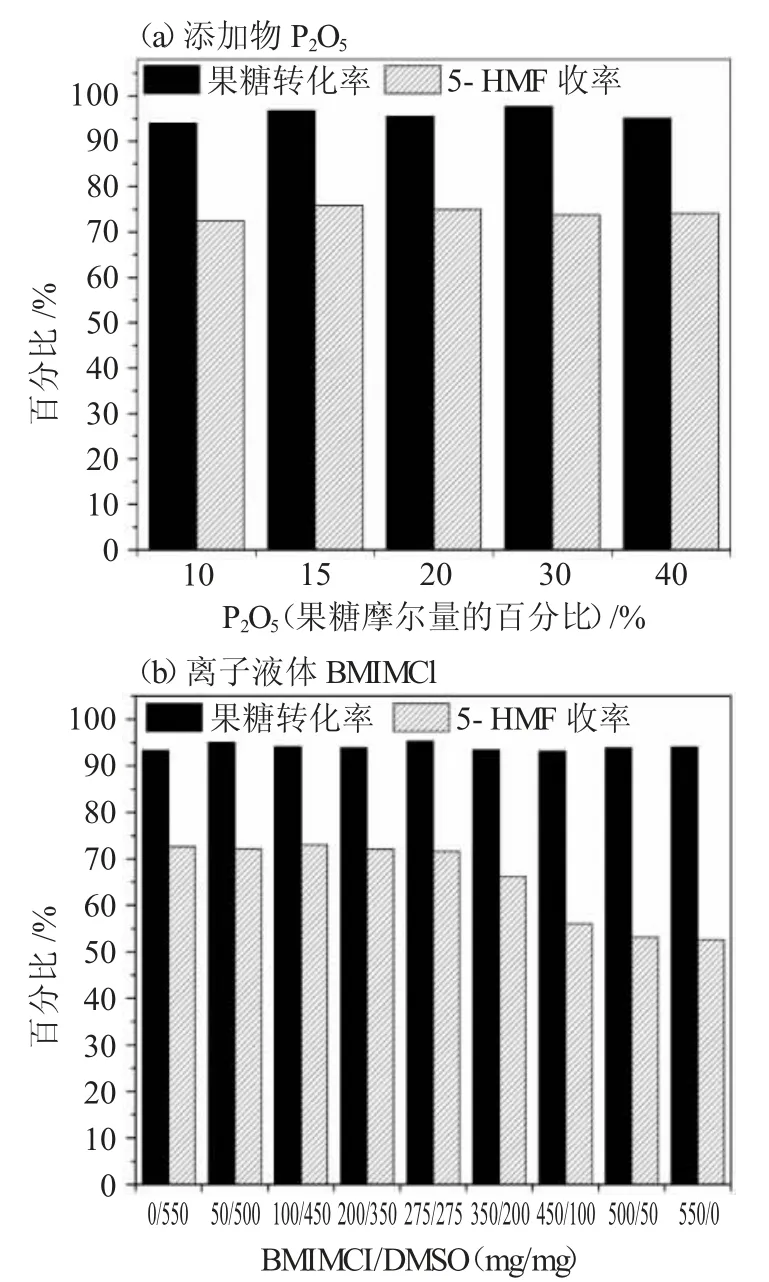
图3 添加物P2O5和离子液体BMIMCl对果糖转化率的影响Fig.3 Effect of P2O5 and ionic liquid BMIMCl additives on the conversion of fructose
由图3a可知,反应在50℃下进行,反应时间为180min,调变P2O5的加入量并未对果糖的转化产生明显影响,说明NbCl5催化果糖转化的原理可能与上述文献报道的不同。Zhang等[6]报道在DMSO中加入一定量的离子液体BMIMCl可以提高果糖在低温下转化的性能。图3b显示在DMSO与BMIMCl按不同质量比例组成的共溶剂体系中NbCl5催化果糖转化的反应性能。随着BMIMCl所占比例的升高,5-HMF的收率出现一定程度的下降,这与Zhang等报道的结果不同,推测是由于BMIMCl的加入量较多会导致反应体系在较低温度下搅拌不均所致。
2.2.3 反应温度和反应时间的影响 为优化反应性能并探究NbCl5能否在更低的温度下催化果糖转化,研究了反应温度和反应时间的影响,见图4。
由图4可知,果糖转化率和5-HMF收率的最高值可在50℃获得,分别约为100%和75%。NbCl5在40℃也能有效地催化果糖转化,但当反应温度进一步降低时,反应速率大幅下降。果糖转化为5-HMF是较强的吸热反应,这可以解释反应温度对果糖转化的影响[12]。

图4 反应温度和反应时间对果糖转化为5-HMF的影响Fig.4 Effect of reaction temperature and time on the conversion of fructose into 5-HMF
2.3 反应机理分析
为研究果糖与催化剂的作用机理,开展了一些对比实验。NbCl5可能与反应中生成的水或溶剂中含有的微量水反应产生H+(Br nsted酸),并催化果糖转化。本工作以浓H2SO4作为Br nsted酸催化剂对比,结果见表1。

表1 对比实验结果Tab.1 Results for the contrast experiments
由表1可知,分别加入果糖摩尔量15%和20%的浓H2SO4时,5-HMF的收率分别为37%和45%,与NbCl5催化的结果相差较大;采用Nb(OH)5作为催化剂时,果糖几乎没有转化,结果表明,NbCl5并非完全通过产生的H+起催化作用。据文献报道,一些金属盐可通过阳离子的Lewis酸性对糖类转化起关键作用[13],据此推测NbCl5可能是通过Br nsted酸(H+)与Lewis酸(Nb5+)的协同作用催化果糖转化。果糖的链状结构可近似认为是一个甘油分子与一个二羟基丙酮分子组成。本工作研究了以甘油和二羟基丙酮分别作为添加物对果糖转化的影响。当加入一定量甘油时,果糖的反应性能没有明显变化,说明催化剂并不是主要与果糖链状结构中的多羟基部分发生作用。当加入一定量二羟基丙酮时,果糖转化率与5-HMF收率均出现明显下降,说明二羟基丙酮和果糖在与催化剂作用方面存在竞争,导致果糖转化性能下降,这从侧面表明催化剂在果糖转化时应该是与其链状结构中端位的羟基和羰基部分发生作用。
2.4 菊糖转化合成5-HMF
自然界中的果糖主要以聚合物形式存在,研究其聚合物的转化对生物质资源的直接利用具有重要意义。菊糖是一种果糖的低聚物,主要由大量果糖分子和少量的端基葡萄糖分子组成。本工作初步探究了NbCl5在低温下催化菊糖转化制5-HMF的反应性能。图5为NbCl5催化菊糖在不同温度下转化为5-HMF的转化率。
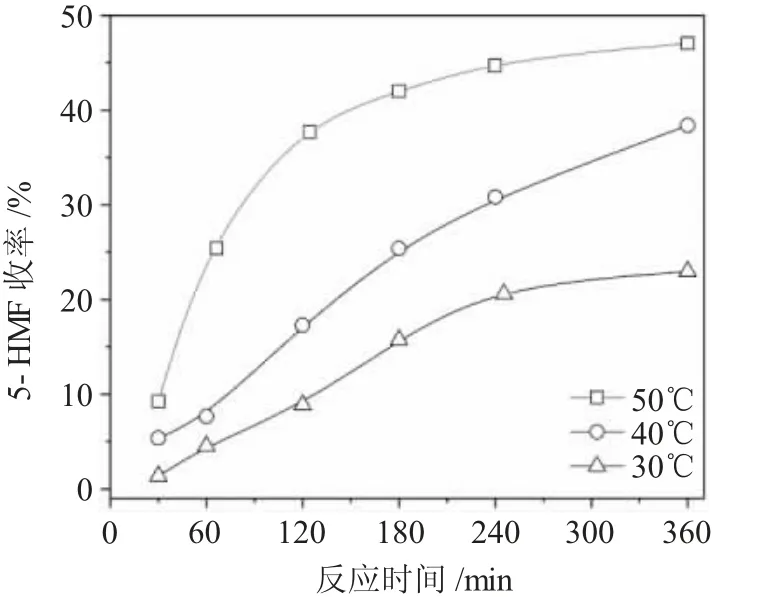
图5 NbCl5催化菊糖在不同温度下转化为5-HMF的转化率Fig.5 Reaction performance on the conversion of inulin into 5-HMF with NbCl5 at different temperatures
由图5可知,菊糖在30℃也能转化为5-HMF,但反应速率很低。反应温度的升高有利菊糖转化,在50℃下,5-HMF的收率最高可达到约47%。
3 结论
NbCl5是一种可用于果糖低温转化制5-HMF的优良催化剂。以DMSO为溶剂,NbCl5用量为果糖摩尔量的15%,在50℃下反应240min,果糖转化率和5-HMF收率分别可达约97%和75%,且该催化体系可在40℃下获得相近的结果。NbCl5可能是通过Br nsted酸和Lewis酸协同作用催化果糖转化,并主要与果糖链状结构中端位的羟基和羰基发生作用。该催化体系也可用于菊糖低温转化制5-HMF。研究结果可为“碳中和”与“节能”背景下生物质资源的利用提供有效参考。
