弥散加权成像对隆突性皮肤纤维肉瘤术前规划的价值初探
2022-10-21柳思宇李小敏赵露露艾松涛
柳思宇,吴 兵,李小敏,赵露露,陈 骏,艾松涛
1.上海交通大学医学院附属第九人民医院放射科,上海 200011;2.上海交通大学医学院附属第九人民医院皮肤科,上海200011
隆突性皮肤纤维肉瘤(dermatofibrosarcoma protuberans,DFSP)是一种起源于真皮下并可浸润至皮下组织的少见中低级别的软组织恶性肿瘤。DFSP 发病率低,占所有恶性肿瘤的0.1%,占所有软组织肉瘤的1.8%~6%[1-3]。临床上常表现为无痛性皮下肿块,最常见部位是躯干、四肢及头颈部[4-5]。
DFSP 以手术切除为主,但切除后的肿瘤复发率可高达60%,且手术时皮损范围过大需行皮瓣移植。如何准确判断肿瘤边界是减少复发及术后美容修复的关键[6-7]。MRI 检查对于显示肿瘤深部范围、查看边界浸润情况、判断周围结构关系、组织学亚型分型及术后复发病变评估均有较大优势[7-10]。常规MRI 可以较好显示肿瘤深部结构组织,主要应用于诊断方面,而遇到肿瘤边缘异常强化或瘤周水肿时则无法精准判断肿瘤边界[11]。研究[11-14]显示MRI弥散加权成像(diffusion-weighted imaging,DWI)通过检测水分子的布朗运动以及扩散运动的受限程度,于细胞水平上提供更多肿瘤周围组织的信息,可以准确反映肿瘤范围,在不同肿瘤治疗中均有应用。准确全面的影像学信息可以优化术前规划,有利于明确手术切除范围及效率[15-17]。本研究回顾性分析上海交通大学医学院附属第九人民医院(简称上海九院)收治的34 例DFSP 患者,以有无DWI 成像分为2 组,分别完成肿瘤边界勾画,利用软件形成皮肤肿瘤报告,辅助设计手术并比较2 组随访复发结果和术后修复满意度评价,旨在探讨DWI 在DFSP 影像规划中的作用。
1 对象与方法
1.1 研究对象
招募2018 年5 月至2022 年3 月期间以DFSP 收治于上海九院的患者病例。纳入标准:①具有手术指征且能耐受手术创伤的DFSP 患者。②无CT 和MRI 检查禁忌证者。③3 个月内未参加过任何临床试验者。排除标准:①缺乏完整临床资料及影像资料者。②图像质量不佳者。所有患者均在术前行CT、常规MRI检查[T1 加权成像(T1 weighted imaging,T1WI)序列、脂肪抑制-T2 加权成像(fat suppression-T2 weighted imaging,FS-T2WI)序列、动态增强磁共振成像(dynamic contrast-enhanced magnetic resonance imaging,DCE) 序列] 及功能MRI 检查(DWI 序列)。将收集的DFSP 病例随机分为MRI 功能成像组(收集的影像资料包含CT平扫+增强、MRI平扫+增强、DWI)及MRI 常规成像组(收集的影像资料包含CT平扫+增强、MRI平扫+增强)。所有患者或其亲属均签署知情同意书。
1.2 检查方法
1.2.1 CT 检查 所有患者均采用64 排螺旋CT 扫描仪(Philips Brilliance,Philips Medical Systems,荷兰)。扫描参数:管电压120 kV,基准管电流220 mA,层厚5 mm,层间距5 mm,矩阵256×256。对比剂为碘佛醇,用量70 mL,速率3 mL/s,重建层厚1 mm。
1.2.2 MRI 检查 所有患者均采用3.0T MR 扫描仪(MAGNETOM Verio 3.0T MRI,Siemens,德国)。扫描序列包括T1WI 序列、FS-T2WI 序列、DCE 序列、DWI 序列。T1WI、FS-T2WI 均为单次激励。T1WI 重复时间(time of repetition,TR) =600 ms,回波时间(time of echo,TE)=12 ms;FS-T2WI 的TR=4 500 ms,TE=83 ms;两者翻转角(flip angle,FA) =9° ~150° , 视 野(field of view, FOV) =360 mm,层厚5 mm,层间距0~1 mm。DCE 序列平均激励次数为1,TR=6.95 ms,TE=2.47 ms,FOV=360 mm,层厚3 mm,层间距1 mm,FA=9°,采集20个时相,每个时相15 s。DWI序列采用单次激发自旋回波平面回波成像(spin echo-echo planar imaging,SE-EPI),TR=6 100 ms,TE=74 ms,FA=90°,FOV=360 mm,层厚3 mm,层间距3 mm,b0值=0 s/mm2,b1值=800 s/mm2。增强扫描对比剂为钆喷替酸葡甲胺(Gd-DTPA),用量10~15 mL,速率2 mL/s,经肘静脉注射。
1.2.3 图像分析 由上海九院2 位具有10 年及以上骨肌系统影像学经验的放射科医师分别对收集的DFSP 图像进行独立观察,分析肿瘤边界浸润情况,判断是否累及筋膜或肌肉,以κ系数评估2 位医师测量结果的一致性。
1.3 CT、MRI图像配准与肿瘤三维重建
使用Medraw 软件打开患者DICOM 数据文件,以CT 增强图像与相应MRI 图像的骨性特征为基础,MRI 功能成像组将CT 增强图像与DWI 图像进行配准,MRI常规成像组将CT 增强图像与DCE 图像进行配准。通过MRI 上勾画出的肿瘤边界在CT 上重建肿瘤,得到肿瘤三维模型,进行肿瘤最大长度、最大高度、最大厚度及病灶体积测算,并在三维模型上标明。以肿瘤区域扩大10~15 mm 作为软组织缺损范围,用作术区扩切范围。将重建的骨质、皮肤及肿瘤三维模型以STL 文件导入C4D 软件,制作三维展示动画,最终形成皮肤肿瘤报告。
1.4 结果评估
记录患者年龄、性别、肿瘤发生部位、肿瘤(最大)直径与体积大小、术式、病理诊断、复发次数、临床随访结果(随访时间截至2022 年3 月),比较MRI 功能成像组和MRI 常规成像组随访复发率和术区美观满意度调查情况。
1.5 统计学分析
应用SPSS 25.0 统计软件分别对数据进行统计分析。定量资料用xˉ±s表示,采用t检验进行组间比较。定性资料用例数(百分比)表示,采用χ2检验或Fisher 确切概率法进行组间比较。所有统计检验均采用双侧检验,P<0.05 表示差异具有统计学意义。
2 结果
2.1 患者临床基本信息
共收集的34 例DFSP 患者中,男性18 例,女性16例;平均年龄(36.56±13.07)岁(7~61岁)。34例均为单发病灶,其中腹壁10 例(29.4%)、胸壁9 例(26.5%)、颌面部4 例(11.8%)、大腿及肩部各3 例(各8.8%)、臀部及腰部各2 例(各5.9%)、足部1 例(2.9%)。34 例中肿瘤直径最大者为5.23 cm,直径最小者为0.98 cm,平均直径为(2.25±0.92)cm。20 例为初发DFSP,14 例为复发DFSP。MRI 功能成像组和MRI 常规成像组各17 例,2 组患者临床基本信息,包括年龄、性别、肿瘤部位、肿瘤体积、发作次数及边界浸润情况组间差异均无统计学意义(均P>0.05,表1)。

表1 患者临床基本信息Tab 1 Clinical characteristics of the two groups
边界浸润情况在2 位放射科医师之间均有中等及以上程度的一致性(均κ>0.41);相较MRI 常规成像组,2 位医师在判断MRI功能成像组肿瘤边界累及筋膜(κ=0.866,表2)和累及肌肉(κ=0.742,表3)时的一致性更佳。

表2 不同医师判断2 组患者肿瘤边界累及筋膜情况的一致性评价Tab 2 Consistency evaluation of different doctors' judgment of fascia involvement in tumor boundary in the two groups of patients
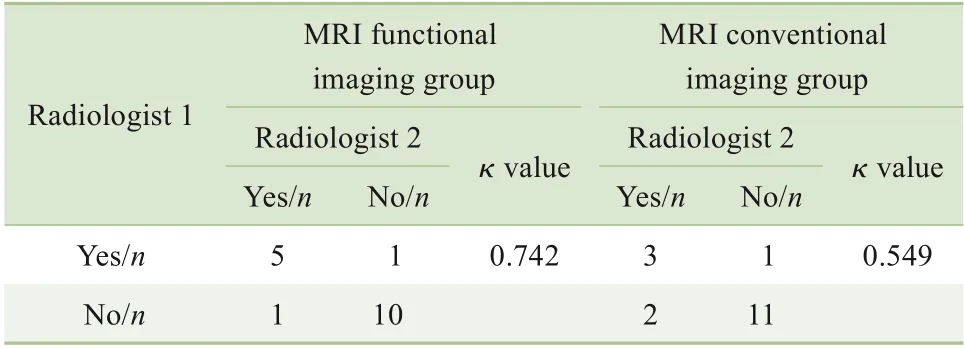
表3 不同医师判断2 组患者肿瘤边界累及肌肉情况的一致性评价Tab 3 Consistency evaluation of different doctors' judgment of muscles involvement in tumor boundary in the two groups of patients
2.2 患者手术及术后临床随访结果
所有患者均行Mohs 显微描记手术,术后病理诊断均为DFSP,组织学亚型包括24 例经典型(2 组各12 例)、2 例萎缩型(2 组各1 例)、1 例色素型(MRI功能成像组)、1 例黏液型(MRI 常规成像组)、2 例纤维肉瘤型(MRI 功能成像组),4 例未行组织学亚型分型(MRI 功能成像组1 例、MRI 常规成像组3 例);2 组组织学亚型分布差异无统计学意义(P=0.416)。34 例DFSP 平均随访时间(9.97±7.82)个月(1~36 个月),MRI 功能成像组患者平均随访时间(8.41±4.91)个月,MRI 常规成像组平均随访时间(11.53±9.84)个月;2 组平均随访时间差异无统计学意义(P=0.251)。MRI 功能成像组患者复发率为0,显著低于MRI 常规成像组患者的29.4%(5/17)(P=0.017)。MRI功能成像组患者术后随访,术区美观总满意度评价高于MRI常规成像组(P=0.001,表4)。
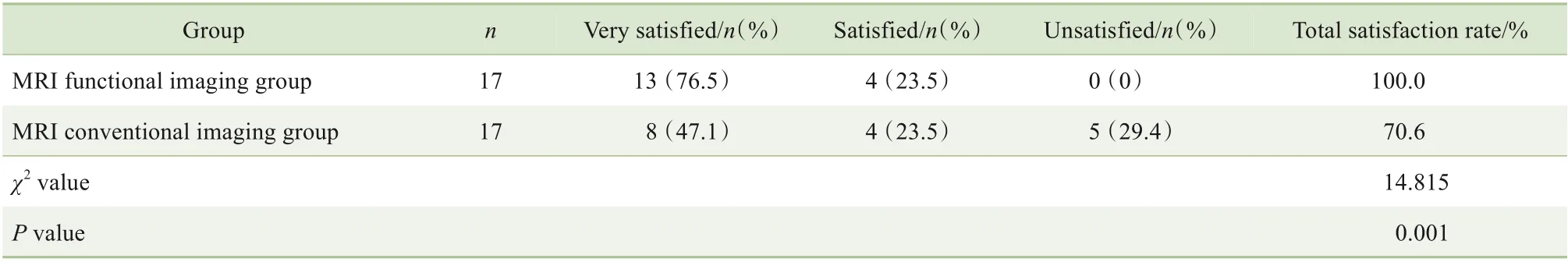
表4 患者术后美观满意度评价比较Tab 4 Comparison of post-operative aesthetic satisfaction evaluation
2.3 典型病例
患者,女,7岁,以“左胸壁DFSP 5年余”收治入院。术前CT 及MRI 检查示左胸壁软组织肿块影,形态不规则,边界欠清,肿瘤直径为3.25 cm,累及左侧胸大肌(图1A~C);DCE 图像中肿瘤区呈不均匀轻度强化,边界模糊不清(图1D);DWI图像中肿瘤呈高信号,可清晰显示边界(图1E)。患者DICOM 数据导入Medraw 软件,于DWI 图像勾画肿瘤边界(图1F);选取CT 增强图像与DWI 图像进行配准,重建肿瘤三维模型(图2A);以肿瘤周围15 mm 作为扩切范围,导出STL 文件(图2B)。于术区勾画实际切除范围(图2C),术中做直径约10 cm大小圆形切口,切开皮肤皮下,切除肿瘤至胸大肌上(图2D),取下完整瘤体(图2E),行带蒂复合组织瓣成形术(图2F)。术后标本病理送检,术中出血约20 mL。
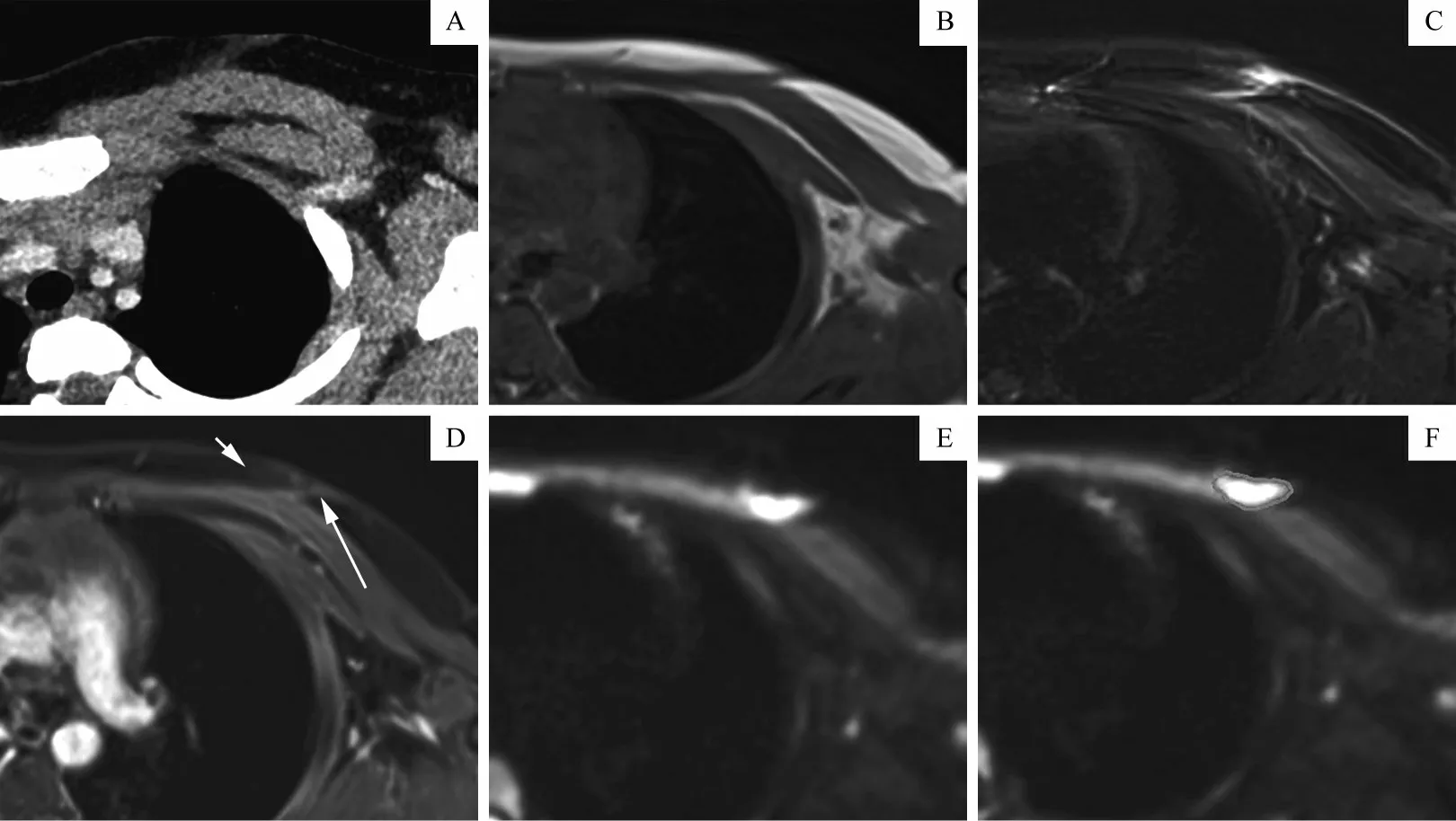
图1 患者肿瘤影像图像示例Fig 1 Example of a patient's tumor images

图2 影像规划辅助手术过程示例Fig 2 Example of image-assisted surgical procedure planning
3 讨论
DFSP 病程长,肿瘤生长缓慢,治疗以手术切除为主,目前临床常使用Mohs 显微描记手术作为惯用术式[18-20]。在术区范围勾画上需考虑2个方面:一方面肿瘤转移率低但原位复发率高,需将肿瘤切除范围包全;另一方面当肿瘤发生于头颈部或生殖器等美容和功能敏感区时,或肿瘤体积过大,切除后创面无法原位复合,需移植皮瓣覆盖病损时,切除范围亦不可过大。故精准判断肿瘤边界和完善的术前规划都显得尤为重要[21-23]。不同的医学影像学技术在软组织肿瘤的诊治中起到不同的作用:超声在检查体积较小的浅表病变中有一定价值,对于初步定性及定位诊断有重要作用,但探查深度有限,当肿瘤体积过大或范围过深时将导致边界情况显示不清,对图像信息展示方式十分单一[24];CT 操作流程简单,成像速度快,与超声相比分辨率高,可以清晰显示病变的解剖部位,但CT 的优势主要体现在骨及钙化的显示,软组织分辨率远低于MRI,且扫描范围大,对于DFSP 这种少见钙化的软组织肉瘤的边界显示能力不足[25];MRI具有无辐射、获取参数多、多方位成像、软组织分辨率高等优点,对于肿瘤基本影像学特征都有较好显示。因此有学者认为在评价软组织肿瘤时,建议所有患者使用MRI 检查,以便准确描述肿瘤内部结构和范围[26]。
DFSP 常突出表面或浸润至皮下组织,有时甚至会累及脂肪层、肌肉、骨组织等[8,27]。本研究中约40%DFSP 累及深浅筋膜层,约28%累及肌肉层,周围组织或器官浸润情况的清晰显示对于准确划定肿瘤边缘,精准规划手术范围,降低原位复发率有着十分重要的意义。DFSP 作为中低级别软组织恶性肿瘤,少见瘤内出血、坏死,瘤周或筋膜水肿等恶性浅表软组织肿瘤征象,但当出现高级别DFSP 组织学亚型,如纤维肉瘤型DFSP 时,在判断肿瘤边缘时则需将瘤周水肿的影响考虑在内[10,28]。常规MRI成像中DFSP的T1WI 及T2WI 信号特征是非特异性的;肿瘤边缘及瘤周水肿表现为高信号或对比度增强,但并不清楚这种高信号是否代表肿瘤浸润或仅为反应性变化,单纯依靠常规MRI 成像确定肿瘤边界的能力是有限的[11,29]。
DWI 是一种通过水分子扩散反映组织细胞特性的技术,能够于细胞水平上为软组织肿瘤范围勾画提供更多有关瘤周组织及侵袭性的信息[11-12]。HONG等[11]对45 例不同软组织肿瘤患者行常规MRI 成像及DWI 成像,以病理结果作为金标准,判断肿瘤边界情况,结果显示常规MRI 结合DWI 成像的受试者操作特征曲线(receiver operating characteristic curve,ROC 曲线)的曲线下面积(AUC)大于单独使用常规MRI 成像的AUC。YOON 等[29]回顾性研究29 例软组织肉瘤的MRI 图像,比较了常规MRI 组与常规MRI 加DWI 组对肿瘤累及筋膜情况的诊断性能,发现常规MRI 加DWI 可以提高筋膜侵犯的诊断能力。由此可见,DWI 可以为DFSP 边界判断提供更大的帮助。
本研究基于DFSP 基本特性、常规MRI 特点、DWI 独特优势分析纳入34 例DFSP 患者。将纳入的病例分为MRI 功能成像组17 例与MRI 常规成像组17例,性别、年龄等基线水平均无明显差异。我们于术前进行图像分析及肿瘤边界勾画时发现使用DWI图像可以提升不同医师判断边界侵犯情况的一致性,于术后也比较了2 组患者随访的复发率和术区美观满意度的区别:术后的随访调查发现,MRI 功能成像组复发率显著低于MRI 常规成像组,且术后术区美观满意度调查结果亦优于MRI 常规成像组。以上结果提示DWI 依靠其在体现肿瘤侵袭性方面的优势,可以有效帮助医师判断肿瘤边界侵犯情况,纠正单纯使用常规MRI 勾画肿瘤边界时忽略的水肿、异常强化或其他细节,精准实现肿瘤边界勾画,既不会因为勾画范围不够而导致肿瘤复发,亦不会因为勾画范围过大而导致术区修复困难。本文所展示的病例是一位女童,肿瘤发生于左胸壁乳头上方的敏感区,精细的手术规划对于患者日后发育十分重要。我们发现在常规MRI 增强图像中肿瘤呈不均匀轻度强化,边缘模糊,边界勾画困难,而在DWI 图像中肿瘤边界显示清晰;且根据DWI 勾画的边界进行手术,随访6 个月未见复发,患者及家属对于术区恢复也非常满意。再者,尽管一些学者使用DWI 进行肿瘤边界浸润性的研究,并使用术后病理证实DWI 的准确性,但仅局限于对原始图像的研究,并未涉及进一步术前规划,或仅为个案报道的手术规划及术后随访,研究结果尚不具有代表性[11,13,29]。我们所纳入的2 组患者在进行肿瘤边界勾画之后均使用Medraw 软件配准了CT 及MRI 图像,重建出DFSP 三维形态,表明扩切范围,为临床医师提供了更加直观的视觉演示,使得临床医师与影像科医师在设计手术方案过程中的沟通更加便捷,便于顺利推进多学科会诊。
本研究仍存在不足之处。首先,纳入的样本量有限,研究结果可能存在偏倚,在后续研究进程中将纳入更多病例;其次,使用人工进行每个序列、逐层勾画肿瘤边界耗时且具有挑战性,主观性过强,考虑后续可能会引入机器学习技术简化人工作业。
综上所述,医学影像学对于DFSP 诊断可靠有效,尤其是MRI 的DWI 序列可以依靠其自身优势,精准判定肿瘤边界,再借助计算机辅助设计软件和图像后处理技术三维重建肿瘤,将肿瘤形态更加直观地展示出来,为制定完善的手术方案提供有力帮助,因而探寻MRI在DFSP手术上的价值具有重要意义。
利益冲突声明/Conflict of Interests
所有作者声明不存在利益冲突。
All authors disclose no relevant conflict of interests.
伦理批准和知情同意/Ethics Approval and Patient Consent
本研究涉及的所有实验均已通过上海交通大学医学院附属第九人民医院伦理委员会的审核批准(文件号2017-451-T3347)。受试对象或其亲属均签署知情同意书。
All experimental protocols in this study were reviewed and approved by the Ethics Committee of Shanghai Ninth People's Hospital,Shanghai Jiao Tong University School of Medicine (Approval Letter No. 2017-451-T3347). Consent letters have been signed by the research participants or their relatives.
作者贡献/Authors'Contributions
柳思宇、吴兵和赵露露参与了资料收集;李小敏、艾松涛和陈骏参与了实验设计;艾松涛提出了研究选题;柳思宇进行了论文撰写和修改。所有作者均阅读并同意了最终稿件的提交。
The data was collected by LIU Siyu,WU Bing and ZHAO Lulu. The study was designed by LI Xiaomin,AI Songtao and CHEN Jun. The research topic was proposed by AI Songtao. The manuscript was drafted and revised by LIU Siyu. All the authors have read the last version of paper and consented for submission.
·Received:2022-06-30
·Accepted:2022-08-08
·Published online:2022-08-28
参·考·文·献
[1] GLOSTER H M Jr. Dermatofibrosarcoma protuberans[J]. J Am Acad Dermatol,1996,35(3 Pt 1):355-374.
[2] MENDENHALL W M, ZLOTECKI R A, SCARBOROUGH M T.Dermatofibrosarcoma protuberans[J]. Cancer, 2004, 101(11): 2503-2508.
[3] MUJTABA B, WANG F, TAHER A, et al. Dermatofibrosarcoma protuberans: pathological and imaging review[J]. Curr Probl Diagn Radiol,2021,50(2):236-240.
[4] CHANG C K, JACOBS I A, SALTI G I. Outcomes of surgery for dermatofibrosarcoma protuberans[J]. Eur J Surg Oncol, 2004, 30(3):341-345.
[5] THWAY K, NOUJAIM J, JONES R L, et al. Dermatofibrosarcoma protuberans: pathology, genetics, and potential therapeutic strategies[J]. Ann Diagn Pathol,2016,25:64-71.
[6] 刘珍如, 周园, 刘梦茜, 等. 隆突性皮肤纤维肉瘤的诊疗进展[J].中国美容医学,2021,30(3):171-174.LIU Z R,ZHOU Y,LIU M X,et al. Research progress in diagnosis and treatment of dermatofibrosarcoma protuberans[J]. Chin J Aesthet Med,2021,30(3):171-174.
[7] SEDAGHAT S, SCHMITZ F, SEDAGHAT M, et al. Appearance of recurrent dermatofibrosarcoma protuberans in postoperative MRI follow-up[J]. J Plast Reconstr Aesthet Surg, 2020, 73(11): 1960-1965.
[8] 王传彬,韦超,李乃玉,等. 隆突性皮肤纤维肉瘤的CT和MRI表现[J].中国医学装备,2021,18(4):58-61.WANG C B, WEI C, LI N Y, et al. The manifestation of dermatofibrosarcoma protuberans on CT and MRI[J]. China Med Equip,2021,18(4):58-61.
[9] 陈开良, 吴文婷. 隆突性皮肤纤维肉瘤的高频超声表现分析[J].肿瘤影像学,2020,29(6):570-573.CHEN K L, WU W T. Analysis of high-frequency ultrasound manifestations of dermatofibrosarcoma protuberan[J]. Oncoradiology,2020,29(6):570-573.
[10] CHOONG P, LINDSAY D, KHOO M, et al. Dermatofibrosarcoma protuberans: the diagnosis of high-grade fibrosarcomatous transformation[J]. Skeletal Radiol,2021,50(4):789-799.
[11] HONG J H,JEE W H,JUNG C K,et al. Soft tissue sarcoma:adding diffusion-weighted imaging improves MR imaging evaluation of tumor margin infiltration[J]. Eur Radiol,2019,29(5):2589-2597.
[12] DOUIS H, DAVIES M A, SIAN P. The role of diffusion-weighted MRI (DWI) in the differentiation of benign from malignant skeletal lesions of the pelvis[J]. Eur J Radiol,2016,85(12):2262-2268.
[13] AMJAD G,ZEINALI ZADEH M,AZMOUDEH-ARDALAN F,et al.Evaluation of multimodal MR imaging for differentiating infiltrativeversusreactive edema in brain gliomas[J]. Br J Neurosurg,2020. DOI:10.1080/02688697.2020.1849541.
[14] KISHIMOTO A O,KATAOKA M,IIMA M,et al. The comparison of high-resolution diffusion weighted imaging(DWI)with high-resolution contrast-enhanced MRI in the evaluation of breast cancers[J]. Magn Reson Imaging,2020,71:161-169.
[15] 曲扬,艾松涛,杨飞,等. CT 和MRI 图像配准融合联合3D 打印技术在难治性骨盆肿瘤术前规划中的应用[J]. 上海交通大学学报(医学版),2017,37(9):1239-1244,1238.QU Y, AI S T, YANG F, et al. Application of CT/MRI image registration and fusion combined with 3D printing technique in presurgical planning of refractory pelvic tumors[J]. J Shanghai Jiao Tong Univ(Med Sci),2017,37(9):1239-1244,1238.
[16] 潘文博,蔡智慧,石军荣,等. 3D 打印技术在卵巢癌手术中的应用价值[J]. 河北医药,2022,44(6):938-942.PAN W B, CAI Z H, SHI J R, et al. The application of 3D printing technique in ovarian cancer surgery[J]. Hebei Med J, 2022, 44(6):938-942.
[17] 郑眉光,刘正豪,李文鹏,等. 3D 打印技术在复杂性颅底肿瘤手术中的应用[J]. 中华神经医学杂志,2021,20(9):927-931.ZHENG M G, LIU Z H, LI W P, et al. Three-dimensional printing technology in surgery of complex skull base tumors[J]. Chin J Neuromedicine,2021,20(9):927-931.
[18] ACOSTA A E, VÉLEZ C S. Dermatofibrosarcoma protuberans[J].Curr Treat Options Oncol,2017,18(9):56.
[19] WONG E,AXIBAL E,BROWN M. Mohs micrographic surgery[J].Facial Plast Surg Clin N Am,2019,27(1):15-34.
[20] 上海交通大学医学院附属第九人民医院皮肤梭形细胞肿瘤多学科精准诊疗团队. 隆突性皮肤纤维肉瘤多学科诊治实施规范:上海交通大学医学院附属第九人民医院专家共识(2020 年版)[J]. 上海交通大学学报(医学版),2021,41(12):1669-1675.Multi-Disciplinary Team for Cutaneous Spindle Cell Neoplasms,Shanghai Ninth People's Hospital, Shanghai Jiao Tong University School of Medicine. Practice for multidisciplinary diagnosis and treatment of dermatofibrosarcoma protuberans:expert consensus of Shanghai Ninth People's Hospital, Shanghai Jiao Tong University School of Medicine (2020 edition)[J]. J Shanghai Jiao Tong Univ(Med Sci),2021,41(12):1669-1675.
[21] HAO X P, BILLINGS S D, WU F B, et al. Dermatofibrosarcoma protuberans: update on the diagnosis and treatment[J]. J Clin Med,2020,9(6):1752.
[22] VELASCO ALBENDEA F J, DOÑA GIRÓN J, BLANCO VILLAR M L, et al. Perianal dermatofibrosarcoma protuberans: a case report,review and update[J]. Rev Esp Patol,2019,52(1):62-68.
[23] LIOU V, CHISHOLM S A, LOGUNOVA V, et al. Giant dermatofibrosarcoma protuberans with bilateral orbital involvement[J].Ophthalmic Plast Reconstr Surg,2019,35(2):e36-e39.
[24] LEE S J, MAHONEY M C, SHAUGHNESSY E.Dermatofibrosarcoma protuberans of the breast:imaging features and review of the literature[J]. AJR Am J Roentgenol, 2009, 193(1):W64-W69.
[25] Expert Panel on Musculoskeletal Imaging. ACR appropriateness criteria®soft-tissue masses[J]. J Am Coll Radiol, 2018, 15(5S):S189-S197.
[26] HOURANI R,TASLAKIAN B, SHABB N S, et al. Fibroblastic and myofibroblastic tumors of the head and neck: comprehensive imaging-based review with pathologic correlation[J]. Eur J Radiol,2015,84(2):250-260.
[27] GARG M K, YADAV M K, GUPTA S, et al. Dermatofibrosarcoma protuberans with contiguous infiltration of the underlying bone[J].Cancer Imaging,2009,9(1):63-66.
[28] 黄曦毅,蔡金辉,刘庆余,等. 隆突性皮肤纤维肉瘤的CT和MRI影像学分析:附10例报道[J]. 罕少疾病杂志,2020,27(4):57-59,70.HUANG X Y, CAI J H, LIU Q Y,et al. The imaging findings of dermatofibrosarcoma protuberans on CT and MRI:10 cases report[J].J Rare Uncommon Dis,2020,27(4):57-59,70.
[29] YOON M A, CHEE C G, CHUNG H W, et al. Added value of diffusion-weighted imaging to conventional MRI for predicting fascial involvement of soft tissue sarcomas[J]. Eur Radiol, 2019,29(4):1863-1873.
