铵盐体系电解锰渣中石膏的转变规律
2022-10-13曾一凡舒建成杨慧敏赵志胜陈梦君杨勇刘仁龙
曾一凡,舒建成,杨慧敏,赵志胜,陈梦君,杨勇,刘仁龙
(1 西南科技大学固体废物处理与资源化教育部重点实验室,四川 绵阳 621000;2 重庆大学化学化工学院,重庆 401331;3 南方锰业集团有限责任公司大新锰矿分公司,广西 南宁 532315)
锰是我国重要的战略资源之一,素有“无锰不成钢”之说。2020 年中国电解金属锰产量为150.13 万吨,占全球总产量的96.5%。然而,电解锰行业在快速发展的同时,也面临着巨大的环境压力,尤其是电解锰生产过程排放的电解锰渣已成为制约我国电解锰行业发展的瓶颈。目前我国锰渣堆存量已突破1.6 亿吨,且每年新增近1000 万吨,这进一步加重了企业环保压力。为此,开展电解锰渣无害化处理和资源化利用研究,对我国电解锰行业发展具有十分重要的现实意义。
国内外学者在电解锰渣处理处置方面已开展了大量工作。填埋和无害化处理的核心在于防止电解锰渣中易迁移的铵根(NH)离子以及包括锰在内的重金属元素进入环境,而要彻底解决锰渣污染问题必须实现其资源化利用。目前有关锰渣资源化利用成功的工业化案例还未见报道,主要原因是电解锰渣中含有大量的难溶硫酸盐,其中石膏是难溶硫酸盐的主要组分,占锰渣的40%~60%(质量分数,下同)。锰渣中含有的石膏是导致锰渣制备出的建筑产品出现泛霜、开裂、破损等现象的主要原因。例如:采用锰渣制备免烧建材产品时,由于石膏溶解度大,制品受潮后,石膏晶体间的结合力减弱,制品强度显著降低;另外,游离水可通过石膏制品的微裂缝和高孔隙进入制品内部,导致制品的强度和耐久性降低。锰渣制备玻璃、陶瓷等烧结制品时,石膏分解产生的SO容易导致制品产生气泡,影响产品质量。锰渣掺入水泥时,由于水泥产品标准要求SO质量分数必须低于3.5%,过高含量的硫会降低水泥强度,增加凝结时间,造成水泥膨胀性裂缝;锰渣用于制备煅烧水泥时,石膏的分解会引起烧成系统结皮堵塞,直接影响水泥生产工艺及产品质量,作土壤改良剂时因石膏含量高,易造成土壤板结。因此,开展锰渣中石膏去除研究,对锰渣的建材资源化高效利用具有十分重要的意义。
事实上,许多研究者在石膏去除方面开展了大量研究,其中宁夏天元锰业采用火法方法实现了锰渣中石膏的去除,石膏最终转变成SO和CaO;陈波等以NH、CO为原料,采用连续反应结晶法转化石膏制备CaCO,Ca 转化率达99.61%;陈红亮等采用NaCO和NHHCO对电解锰渣进行处理,实现了锰渣中Mn的固定和石膏转化;孙红娟等利用NHCl的盐效应增加石膏的溶解度,提高石膏的浸出率;杨晓红等采用HCl浸出电解锰渣中的石膏,浸出率可达94.2%;冯雅丽等采用NHHCO溶液,实现了石膏向CaCO的转化,热解后可制备出高纯CaO;刘佳利用磷石膏制备(NH)SO,硫酸根转化率达97.01%。为此,采用NHHCO与NHCl铵盐体系对电解锰渣中石膏进行浸出,在理论上是可行的。
本文探究了NHHCO和NHCl用量、浸出初始pH、浸出时间、浸出温度对石膏转变的影响。采用X 射线衍射(XRD)、扫描电镜-能量分布面扫描(SEM-EDS-Mapping)、傅里叶变换红外光谱(FTIR)、X射线荧光光谱(XRF)等现代分析手段,对浸出前后电解锰渣的基本理化特性、石膏转变规律进行了分析,研究成果将为电解锰渣的资源化利用提供理论和技术支持。
1 材料与方法
1.1 材料
采用的电解锰渣来自于某渣库,参照《工业固体废弃物采样制样技术规范》进行采样。电解锰渣样品均匀混合后,在60℃下烘干至恒重,过60目筛备用。本实验采用的化学试剂有碳酸氢铵(NHHCO)、盐酸(HCl)、氯化铵(NHCl)、氨水(25%,NH·HO)、乙二胺四乙酸二钠镁(CHMgNNaO·4HO)、氧化锌(ZnO)、二水合乙二胺四乙酸二钠(CHNONa·2HO)、氯化钡(BaCl)、硫酸钠(NaSO)、无水乙醇(30%,CHOH)、铬黑T指示剂(CHNNaOS),均为分析纯。
1.2 电解锰渣中石膏的转变
首先将备用的电解锰渣样品与蒸馏水按照不同固液比(1∶1~1∶8)配置于烧杯中,混合均匀后采用稀盐酸(0.1mol/L)和稀氨水(1%)调节至不同的浸出初始pH(5.5~10.5)。根据设定的实验方案,依次添加不同质量分数的NHHCO(10%~70%)和NHCl(2.5%~12.5%),随后放置到设定温度(60~90℃)的水浴锅中进行加热,在相同转速下设定不同浸出时间(0~120min)。反应结束后进行固液分离,用超纯水洗涤浸出渣两次,在60℃下进行干燥至恒重。石膏浸出率以式(1)计算。


1.3 分析测试仪器
根据《制盐工业通用试验方法硫酸根的测定》(GB/T 13025.8—2012)方法,测定浸出液中SO浓度。根据《制盐工业通用试验方法钙的测定》(GB/T 13025.6—2012)方法,测定浸出液中Ca浓度。采用电感耦合等离子体发射光谱仪(ICPOES;Thermo Fisher Scientific,Agilent7700,US)对浸出液中金属离子浓度进行测定。电解锰渣物相采用日本理学株式会社生产的X’Pert PRO 型X 射线衍射仪分析(厂家:Rigaku,Japan。型号:Ultima Ⅳ)。化学成分采用Axios型X射线荧光光谱仪分析,生产厂家为荷兰帕纳科有限公司,仪器工作条件:Rh靶,陶瓷X射线,最大功率2.4kW,测角仪扫描模式/2模式,含量范围为0.01%~100%(厂家:Rigaku,Japan。型号:Ultima Ⅳ)。样品的微观形貌采用日本日立公司SU9000 型扫描电镜分析,观测电压1kV。样品的分子结构和化学基团的测定采用日本岛津制作所IRPRESTIGE-21 型傅里叶变换红外光谱仪分析,光度范围为4000~750cm。滴定实验采用江苏智捷生产的25mL酸式滴定管及碱式滴定管。
2 结果与讨论
2.1 NH4HCO3用量和浸出初始pH 对石膏浸出率的影响
由图1(a)可知,当NHHCO用量从锰渣的10%增加到70%,电解锰渣中石膏的浸出率呈现先上升后下降的趋势,而溶液pH 持续上升。当NHHCO用量为锰渣的40%时,石膏的浸出率高达86.5%,继续增加NHHCO用量到70%,石膏浸出率从86.5%下降到72.0%。其原因是NHHCO在水溶液中HCO易发生水解,且水解程度大于电离程度,溶液呈碱性。在70℃下NHHCO受热分解释放NH和CO,从而造成NHHCO的消耗。另外,随着NHHCO用量增加,浸出体系碱性增强,镁离子活度提高,水中镁离子结晶析出后会产生氢氧化镁[Mg(OH)]沉淀。大量研究表明,Mg(OH)会对CaCO的结晶速率和表面形貌造成影响,导致CaCO结晶速率下降,从而降低电解锰渣中石膏的浸出。由图1(b)可知,当NHHCO用量为锰渣的40%,采用稀盐酸和稀氨水调节浸出初始pH 从5.5~7.5时,石膏浸出率从83.1%增加到89.1%,当浸出初始pH 从7.5 增加到10.5,石膏浸出率从89.1%下降到76.8%。其原因是在弱碱性条件下,镁离子难形成抑制CaCO结晶的Mg(OH)沉淀,从而导致CaCO结晶速率上升,石膏浸出率升高;在强碱性环境下,随着镁离子活度升高,Mg(OH)开始大量形成,大量镁离子进入CaCO晶格,降低了CaCO诱导结晶速率,导致石膏浸出率降低。因此,本研究选取NHHCO用量为锰渣的40%,浸出初始pH为7.5作为最佳反应条件。

图1 NH4HCO3用量和浸出初始pH对石膏浸出率的影响
2.2 NH4Cl用量和固液比对石膏浸出率的影响
由图2(a)可知,随着NHCl 浓度的增加,石膏浸出率逐渐增加。当NHCl用量为锰渣的7.5%时,石膏浸出率为90.0%。当NHCl 用量增加到锰渣的10%时,石膏浸出率开始缓慢下降至88.07%。当NHCl 用量持续增加到12.5%时,石膏浸出率降低到84.3%。随着浸出体系中NHCl 浓度增加,溶液中的离子总浓度增加,由于盐效应作用,强电解质NHCl 增加了溶液的离子强度。在固定温度下,CaSO·2HO的溶度积保持不变,溶液的离子强度增加,则相应的活度系数(SO)、(Ca)和(HO)减小,溶液中SO、Ca、HO 的浓度增加,作为盐试剂的NHCl 促进了电解锰渣中石膏的转化。此外,当NHCl用量大于锰渣的7.5%时,CaSO·2HO的溶解度增大,石膏浸出速率下降,原因可能是NHCl浓度提高后,溶液黏性增强,Cl和NH+吸附在石膏表面,阻碍了未溶解的CaSO·2HO 溶出;另一方面,随着溶液中NHCl浓度的升高,由于同离子效应,溶液中SO2阻碍了CaSO·2HO 的持续溶解。由图2(b)可知,当电解锰渣与水固液比从1∶1 增加到1∶5 时,石膏浸出率从83.4%增加到90.0%,当固液比增加至1∶8,石膏浸出率下降。其原因是随着固液比的增加,溶液体系中的同离子效应减弱,降低了Cl和NH+在石膏表面的吸附;此外,过高的固液比将产生大量的浸出液,导致浸出液处理成本提高。因此,本研究选取NHCl质量分数为7.5%、固液比为1∶5作为最佳反应条件。

图2 NH4Cl用量与固液比对石膏浸出率的影响
2.3 浸出温度和浸出时间对石膏浸出率的影响
由图3 可知,当浸出时间小于30min、浸出温度在60~80℃时,石膏的浸出率与浸出温度呈正相关,且随着浸出时间增加而增加,这是因为浸出时间和浸出温度的增加提高了锰渣中CaSO·2HO 的溶解度。当浸出时间超过30min后,浸出温度80℃和90℃条件下石膏浸出率逐渐下降,且石膏在浸出温度90℃下的浸出率低于80℃,这可能是由于高温加剧了HCO-消耗,导致NHHCO与电解锰渣的反应减弱。而浸出温度在60℃和70℃时,石膏浸出率随着反应时间的增加而提高,反应120min时石膏的浸出率基本保持不变,其原因是电解锰渣在NHHCO与NHCl铵盐体系下的化学反应已趋于平衡。当电解锰渣与NHHCO以及NHCl质量比为20∶8∶1.5、电解锰渣与水固液比为1∶5、浸出初始pH 为7.5、浸出温度70℃、浸出时间为120min时,石膏的浸出率达到90%。

图3 浸出温度和浸出时间对石膏浸出率的影响
2.4 电解锰渣中石膏转变规律
由表1可知,与原电解锰渣相比,浸出锰渣中SO含量显著降低,SiO、CaO、MnO、FeO、MgO、AlO等金属氧化物含量增加。在最佳反应条件下,采用NHHCO与NHCl铵盐体系浸出得到的锰渣中SO质量分数从未浸出前的30.3%下降到3.19%,SiO、MnO、MgO、AlO等金属氧化物的质量分数分别从未浸出前的23.61%、14.71%、1.84%、2.56%上升到32.42%、14.71%、4.12%、3.36%。事实上,锰渣中SO的含量降低以及SiO、MnO、MgO、AlO等金属氧化物含量的增加,能够提高锰渣在建材领域的掺入量,同时经过铵盐体系浸出得到的锰渣中含有大量氨氮,可作为土壤改良剂或者肥料。

表1 不同条件下电解锰渣的化学成分单位:%(质量分数)
由图4(a)可知,原电解锰渣中S主要以CaSO·2HO形式存在;此外,电解锰渣中还含有大量SiO及少量

图4 不同温度下浸出电解锰渣XRD和FTIR分析
CaMn(OH)SiO·2(HO)、 MgAlFeSiAlO(OH)、KAlSiO(OH)等。在浸出温度60℃、70℃和80℃条件下,原电解锰渣中CaSO·2HO 特征峰消失,而CaCO、SiO、MnCO以 及CaMn(OH)SiO·2HO 等物相特征峰出现,这些特征峰在60~80℃条件下未发生明显变化,说明在60~80℃条件下CaSO·2HO能够转化成CaCO。当浸出温度达到90℃时,浸出锰渣的X射线衍射图中出现了CaSO·2HO特征峰,这说明高温不利于锰渣中CaSO·2HO 转化,其原因可能是随着反应温度升高,溶液中的NHHCO、Ca(HCO)、Mg(HCO)受热分解,溶液中HCO-被消耗,从而减少了CaCO的生成。
由图4(b)可知,原电解锰渣在3404cm和1622cm附近可观察到HO 的伸缩振动峰,说明原电解锰渣中含有结晶水。处理后锰渣样品在1417cm和872cm附近出现了CO2的伸缩振动峰,说明处理后的电解锰渣中出现了CO。在1124cm、797cm处分别出现了SiO2和MnO-振动带,670cm和602cm处观察到SO2伸缩振动峰,结合XRD 分析可知原电解锰渣中含有SiO、锰盐以及硫酸盐。另外,随着浸出温度增加,在670cm和602cm处出现的SO2伸缩振动峰增强。由表2可知,随着浸出温度从60℃升高到90℃,浸出液中Mg浓度呈现先上升后下降趋势。其原因是随着温度增加,溶液中的HCO-与Mg反应,降低了溶液中Mg和HCO-浓度。浸出液中Mn、Cu和Zn的浓度上升,这说明在NHHCO-NHCl体系下,锰渣中的Mn、Cu、Zn和Mg容易被浸出。

表2 不同反应条件下浸出液中重金属元素浓度单位:mg/L
由图5 中Mapping 可知,图中代表C、O、Ca的颜色较深且分布较广,代表Si 元素的颜色较深分布较为集中,而代表Mg、Fe、S、Mn 元素的颜色分布较松散且较为均匀。说明CaCO晶种表面附着有较多细小颗粒物,这些细小颗粒物是由Fe、Mn、Mg、S 颗粒沉淀产生,产生的细小颗粒物会诱导CaCO结晶,而铁离子和锰离子会提升CaCO结晶速率。由图5 中EDS 可知,与原锰渣相比,处理后锰渣中S含量占比下降,Mn含量占比提高。综上分析可知,采用NHHCO与NHCl铵盐体系浸出锰渣可能发生的反应如式(2)~式(14)。

图5 浸出锰渣SEM、EDS、Mapping图谱
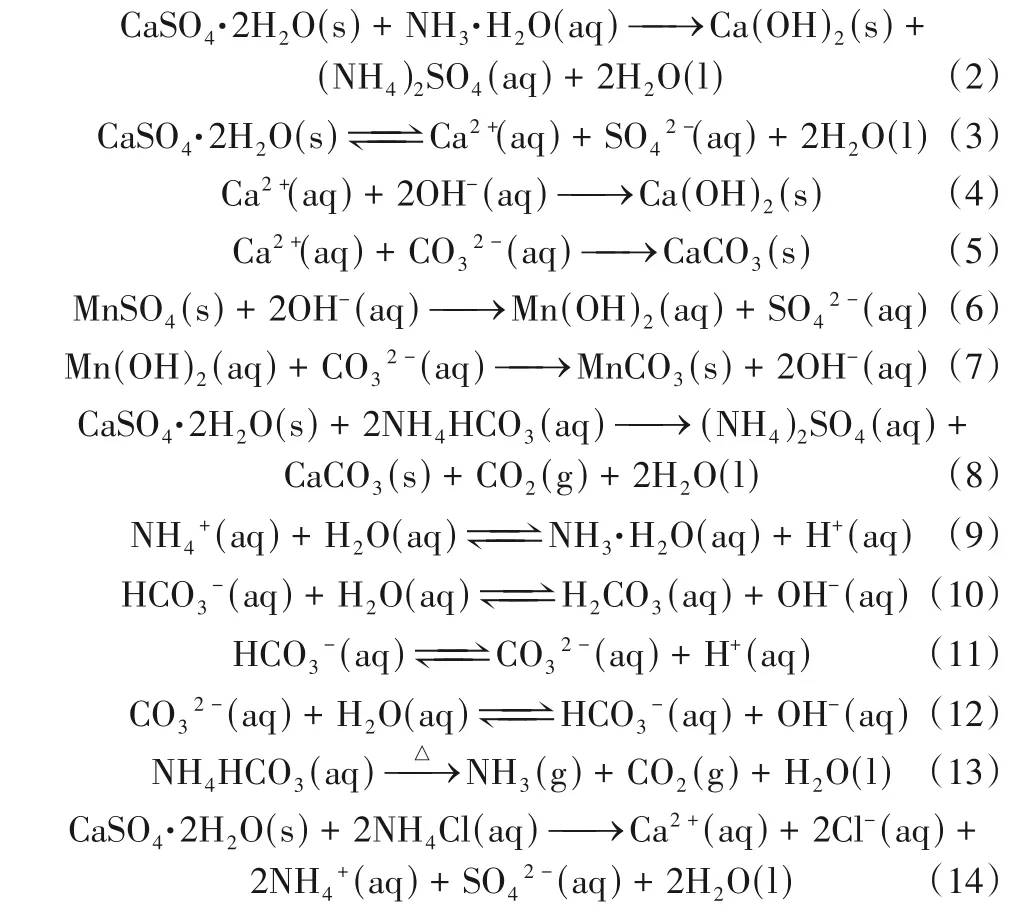
3 结论
研究了NHHCO和NHCl用量、浸出初始pH、浸出时间、浸出温度对锰渣中石膏转变的影响。采用XRD、SEM-EDS-Mapping、FTIR、XRF 等现代分析手段,揭示了电解锰渣中石膏转变规律。得出如下主要结论。
(1)当电解锰渣与NHHCO以及NHCl质量比为20∶8∶1.5、电解锰渣与水固液比为1∶5、浸出初始pH 为7.5、浸出温度70℃、浸出时间120min 时,石膏浸出率达到90.0%,浸出锰渣主要物相含有CaCO、SiO、CaMn(OH)SiO·2HO、MgAlFeSiAlO(OH)以 及KAlSiO(OH)等,其中浸出锰渣中MnO 含量由未浸出前的7.45%提高到14.71%。
(2)浸出机理表明,NHHCO与锰渣中石膏反应转变成(NH)SO和CaCO,而NHCl 作为盐试剂可进一步促进石膏溶解,从而提高锰渣中石膏浸出率。
